氧化物修饰杂原子B-Beta分子筛催化剂的制备及其对丙烷脱氢的催化性能研究
2020-04-17顾建峰臧云浩高峰钒
顾建峰 臧云浩 高峰钒


摘要:以工业柱层硅胶、硼酸等为主要原料,采用水热法合成了NaB\|Beta,NaB\|ZSM\|5,Si\|Beta,HB\|Beta和HB\|ZSM\|55种形式的杂原子分子筛;以其为载体,采用浸渍法负载钒氧化物VOx制备了一系列丙烷脱氢催化剂样品,并对其丙烷脱氢催化性能和结构进行分析和表征.结果表明:以HBBeta分子筛为载体、负载8%(质量分数)的VOx制得的样品(8VOx/HBBeta)丙烷脱氢的催化活性最好,在600℃条件下反应30min,丙烷转化率为43%,丙烯选择性为78%,丙烯收率为34%;HBBeta分子筛更有利于钒氧化物VOx的分散,进而形成单分散的钒氧化物VOx.这些高分散的钒氧物种和载体一定的酸量,是该类丙烷脱氢催化剂具有高活性的关键因素.
Abstract:Usingcolumnarsilicagelandboricacidasthemainrawmaterials,fivetypesofheteroatommolecularsieves,NaB\|Beta,NaB\|ZSM\|5,Si\|Beta,HB\|BetaandHB\|ZSM\|5weresynthesizedbyhydrothermalmethod.Asacarrier,aseriesofpropanedehydrogenationcatalystsampleswerepreparedbyimpregnatingVOx,andtheirpropanedehydrogenationcatalyticperformanceandstructurewereanalyzedandcharacterized.Theresultsshowedthatthesample(8VOx/HB\|Beta)preparedwithHB\|Betamolecularsieveasthecarrierand8%(massfraction)ofVOxhadthebestcatalyticactivityforpropanedehydrogenation.Thereactionwascarriedoutat600℃for30min,theconversionratewas43%,thepropyleneselectivitywas78%,andthepropyleneyieldwas34%.HB\|BetamolecularsievewasmoreconducivetothedispersionofvanadiumoxideVOx,andthenmonodispersedvanadiumoxideVOxwasformed.Thesehighlydispersedvanadiumspeciesandacertainamountofacidonthecarrierwerethekeyfactorsforthehighactivityofthistypeofpropanedehydrogenationcatalyst.
關键词:杂原子BBeta分子筛;钒氧化物;丙烷脱氢反应;负载
Keywords:heteroatomBBetamolecularsieve;vanadiumoxide;propanedehydrogena\|tion;loading
0引言
丙烷脱氢制丙烯不仅可以实现炼厂气和油田伴生气中低碳烯烃资源的优化利用,还可以缓解丙烯供求日趋加剧的矛盾,具有重要的研究意义.当前,丙烷脱氢制丙烯的工艺主要有丙烷直接脱氢(PDH)和丙烷氧化脱氢[1-2]两种.PDH的催化剂主要为负载型Pt催化剂[1-4]和负载型Cr催化剂[1,5],丙烷氧化脱氢的催化剂主要为V负载催化剂[1,6].B.Schimmoeller等[7]研究发现,烷烃氧化脱氢的催化活性受活性物种钒氧化物VOx的影响,其在载体上表现出的单体、低聚体和高聚体形式对应的催化活性也不同.H.Y.Kim等[8]研究发现,当VOx的负载量超过单层覆盖率(8~9V/nm2)时,丙烷脱氢的催化活性将会显著降低.为了获得更高的催化活性,很多学者都在寻找一种有利于钒氧化物VOx更好分散的载体结构,目前研究主要围绕具有均一孔径的高比表面积的材料展开,如MCM\|41,SBA\|15,Al2O3,ZrO2等[9-12],这些材料作为载体制备的丙烷脱氢催化剂,展示出相对优异的催化活性.
分子筛材料以其独特的性质在丙烷脱氢催化剂中显示出较好的发展前景.其中,载体分子筛多为拓扑结构,骨架基本由硅和氧原子或硅、金属和氧原子组成.这些以非Al2O3为载体的新型脱氢催化剂具有良好的脱氢活性和稳定性.姜健准等[13]研究开发了ZSM\|5负载Pt基丙烷脱氢催化剂,在反应温度600℃,丙烷的重时空速3h-1和常压条件下,反应40h,丙烷转化率约为40%,丙烯选择性约为94%.P.L.D.Cola等[14]在NaZSM\|5,NaZSM\|11,Na\|Beta,Na\|MOR,K\|L,Na\|Y等含Zn的沸石上,通过浸渍法负载质量分数0.5%的Pt,将所制得的脱氢催化剂用于丙烷脱氢反应,发现不同的载体对丙烷脱氢反应性能影响明显,其中,0.5Pt/2.6Zn\|Beta催化剂在反应温度550℃条件下,丙烷转化率接近热力学平衡值(29%),丙烯选择性大于90%.C.Chen等[15]以脱铝后的Beta分子筛(SiBeta)作为V催化剂载体制备了丙烷脱氢催化剂,并将其用于丙烷脱氢反应,在反应温度600℃的条件下,丙烷转化率接近40%,丙烯选择性约90%,这表明Beta分子筛作为载体具有优异的丙烷脱氢催化性能.
一般的硅铝酸盐分子筛的酸性太强,以其为载体制备的丙烷脱氢催化剂芳构化严重,丙烯选择性太差,需要添加助剂等进行酸性调变.而纯硅分子筛酸性又太弱,一般不利于丙烷脱氢的进行.因此,开发一种酸性适中的分子筛催化剂就显得很有意义.鉴于此,本文拟采用水热法一步合成新型低酸量的杂原子硼硅酸盐B\|Beta分子筛,以其作为载体,通过浸渍法负载钒氧化物VOx制得一系列催化剂样品,通过对样品丙烷脱氢催化性能的分析和结构表征,为丙烷脱氢催化剂的开发提供一种新的思路.
1材料与方法
1.1主要试剂与仪器
主要试剂:工业柱层硅胶(工业级,SiO2质量分数为93%),青岛美高化工有限公司产;NaOH(分析纯),天津化学试剂三厂产;NH4NO3(分析纯),天津科威有限公司产;四乙基氢氧化铵(分析纯),天津光复精细化工研究所产;硼酸(分析纯),偏钒酸铵(分析纯),国药集团化学试剂有限公司产;H\|Beta分子筛,南开大学催化剂有限公司产;丙烷(高纯),比欧西气体(天津)有限公司产;N2(高纯),天津六方高科气体有限公司产.实验用水均为去离子水.
主要仪器:不锈钢反应釜(120mL),南开大学精工厂产;JJ-1型电动搅拌器,江苏金坛市环宇科学仪器厂产;SK2-2-12型管式电炉,天津中环实验电炉有限公司产;DG-204型电热恒温鼓风干燥箱,天津天宇实验仪器有限公司产;AK-1140型电子天平,梅特勒-托利多仪器有限公司产;RigakuD/max-2500型X射线衍射仪,日本理学株式会社产;QuantachromeNOVA-2000e型氮氣吸附仪,CHEMBET-3000型氨气程序升温脱附仪和氢气程序升温还原仪,美国康塔公司产;Perkin\|ElmerPHI-5600型X射线光电子能谱仪,美国珀金埃尔默公司产;JASCOV-570型紫外可见漫反射仪,日本日立仪器公司产;Q600型同步DSC/TGA分析仪,德国耐驰公司产.
1.2分子筛的制备
NaB\|Beta分子筛的合成:采用水热合成法,以四乙基氢氧化铵为模板剂,分别以硼酸和柱层硅胶为硼源和硅源,合成物料比为n(Na2O)GA6FAn(SiO2)GA6FAn(B2O3)GA6FAn(TEAOH)GA6FAn(H2O)=1.9GA6FA30GA6FA1.0GA6FA3.5GA6FA300.常温下,将一定量的NaOH加入盛有一定量水的烧杯中,一边搅拌一边依次加入一定量的硼酸、柱层硅胶和四乙基氢氧化铵,搅拌陈化2h得到凝胶.将该凝胶转移至带有聚四氟乙烯内衬的不锈钢反应釜中,于150℃温度下晶化72h.所得产物经抽滤、洗涤、干燥,再置于550℃电炉中焙烧5h脱除模板剂,即得Na型B\|Beta分子筛原粉,记为NaB\|Beta分子筛.
NaB\|ZSM\|5分子筛的合成:以四乙基氢氧化铵为模板剂,分别以硼酸和柱层硅胶为硼源和硅源,合成物料比为n(Na2O)GA6FAn(SiO2)GA6FAn(B2O3)GA6FAn(TEAOH)GA6FAn(H2O)=3.0GA6FA30GA6FA1.0GA6FA3.5GA6FA300.其他合成步骤和条件同NaB\|Beta分子筛的合成方法,所得产物记为NaB\|ZSM\|5分子筛.
纯Si\|Beta分子筛的合成:以四乙基氢氧化铵为模板剂,柱层硅胶为硅源,合成物料比为n(Na2O)GA6FAn(SiO2)GA6FAn(TEA)GA6FAn(H2O)=2.3GA6FA30GA6FA6GA6FA300.其他合成步骤和条件同NaB\|Beta分子筛的合成方法,所得产物记为Si\|Beta分子筛.
氢型B\|Beta和氢型B\|ZSM\|5分子筛的制备:称取一定量的NaB\|Beta和NaB\|ZSM\|5分子筛原粉置于烧杯中,分别用1.0mol/L的NH4NO3溶液按照分子筛和溶液质量比1GA6FA10搅拌混合,80~90℃下重复离子交换3—4次.所得产物经抽滤,干燥,再置于500℃电炉中焙烧3h,即得氢型B\|Beta和氢型B\|ZSM\|5分子筛,分别记为HB\|Beta和HB\|ZSM\|5.
1.3VOx负载催化剂的制备
nVOx/分子筛的制备:分别以HB\|Beta,H\|Beta,Si\|Beta和HB\|ZSM\|5分子筛为载体,以NH4VO3为VOx的前驱体,在80℃条件下,采用浸渍法将不同质量浓度的NH4VO3负载到各载体上,磁力搅拌3h,然后将所得产物置于100℃的烘箱中干燥24h,最后置于600℃管式电炉中焙烧3h.根据需要制备不同V2O5负载量的催化剂,命名为nVOx/分子筛,其中n代表钒氧化物VOx的质量分数/%.
nVOx/HB\|Beta系列催化剂的制备:在80℃条件下,将一定量的HB\|Beta分子筛加入到不同质量浓度的NH4VO3溶液中,共浸12h后,干燥,置于600℃马弗炉中焙烧3h.根据需要制备不同VOx负载量的催化剂,命名为nVOx/HB\|Beta,其中n代表钒氧化物VOx的质量分数/%.
1.4催化剂样品的表征和测试方法
采用X-射线衍射仪进行样品的物相分析:辐射源CuKα,管电流100mA,管电压40kV,扫描速度2°/min,扫描范围3°~50°.
采用吸附仪进行样品的比表面积和孔结构比表面积测定:样品在200℃条件下抽真空预处理4h,然后在液氮(-196℃)中进行静态氮吸附,以BET公式计算求得相应的比表面积.
采用紫外-可见(UV\|Vis)漫反射光谱仪对样品存在价态进行分析:将一定量的样品粉末置于石英管中,经550℃空气焙烧1h后冷却至室温,在干燥空气气氛中测定样品的UV\|Vis谱,波长范围190~800nm,波长精度0.1nm.
采用傅立叶变换红外光谱仪对样品的结构进行分析:将样品与KBr混合压成20mm厚的薄片,在400~4000cm-1范围内扫描,记录红外光谱图.
采用H2-程序升温还原法(H2\|TPR)测试样品的还原性能:取200mg样品,在200℃条件下,通高纯He吹扫1h后冷却至室温,切换通入体积分数分别为5%和95%的H2和Ar混合气.待仪器基线平稳后,以10℃/min的速率升温,用TCD热导检测耗氢量.
采用NH3-程序升温脱附法(NH3\|TPD)测试样品的酸强度:准确称量200mg,40~80目的样品置于样品管中,以He为载气,以10℃/min的速率升温至600℃,吹扫1h后降温至80℃,通入体积分数分别为5%和95%的NH3和Ar混合气,直至吸附饱和约30min,然后转至纯Ar吹扫,除去物理吸附的NH3,以10℃/min的速率升温至700℃,用TCD热导检测脱附氨信号,通过脉冲滴定测得样品的酸性.
采用光电子能谱仪(XPS)进行负载元素结合能分析:以MgKα作为X射线源,操作电压为13kV,功率250W,真空度优于10-7Pa,样品结合能以C1s(Eb=284.6eV)为内标进行荷电校正.
采用热重-差热分析仪对样品的重量变化进行测定:准确称量50mg样品置于样品管中,在N2氛围下,升温速率10℃/min,采集温度区间为常温~800℃,用TCD热导连续检测.
1.5催化剂的活性分析方法
采用固定床微反装置进行丙烷脱氢反应催化剂的活性分析:反应管内径6mm,长400mm,催化剂装填量400mg,反应前将反应器升温至35℃,N2吹扫2h,然后将反应器温度降至常温开始反应.反应条件设置为反应温度450~600℃,原料气体组成为V(N2)GA6FAV(C3H8)=40GA6FA2,空速3600mL/(h·g).通过气相色谱仪(HP-Plot型毛细光柱,FID检测)对反应产物进行在线分析,利用面积归一法进行计算.
丙烷转化率、丙烯选择性和丙烯收率的具体计算方法分别如下:
丙烷转化率=丙烷反应物质的量反应器中丙烷物质的量×100%
丙烯选择性=丙烷生成物质的量丙烷反应物质的量×100%
丙烯收率=丙烷转化率×丙烯选择性=
丙烯生成物质的量反应器中丙烷物质的量×100%
2结果与讨论
2.1不同催化剂样品对丙烷脱氢反应性能的影响分析
2.1.1不同分子筛基催化剂样品
不同分子筛载体负载相同量的VOx制备的催化剂对丙烷脱氢反应性能的影响如图1和图2所示.从图1可以看出,在600℃条件下反应30min,各催化剂的丙烷转化率从高至低依次为8VOx/HB\|Beta>8VOx/H\|Beta>8VOx/Si\|Beta>8VOx/HB\|ZSM\|5.从图2可以看出,在600℃条件下反应30min,各催化剂的丙烯选择性从高至低依次为8VOx/HB\|ZSM\|5>8VOx/Si\|Beta>
8VOx/HB\|Beta>8VOx/H\|Beta.由此可得出,丙烯收率从高至低依次为8VOx/HB\|Beta>8VOx/Si\|Beta>8VOx/H\|Beta>8VOx/HB\|ZSM\|5.以HB\|Beta分子筛为载体制备的丙烷脱氢催化剂
8VOx/HB\|Beta,其丙烷转化率为43%,丙烯选择性为78%,丙烯收率为34%,表明其具有良好的催化性能.这是由于丙烷脱氢反应是一个酸催化反应,催化剂中适当酸量的存在对脱氢反应的进行极为重要.但是,催化剂中过量酸性中心的存在,在促进丙烷脱氢反应的同时,也加速了丙烷裂解、氢解等副反应的发生,降低了催化反应的产物选择性.通过丙烷脱氢反应的数据可知,HB\|Beta分子筛是制备丙烷脱氢催化剂的一个优异载体.
2.1.2nVOx/HB\|Beta催化剂样品
nVOx/HB\|Beta催化剂对丙烷脱氢反应性能的影响如图3所示.从图3可以看出,各催化剂的丙烷转化率均随反应温度的升高而升高,丙烯选择性则呈现相反的变化趋势,即随着反应温度的升高、反应速率的加快,致丙烯选择性降低.随着VOx负载量的增加,丙烯转化率呈现先升高后降低的趋势,当VOx负载量为8%时,丙烷转化率达到最高,为43%,丙烯选择性也高达78%,显示了对丙烷脱氢优异的催化活性.这可能是由于VOx是VOx/HB\|Beta催化剂的主要活性中心,丙烷脱氢反应主要发生在VOx表面,其负载量越大则催化活性越高.但是,VOx负载量的增加,在有利于丙烷脱氢反应的同时,也降低了催化剂的比表面积,还加速了催化剂表面氢解副反应的发生,降低了丙烯选择性.值得注意的是,当VOx负载量高达16%时,VOx/HB\|Beta催化剂的丙烷转化率明显降低,只有19.8%.这可能是由于高负载量的VOx堵塞了载体的孔道,降低了催化剂的比表面积,使VOx物种活性位与催化剂载体之间没能产生良好的构效关系.同时,高负载量的VOx会形成V2O5,不利于丙烷转化为丙烯,并增加了反应过程中积碳前驱体的产生,导致催化剂表面积碳量增加,所有这些都不利于丙烷脱氢反应的进行.因此,在本实验中,最佳的丙烷脱氢催化剂的VOx负载量为8.0%.
图4为8VOx/HB\|Beta催化剂样品对丙烷脱氢反应活性的影响.从图4可以看出,虽然8VOx/HB\|Beta催化剂的初始活性比较高,但反应的稳定性相对较差,反应12h后,丙烷的转化率从43%降至17%,其丙烯的选择性由76.4%增至近95%.这可能是由于反应过程中产生的积碳将催化剂表面活性中心覆盖,尤其是载体的酸性位,使得一系列副反应受到抑制,從而提高了催化反应的选择性.从这种意义来讲,积碳类似一种助剂,可以提高催化剂的脱氢选择性[13].
2.2催化剂样品的表征结果分析
2.2.1样品的物相分析
图5为nVOx/HB\|Beta催化剂样品的XRD图.从图5可以看出,当VOx的负载量小于16%时,催化剂样品在2θ为10°~70°范围内没有出现V2O5的特征衍射峰,说明钒能够在HB\|Beta载体表面高度分散.当VOx的负载量达到16%时,出现了V2O5的特征衍射峰,同时载体结晶度明显降低.这表明,在具有较高催化活性的8VOx/HB\|Beta催化剂上,存在着高度分散的较高浓度的钒物种,这可能是其表现出较好催化活性的原因.
2.2.2样品的BET结果分析
表1为nVOx/HB\|Beta催化剂样品的BET表征结果.从表1可知,HB\|Beta作为一种孔道有序的微孔分子筛,比表面积高达559m2·g-1.催化剂样品的比表面积随着VOx负载量的增加而降低.这可能是由于钒氧物种的增加覆盖了分子筛表面、堵塞了分子筛孔道的缘故.
2.2.3样品的价态分析
为了研究负载量对钒配位环境的影响,测定了不同催化剂样品的UV\|Vis漫反射光谱,结果如图6和图7所示.
根据文献[16]的研究结果,265nm处的峰可归属为高度单分散四配位V5+物种(VO4),340nm处的峰可归属为低聚的四配位V5+物种,378nm处的谱带可归属为聚合的四配位V5+物种,450nm处的谱带可归属为V2O5微晶.
基于此,由图6可以看出,8VOx/HB\|Beta催化剂上的钒氧物种,主要以高度分散的四配位V5+物种和低聚的四配位V5+物种的形式存在,而基本上无高度聚合的V5+物种或V2O5微晶.但8VOx/H\|Beta催化剂在265nm处的谱带强度大为减弱,其谱带主要出现在300nm以上,这表明8VOx/H\|Beta催化剂的钒氧物种主要以高聚的四配位V5+物种形式存在.对于8VOx/Si\|Beta来说,UV\|Vis光谱上没有体现出所设想的四配位V5+物种的明显存在,原因可能是过多的水覆盖了信号峰.
由图7可以看出,VOx/HB\|Beta系列催化剂在265nm,340nm,375nm和440nm附近都出现了紫外吸收峰,分别归属为高度分散的钒氧四面体和多聚V—O—V中氧与配位钒之间的电荷转移[17-20].当VOx负载量小于8%时,催化剂样品只在265nm和375nm附近出现紫外吸收峰,说明当催化剂中钒含量较低时,钒主要以高分散的低四配位的钒氧四面体形式存在.375nm处的峰一般归属为准六配位的孤立态V5+,这一物种与四配位的V5+物种之间通过吸水、脱水相互转化[21].当催化剂中VOx负载量增加到16%时,在440nm附近出现了新的吸收峰,归于类似晶体的V2O5结构,这说明随着VOx负载量的增加,钒物种的聚合度增大.对于VOx/HB\|Beta催化剂样品在丙烷脱氢反应中的催化活性,8VOx/HB\|Beta表现出了最高的丙烷转化率和很好的丙烯选择性,说明高分散的、四配位的钒氧四面体比多聚钒氧物种的丙烷脱氢的催化性能好.这种高分散的四配位钒氧物种可能是负载过程中B\|Beta分子筛骨架脱硼产生的空位被钒占据产生的,这种缺陷较多的Beta分子筛更有利于形成四配位的钒氧化物,而这些物种对丙烷脱氢反应是有利的.
2.2.4样品的结构分析
图8为nVOx/HB\|Beta催化剂样品的FT\|IR谱图.随着VOx负载量的增加,在960cm-1[22-23]处存在的有争议的红外振动峰,其强度随钒负载量的升高先减弱后增强,并向低波数移动.在940cm-1附近处出现一个较大的吸收峰,归于Si—O—V键的振动吸收峰[24].诱发此畸变的原因可能有两个:一是外来客体分子如金属离子等与载体间产生的键合作用;二是晶体本身结构发生变化,导致硅氧四面体的畸变.负载VOx的催化剂样品中,此处的谱峰向低波数发生位移(蓝移),并且强度增强,联系前面的表征进行推测,在负载VOx的催化剂样品中,一部分钒进入了分子筛的骨架中,即使对16VOx/HB\|Beta催化劑样品,在1017cm-1和831cm-1处也没有发现归属于晶态V2O5中的VO伸缩振动峰和V—O—V的弯曲振动峰[25].另外,起Lewis酸作用的骨架三配位B[3]在1385cm-1处的吸收峰随着钒负载量的增加,其强度发生了变化,说明分子筛的骨架振动发生了改变.
2.2.5样品的酸度分析
对于VOx负载分子筛制备的丙烷脱氢催化剂,不同分子筛载体的NH3\|TPD谱图见图9.由图9可以看出,不同的分子筛载体因其孔道和酸性存在差异,在丙烷脱氢反应中的活性表现不同,具体数据见表2.从表2可知,分子筛酸量大小依次为H\|Beta>HB\|Beta>HB\|ZSM\|5>Si\|Beta.
nVOx/HB\|Beta催化剂样品的NH3\|TPD曲线见图10.从图10可以看出,负载VOx之前的HB\|Beta分子筛分别在187℃和385℃处出现较大的脱附峰和微小的脱附峰,分别对应其表面的弱酸(Acidw)脱附峰和强酸(Acids)脱附峰,可分别归属为骨架内B[3]和杂质产生的吸收峰.负载VOx之后,分子筛表面酸量发生了很大的变化,对4VOx/HB\|Beta催化剂样品而言,其NH3脱附峰面积发生了很大的变化,在220℃左右处出现了一个宽峰,说明分子筛负载钒物种后覆盖了其酸中心,并导致低温脱附峰向高温偏移.增大钒负载量分别至8%和12%时,发现催化剂样品的脱附峰发生了变化,除了在180~220℃之间出现较大的脱附峰外,还在265℃左右出现了一个新的中强酸脱附峰,可归属于钒占据缺陷位与分子筛形成的四面体结构的(SiO)3VO[26],这说明钒的引入调变了分子筛的酸强度和酸量.
2.2.6样品的还原性能分析
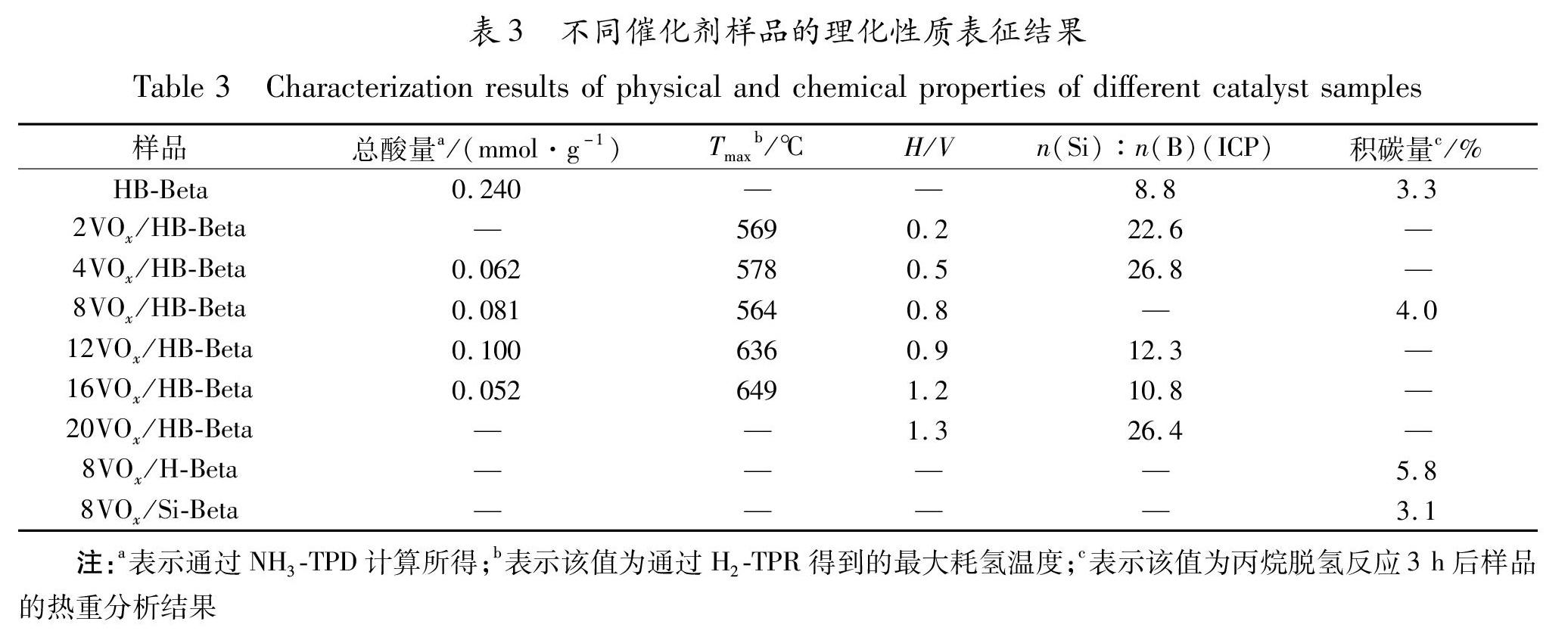
表3为不同催化剂样品的理化性质表征结果.从表3可知,随着钒的引入,分子筛表面的总酸量由0.24mmol/g(HB\|Beta)降低至0.052mmol/g(16VOx/HB\|Beta),新出现的中强酸中心的NH3吸附量呈现先增大后降低的趋势.综上可见,钒的引入调变了分子筛表面的酸强度和酸中心数,并且在其表面产生了部分中强酸度的酸中心,对丙烷脱氢反应是有利的.将丙烷脱氢在600℃条件下反应3h的催化剂8VOx/HB\|Beta,8VOx/H\|Beta和8VOx/Si\|Beta进行了TG\|DSC积碳分析,结果显示,积碳和载体的酸性呈正比关系,酸性大的载体积碳更为严重,这种积碳导致了催化剂活性的下降.
图11为nVOx/HB\|Beta催化剂样品的H2\|TPR谱图.从图11可以看出,2VOx/HB\|Beta样品在565℃处出现了一个宽的H2\|TPR峰,归属于V5+还原为V4+消耗的H2峰.增加VOx的
负载量,4VOx/HB\|Beta样品的H2还原峰向高温590℃方向发生偏移,同时有一个较小的低温(530℃)还原峰出现.继续增加VOx的负载量可以发现,8VOx/HB\|Beta样品在564℃处出现一个较大的H2还原峰,12VOx/HB\|Beta样品分别在554℃和665℃出现还原峰,16VOx/HB\|Beta样品的H2还原峰面积变大,还原温度变高.而V2O5粉末的两个H2\|TPR峰分别位于675℃和708℃[29],可见,nVOx/HB\|Beta催化剂中V2O5的还原温度比纯V2O5粉末要低得多,表明VOx负载到HB\|Beta分子筛后更容易被还原.笔者将568~590℃处的H2还原峰归属于分子筛表面高分散的四配位的V5+的还原,将665℃附近的H2还原峰归属于聚合的或类晶态的钒氧物种的还原[27-30].这说明,高分散的准四配位的钒氧四面体比多聚的钒氧物种更容易被还原,在丙烷氧化脱氢反应中表现了优异的催化性能.
隨着VOx负载量的增加,H2消耗量也呈递增趋势但并不呈线性关系.这是由于VOx负载量较高时,钒氧化物的状态不是单纯的一种物种,其中存在少量的更易于还原的钒氧物种,如16VOx/HB\|Beta,最高的还原峰温度向低温偏移,预示着消耗更多的H2[31].通过H2\|TPR的耗H2量,可以计算H/V值来获得催化剂上钒氧物种确切的存在价态.一般H/V=2代表钒氧物种的V5+完全还原为V3+.结合表3可知,所有样品的H/V值都小于2,这归属于四配位的V5+还原(V5+→V4+).对活性较好的8VOx/HB\|Beta样品,其H/V=0.8,可推测出其表面绝大部分为高分散的四配位V5+物种,这种高分散的四配位V5+物种归为丙烷脱氢的活性位.
2.2.7样品负载元素结合能分析
用X-射线电子能谱(XPS)对8VOx/HB\|Beta样品的表面VOx的价态进行分析,结果见图12.从图12可以看出,该催化剂样品的O1s和V2p3/2峰分别位于532.7eV和517.6eV,分别归属为VO键和V5+物种[32-35].说明该催化剂表面为高分散的进入分子筛骨架的四配位V5+物种.
3结论
本文采用水热法合成了NaB\|Beta,NaB\|ZSM\|5,Si\|Beta,HB\|Beta和HB\|ZSM\|55种形式的杂原子分子筛,以其为载体,采用浸渍法负载VOx,制备了一系列丙烷脱氢催化剂样品.将催化剂样品用于丙烷脱氢反应,并对其催化活性进行分析,结果表明,弱酸性的杂原子B\|Beta分子筛HB\|Beta负载VOx后所得催化剂样品8VOx/HB\|Beta具有相对优异的催化性能,在600℃条件下反应30min,其丙烷转化率为43%,丙烯选择性为78%.对催化剂样品的表征结果显示,弱酸性的、较多缺陷的HB\|Beta分子筛更有利于VOx的负载,形成单分散的钒氧化物VOx,这是催化剂高活性的关键.以此杂原子HB\|Beta分子筛为载体制备的钒基丙烷脱氢催化剂,有望成为新型丙烷脱氢催化剂一个更好的研究方向.
参考文献:
[1]HUZP,YANGDD,WANGZ,etal.Stateoftheartcatalystsfordirectdehydrogenationofpropanetopropylene[J].ChineseJournalofCatalysis,2019,40(9):1233.
[2]李思漩,张惠民,夏蕾,等.丙烷脱氢制丙烯催化剂研究进展[J].现代化工,2018,38(2):14.
[3]BENDNAROVAL,LYMANCE,RYTTERE,etal.EffectofsupportonthesizeandcompositionofhighlydispersedPtSnparticles[J].JournalofCatalysis,2002,211(2):335.
[4]BARIASOA,HOLMENA,BLEKKANEA.PropanedehydrogenationoversupportedPtandPt\|Sncatalysts:Catalystpreparation,characterization,andactivitymeasurements[J].JournalofCatalysis,1996,158(1):1.
[5]SANTHOSHKM,HAMMERN,RNINGM,etal.ThenatureofactivechromiumspeciesinCrcatalystsfordehydrogenationofpropane:Newinsightsbyacomprehensivespectroscopicstudy[J].JournalofCatalysis,2009,261(1):116.
[6]LIUG,ZHAOZJ,WUT,etal.NatureoftheactivesitesofVOx/Al2O3catalystsforpropanedehydrogenation[J].ACSCatalysis,2016,6(8):5207.
[7]SCHIMMOELLERB,JIANGY,PRATSINISSE,etal.Structureofflamemadevanadia/silicaandcatalyticintheoxidativedehydrogenationofpropane[J].JournalofCatalysis,2010,274(1):64.
[8]KIMHY,LEEHM,PALARG,etal.Oxidativedehydrogenationofmethanoltoformaldehydebyisolatedvanadium,molybdenum,andchromiumoxideclusterssupportedonrutileTiO2(110)[J].JournalofPhysicalChemistryC,2009,113(36):16083.
[9]PIECKCL,BAARESMA,FIERROJLG.PropaneoxidativedehydrogenationonVOx/ZrO2catalysts[J].JournalofCatalysis,2004,224(1):1.
[10]LIUYM,CAOY,YIN,etal.VanadiumoxidesupportedonmesoporousSBA15ashighlyselectivecatalystsintheoxidativedehydrogenationofpropane[J].JournalofCatalysis,2004,224(2):417.
[11]KONDRATENKOE,CHERIANM,BAERNSM,etal.OxidativedehydrogenationofpropaneoverV/MCM41catalysts:ComparisonofO2andN2Oasoxidants[J].JournalofCatalysis,2005,234(1):131.
[12]HARLINME,NIEMIVM,KRAUSEAOI,etal.EffectofMgandZrmodificationontheactivityofVOx/Al2O3catalystsinthedehydrogenationofbutanes[J].JournalofCatalysis,2001,203(1):242.
[13]姜健準,冯静,刘晓玲,等.纳米薄片PtSnNa/MFI催化剂的制备及其丙烷脱氢性能研究[J].石油化工,2019,48(4):327.
[14]COLAPLD,GLASERR,WEITKAMPJ.NonoxidativepropanedehydrogenationoverPtZncontainingzeolites[J].AppliedCatalystA,2006,306(1):85.
[15]CHENC,SUNML,HUZP,etal.NatureofactivephaseofVOxcatalystssupportedonSiBetafordirectdehydrogenationofpropanetopropylene[J].ChineseJournalofCatalysis,2020,41(2):276.
[16]LUOQX,ZHANGXK,HOUBL,etal.CatalyticfunctionofVOx/Al2O3foroxidativedehydrogenationofpropanesupportmicrostructure\|dependentmasstransferanddiffusion[J].CatalSciTechnol,2018,8(19):4864.
[17]ZHANGSG,HIGASHIMOTOS,YAMASHITAH,etal.CharacterizationofvanadiumOxide/ZSM5zeolitecatalystspreparedbythesolidstatereactionandtheirphotocatalyticreactivity:Insituphotoluminescence,XAFS,ESR,FTIR,andUV\|visinvestigations[J].JournalofPhysicalChemistryB,1998,102(29):5590.
[18]CHAOKJ,WUCN,CHANGH,etal.IncorporationofVanadiuminmesoporousMCM41andmicroporousAFIzeolites[J].JournalofPhysicalChemistryB,1997,101(33):6341.
[19]KOMATOWSKIJ,WICHTERLOVAB,ROZWADOWSKIM,etal.Simultaneousoccurrenceofdifferentlycoordinatedframeworkheteroatomsinonezeolite:MFItypevanadiumsilicalite,KVS5[J].StudiesinSurfaceScienceandCatalysis,1994,84(1):117.
[20]AMOLDABJ,NIEDERERJPM,NIESSENTEW,etal.Theinfluenceofsynthesisparametersonthevanadiumcontentandporesizeof[V]MCM41materials[J].MicroporousandMesoporousMaterials,1999,28(1):353.
[21]KHODAKOVA,OLTHOFB,BELLAT,etal.Structureandcatalyticpropertiesofsupportedvanadiumoxides:Supporteffectsonoxidationdehydrogenationreactions[J].JournalofCatalysis,1999,181(2):205.
[22]BOCCUTIMR,RAOKM,ZECCHINAA,etal.Spectroscopiccharacterizationofsilicaliteandtitaniumsilicalite[J].StudiesinSurfaceScienceandCatalysis,1989(48):133.
[23]CAMBLORMA,CORMAA,PEREZPARIENTEJ.Infraredspectroscopicinvestigationoftitaniuminzeolites:Anewassignmentof960cm-1band[J].JournaloftheChemicalSociety,ChemicalCommunications,1993(6):557.
[24]LIUYM,CAOY,YIN,etal.VanadiumoxidesupportedonmesoporousSBA15ashighlyselectivecatalystsintheoxidativedehydrogenationofpropane[J].JournalofCatalysis,2004,224(2):417.
[25]CENTIG,TRIFIROF.CatalyticbehaviorofVcontainingzeolitesinthetransformationofpropaneinthepresenceofoxygen[J].AppliedCatalystA,1996,143(1):3.
[26]MOREYM,DAVIDSONA,ECKERTH,etal.PseudotetrahedralO3/2VOcentersimmobilizedonthewallsofamesoporous,cubicMCM48support:Preparation,characterization,andreactivitytowardwaterasinvestigatedby51VNMRandUVVisspectroscopies[J].ChemistryofMaterials,1996,8(2):486.
[27]HUP,LANGWZ,YANX,etal.Vanadium\|dopedporoussilicamaterialswithhighcatalyticactivityandstabilityforpropanedehydrogenationreaction[J].AppliedCatalystA,2018,553:65.
[28]BERNDTH,MARTINA,BRUCKNERA,etal.StructureandcatalyticpropertiesofVOx/MCMmaterialsforthepartialoxidationofmethanetoformaldehyde[J].JournalofCatalysis,2000,191(2):384.
[29]KERANENJ,AUROUXA,EKS,etal.Preparation,characterizationandactivitytestingofvanadiacatalystsdepositedontosilicaandaluminasupportsbyatomiclayerdeposition[J].AppliedCatalystA,2002,228(1):213.
[30]KORANNEMM,GOODWINJG,MARCELING.Characterizationofsilicaandaluminasupportedvanadiacatalystsusingtemperatureprogrammedreduction[J].JournalofCatalysis,1994,148:369.
[31]SHIJUNR,ANILKUMARM,MIRAJKARSP,etal.Oxidativedehydrogenationofethylbenzeneovervanadiaaluminacatalystsinthepresenceofnitrousoxide:Structureactivityrelationship[J].JournalofCatalysis,2005,230(2):484.
[32]HARLINME,NIEMIVM,KRAUSEAOI.Aluminasupportedvanadiumoxideinthedehydrogenationofbutanes[J].JournalofCatalysis,2000,195(1):67.
[33]MOSERTP,SCHRADERGL.StabilityofmodelV\|P\|Ocatalystsformaleicanhydridesynthesis[J].JournalofCatalysis,1987,104(1):99.
[34]BAIP,MAZ,LIT,etal.RelationshipbetweensurfacechemistryandcatalyticperformanceofmesoporousγAl2O3supportedVOxcatalystincatalyticdehydrogenationofpropane[J].ACSAppliedMaterialsInterfaces,2016,8:25979.
[35]FUKUDOMEK,SUZUKIT.HighlyselectiveoxidativedehydrogenationofpropanetopropyleneoverVOxSiO2catalysts[J].CatalysisSurveysfromAsia,2015,19(3):172
