动态血管模型在六氟化硫微泡联合高强度聚焦超声消融富血供子宫肌瘤中的增效作用
2020-04-11寸江平范宏杰易根发姚瑞红
寸江平,赵 卫,范宏杰,易根发,王 滔,姚瑞红
高强度聚焦超声(high intensity focused ultrasound,HIFU)消融子宫肌瘤的疗效已得到肯定,但对于富血供肌瘤能量沉积困难,影响疗效和治疗工作效率的提升[1-2]。大量的临床研究显示超声微泡增强对比剂具有HIFU 消融增效作用[3-4],但微泡对比剂并不具有靶向运动,正常组织内也存在,这可能导致周围组织的副损伤,且不同类型的肌瘤以及周围不同组织结构的增强时机和强度不同。动态血管模型(dynamic vascular pattern,DVP)是利用对比剂增强超声造影(contrast-enhanced ultrasound, CEUS)动态显示病灶及组织器官内超声微泡对比剂填充过程的分析技术,可定量分析肌瘤内超声微泡的浓度、滞留时间及廓清速度[5]。DVP 联合六氟化硫微泡(声诺维,SonoVue)有望进一步提高HIFU 消融疗效、工作效率及安全性。本文旨在探讨DVP 指导下声诺维联合HIFU 消融富血供子宫肌瘤的增效作用及安全性。
1 材料与方法
1.1 材料
本文分别回顾性收集了2014 年7 月至2016 年10 月于昆明医科大学第一附属医院36 例患者(仅采用声诺维进行术前评估和术后疗效评价,即治疗过程中未使用声诺维)作为空白对照(对照组);前瞻性收集了60 例富血供子宫肌瘤患者(术前肌瘤MRI 增强扫描呈明显强化,即肌瘤强化程度高于正常子宫肌层的强化程度),并根据随机数字表随机分两组,其中32 例为非DVP 增效组(非DVP 组),在声诺维推注后1min 接受HIFU 治疗;28 例为DVP组,在DVP 指导下选择最佳时机行HIFU 消融治疗。
1.2 方法
1.2.1 HIFU 消融 患者在镇静镇痛下,采用JC200聚焦超声肿瘤治疗系统(重庆海扶科技有限公司)。DVP 组治疗前将监控超声探头调整至肌瘤最大层面至造影状态,经手背静脉团注法快速注射1.5 mL声诺维,再用5 mL 0.9%NaCl 溶液冲洗静脉通道,保持超声探头不动,直至微泡对比剂完全廓清,然后将造影动态图像传输至SonoLiverCAP 软件进行分析,获得声诺维在肌瘤内及肌层的时间强度曲线(time intensity cures,TIC),进一步处理病灶与周围组织的增强水平得到DVP。DVP 组患者在DVP 指导下,当肌瘤内声诺维处于上升时间或达到高峰且周围正常组织处于廓清时段时开始HIFU 消融,当声诺维在体内完全代谢完(8 min),再次同等剂量推注声诺维,随后相同间隔时间开始HIFU 消融,共推注4次,总剂量为6 mL,待消融满意结束手术。 非DVP组患者在静脉推注1.5 mL 声诺维后1 min 开始行HIFU 治疗,待声诺维代谢完后继续推注声诺维间隔1 min 继续消融,直到肌瘤内出现大片状团块状灰度变化,造影明确后结束手术。对照组患者第一次推注声诺维后待其完全廓清后开始消融,治疗过程中不使用声诺维,待造影明确消融效果后结束手术。记录HIFU 治疗参数,包括手术时间(min)、灰度变化时间(s)、超声辐照时间(s)。治疗剂量(J)=超声辐照时间(s)×治疗功率(W)。
1.2.2 MRI 扫描 MRI 检查采用Achieva 3.0T 成像仪(Philips 公司,荷兰)及HD×t 3.0T 成像仪(GE公司,美国)。根据术前盆腔MRI,记录基线数据:子宫位置(前位、中位、后位)、肌瘤的位置(前壁、后壁、侧壁、宫底)、肌瘤类型(肌壁间、浆膜下、黏膜下)、肌瘤T2WI[6-7]:低信号(信号强度与骨骼肌相似);等信号(信号强度高于骨骼肌但是低于子宫肌层);混杂信号(肌瘤内混有2 种或2 种以上的信号类型);高信号(肌瘤信号相似或高于子宫肌层)。基于MRI-T2WI 分别测量肌瘤的3 个径线,即上下径(D1)、前后径(D2)、左右径(D3)。对于多发性子宫肌瘤,计算最大子宫肌瘤体积。计数直径大于2 cm 的肌瘤。
1.2.3 术后随访 术后3 d 在增强MRI 的失状位、冠状位及横断位采用同样的测量方法测量肌瘤内无灌注区(non-perfused volume, NPV) 的3 条径线(D1、D2、D3)。并采用椭圆的计算公式计算肌瘤体积(V)、无 灌 注 区 体 积(NPV),V=4π/3×(D1×D2×D3)。计算肌瘤消融率=NPV/V×100%。依 据 能 效 因 子EEF=η .Pt/V(J/mm3),η 为0.7,Pt 为治疗能量(J),P 为治疗功率,t 为超声辐照时间,算出能效因子;治疗效率(mm3/s)=NPV/超声辐照时间。术后6 个月复查MRI,测量计算出子宫肌瘤缩小率。
1.3 疗效及安全性评价
1.3.1 症状评价 月经量改善率:HIFU 术后月经量情况日记卡计分与术前相比的减少值占术前计分的比例[8]。生命质量评价:采用UFS-QOL 评分表。
1.3.2 临床疗效评价 HIFU 治疗后6 个月疗效评价标准:显效,指月经量较基线减少≥50%,且肌瘤体积缩小≥50%;有效,指月经量较基线减少≥50%,且肌瘤体积缩小≥20%;无效,指月经量较基线减少<50%,或肌瘤体积缩小<20%。 临床有效率=显效率+有效率
1.3.3 安全性评价 参照国际介入放射治疗协会(Society of Interventional Radiology, SIR)并发症分类标准[9]进行分级:①A 级,无需治疗,无不良后果;②B 级,无不良后果,仅需临床观察;③C 级,需要治疗,住院时间<48 h;④D 级,需要进一步治疗,包括意外增加护理水平或延长住院时间(>48 h);⑤E级,永久性不良后遗症;⑥F 级,死亡
1.3 统计学方法
所有数据使用SPSS 17.0(IBM, Amonk, NY)统计软件进行分析,采用双侧检验,P<0.05 为差异有统计学意义。计量资料服从正态分布采用均数±标准差(±s) 表示,组间比较采用单因素方差分析,两两比较采用LSD-t 检验。计数资料用频数、频率表述,组间比较采用行×列表χ2检验。临床疗效评估为等级资料用秩和检验。
2 结果
2.1 患者一般情况
表1 可见所有患者的基线资料,3 组间比较差异无统计学意义(P>0.05)。
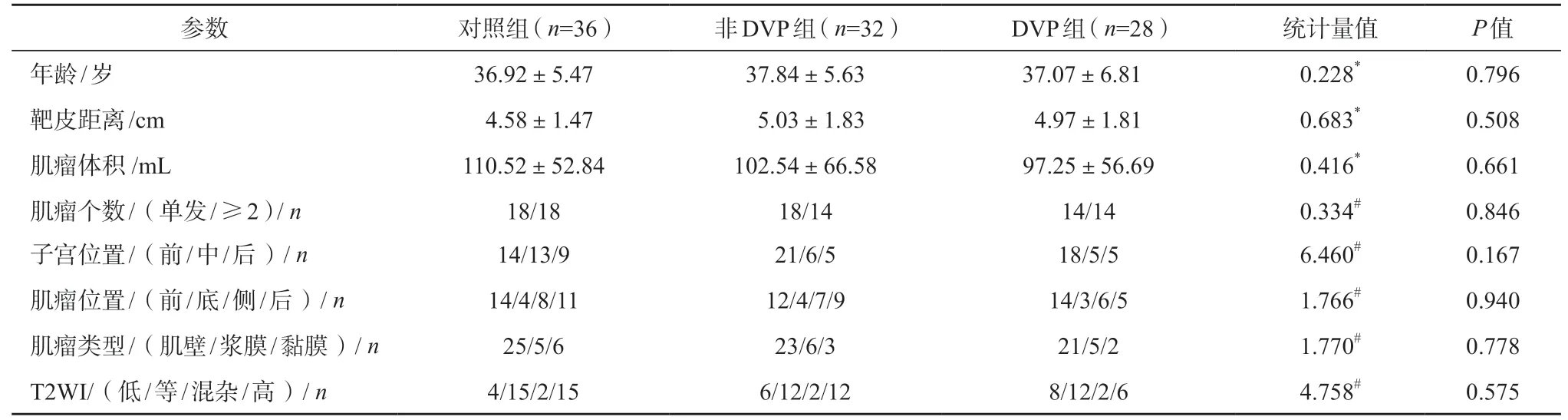
表1 3 组患者基线数据
2.2 治疗情况
消融率、EEF、治疗效率、治疗剂量、NPV 等治疗参数组间比较差异有统计学意义(P 均<0.05);而超声辐照时间、治疗时间、灰度变化时间、治疗功率3 组间比较差异无统计学意义(P 均>0.05),对照组治疗过程中不使用声诺维, 声诺维使用量在非DVP 组和DVP 组间比较差异无统计学意义(P >0.05)见表2。

表2 治疗参数比较
将单因素方差分析有统计学意义的治疗参数采用LSD-t 检验进行两两比较(见表3),DVP 组比对照组:消融率、EEF、治疗效率、治疗剂量和NPV 组间比较差异有统计学意义(P 均<0.05);DVP 组比非DVP 组:消融率、EEF、治疗效率组间比较差异有统计学意义(P 均<0.05),而治疗剂量和NPV 组间比较差异无统计学意义(P 均>0.05);非DVP 组比对照组:EEF、NPV 两组间比较差异有统计学意义(P 均<0.05),而消融率、治疗效率和治疗剂量组间比较差异无统计学意义(P 均>0.05)。
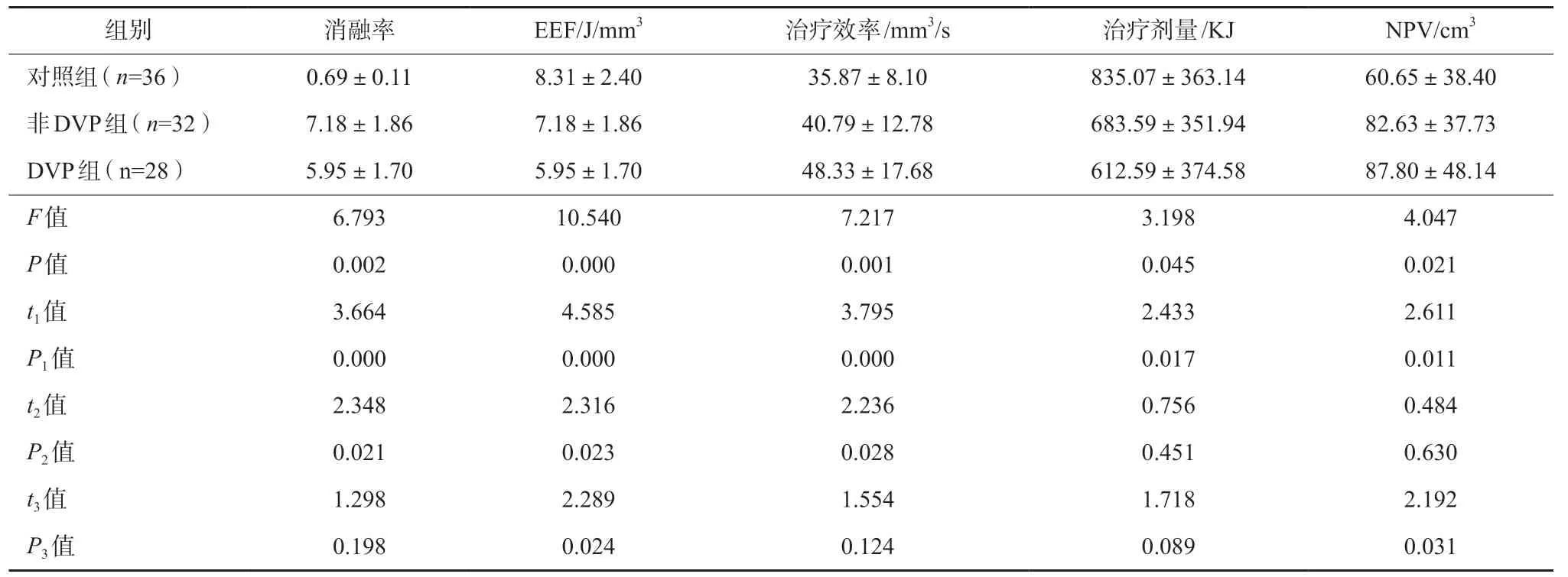
表3 采用LSD-t 进行两两比较的结果
2.3 随访
6 个月随访是3 组患者的症状评分、UFS-QOL子量表评分及月经评分与基线平均值相比较有显著统计学差异(P<0.001)。基线平均值进行两两比较,差异均无统计学意义(P>0.05)。6 个月随访,DVP 组与对照组比较,症状评分、生活质量评分、月经量评分及子宫肌瘤体积缩小率均有显著差异(P <0.001);DVP 组与非DVP 组、非DVP 组与对照组比较,症状评分、生活质量评分、月经评分及子宫肌瘤体积缩小率均有差异(P<0.05)(表4)。
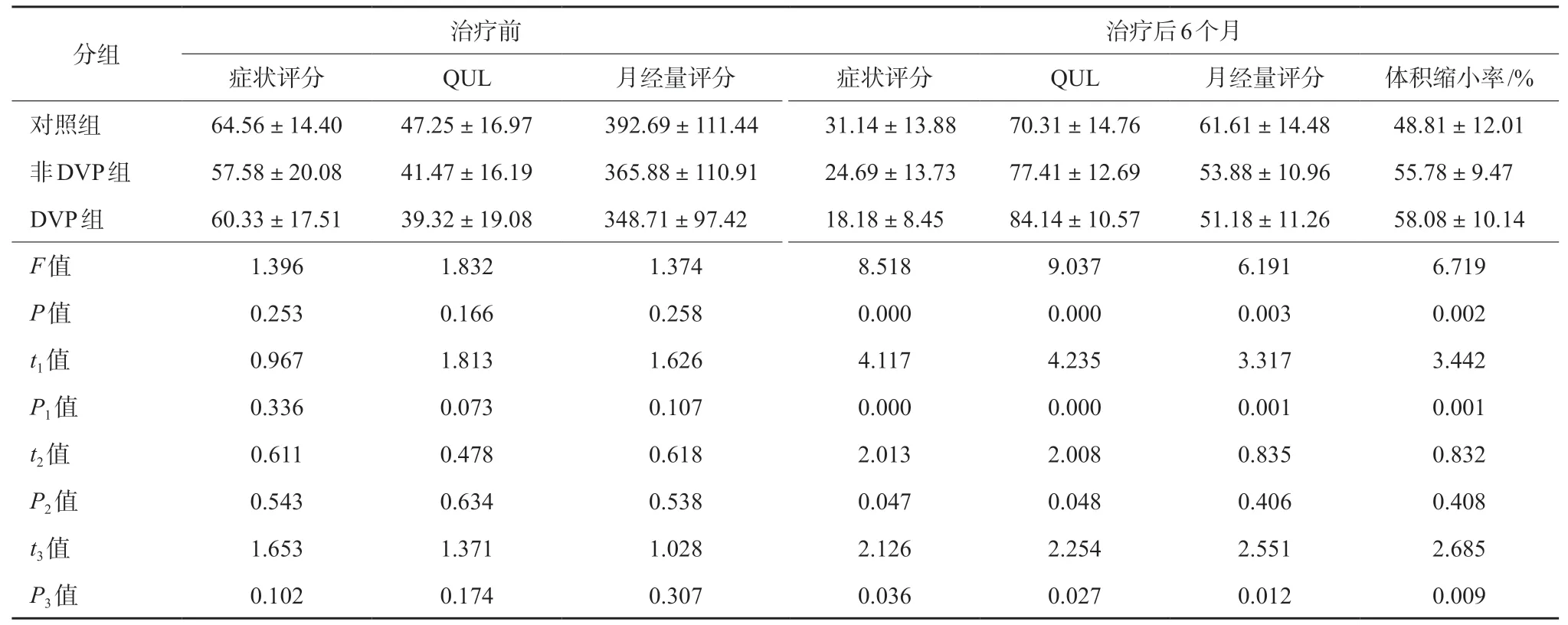
表4 治疗前和治疗后6 个月各临床症状评分比较
2.4 临床疗效评估
3 组HIFU 治 疗 后6 个 月 疗 效 评 价 采 用Kruskal-Wallis 秩和检验,结果见表5。显效41 例(42.7%),有效42 例(43.8%),无效13 例(13.4%),临床有效率83(85.6%),3 组间比较差异无统计学意义(P >0.05)。

表5 各组HIFU 治疗后6 个月临床疗效评价
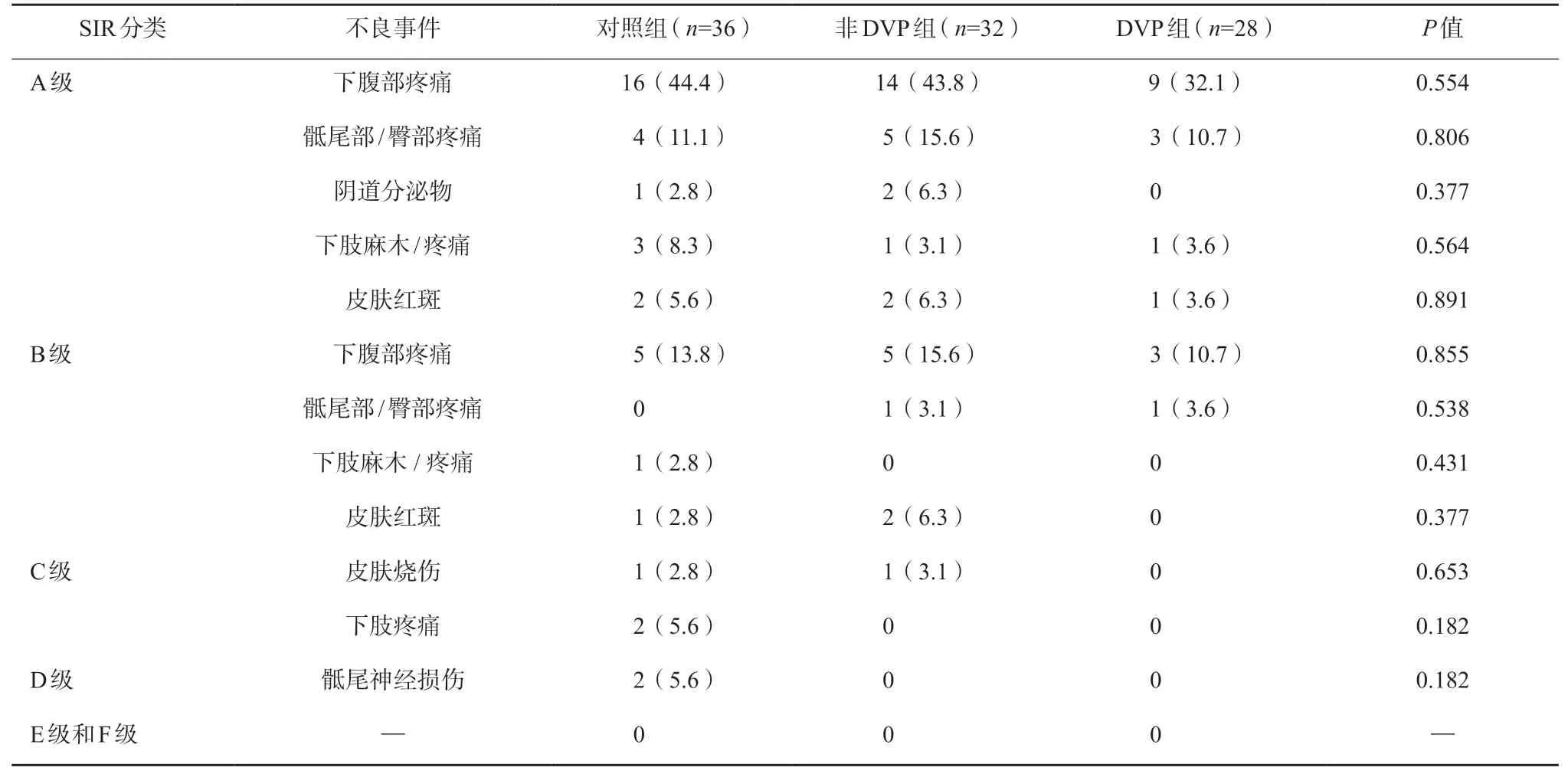
表6 HIFU 术后不良事件n(%)
2.5 不良事件
按照表6 所示的SIR 分类,共有47 例(48.5%),归为A 类17 例(17.5%),归 为B 类4 例(4.1%),归为C 类2 例(2.1%)归为D 类。未发生E 类或F 类不良事件。在A 类不良事件中,主要是下腹痛(40.2%)所有这些不良事件在HIFU 消融后3 天内自行恢复,未经任何治疗。在B 类不良事件中,13.4%患者有下腹痛。骶骨/臀部疼痛的患者在非DVP 组和DVP 组中分别有1 例,对照组中出现1 例腿部麻木和疼痛,共有3 例患者出现皮肤红斑。所有B 类不良事件患者仅住院观察,未经任何治疗痊愈。在C 类不良事件中,2 例患者出现皮肤烧伤(1 例浅Ⅱ度,创面经清洁换药处理后再生修复;I 例深Ⅱ度,经外科切除创面融合修复)。在D 类不良事件中,2例患者出现坐骨神经损伤,并且在NSAID 治疗3 个月后出现症状缓解。两组患者术后不良事件无统计学差异(P >0.05)。
3 讨 论
本研究通过对3 组患者在治疗过程中的EEF、治疗效率、治疗剂量、超声辐照时间、超声灰度变化时间、治疗时间、消融率及NPV 等治疗参数进行比较,结果显示,DVP 组的消融率、治疗效率均明显高于非DVP 组和对照组,而EEF 和治疗剂量均明显低于非DVP 组和对照组;其次DVP 组的消融率、EEF 及消融效率均高于非DVP 组。可较容易看出,声诺维可提高HIFU 治疗子宫肌瘤的疗效,且DVP的应用可进一步提高HIFU 治疗的增效作用。本研究与Peng 等[3]研究的结果一致,治疗过程中应用声诺维可显著提高消融率和治疗效率。而本研究中治疗时间、超声辐照时间及灰度变化,组间无明显差异,可能是因为在DVP 生成的过程中增加了总治疗时间。超声灰度变化尚无统一的标准,且仍有20%的肿瘤并不存在灰度变化[10]。故需要进一步优化HIFU 术前肌瘤造影分析流程,缩短总治疗时间。
Cheng 等[10]回顾性分析了2 604 例接受 HIFU治疗的子宫肌瘤患者,其中1300 例患者在治疗过程中使用了声诺维,结果发现 HIFU 治疗过程中,下肢疼痛、骶部/臀部疼痛、腹股沟区疼痛、治疗区域疼痛和皮肤不适热感的发生率比未使用组更高;在术后不良反应中,下腹痛的发病率在声诺维组为51.2%,显著高于未使用组的39.9%, 声诺维可能增加HIFU 治疗中一些常见 HIFU 相关不良反应的发生率,能导致靶组织以外的器官损伤,这可能与声诺维的不完全靶向运动和不同类型子宫肌瘤与周围组织血流灌注差异有关。富血供型肌瘤内声诺维浓度高、滞留时间长、廓清慢,而乏血供肌瘤内声诺维浓度较肌层低、滞留时间短、廓清快,而既往的研究并未对肌瘤进行分类研究,由此导致整体并发症高。因此采用声诺维在肌瘤内的定量分析技术,在DVP的指导下明确肌瘤内声诺维的浓聚时机,同时声诺维在周围组织中已完全廓清时进行HIFU 治疗,有望在确保安全性的前提下提高疗效。本研究结果显示DVP 联合声诺维可显著提高HIFU 治疗效率,降低EEF 和减少治疗剂量,同时DVP 联合声诺维未发生C~F 级不良事件,其不良事件主要为A 级和B 级,是常见的HIFU 治疗并发症,且相较于单纯声诺维治疗组和空白对照组,A 级和B 级不良事件发生率较低。与程重庆[11]研究相比较,本研究采用既往研究得出的最佳消融时机(声诺维引入后1 min开始消融)为对照,得出了DVP 联合声诺维可有效地增强消融疗效,同时降低不良反应的发生。
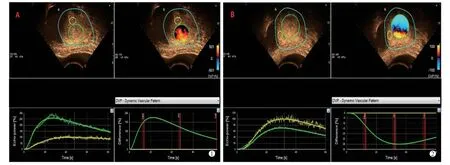
图1 不同血供子宫肌瘤的DVP 曲线图
子宫肌瘤患者中近50%有不同程度的临床症状,严重影响患病女性的身体、心理、社会和经济等方面的生活质量。如果患者接受治疗后月经量减少,个人的生活质量感知得到改善,则视治疗手段较为理想。Gizzo 等[12]研究使用UFS-QOL 问卷来测量症状缓解,结果发现HIFU 消融术后NPV 比率越大,症状缓解越明显,二者间存在显著的相关性,通过长期随访发现,肌瘤再干预率较低。Mindjuk等[13]对单中心的252 例患者进行了研究,结果发现在NPV 比率为80%或更高时,子宫肌瘤体积减少较为显著,从而达到良好的临床效果。 本研究采用DVP 联合声诺维消融技术治疗子宫肌瘤的临床有效率是通过术后NPV、6 个月的临床症状和肌瘤的缩小情况综合评估,其中NPV 和肌瘤的缩小率是基于MRI 成像测量计算得出的评价指标,是客观、定量的预测因子。在该研究中,平均NPV 为(75.01±42.67) cm3, 6 个月的平均肌瘤体积减少为(53.85±11.32)%。治疗后患者的症状评分、UFSQOL 子量表评分及月经评分显著改善,其中DVP 联合声诺维治疗组的临床有效率改善较显著。分析其原因可能是:DVP 曲线联合声诺维治疗组利用动态血管模型显示肌瘤内声诺维的填充过程,根据DVP 的定量分析(见图1),当肌瘤内声诺维浓度最高时进行HIFU 消融,最大程度发挥微泡的热效应及空化效应,进而使更多靶区内的微泡经历快速振荡、剧烈坍塌,同时伴随着气泡破坏和碎裂,以增强靶区热能沉积破坏肿瘤细胞。因此DVP 联合声诺维消融子宫肌瘤可最大程度提高其消融率,降低了肌瘤的复发,以增强HIFU 治疗的临床疗效。
