银耳多糖醇沉级分对酪氨酸酶的抑制作用
2020-04-03杨芳王艺涵袁辛锐迟原龙姚开贾冬英
杨芳,王艺涵,袁辛锐,迟原龙,姚开,贾冬英*
1. 四川大学轻工科学与工程学院(成都 610065);2. 四川白家食品产业有限公司(成都 610065)
酪氨酸酶是含铜的氧化还原酶,广泛分布于生物体中,具有双重催化活性,既可催化L-酪氨酸羟基化生成L-多巴,也可将L-多巴氧化生成多巴醌,后者进一步氧化聚合形成黑色素[1],是参与人体皮肤黑色素形成的关键酶。抑制酪氨酸酶活性可减少体内黑色素和色斑的生成,从而起到美白祛斑的作用[2-3]。从天然食材中提取分离得到安全、高效的酪氨酸酶抑制剂已成为目前研究热点[4]。研究表明,某些植物多糖对酪氨酸酶活性具有一定抑制作用。Yang等[5]发现,龙眼果皮多糖具有良好的酪氨酸酶抑制活性,能够抑制L-酪氨酸生成L-多巴;Tang等[6]研究显示,板栗多糖可抑制酪氨酸酶活性,该抑制作用属于竞争性抑制。
银耳俗称白木耳、雪耳,自古以来就是女性美容养颜佳品。多糖是银耳的主要活性物质,具有增强免疫力、抗氧化、抗衰老、抗肿瘤、抗炎、修复记忆障碍等生物活性[7-9]。来吉祥等[10]发现,银耳多糖具有优良的保湿功效,用于化妆品中可减轻皮肤粗糙度,增强皮肤弹性。刘卉[11]研究显示,化妆品中以0.05%银耳多糖替代0.02%透明质酸能达到更好的保湿效果。然而,关于银耳多糖对酪氨酸酶的抑制作用却鲜有报道。基于此,试验比较不同银耳多糖醇沉级分对酪氨酸酶的抑制作用,探讨其对酪氨酸酶的抑制作用类型,以期为银耳多糖在化妆品中的高附加值利用提供理论依据。
1 材料与方法
1.1 材料与试剂
福建古田银耳(市售)。
酪氨酸酶(730 U/mg)、L-酪氨酸、L-多巴(上海源叶生物科技有限公司);1, 1-二苯基-2-三硝基苯肼(DPPH)、葡聚糖系列标准品(2.5~5 348 kDa,色谱纯试剂)(美国Sigma公司)。
1.2 仪器与设备
SNB-2数字黏度计(上海精天仪器有限公司);UV6000PC-1100型紫外可见分光光度计(上海元析仪器有限公司);Spectra Max 190全波长酶标仪(美国Molecular Devices公司);Waters Breeze GPC凝胶渗透色谱仪(美国沃特斯有限公司)。
1.3 试验方法
1.3.1 银耳多糖分步醇沉级分的制备与纯化
1.3.1.1 银耳多糖分步醇沉级分的制备
参考高温高压法[12]提取银耳多糖,并稍作修改。称取一定质量的干银耳,加入其60倍质量的饮用纯净水,浸泡20 min后打浆,将所得浆液于0.1 MPa、121℃下加压提取30 min,离心后得到上清液,于60 ℃下真空浓缩使其黏度达到3.4±0.1 Pa/s(25 ℃,转子#4,60 r/min),得到浓缩液。
在浓缩液中加入无水乙醇使体系乙醇体积分数达20%,搅拌后于4 ℃下静置24 h,离心后分别收集沉淀物与上清液;将所得沉淀物用无水乙醇及丙酮洗涤、抽滤后进行真空冷冻干燥,得到银耳多糖醇沉级分STP 20。将所得的上清液真空浓缩至上述黏度,加入无水乙醇调整体系乙醇体积分数40%,搅拌后按照上述方法进行静置沉淀和离心、洗涤、抽滤、干燥得到STP 40。将所得上清液按照上述方法依次调整体系的乙醇体积分数分别达到60%,80%得到银耳多糖级分STP 60、STP 80。将得到的4种银耳多糖级分称质量后按照式(1)计算其得率。

式中:m为干燥多糖级分质量,g;M为干银耳质量,g。
1.3.1.2 银耳多糖醇沉级分STP 60的纯化
采用DEAE-Cellulose 52柱层析,湿法装柱(Φ2×30 cm)。配制10 mg/mL的STP 60水溶液,以0.4 mL/min流速上样10 mL后先用多于1倍柱体积的去离子水洗脱,依次用0.2,0.4和0.6 mol/L的NaCl溶液进行梯度洗脱,每10 min收集1管;隔管取0.5 mL,用苯酚-硫酸法检测其多糖含量,绘制洗脱曲线;收集同一洗脱峰溶液,经透析、浓缩、冻干后得到纯化STP 60。
1.3.2 银耳多糖醇沉级分纯度测定
以葡萄糖溶液为标准品,苯酚-硫酸法[13]测定其在不同质量浓度下反应液的吸光度,以浓度为横坐标、吸光度为纵坐标绘制标准曲线,进行线性回归后得到回归方程y=0.008 1x-0.010 6(R2=0.999 1)。按照同样方法测定4种银耳多糖醇沉级分溶液的吸光度,将其代入回归方程后计算出多糖样品的纯度。
1.3.3 银耳多糖醇沉级分的相对分子质量与纯化STP 60的单糖组成分析
1.3.3.1 醇沉级分的相对分子质量测定
参照Mao等[14]所述凝胶渗透色谱法测定银耳多糖级分的相对分子质量。GPC色谱条件:色谱柱为Ultrahyrogel linear(7.8 mm×300 mm),检测器为2400示差折光检测器,柱温40 ℃,流动相为0.2 mol/L NaNO3溶液,pH 6.0,流速0.6 mL/min,对照品为窄分布的葡聚糖。
1.3.3.2 纯化STP 60的单糖组成分析
参考Dai等[15]所述的3-甲基-1-苯基-5-吡唑啉酮(PMP)柱前衍生HPLC法,测定纯化STP 60的单糖组成。以鼠李糖、岩藻糖、核糖、阿拉伯糖、木糖、甘露糖、葡萄糖醛酸、葡萄糖、半乳糖和半乳糖醛酸为对照品。
HPLC条件:色谱柱为SHISEIDO C18柱(4.6 mm×250 mm,5 μm)、柱温25 ℃、流动相为0.1 mol/L磷酸缓冲液(pH 6.8)和乙腈混合液(82︰18,V/V)、流速1.0 mL/min、检测波长245 nm。
1.3.4 银耳多糖对酪氨酸酶的抑制作用
1.3.4.1 对酪氨酸酶单酚酶的抑制作用
参考Maisuthisakul等[16]方法,并稍作修改。将90 μL磷酸盐缓冲溶液(PBS,pH 6.8)和50 μL 100 μg/mL酪氨酸酶溶液依次加入到50 μL 1 mg/mL银耳多糖醇沉级分溶液中,混合均匀后于37 ℃下预热5 min,加入60 μL 2.5 mmol/L的L-酪氨酸溶液,混匀后于该温度下保持10 min,振荡后立即于490 nm处测定反应液的吸光度。以维生素C作为阳性对照,每一样品重复测定3次。按照以式(2)计算样品对酪氨酸酶单酚酶的抑制作用。
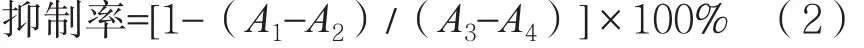
式中:A1、A2、A3、A4分别是样品组、样品背景组(PBS代替酪氨酸酶)、空白组(蒸馏水代替样品)、空白背景组(蒸馏水代替样品、PBS代替酪氨酸酶)的吸光度。
1.3.4.2 对酪氨酸酶双酚酶的抑制作用
参照上述单酚酶抑制作用步骤,以2.5 mmol/L L-多巴溶液替代2.5 mmol/L L-酪氨酸溶液,于37 ℃下继续保持2 min,振荡后立即于490 nm处测定吸光度。按照式(2)计算样品对酪氨酸酶双酚酶抑制率。
1.3.5 银耳多糖STP 60对酪氨酸酶单酚酶的抑制作用类型与动力学分析
1.3.5.1 抑制作用类型分析
固定底物L-酪氨酸溶液浓度2.5 mmol/L,改变酪氨酸酶浓度,测定4种质量浓度STP 60时的酶活力,以酪氨酸酶浓度为横坐标、酪氨酸酶活力为纵坐标作图,根据二者的关系判断STP 60对该酶的抑制作用[17]。
1.3.5.2 抑制作用动力学分析
固定酪氨酸酶质量浓度为100 μ g/mL,改变底物L-酪氨酸浓度,测定4种质量浓度STP 60时的酶活力,根据Lineweaver-Burk法绘制底物浓度与酶反应速率的双倒数图,分析STP 60对酪氨酸单酚酶的动力学[18]。
1.3.6 数据分析
除分子量外,其余试验结果均以均数±标准差表示,采用OriginPro 2017绘图,采用SPSS 21.0进行统计分析。
2 结果与分析
2.1 银耳多糖醇沉级分的得率和纯度及相对分子质量与单糖组成
4种银耳多糖醇沉级分的得率、纯度及分子量见表1。4种银耳多糖级分的得率和纯度差异显著,以STP 60为最高,表明银耳多糖主要是由STP 60为代表的中分子量多糖构成。随着醇沉时乙醇体积浓度增大,银耳多糖级分的重均分子量和数均分子量逐渐减小,但均在同一数量级;4种级分的多分散系数远大于1,表明其分子量分布范围较广,以STP 60最为明显。

表1 银耳多糖分步醇沉级分的得率和纯度与相对分子质量
纯化STP 60经PMP柱前衍生后的HPLC检测图谱如图1所示。STP 60是由甘露糖、岩藻糖、木糖、葡萄糖醛酸、葡萄糖、半乳糖、阿拉伯糖、鼠李糖、核糖和半乳糖醛酸组成,其摩尔比为871.72︰323.94︰251︰218.03︰15.51︰3.95︰2.01︰1.66︰1.03︰0.74。银耳多糖的单糖组成以甘露糖、岩藻糖、木糖和葡萄糖醛酸为主,甘露糖含量最高,因此STP 60可能是以甘露聚糖为主链的酸性杂多糖。试验结果与Ukai等[19]得到的银耳子实体多糖的单糖组成相似,但其含量差异较大,尤其是岩藻糖的含量明显偏高,这可能与银耳的产地、栽培方式及多糖的提取方法有关。
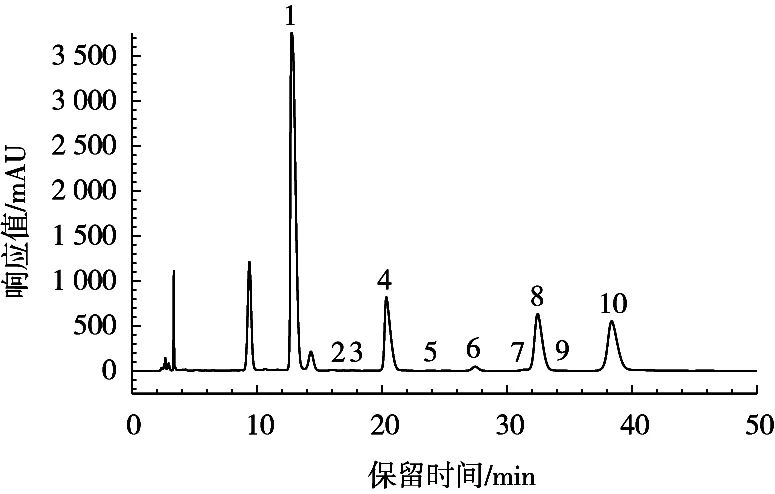
图1 纯化STP 60的HPLC色谱图
2.2 银耳多糖对酪氨酸酶的抑制作用
4种银耳多糖级分对酪氨酸酶单酚酶和双酚酶的抑制作用如图2所示。它们对酪氨酸酶均有一定抑制作用,其对单酚酶活性的抑制作用明显强于双酚酶,其中STP 60的抑制作用最大,STP 20的抑制作用最小。4种级分的抑制作用与其纯度呈正相关,纯度越高,其抑制作用越大。纯度最高的STP 60在质量浓度为1 mg/mL的条件下,对单酚酶和双酚酶的抑制率分别为37.55%和9.94%,其抑制作用明显高于羊栖菜多糖[20]和板栗多糖[6]。然而,银耳多糖级分对酪氨酸酶的抑制作用明显低于维生素C,这主要是因为后者既是一种强抗氧化剂,也是一种金属离子螯合剂,它可以通过强大的抗氧化和螯合铜离子2种途径产生明显的抑酶作用。
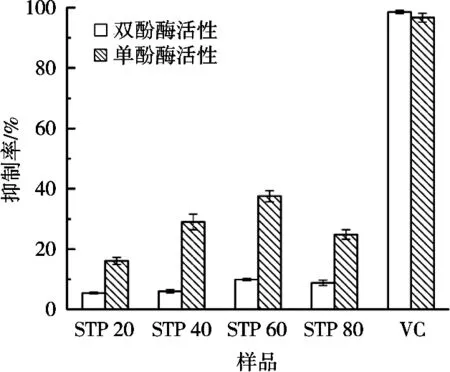
图2 银耳多糖级分对酪氨酸酶的抑制作用
2.3 STP 60对酪氨酸单酚酶的抑制作用类型与抑制动力学
抑制剂对酶活性的抑制作用分为可逆抑制和不可逆抑制。利用酶活性与酶的关系图区分可逆抑制剂和不可逆抑制,直线过原点为可逆抑制,直线平行则为不可逆抑制。在酶活测定体系中,加入不同质量浓度的STP 60,以酪氨酸酶浓度为横坐标、酶活力为纵坐标作图,得到二者之间的关系,如图3所示。可以看出,4条直线均通过原点,且随着STP 60浓度增大,直线斜率变小,说明STP 60对酪氨酸酶的抑制作用具有可逆性,与酶之间以非共价键发生可逆结合[16],不会使酪氨酸酶永久失活。
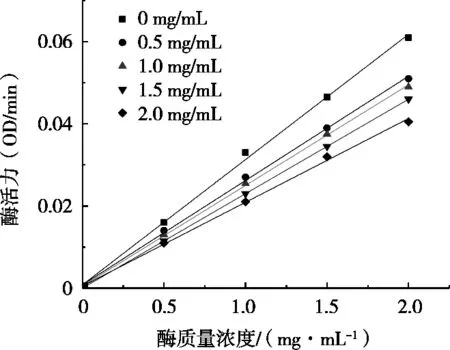
图3 酪氨酸酶单酚酶活性与酶浓度的关系
图4 为4种质量浓度的STP 60对酪氨酸酶单酚酶活性的Lineweaver-Burk双倒数图。4条直线均相交于第二象限X轴上一点,随着STP 60浓度增大,直线与纵坐标截距增大,也就是说,随着STP 60浓度增加,米氏常数Km保持不变,最大反应初速度Vmax逐渐减小。参数变化表明,STP 60对酪氨酸酶的抑制作用为非竞争性抑制,即底物、抑制剂和酶之间的结合无竞争性。因此,STP 60对酪氨酸酶的抑制作用为非竞争性可逆抑制,这一结果与Yang等[5]关于龙眼皮多糖的研究结果一致。对酪氨酸酶而言,其非竞争性抑制剂通常是由于结合酶活性中心以外的残基而影响了酶活性,也可能是由于抑制剂对氧自由基的清除作用阻碍酶催化反应[4]。
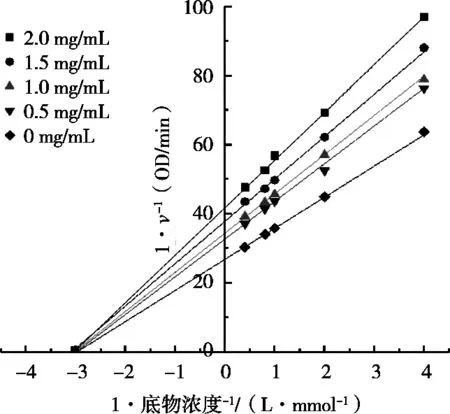
图4 STP 60对酪氨酸酶单酚酶活性的Lineweaver-Burk双倒数图
3 结论
4种银耳多糖醇沉级分对酪氨酸酶的单酚酶活性和双酚酶活性均具有一定抑制作用,且对单酚酶活性的抑制作用明显强于双酚酶活性抑制,其中STP 60对单酚酶活性的抑制作用最大,属于非竞争性可逆抑制。有关银耳多糖对此酶的抑制作用机理有待深入探讨。
