特发性扩张型心肌病患者左心室逆重构的发生率、预测因素和预后分析
2020-03-31牛保松慕春言赵玉兰侯爱琴
牛保松 慕春言 赵玉兰 侯爱琴
454001 焦作市第二人民医院心血管内科
左心室逆重构(left ventricular reverse remodeling, LVRR)的概念可以追溯到有关心肌成形术的研究[1],包括射血分数保留的心力衰竭LVRR和射血分数降低的心力衰竭LVRR。射血分数降低的心力衰竭是指心力衰竭患者的左心室射血分数(left ventricular ejection fraction,LVEF)或左心室缩短分数下降,伴或不伴左心室舒张末期内径(left ventricular end diastolic dimension,LVEDd)或容积增加[2],本文探讨的即是指射血分数降低的心力衰竭LVRR。一些能够提高患者生存率的药物(β受体阻滞剂、血管紧张素转换酶抑制剂/血管紧张素受体拮抗剂和螺内酯等)及介入或外科手术治疗均已被证实可促进LVRR,或可改善患者预后[3]。研究表明,LVRR与心力衰竭患者的预后改善相关[4-6]。不过,国内关于特发性扩张型心肌病LVRR的文献报道较少;再者,既往有关扩张型心肌病的研究通常包括了获得性扩张型心肌病如围生期心肌病和酒精性心肌病,而这些疾病的病理生理机制显然与特发性扩张型心肌病不同。因此,本研究旨在评估特发性扩张型心肌病患者的LVRR发生率,并探讨和分析其预测因素和预后情况。
1 对象和方法
1.1 研究对象
回顾性分析2014年1月至2017年5月于焦作市第二人民医院住院治疗的特发性扩张型心肌病患者305例,因病例资料重复、未能满足纳入标准、临床资料不全等,最终51例患者纳入研究,其中男性33例,女性18例,年龄29~83岁,平均(56.7±12.3)岁。纳入标准:依据中国2007年《心肌病诊断与治疗建议》中推荐的国人扩张型心肌病的诊断标准:(1)LVEDd>5.0 mm(女性)和>5.5 cm(男性);(2)LVEF<45%和(或)左心室缩短分数<25%;(3)LVEDd>2.7 cm/m2,体表面积(m2)=0.0061×身高(cm)+0.0128×体重(kg)-0.1529,同时伴有左室室壁运动弥漫性减低[7]。排除标准:任何引起心肌损害的其他疾病,如高血压性心脏病、缺血性心肌病、围生期心肌病等;已行心脏再同步化治疗、心室成形术、左心室辅助装置和心脏移植的患者。本研究经医院医学伦理委员会批准,所有患者均签署知情同意书。
1.2 研究方法
1.2.1 资料收集 收集患者入院时的一般临床资料,包括纽约心脏病协会(NYHA)心功能分级、N末端B型利钠肽原(N-terminal pro B-type natriuretic peptide,NT-proBNP)等。
1.2.2 超声心动图检查 所有患者于首次住院和再次住院或门诊复查时接受标准的经胸超声心动图检查,采用M-法经胸骨旁长轴平面测量LVEDd,Simpson法计算LVEF[8],评估患者的左心室结构和功能。
1.2.3 抗心力衰竭治疗 所有患者接受标准的抗心力衰竭治疗,包括β受体阻滞剂、血管紧张素转换酶抑制剂或血管紧张素受体拮抗剂、螺内酯、利尿剂;并根据心率、血压、肾功能、电解质等,调整患者药物种类及剂量。
1.2.4 随访计划 入选患者从2014年1月开始通过门诊或电话随访,每3~6个月复查超声心动图;随访终点为患者任何原因死亡或因心力衰竭恶化再次住院,截止时间2017年5月。
1.2.5 LVRR的判断 以首次住院超声心动图LVEF为基础,以末次复查时(截止时间之前)LVEF绝对值增加10%以上为LVRR组,绝对值增加低于10%为非LVRR组(NLVRR组);不包含LVEDd的数据。
1.3 统计学方法
2 结果
2.1 一般临床资料
51例特发性扩张型心肌病患者中26例发生LVRR,发生率为51.0%,平均随访(13.1±11.3)个月。
LVRR组患者的首次LVEDd略高于NLVRR组,末次LVEDd略低于NLVRR组,提示LVRR患者的LVEDd有减小趋势。两组比较,LVEF、住院次数和死亡病例的差异均有统计学意义,见表1。
2.2 单变量和多变量logistic回归分析
经logistic回归分析显示,特发性扩张型心肌病LVRR的预测因素为心力衰竭病史小于1年(OR=0.065,95%CI:0.007~0.0562,P=0.013)和首次LVEF≥35%(OR=23.457,95%CI:2.687~204.770,P=0.004),见表2。
2.3 预后分析
至2017年5月随访结束时,共有4例失访(两组各2例),11例死亡(LVRR组3例,NLVRR组8例),死亡原因包括猝死、心力衰竭恶化、恶性心律失常。Kaplan-Meier生存曲线显示,LVRR组预后(95%CI:96.442~120.323)优于NLVRR组(95%CI:69.909~98.364),P=0.017,见图1。

表1 两组一般临床资料比较
注:a为LVRR组与NLVRR组比较
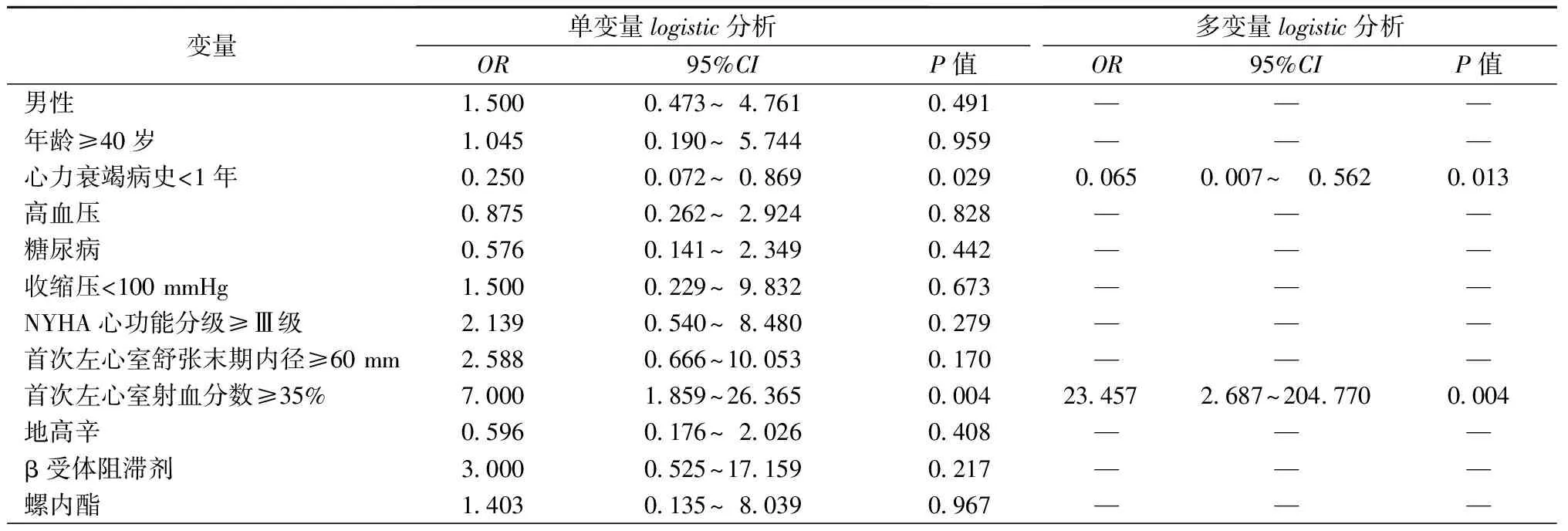
表2 特发性扩张型心肌病患者LVRR预测因素的logistic回归分析

图1 两组患者的Kaplan-Meier生存曲线
3 讨论
基于患者超声心动图LVEDd测量偏差大,与临床症状匹配度差,本研究中LVRR定义为复查LVEF绝对值增加至少10%,而不包含LVEDd的变化,与既往研究有所不同:Banno等[9]的研究中LVRR的诊断标准为LVEDd缩小至少15%,LVEF增加至少25%;还有的研究中LVRR标准为既有左心室收缩期内径和舒张期内径变化的指标,还有LVEF和左心室重构指数变化的指标[10-12]。
在本研究中,特发性扩张型心肌病LVRR的发生率为51.0%,与大多数既往研究中LVRR的发生率为50%~60%基本一致[10, 13-16]。
就形成LVRR的时间而言,Banno等[9]以400 d为分界,400 d以内形成LVRR为早期LVRR,超过400 d的LVRR则为晚期LVRR,研究显示早期LVRR较晚期LVRR有更好的预后。在Steimle等[17]的研究中,早期恢复的患者在随访(8.0±6.0)个月时LVEF明显改善。Kim等[18]的研究中,34例(占总例数的31.8%)左心室功能恢复正常的平均时间为(6.3±11.8)个月。本研究中,采用末次LVEF较首次绝对值增加10%以上定义LVRR形成,基于此,形成LVRR的时间为(11.0±6.8)个月,与上述研究中的早期LVRR类似。
既往多个研究提示,LVRR的预测因素包括女性、高血压、糖尿病、心肌病病因、无冠心病和慢性肾脏疾病、较高的NYHA心功能分级、无左束支传导阻滞、高水平的血清钠离子、较低的利钠肽水平、较高的LVEF、较低的LVEDd(基线时)和无二尖瓣反流、肺动脉高压[19-26]。而本研究显示,LVRR的预测因素为心力衰竭病史小于1年和首次LVEF≥35%,与既往研究不一致。考虑原因如下:心力衰竭时间长可以理解为左心室重构时间长,左心室心肌纤维化更明显,故短期内不易形成LVRR,或LVRR需要更长时间;而较高的基线LVEF,提示左心室收缩功能无明显下降,射血能力无明显下降,低血压相对更少,更易耐受血管紧张素转换酶抑制剂或血管紧张素受体拮抗剂和β受体阻滞剂,神经内分泌异常机制改善更明显,更易形成LVRR。
Kaplan-Meier生存分析结果表明,LVRR组患者的存活率优于NLVRR组,与既往研究一致。Steimle等[17]研究显示,新发扩张型心肌病伴LVRR患者的3年存活率显著优于慢性扩张型心肌病患者,而新发扩张型心肌病不伴LVRR患者的3年存活率明显低于前两者。Kawai等[10]发现,强化药物治疗2年达到LVRR的患者5年无心脏原因死亡的存活率及无事件率(死亡或心力衰竭恶化再入院)均优于NLVRR患者;两组心力衰竭恶化住院率比较,LVRR组的住院次数少于NLVRR组,提示LVRR是抗心力衰竭治疗有效的一个标志,可以减少住院次数,同时LVRR也是预测患者长期预后的一个指标。
本研究为回顾性研究,研究效力不及前瞻性研究;因未满足研究条件,最终入选的病例数偏少;LVRR的标准与既往文献不一致;存在失访病例,可能对研究结论有所影响。
利益冲突:无
