SiO2纳米孔对常见工业废气吸附的分子动力学研究
2020-02-18周春宇梁俊玺孙初锋
白 俊,周春宇,段 钰,谢 鑫,梁俊玺,孙初锋
(1.西北民族大学 化工学院,甘肃 兰州 730030;2.甘肃省高校环境友好型复合材料及生物质利用省级重点实验室,甘肃 兰州 730030)
通常来说纳米孔被定义为内径尺寸介于1~100 nm之间的微小孔洞[1]。纳米孔材料较好的稳定性和耐用性使得其在保证吸附剂严格温度、压力和其他化学条件下能够进行有效吸附,并且有较长的使用寿命和实用价值,这使得纳米孔材料吸附剂被广泛应用。稳定的反应条件、精确地合成方法以及成熟的纳米孔合成技术是制备高效的纳米孔材料的必备条件[2]。评判纳米孔材料的合成成功与否不仅要看合成的纳米孔材料是否具有高吸附量,其材料的稳定性也是纳米孔材料合成的一个重要条件[3-4]。
多孔材料近些年来非常受欢迎,目前被广泛应用于催化,吸附等领域[6-8]。在1992年首次报道合成MCM-41后,石英以其丰富的储量,二氧化硅多孔材料被认为是最有前景的吸附剂。一些专家研究了吸附具有不同几何形状的纳米二氧化硅材料中流体的结构和动力学[5],众所周知的是CO2在二氧化硅中的运移,这些研究为纳米过滤[9],分离[10]和催化等技术的应用提供了理论借鉴。这些研究为分子的捕获和储存提供了重要的依据,使人们清楚地认识到纳米孔内气体的行为与其吸附和扩散性质有关,而且二氧化硅中的选择性吸附仍有待进一步研究,这对于设计不同气体的吸附剂至关重要。
碳纳米管具有较高的气体吸附选择性。相比之下,二氧化硅纳米孔内气体的情况受到的关注较少,尤其是在单纯实验研究方面。近年来,通过计算机模拟研究了简单流体的动力学行为,发现在二氧化硅表面附近表现有CO2富集。显然,分子水平上的模拟为多孔二氧化硅的应用提供了一种补充实验的手段。最著名的例子是MCM-41,其具有有序的六面体结构,中孔的尺寸范围2~10 nm。它们可以表现出大的表面积(高达约1000 m2/g),大孔体积(接近1 cm3/g),孔径分散小,热稳定性高。纳米细化还导致吸收的分子的扩散率较低,其中在1 nm直径的孔中最为常见。
此外,Gadikota等人提出气体粘土表面的亲和力与吸附分子的大小有关。 在这些先前研究的推动下,在这项工作中,我们将展示分子动力学模拟的结果,该模拟揭示了限制在羟基化二氧化硅纳米孔内的不同气体的行为,来判断使用二氧化硅纳米孔作为气体的吸附剂是否合适。其中利用NVT系综分子动力学模拟和巨正则蒙特卡洛方法(GCMC),Bourg和Steefel等人分别在273 K,298 K和300 K进行模拟7种单组分气体分子在1nm直径的二氧化硅孔隙中的吸附。
通过对SiO2纳米孔对工业常见废气(CH4、CO2、SO2、NO2、CO、HF、H2S)的吸附模拟研究,为进一步揭示硅胶吸附剂的吸附机理以及应用于气体吸附方面的SiO2纳米新材料的生产应用提供了一定理论基础。
1 模拟计算方法
利用MS软件中COMPASS力场进行建模,利用温度等温线完成体系压力的确定。为了使模拟体系接近真实体系,模型的构建采用三维周期性边界条件,选取能量最低、体系最稳定的周期边界作为初始构型,对SiO2纳米孔模拟体系进行能量优化处理,使得体系达到平衡状态,最后对模拟体系吸附分子进行MSD和RDF模拟计算。本文中的所有的模拟操作全部在Materials Studio 6.0版本上进行。
2 模型构建与优化
首先建立七种工业污染气体(CH4、SO2、CO2、NO2、HF、H2S、CO)分子模型,然后建立SiO2吸附模型,通过系统导入SiO2分子模型,调整参数构建超晶胞,从SiO2纳米超晶胞中心删除一定孔径的原子,得到内径为1 nm的SiO2纳米孔。根据需要可在SiO2吸附模型中改变参数,得到1.5 nm和2 nm孔径的SiO2吸附模型。实验为了使结构达到最优化的构型,所有原子在能量最小化阶段保持松弛不被约束。其次对优化后的吸附系统进行分子动力学模拟,采用NVT系综,模拟运行时间为100 ps,时间步长为1 fs,每1 ps输出一次结果并保存所有构型,采用恒温器控制温度(298 K、323 K、273 K三个体系)。
3 实验现象分析
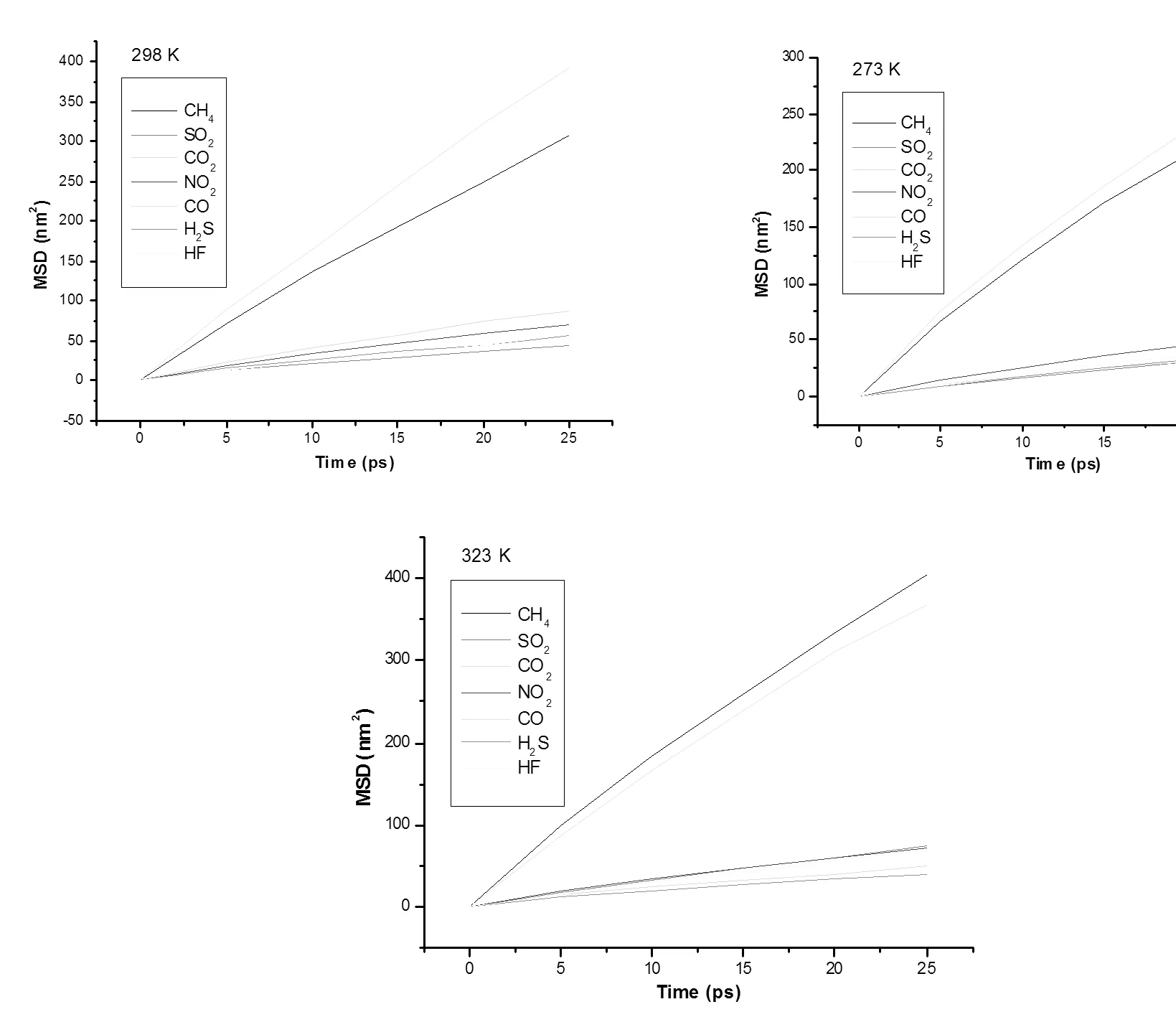
图1 在不同温度下给定气体的MSD与时间的关系
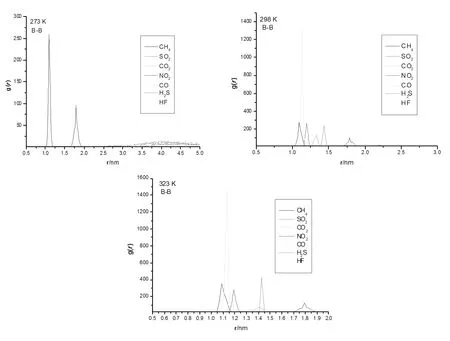
图2 在不同温度下给定气体分子的RDF图
为了提高计算效率,在分子动力学模拟阶段石英砂层被固定,这种处理方法是合理的,因为石英砂通常可以被作为理想的平面处理,最后对所得的模拟结果进行分析对比。
在吸附过程中,首先进行的是323 K,6000 kPa(通过温度等温线确定)、1 nm孔径等恒定参数的分子动力学模拟计算,以温度为323 K时SiO2纳米孔气体的吸附情况为例,我们发现CH4、CO的吸附状态是最完美的,基本吸附在SiO2纳米孔内壁周围;SO2、CO2吸附情况类似,除了在SiO2纳米孔内壁周围有大量分子,在空腔中也分布一些分子,但是相对于内壁周围分布的分子,空腔中分布的分子相对较少;从HF、H2S吸附构型中可以看到,HF分子除了在SiO2纳米孔内壁周围有部分分子外,SiO2纳米孔空腔中分布有大量分子,同时可以看到空腔中分子的数量明显比孔壁周围分布的分子数量多很多。
通过气体吸附的MSD和RDF 数据分析可以看到,吸附状态并不能完全说明气体的吸附能力,但是往往吸附状态最好的构型,其对应的气体吸附体系反映的吸附能力也是最强的。
4 实验结果与讨论
(1)在单组分气体吸附体系中,CH4和CO在SiO2纳米孔中吸附的分子数量是七个吸附体系中吸附数目最少的,即其吸附能力是最弱的。但两者在SiO2纳米孔中的吸附状态均为束缚态,其吸附状态是最好的。另外,对于SO2、CO2、H2S和HF四个吸附体系吸附状态类似,即其气体分子除在SiO2纳米孔内壁周围有大量分布外,在孔腔中也有一部分分布,其中HF的总分子吸附量很高,表现其孔对其具有最强的吸附能力。值得注意的是,在NO2吸附体系中,气体分子与SiO2纳米孔某侧具有非常强的相互作用力,导致其出现单侧吸附的特殊吸附现象。根据气体在SiO2纳米孔中吸附分子数量的多少,其被吸附能力的顺序可预测为:HF﹥CO2﹥H2S﹥NO2﹥SO2﹥CH4﹥CO。
(2)随着温度的变化,被研究气体在SiO2纳米孔中的扩散强度发生了变化,同时,其孔对气体的吸附能力及气体在其孔内的吸附状态也发生了变化。根据不同温度下气体在SiO2纳米孔中扩散速率以及在其孔中存在的分子数可以得到,吸附体系中气体的扩散能力及其孔对其的吸附能力与温度有关。CH4、SO2、NO2、HF吸附体系随着温度的升高而升高,其气体扩散能力增强,而对于CO2、CO、H2S吸附体系,其气体扩散能力先增后减。当对SiO2纳米孔对气体的吸附能力进行观察,CH4、HF、H2S吸附体系随着温度升高而升高,显示其吸附能力降低;NO2吸附体系,先降低后增加;CO2吸附体系,先增后减;SO2、CO吸附体系,吸附能力没有发生太大变化。值得注意的是随着温度的变化,NO2吸附体系出现了不同侧吸附的现象且吸附出现位置没有规律性,而在其他吸附体系中,气体的吸附状态在不同温度下没有发生太大的变化。
目前为止,仅仅针对CH4、SO2、CO2、NO2、HF、H2S、CO七种气体基于SiO2纳米孔的吸附情况进行了初步研究,总体来看,本研究尚且存在诸多不足之处,需要在后续工作中进一步完善,后续研究会探究压强、孔径接触面积以及尺寸等因素对吸附体系气体吸附的影响,另外很多吸附情况涉及的机理问题,解释的还不够完善,后续通过结合大量的实验数据以及优秀研究者的文献来进一步充实本文所涉及的机理问题。
