近红外光谱法测定头孢曲松钠含量
2020-02-18冯丽雄吴伟东万恒兴
冯丽雄,彭 莺,吴伟东,万恒兴
(深圳技师学院 应用生物系,广东 深圳 518116)
头孢曲松钠是第三代半合成头孢菌素类抗生素,其抗菌谱广,抗菌原理是通过抑制细菌的细胞壁合成,对革兰氏阳性及阴性菌均有中等强度的抗菌作用[1],在临床中广泛应用[2-4]。测定头孢曲松钠的含量的方法主要是高效液相色谱法,但高效液相色谱法检测样品制备和操作步骤复杂[5-7],检验时间长,试剂耗材成本高,环境污染大,是现代企业面临需要解决的问题。
近年来,在分析领域里发展迅速的近红外光谱(Near-infrared Spectroscopy,简称NIR)分析技术,具有测量速度快、测试成本低、无需化学试剂、样品无需预加工等优点[8-9],在化工、制药等许多领域具有广阔的应用前景[10]。NIR技术已成功应用于测定注射用头孢派酮钠[11]、注射用头孢他啶[12]和注射用五水头孢唑林钠[13]含量近红外定量模型的报道。本文对建立的模型进行验证并将该方法应用于头孢曲松钠原料及成品的含量测定。
1 仪器和样品
1.1 仪器
瑞士万通NIRS XDS Rapid Liquid Analyzer近红外光谱分析仪,配单色仪400 nm至2500 nm的波长;石英比色皿厚度1 mm,数据收集和处理等通过Vision软件完成。美国Waters高效液相色谱仪,e2695四元梯度洗脱系统,2489双波长紫外检测器,Waters柱温箱,Empower2色谱工作站软件,色谱柱为岛津 ODS-3 C18(150*4.6 mm,5 μm)。XP205分析天平(感量:0.00001 g,瑞士Mettler Toledo),瑞士Mettler Toledo S20 pH计。
1.2 样品
头孢曲松钠工作对照品(国药集团致君(深圳)制药有限公司,批号:180601);头孢曲松反式异构体对照品(中国药品生物制品检定所,批号:130660-201702);头孢曲松钠原料由珠海丽珠药业有限公司和齐鲁安替制药有限公司生产(共25批);注射用头孢曲松钠成品(国药集团致君(深圳)制药有限公司生产共25批)。
2 方法和结果
2.1 标准溶液及供试品溶液配制
标准溶液配制方法:分别精密称取含头孢曲松钠工作对照品2、1.75、1.5、1.25、1、0.75、0.5、0.25、0.1 g置10 mL 容量瓶中,用纯化水溶解并定容至刻度,制成 200、175、150、125、100、75、50、25、10 mg,制成-1 的头孢曲松钠标准溶液。
供试品溶液配制方法:精密称取头孢曲松钠1 g,置于10 mL容量瓶中,用纯化水溶解并定容至刻度,制得100 mg制得水-1 溶液。
2.2 光谱扫描
仪器预热30 min,并进行性能测和波长确认,通过测试后方可检测。光谱范围400~2500 nm,分辨率8.75 nm,扫描次数32 次,扫描平衡时间5 s,平衡温度30℃。
2.3 模型建立及参数选择

图1 对照溶液(100 mg·mL-1)近红外光谱二阶导迭加图Fig.1 The overlap spectra of reference solutions (100 mg·mL-1)NIR second derivative
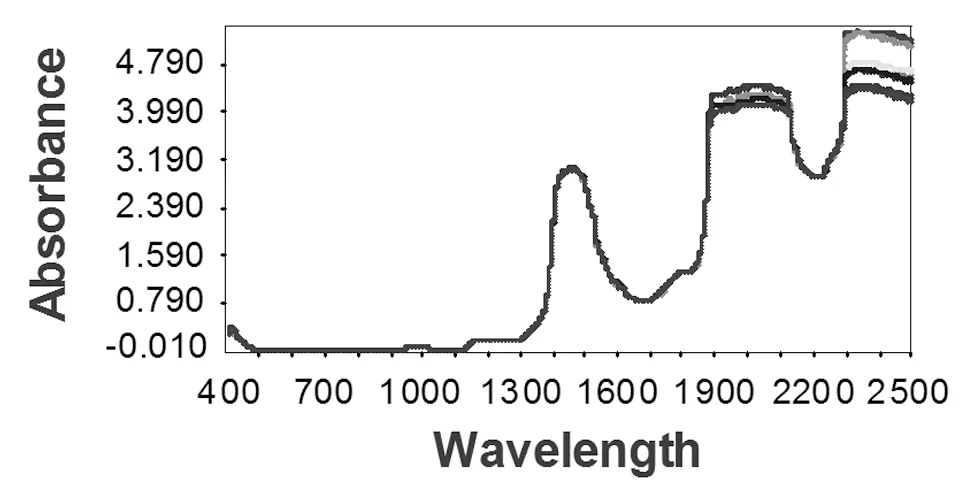
图2 对照溶液(100 mg·mL-1)近红外透射光谱图Fig.2 The initial NIR transmission spectrum of reference solutions(100 mg·mL-1)
通过近红外光谱仪采集16个含头孢曲松100 mg0孢曲-1 的对照溶液,比对二阶导迭加图,其中:在420~1400 nm和1500~1800 nm两个区域重叠吻合度高(见图1),具有较好的稳定性,但在500~900 nm波段范围内吸收值低(接近-0.010)(见图2),故对波段420~500 nm和900~1800 nm进行变量筛选。定量模型的评价可以通过内部验证和外部验证来评估,内部验证主要通过“留一法”交叉验证[14]来评价模型的稳定性及预测能力。相关系数(Corr.Coeff.),预测残差平方和(PRESS),校正均方差(RMSEC)和预测均方差(RMSEP)作为评价指标对选择的波段模型进行评估。相关系数R2的值介于0~1之间,值越大拟合性越好,RMSEC和RMSEP用于衡量预测值和测量值之间的平均偏差,数值越小说明模型的稳健性越好,PRESS越小预测能力越好[15]。建模过程中通过考察预测残差平方和(PRESS)确定主因子数(Factor),PRESS值越小,模型的预测能力越好[16]。本实验通过人工选择不同光谱区域建立定量模型,结果见表1所示。在1600~1700 nm和1700~1800 nm波段,相关系数分别为0.9997和0.9993,表明这两个波段的模型拟合性高;校正均方差、预测残差平方和数值均是最小的,分别是为0.2725、0.4903和0.3682、0.6362,表明这两个波段模型的稳健性好,故选择1600~1800 nm波段进行建模。当主因子数是5时,PRESS值3.5291最小,见图3,故选择最优因子数5;头孢曲松钠对照溶液在10~200 mg0对照-1范围内与计算浓度相关系数接近1(R2=0.9999),见图4;RMSEC(校正均方差)与RMSEP(预测均方差)数值接近,表明该模型具有较好的稳定性。
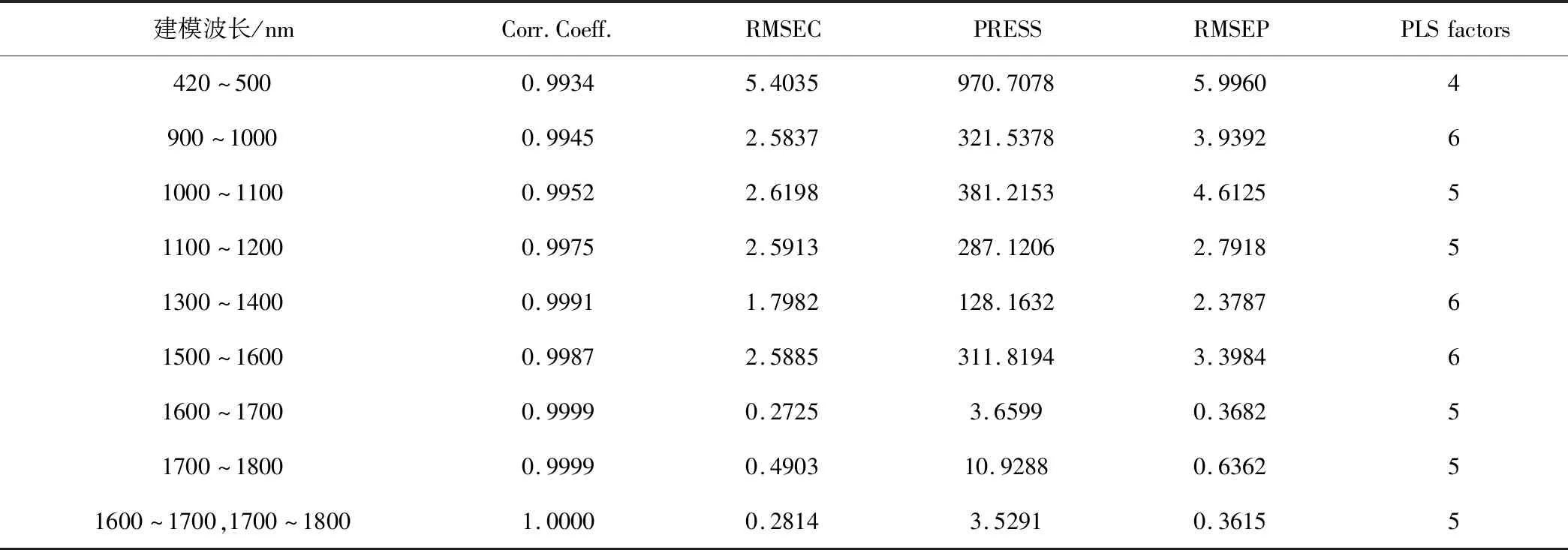
表1 光谱区域对建模结果的影响Table 1 Influence of spectral range on the results of the model
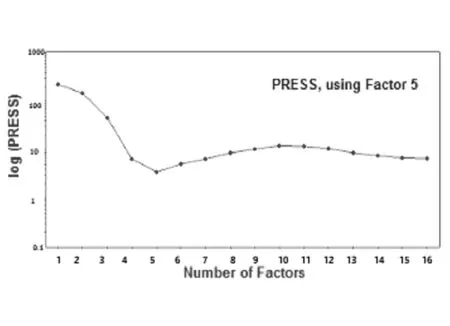
图3 主因子数和预测残差平方和关系
Fig.3 Correlation of the principal factors numberto the PRESS

图4 对照溶液浓度和计算浓度相关性(10~200 mg0液浓-1)
Fig.4 Correlation of calculated values to reference values (10~200 mg·mL-1)
2.4 定量模型的检验
采用外部验证的方法对模型的实际预测能力进行评估,即用定量模型近红外光谱法测试头孢曲松钠样品(原料及成品各25批)结果与高效液相色谱法[17-18]测定的结果进行比较,计算近红外光谱法(C)与高效液相色谱法(M)的偏差(%)=(C-M)/MM差(相%。结果见表 2,偏差在-1.64%~1.78%内,平均相对偏差0.87%。配对t检验表明,在α=0.05 显著性水平上,两者无显著性差异。证明近红外光谱法可以用于快速预测头孢曲松钠含量。
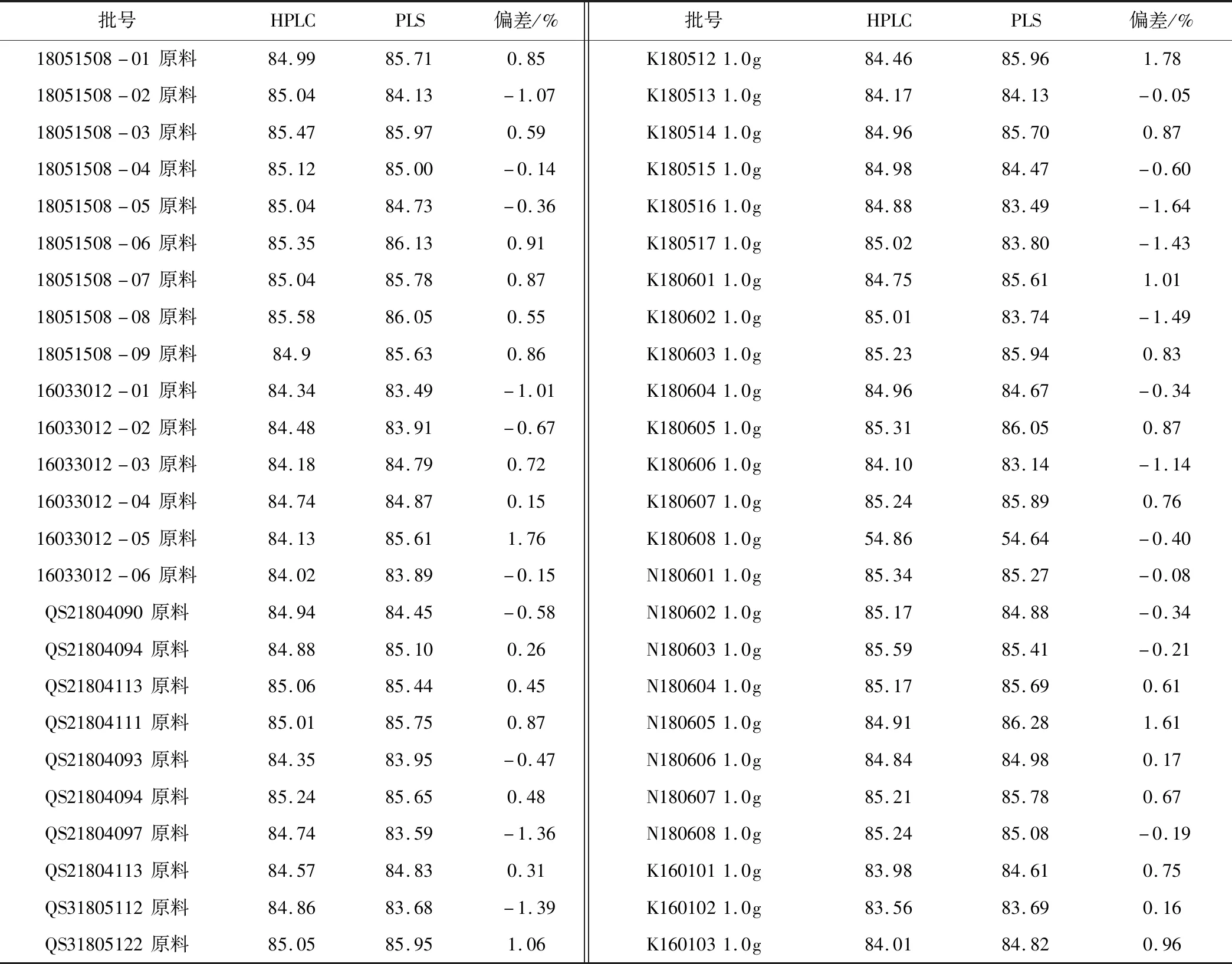
表2 头孢曲松钠近红外光谱PLS和HPLC 法测定结果比较Table 2 Comparison of the ceftriaxone content by NIRS PLS and HPLC
2.5 精密度实验
取头孢曲松钠原料(批号:QS21804090),分别制成含头孢曲松浓度为 200、175、150、125、100、75、50、25、10 mg为含头-1的溶液,连续5次取样并测定其近红外光谱,代入模型,用 PLS 法计算样品的含量。5次平行测定的含量 RSD 结果分别为0.05%、0.06%、0.10%、0.06%、0.07%、0.19%、0.34%、0.53%和1.83%,表明精密度良好。
3 讨论
本实验首先对头孢曲松钠溶液近红外光谱,最终选择1600~1800 nm(C-H键一级伸缩振动一级倍频峰吸收区)波段,采用偏最小二乘法建立近红外定量分析模型。因为水溶液中的液态水分子缔合,吸收带的细节带消失,形成了较宽的谱带[19]。水分子O-H 伸缩振动的一级倍频在约1440 nm,合频在 1940 nm附近有较强的吸收,在建模需避开这两个波段。
本文建立的近红外偏最小二乘法定量模型,对照溶液浓度在10~200 mg0液浓-1范围内相关系数良好(0.9999)。通过高效液相色谱法进行外部验证实验比较,近红外偏最小二乘法定量模型与高效液相色谱法检测的结果基本一致,但在精密度实验中发现测试低浓度溶液(10 mg精密度-1,RSD=1.83%)和高浓度的溶液(200 mg0浓度-1,RSD=0.05%)RSD有差异,高浓度溶液精密度更好。
头孢曲松钠含量测定近红外光谱法与高效液相色谱法相比,近红外光谱法检测无需对照品和特殊试剂,现场快速测定,可以减少企业检验成本,是一种环境友好型分析测试方法。
