铁镍电池Ni(OH)2正极材料的掺杂及电化学性能研究
2019-12-13杨少华刘晟林
刘 达,杨少华,田 阳,刘晟林
(1.沈阳理工大学 环境与化学工程学院,沈阳 110159;2.辽宁省特种储备电源工程技术中心,沈阳 110159)
化学电源是现代非常重要的发明,是人类社会发展的动力保障,但化学电源耗损很大,我国每年约有废旧铅酸电池5000多万只,其重量高达50万吨[1],污染非常严重。铁镍电池因其安全环保、价格低廉、耐过充、放电深度大、使用寿命长和维护简单等优点在1910到1960年间备受青睐,广泛应用于电力机车的电源灯、电网储能、铁路客车服务等领域[2]。铁镍电池是由Ni(OH)2正极、铁负极、添加剂、集流体、碱性电解液、电解质隔膜和电池壳体等组成[3]。因为Ni(OH)2价格低廉、绿色环保、有较高的放电容量等优点被大规模应用于碱性二次电池中。Ni(OH)2制成电极的形式有袋式镍电极、纤维镍电极、粘结式镍电极和泡沫镍电极等[4]。Ni(OH)2有α和β两种晶型,因为α-Ni(OH)2在碱性条件下会转变成稳定的β-Ni(OH)2,所以镍正极一般采用β-Ni(OH)2[5]。纯氢氧化镍电化学性能差,为改善氢氧化镍的质量比容量、导电性和充放电循环等电化学性能,可加入其它金属元素:添加Zn2+、Al3+可使Ni(OH)2形成稳定的β-Ni(OH)2,掺杂Co2+可增加导电性[5]。
本文采用泡沫镍电极,单一掺杂Co2+、Zn2+、Al3+到镍电极及复合掺杂Co2++Zn2++Al3+到镍电极,作为铁镍电池的正极材料制备成电池,进行充放电测试。
1 实验
1.1 Ni(OH)2的制备
用分析天平称取3.8gNiCl·6H2O粉末溶于210mL去离子水中,将提前稀释好的5%wt.NH3·H2O以一定的速度滴加到该溶液中,滴加过程中注意搅拌;观察沉淀生成情况,并根据文献[5]调节溶液的pH至9.5,在同一搅拌速度下搅拌4h。倒入循环水式真空泵抽滤洗涤至中性,得到潮湿的绿色膏状物,最后放入鼓风干燥箱调至100℃烘干12h,取出研磨即为所制材料。
1.2 性能表征
XRD衍射分析实验(日本理学D/max-RB 12kW转靶X射线衍射仪)对正极活性物质进行物相分析。测试条件:CuKα辐射,闪烁计数器前加石墨弯晶单色器,管压40KV,管流40mA,光阑系数为DS=SS=1°,RS=0.1mm,采用θ-2θ连续扫描,步长为0.02°,扫描速度6°/min。
1.3 铁镍电池组装
正极材料具体制作过程如下:在氢氧化镍中按照一定比例加入碳粉、CMC、PTFE乳液,并加入三氧化二铝、氧化锌、氢氧化钴添加剂,用水调成膏状,均匀涂抹在泡沫镍一侧上,烘干,压片,进行电池测试。
本实验负极材料选用工业铁镍电池用的铁粉,在工业铁粉中按照一定比例加入碳粉、PTFE乳液、PVA,并用PVA水溶液调成膏状,均匀涂抹在泡沫镍两侧,烘干,压片,进行电池测试。
电池组装过程如下:裁剪2.5cm×5cm的泡沫镍,记录泡沫镍的重量M0。将调好的膏状正负物料均匀涂抹在泡沫镍2.5cm×4cm的面积上,正极涂一面,负极涂两面,记录湿泡沫镍重量M1,在100℃烘箱内进行烘干;烘干后,利用辊压机辊压。在电极片上包裹锡纸,防止电极材料脱落。用0.5cm厚度辊压机对涂有正极材料的泡沫镍进行压片,用0.6cm厚度辊压机对涂有负极材料的泡沫镍进行压片,观察压片的薄厚和明亮度,可适当加入纸张控制辊压的厚度。将辊压后的物料在分析天平上进行称重,记录数据M2。利用点焊机在正极和负极上沿焊上镀镍不锈钢条,并用窄透明胶带缠绕,防止正负极缠有导电片的部分接触发生短路现象。正负电极片用无纺布包裹,两层纺布间加上一层聚四氟乙烯薄膜,聚四氟乙烯薄膜比电极稍微大一些,防止正负极直接接触,造成短路现象。用透明胶带对正极材料缠绕固定,装入自制密封袋,用电池盒或夹板夹紧电池,使其反应充分。在密封袋中加入配好的碱性电解液,连接到蓝电电池测试系统上进行充放电性能测试;可在密封袋口夹上夹子,防止空气中的CO2使电解液碳酸化。
实验测试采用LAND电池测试系统,将组装好的单电池连接到LAND系统上,设置启动参数:①静置1min;②正极上活性物质的质量按照96mA/g的标准进行,直到充电容量达到160mAh结束;③静置10min;④再按照32mA/g的标准进行放电,直至电压≤0.7V;⑤静置15min。如果充放电的循环少于20圈,将回到程序②继续充电,按照16mA/g的标准放电到0.7V,直到满足循环次数或满足放电容量稳定,停止实验并记录数据。
2 结果与讨论
2.1 XRD分析
图1为Ni(OH)2的XRD表征图。

图1 Ni(OH)2的XRD表征图
从图1中可以看出,通过共沉淀法制备的Ni(OH)2分别在衍射角19.3°、33.1°、38.5°、52.1°、59.1°、62.7°、70.5°、72.7°处出现特征峰,与数据库里Ni(OH)2的标准卡(PDF#1-1047)相对应(制备过程形成极少量的NiOOH略微影响了峰的偏移,但不影响实验效果),自制的Ni(OH)2与标准卡的峰位置及形状基本一致,说明本次合成的实验主要成分氢氧化镍是β-Ni(OH)2。
2.2 单一添加剂对电池放电性能的影响
本文选用的添加剂有氢氧化钴、氧化铝、氧化锌。以通过共沉淀法制备的Ni(OH)2为正极材料核心活性物质,向纯镍中分别加入质量百分比为1%、1.5%、2%等含量的添加剂制成改性正极,如比较不出最优,可增加2.5%含量的添加剂测试,比较出最优的测试比例,电池负极采用工业铁镍电池的负极,对铁镍电池进行组装,设置成多个单电池,利用LAND电池测试系统对其进行电池的充放电性能测试。
2.2.1 Co(OH)2用量对正极材料放电的影响
图2为Co(OH)2含量1%Co(OH)2-Ni(OH)2、1.5%Co(OH)2-Ni(OH)2、2%Co(OH)2-Ni(OH)2的放电比容量曲线,测试结果如表1所示。

表1 掺有不同比例Co(OH)2的镍正极电池比容量

图2 掺杂不同比例的Co(OH)2的电池放电比容量曲线
由图2中曲线可知,最初两圈没有参数,是电池的静置过程;从第3圈开始到充放电循环20圈之间,电池放电性能趋于平稳。且观察曲线可以发现,掺有Co(OH)2的镍正极放电性能要远好于纯镍正极放电性能,纯镍正极铁镍电池放电比容量只有223.9mAh/g。Co(OH)2添加到镍正极中在电池充电时生成CoOOH,CoOOH是良好的导电网,可以降低铁镍电池镍正极发生电化学反应时电荷转移产生的电阻,提高电子和质子在铁镍电池镍正极材料中的传导性,进而提高电池的充电效率和放电深度。实验表明,正极中添加不同比例Co(OH)2时电池的放电效果从大到小为:1.5%Co(OH)2-Ni(OH)2>2%Co(OH)2-Ni(OH)2>1%Co(OH)2-Ni(OH)2;掺1.5%Co(OH)2的电池比容量可达到307.7mAh/g。
2.2.2 Al2O3用量对正极材料放电的影响
本组实验设计的氧化铝含量为1%Al2O3-Ni(OH)2、1.5%Al2O3-Ni(OH)2、2%Al2O3-Ni(OH)2、2.5%Al2O3-Ni(OH)2,放电比容量曲线见图3所示,测试结果如表2所示。

表2 掺有不同比例Al2O3的镍正极电池比容量
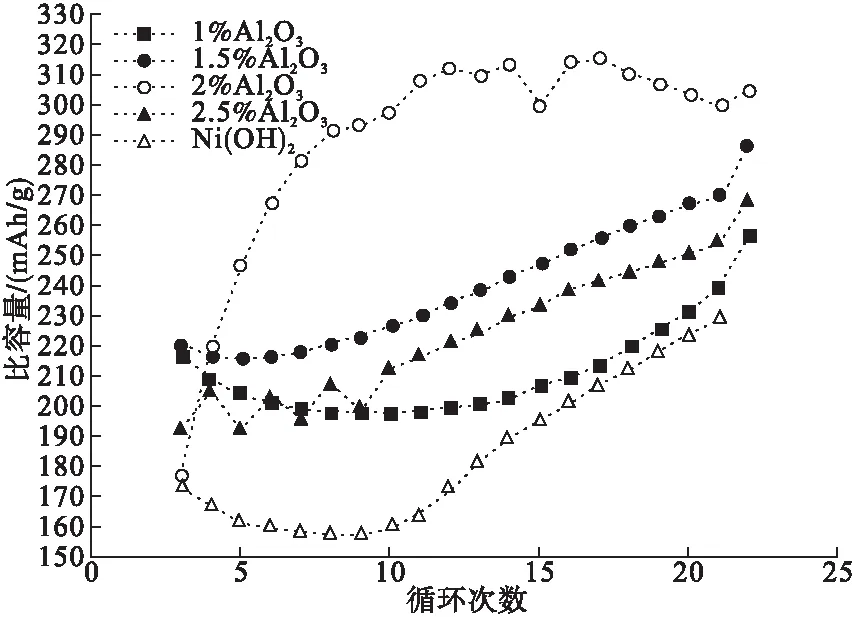
图3 掺有不同比例Al2O3时的电池放电比容量曲线
由图3可知,前两圈没有参数,是电池的静置过程;第3圈到第10圈2.5%Al2O3的循环过程中放电性能不稳定,原因是测试过程中对充电电流和充电时间的变化导致;在充放电循环10圈后,随着电极反应的进行,电池放电比容量随循环次数的增加而增大。由上述曲线可以看出,掺有Al2O3的镍正极铁镍电池放电性能要远远好于纯镍正极铁镍电池,纯镍正极铁镍电池放电比容量只有223.9mAh/g;掺2%Al2O2的电池放电性能最好,比容量为304mAh/g。这是因为加入Al2O3,Al3+取代Ni2+,NiO2层间引入水分子和阴离子,使层间结构稳定性增加,帮助形成稳定的β-Ni(OH)2[2]。通常固相反应法制备出的β-Ni(OH)2不稳定,会在强碱性的电解液中转变成α-Ni(OH)2,所以要在镍正极中加入合适比例的Al2O3,来改善铁镍电池的充放电性能;且铝相比于钴价格便宜,对环境污染较小。实验表明,正极中添加不同比例Al2O3时电池的放电效果从大到小为:2%Al2O3-Ni(OH)2>1.5%Al2O3-Ni(OH)2>2.5%Al2O3-Ni(OH)2>1%Al2O3-Ni(OH)2。
2.2.3 ZnO用量对正极材料放电的影响
图4为ZnO含量1%ZnO-Ni(OH)2、1.5%ZnO-Ni(OH)2、2%ZnO-Ni(OH)2,的放电比容量曲线,测试结果如表3所示。

表1 掺有不同比例ZnO的镍正极电池比容量

图4 掺有不同比例ZnO时的电池放电比容量曲线
观察图4可知,在充放电循环20圈后,掺有ZnO的镍正极铁镍电池放电性能要远远好于纯镍正极铁镍电池,纯镍正极铁镍电池放电比容量只有223.9mAh/g。锌与铝的作用相似,都是使NiO2层间结构稳定性增加,帮助形成稳定的β-Ni(OH)2,来改善铁镍电池的充放电性能。加入ZnO,Zn2+作为过剩正电荷成对排列在NiO2层两侧,使β-Ni-(OH)2结构更稳定。实验表明,正极中添加不同比例氧化锌时电池的放电效果从大到小为:1%ZnO-Ni(OH)2>1.5%ZnO-Ni(OH)2>2%ZnO-Ni(OH)2。掺1%ZnO的电池放电性能最好,且随着ZnO含量的增加电池放电性能减弱。1%ZnO曲线在20圈之前比容量较低,因为测试设置的程序存在偏差,充电时间过短,没有达到其他实验测试单组的设置容量160mAh,因此导致放电容量过低。修改程序续接测试,从20圈开始,该测试组充电容量达到与其他测试组相比较的标准水平,在第24圈时达到最高,比容量为316.5mAh/g,而后开始下降,原因可能是随着反应时间的延长,电极内活性物质降低导致。
2.3 混合添加剂对电池放电性能的影响
考虑到单一添加剂对铁镍电池的放电促进作用单一,采用正交设计L9(34)复合3种添加剂,研究对铁镍电池的放电性能影响。测试结果如表4所示。图5为掺有混合添加剂的电池放电比容量曲线,对比分析这9个实验组对铁镍电池放电的影响。1~9组分别代表:1%Co-1%Zn-1%Al、1%Co-1.5%Zn-1.5%Al、1%Co-2%Zn-2%Al、1.5%Co-1%Zn-1.5%Al、1.5%Co-1.5%Zn-2%Al、1.5%Co-2%Zn-1%Al、2%Co-1%Zn-2%Al、2%Co-1.5%Zn-1%Al、2%Co-2%Zn-1.5%Al。
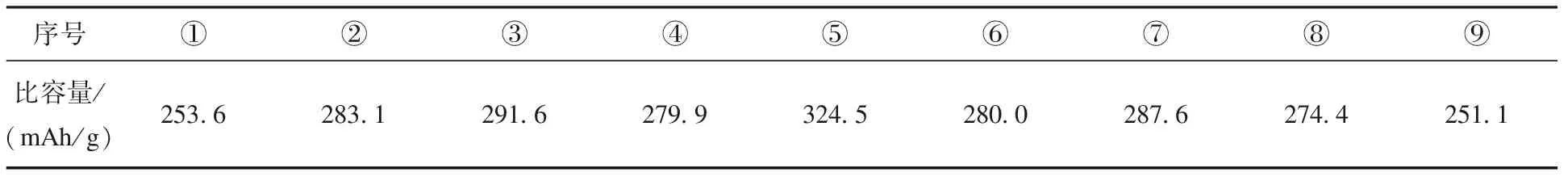
表4 混合添加剂的放电比容量

图5 掺有混合添加剂的电池放电比容量曲线
图5中,把九个测试组分成两种,一种是③、②、⑨,即1%Co-2%Zn-2%Al、1%Co-1.5%Zn-1.5%Al、2%Co-2%Zn-1.5%Al。电池比容量随充放电循环次数的增加先急剧上升,在第10圈达到最高,然后开始下降;这3个实验组在循环过程中放电性能不稳定,原因可能是电池的极化作用导致电池放电容量呈现急剧上升趋势,10圈后开始逐渐下降。另一种是①、④、⑤、⑥、⑦、⑧,即1%Co-1%Zn-1%Al、1.5%Co-1%Zn-1.5%Al 、1.5%Co-1.5%Zn-2%Al、1.5%Co-2%Zn-1%Al、2%Co-1%Zn-2%Al、2%Co-1.5%Zn-1%Al,这6个实验组则在整个充放电循环过程中呈现平稳趋势,随着充放电循环次数的增加,电极反应的进行,电池放电比容量随循环次数的增加而平稳升高。由此可判断第一种情况的3个实验组性能较第二种差。虽然③、②、⑨在某一时刻放电容量大,但不适合使用要求。⑤号测试组在整个充放电测试过程中性能平稳,且比容量达到324.5mAh/g。
3 结论
(1)通过共沉淀法制备的氢氧化镍分别在衍射角19.3。、33.1。、38.5。、52.1。、59.1。、62.7。、70.5。、72.7。处出现特征峰,与标准卡(PDF#1-1047)相对应,说明本次实验合成的氢氧化镍是β-Ni(OH)2。
(2)正极中添加不同比例Co(OH)2时,电池的放电效果从大到小为1.5%Co-Ni(OH)2>2%Co-Ni(OH)2>1%Co-Ni(OH)2,既掺1.5%Co(OH)2的电池放电性能最好,比容量可达到307.7mAh/g。添加不同比例Al2O3时电池的放电效果从大到小为2%Al-Ni(OH)2>1.5%Al-Ni(OH)2>2.5%Al-Ni(OH)2>1%Al-Ni(OH)2;添加不同比例ZnO时电池的放电效果从大到小为1%Zn-Ni(OH)2>1.5%Zn-Ni(OH)2>2%Zn-Ni(OH)2。
(3)采用正交设计复合3种添加剂,将Co2+、Zn2+、Al3+混合掺杂到镍电极。当镍正极中添加1.5%Co+1.5%Zn+2%Al时,铁镍电池正极材料的放电效果最佳,可达到324.5Ah/g左右,比纯净Ni(OH)2正极提高了101.6mAh/g左右。
