食品及食品接触材料中烃类矿物油分析技术进展
2019-12-05郑建国陈燕芬钟怀宁吴梓潼
郑建国,陈燕芬,钟怀宁*,李 丹,吴梓潼
(1.广东省动植物与食品进出口技术措施研究重点实验室,广东 广州 510623;2.广州海关技术中心,广东 广州 510623;3.广州市天河外国语学校,广东 广州 510627)
烃类矿物油(Mineral oil hydrocarbons,MOH)是一类由多种烃类物质组成的复杂混合物,主要由原油经蒸馏、萃取、酸处理、加氢反应等过程或是由天然气、煤及其它生物材料通过合成反应制成。MOH主要包括环烷烃、直链及支链的饱和烃类矿物油(Mineral oil saturated hydrocarbons,MOSH)及由烷基化合物组成的芳香烃类矿物油(Mineral oil aromatic hydrocarbons,MOAH)。由于碳原子数小于10的烃类矿物油具有挥发性,残留并污染食品的可能性小;而碳原子数大于50的烃类矿物油分子量大,不易被人体吸收。因此,现阶段的风险评估主要关注碳原子数范围为C10~C50的矿物油。对于矿物油的毒性,国外已有诸多研究,但仍然存在较大争议。研究表明,烷烃类矿物油具有生物蓄积效应,目前普遍认为C16~C35具有最高风险,主要蓄积在脂肪组织、淋巴结、脾脏和肝脏等器官中[1];而芳香烃类矿物油具有致突变性,高度烷基化的芳烃可能会诱发肿瘤,一些结构简单的芳烃有细胞毒性[1],含有3个以上苯环的芳烃有遗传致癌性[2]。因此,矿物油的污染不容忽视。调查研究表明,矿物油大多存在于有印刷的食品包装纸和回收纸包装材料中,通常以气态扩散或直接接触的方式迁移到食品中,是目前食品中矿物油污染的主要来源[3]。
烃类矿物油成分复杂,且干扰物质较多,采用现有技术检测存在较大的局限性。多年来,研究者在前处理技术的简化、干扰物质的排除、MOSH和MOAH的有效分离及定性和定量分析、仪器配置的开发和应用等方面进行了不断探索和优化。本文综述了国内外近十年来矿物油检测技术的研究进展,及其在食品及食品包装材料中的应用,旨在为相关企业和机构的检测工作提供方法与技术参考。
矿物油测定时需要对MOSH和MOAH的总量进行定量分析,其一般检测流程如图1所示:提取净化后,对MOSH和MOAH进行分离,采用GC/FID定量(必要时采用GC-MS进行定性分析)。

图1 矿物油的常规检测流程Fig.1 Routine detection process of mineral oil
1 样品前处理技术
食品中的很多物质与矿物油结构相近,在色谱上难以与矿物油实现分离,从而对检测产生较大干扰。因此要得到准确的定量结果,必须实现矿物油的有效提取、净化和分离。
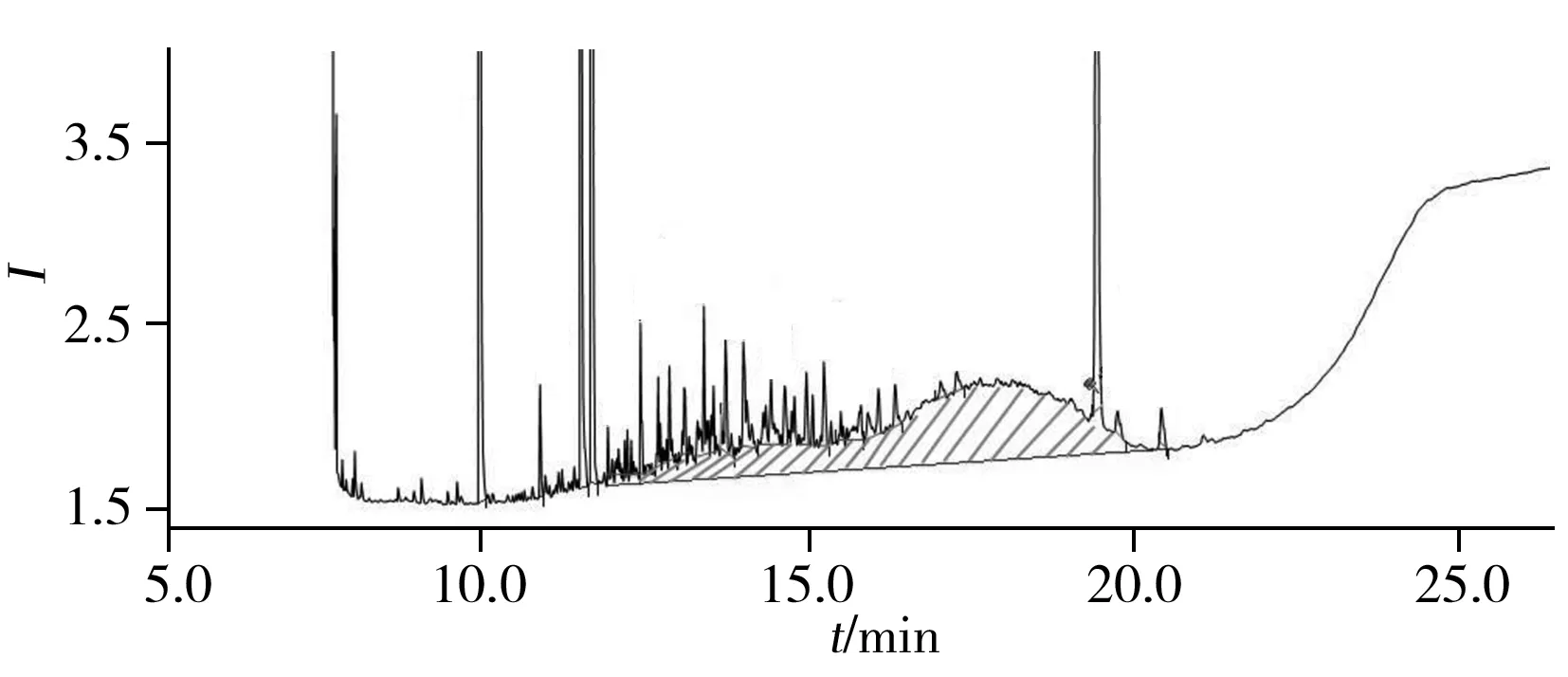
图2 MOSH的色谱图Fig.2 Chromatogram of MOSH
1.1 提取及浓缩方法
食品及食品接触材料的传统提取方法是采取正己烷或正己烷-乙醇提取,根据测试对象种类选择不同的提取时间,如奶粉为静置过夜提取,而纸制品中矿物油含量的提取时间为2 h[4-5]。而针对含油脂的食品,通常需要皂化去除甘油三酯等,导致分析净化步骤繁琐、费时,且消耗大量的试剂。为了提高效率,Moret等[6]采用微波皂化萃取法将提取、皂化在高温高压微波下同步完成,节约了试剂,简化了浓缩步骤,实现了快速提取。也有研究通过快速溶剂萃取法[7]大大缩短了矿物油的提取时间。
矿物油为一大类同系物质,在色谱上通常以“驼峰”的形态出现,如图2。为避免前处理过程中低碳链矿物油的损失,需选用合适的方式对提取液进行浓缩。Fiorini等[8]建立了植物油和干性水果食品中矿物油的检测方法,研究了不同浓缩方式对检测结果的影响,发现相比氮吹浓缩法,旋转蒸发浓缩法(40 ℃)造成的目标物损失更少,效果更优。
1.2 净化方法
植物油中的甘油三酯、原生烃类和烯烃物质是在对植物油中的矿物油进行测定时的主要干扰物质。
1.2.1 皂化法——去除甘油三酯的干扰甘油三酯作为植物油的主要成分,能与矿物油成分共存于有机溶剂中,且沸点较矿物油高,在FID色谱上的出峰相对靠后,既可能掩盖目标物,也容易造成色谱柱和检测器的污染,无法实现样品的准确分析,如图3。因此,对于植物油类或含油脂成分较高的样品,需采用皂化法去除油脂的干扰[6,9]。
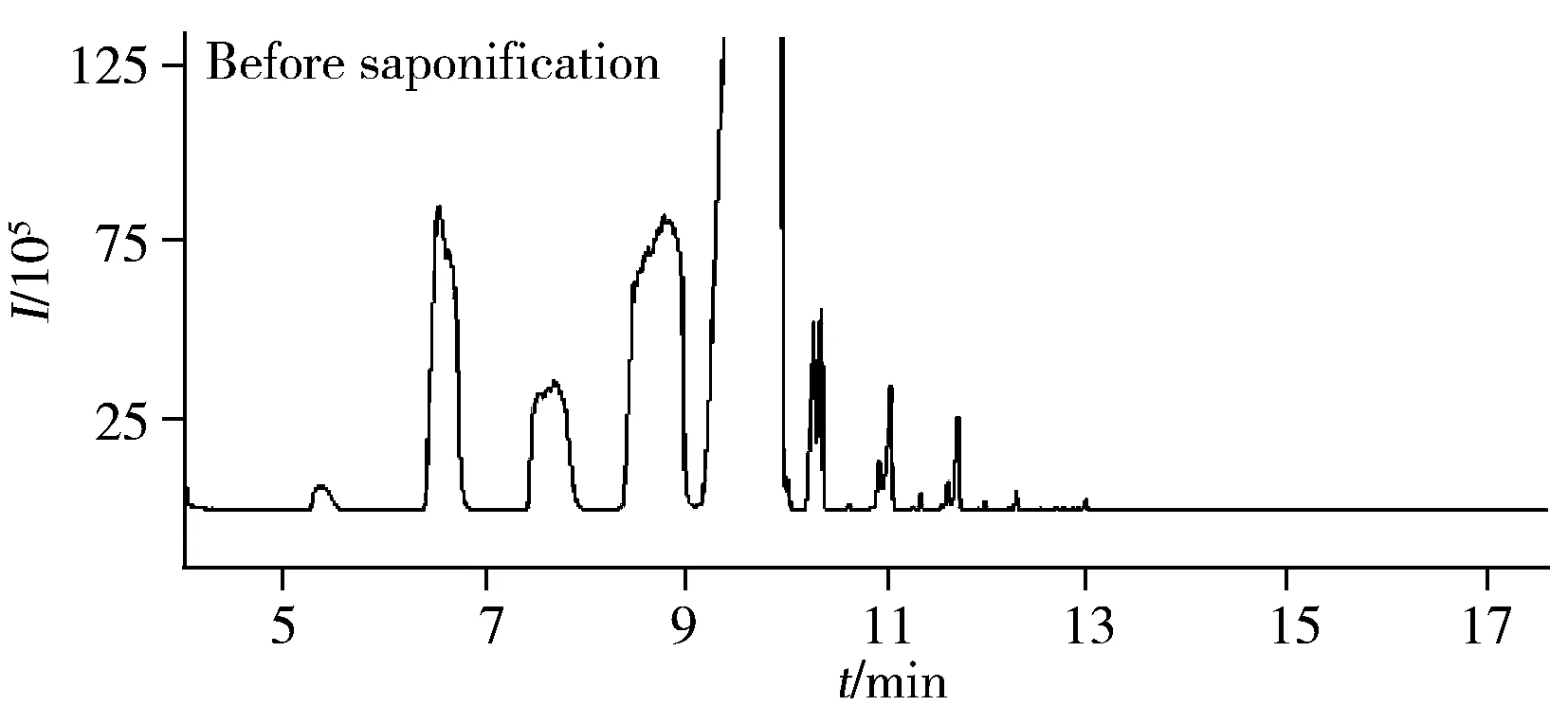
1.2.2 氧化铝法——去除原生烃类物质的干扰原生烃类物质主要为奇数碳的正构烷烃(C23~C33),其性质与MOSH相同,常规的前处理步骤无法将两者有效分离。样品中存在该类物质时,其色谱峰往往竖立于MOSH之上,对MOSH的定性和定量造成干扰,或导致假阳性结果。活性氧化铝对正构烷烃具有一定的滞留作用,可去除该类物质对矿物油检测的干扰,已广泛应用于油脂类食品的检测[10-11]。但也有研究表明,氧化铝法在有效降低干扰的同时,会造成一定程度的矿物油目标物的损失[12-14]。实际应用时是否使用活性氧化铝应视具体情况而定:当原生烃类物质的出峰对MOSH干扰较小时,可不进行氧化铝的净化步骤,直接通过手动积分扣除“驼峰”轮廓以上的原生烃类物质(尖峰);而当原生烃类物质含量过高,会对MOSH所产生的“驼峰”造成“压迫”,导致定量不准确时,则需选择氧化铝去除原生烃的干扰。
1.2.3 环氧化法——去除烯烃类物质的干扰植物油中含有的角鲨烯、胡萝卜素、萜烯、植物甾烯等烯烃类物质的干扰是矿物油分析时需解决的难题之一。目前一般通过环氧化反应和溴醇反应等方法将烯烃物质氧化除去。其中,环氧化反应的应用较为普遍,其原理是采用过氧化物,如间氯过氧化苯甲酸(M-chloroperoxide benzoic acid,mCPBA)[14]与烯烃反应使双键环氧化,环氧化物极性强于MOAH,可更好地滞留在银硅胶柱上,洗脱过程中不再与MOAH共流出,从而实现两者分离。同样,环氧化也会因样品基质的不同,造成不同程度的目标物损失[14-16]。目前采用此方法对样品净化的报道不多,其适用范围、精密度、回收率等尚处在探索之中。
1.3 MOSH与MOAH的分离方法
由于硝酸银具有保留烯烃和MOAH的能力,因此,目前主要采用硝酸银硅胶填料进行净化。先通过正己烷对MOSH进行洗脱,收集MOSH组分后,再以一定比例的正己烷和二氯甲烷混合溶剂解除固相萃取柱对MOAH的吸附,从而实现两者的分离。目前该方法已经得到了广泛的应用[4-5,12,17-21]。在LC-GC分析中,有研究采用含银的液相色谱柱,实现了在线分离,有效提高了净化效率[22]。
2 矿物油检测方法
2.1 气相色谱法(GC)
GC/FID是目前公认的矿物油检测方法。根据FID检测原理,FID几乎对所有烃类化合物有一致的响应,无明显的歧视效应。矿物油的烃类化合物在色谱图上表现为一定沸程的连续“驼峰”。矿物油来源和提炼手段的不同,导致其种类繁多,由于缺乏标准对照物进行一一定量,只能采用与矿物油性质相似的特定物质作为参照,依据保留时间对连续的“驼峰”进行分段和半定量(如采用双环己烷对MOSH进行定量)。目标峰的积分面积为水平基线及“驼峰”上端轮廓之间的面积(如图2的阴影部分),轮廓以上的尖峰不属于矿物油成分。
采用硝酸银硅胶柱分离MOSH和MOAH,GC/FID进行定量的方法在食品及食品接触材料的矿物油分析中得到了广泛应用[4-5,11-12,17-21,23]。李克亚等[18]建立起了纸制品包装材料中矿物油的SPE/GC方法,并将其应用到6类食品包装材料的检测中,SN/T 4895-2017[24]方法即是在该方法的基础上进行优化和改善而建立的。
GC/FID结合大体积进样技术,能有效提高检测灵敏度和降低检出限,相比于LC-GC联用技术,该方法可操作性强,成本低,实用性更强[21,25]。
2.2 气相色谱-质谱法(GC-MS)
质谱技术通过测量离子质荷比对目标物质进行定量。质量相同,结构不同的烃类物质,在色谱图上的响应不同,使得GC-MS在矿物油的检测中往往只能作为MOSH和MOAH定性的辅助方法,目前应用GC-MS 法对矿物油进行定量的报道较为少见,仅有Lionel等[9]采用GC-MS方法对巧克力和谷物类食品中的矿物油进行了同时鉴定和定量,并将测定结果与LC-GC/FID进行了对比,证明了该方法具有一定的可行性。
2.3 液相-气相色谱联用法(LC-GC)
LC-GC采用液相色谱柱,成功实现了对MOSH和MOAH的在线分离,在近几十年来,该方法得到广泛使用和完善[7,16,26-33]。液相色谱柱一般采用硅胶正相柱,如 LiChrospher Si60 和 Supercosil LC-Si,分离原理与SPE小柱相同。另外,溶剂蒸发浓缩技术及Y接口技术[34]的开发和运用,实现了不同检测器的连接组合,LC-GC仪并联两根气相色谱柱及双检测器,可实现多种组合,如LC-GC/FID/FID、LC-GC/FID/MS或LC-GC/FID/FID/MS等,使得从液相色谱柱流出的MOSH 和 MOAH组分分别流入两根气相色谱柱中,进行同步的定性定量分析,满足了不同实验室的检测需求,并大大提高了分析效率。
LC-GC 联用仪具有明显的优势。首先,其灵敏度高:经液相色谱柱的分离净化后,MOSH和MOAH 依次流出,通过LC-GC的接口技术将全部矿物油馏分送入GC后,进入大体积进样系统,挥发除去大部分的溶剂即可使MOSH和MOAH得到在线的浓缩,提高检测灵敏度,降低检出限。其次,LC-GC实现了在线的全样品分析,自动化程度高,节省了人工操作和成本,降低了样品损失和引入外来污染的风险,提高了方法的可靠性。再者,LC-GC可有效减少样品和溶剂的用量,具有环境友好的优点。然而LC-GC成本高,仪器维护及运行成本较高,对操作人员的技术要求较高,目前国内仅有极少数的检测机构拥有该技术。
2.4 其他技术
2.4.1 二维气相色谱法(GC×GC)在GC×GC检测中,试样进入第一根色谱柱后,化合物根据沸点不同进行分离,因沸点相近而未充分分离的化合物在第二根色谱柱中根据极性大小进行纵向的分离,检测器采集到的信号形成三维立体图或二维轮廓图。根据化合物所属类型,GC×GC谱图被分割成不同的区带,每一区带代表特定的族,同族化合物在其区带内按照沸点不同进行分离,如烷烃、环烷烃、单环芳烃和多环芳烃等,这为食品中矿物油来源的分析提供了方法。近年来,该技术被用于植物油[35]、回收纸[36]、食品和化妆品[4,32,37]和人体器官中矿物油的污染来源分析[2,38],为矿物油的溯源和管控提供了有力的依据。
2.4.2 核磁共振技术烃类树脂和裂解汽油中的矿物油由于结构中含有苯环,使用核磁共振分析时具有更好的选择性。目前已有研究使用核磁共振方法实现了不同类型矿物油的定量分析[39]及食品中热熔胶迁移量的研究[40]。而二维气相色谱结合核磁共振技术,也为矿物油的来源分析开辟了新的路径[40]。
3 食品及食品接触材料中矿物油的研究
3.1 食品中矿物油的检测
目前,矿物油的检测技术已经广泛地用于食品中。欧洲食品安全局(European Food Safety Authority,EFSA)在2012年发布的评估报告[41]中指出,MOSH几乎存在于所有食品中,在收集的1 000多份食品的检测数据中,不同类别食品中MOSH的平均含量依次为:面包>谷物>非巧克力类糕点>植物油>鱼类罐头>油籽>动物油脂,原因可能是,面包和谷物在加工过程中使用了含有高浓度烃类矿物油的脱模剂和抛光剂。
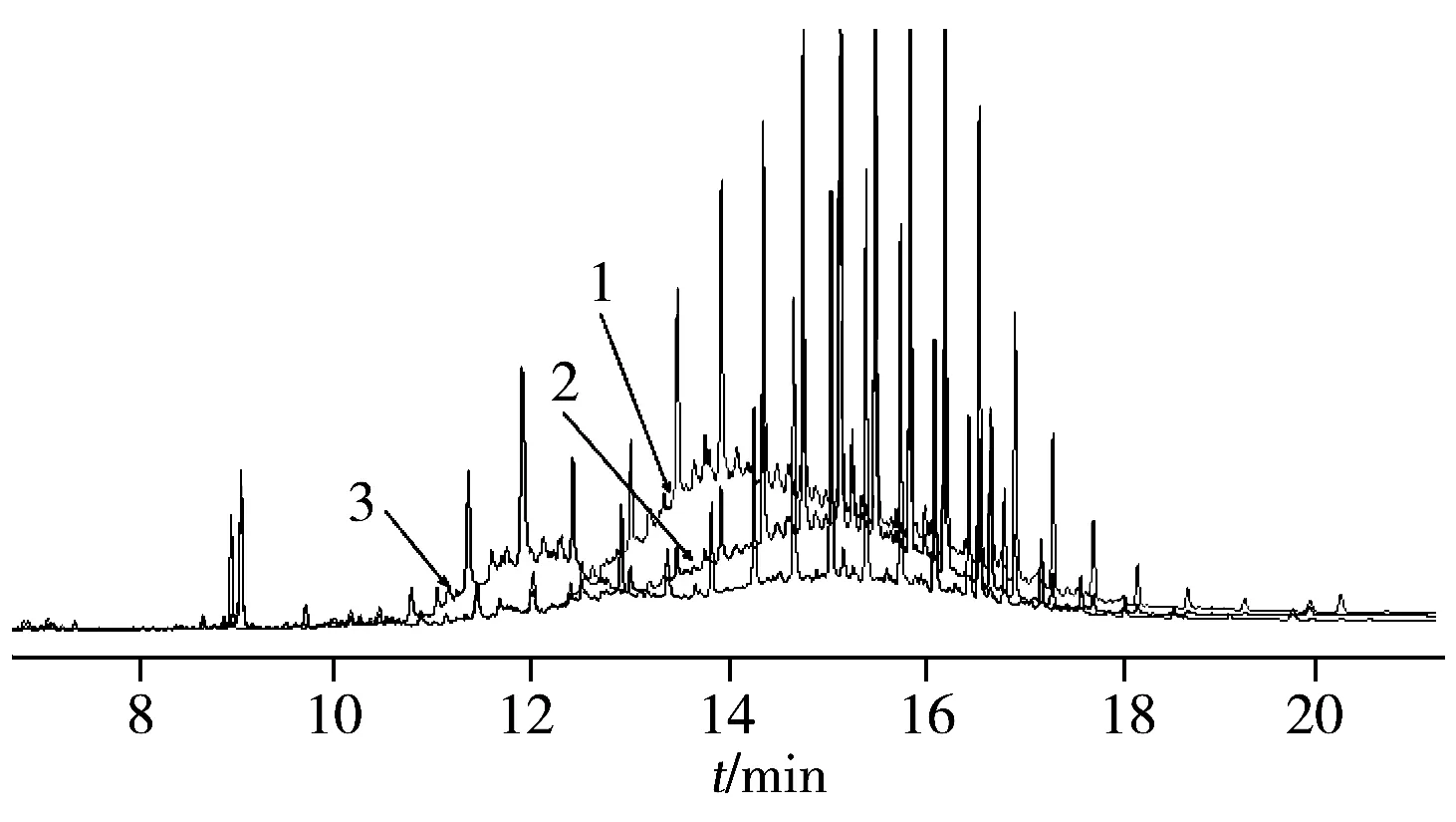
Van Heyst等[42]对比利时市场上的198种食品进行调查,其中142种食品中检出MOSH,糖果的最大检出值为85 mg/kg;23种食品中检出MOAH,含量为0.6~2.24 mg/kg,其中咖啡、可可、茶等干性食品中的MOAH含量最高。 Canavar等[43]对20种干性食品和食品包装纸中的矿物油进行计算和分析,发现回收纸中的矿物油是食品中MOAH的主要贡献来源,29%的食品中MOAH的含量大于1 mg/kg;MOSH( 3.2.1 含量的研究食品接触材料是食品矿物油污染的一个非常重要的来源,包括:食品包装油墨中的连接料和脱模剂、食品包装用的纸和纸板、大宗商品包装用的黄麻袋、食品包装生产上用的润滑剂、加工助剂等。从食品生产到消费的各个环节,矿物油可以通过包装材料与食品直接接触而发生迁移,也可以通过气相传质方式(挥发、扩散)进入到干性食品中。研究表明,含有回收纸纤维的纸和纸板是食品中矿物油污染的重要来源[44-45,47,49],回收纸制品所用的纸纤维往往为旧报纸和刊物等用纸,尽管使用前已经过化学消解,但仍无法完全去除回收纸制品中的油墨、粘合剂等含烃类矿物油的物质或材料。Biedermann和Vollmer等[44-45]发现采用回收纸制成的食品包装中矿物油含量最高可达3 800 mg/kg,远超由粮农组织/世界卫生组织食品添加剂联合专家委员会(Joint FAO/WHO Expert Committee on Food Additives,JECFA)给出的临时每日允许摄入量(Acceptable daily intake,ADI)值所推导的0.6 mg/kg安全限值,而回收纸直接接触的食品中矿物油的含量明显高于该类食品本身矿物油的含量,说明回收纸的使用存在加大矿物油迁移污染的可能性。 3.2.2 迁移行为的研究烃类矿物油向食品发生的迁移受组分特性、环境和材料阻隔性等多种因素的影响。研究表明[45-47],在缺乏功能阻隔层的情况下,矿物油可从食品接触材料向干性食品中迁移,经过漫长货架期之后,外层包装材料中的矿物油也能够透过内层包装袋进入内容物中,因此在对食品进行检测时,应取货架期最后阶段样品的测试结果进行合规判定。 采用干性模拟物对包装材料中矿物油的迁移行为进行研究[28]时发现,随着温度的升高,聚丙烯层阻隔效果逐渐下降。Lorenzini等[46]研究了纸包装中矿物油迁移至干性食品的规律,结果发现,长期贮存下,60%~80%的低沸点矿物油( 目前,行业对矿物油的定义存在分歧,如法典委将矿物油按粘度大小来划分,认为安全风险集中在中低黏度的矿物油中,主要关注的碳链范围为C10~C50,认为该范围的矿物油会对人体健康造成危害[1,48]。而EFSA将其划分为MOSH和MOAH,关注的是C16~C35。我国GB 2760-2014中则规定白油可以用作油脂加工工艺的助剂,包括消泡剂、润滑剂和脱模剂等。对于该类物质是否应归属于矿物油的管控范围,在检测过程中是否需进行区分,目前仍存在争议。因此行业呼吁权威机构进一步明晰矿物油的定义,以便更好地区分污染来源与天然来源的烃类物质,进行必要的管控。 现阶段,针对烃类矿物油毒理学评估的数据较为缺乏,来自动物实验的毒理学数据能否外推至人体也存在较大争议。此外,已有研究多集中于MOSH,对于MOAH的毒理评估报道较少。EFSA使用暴露边界阈值评价方法对不同人群的膳食暴露量进行评估,考虑到部分MOAH具有致癌性,认为人群暴露于矿物油的健康风险值得关注。 鉴于以上情况,笔者认为,开发能够定性定量分析不同组分烃类矿物油的技术,并对混合以及特定组分矿物油的毒理学研究和暴露进行评估[41],完善对矿物油的科学评估和立法尤为重要。 图4 不同纸制品中矿物油的色谱图Fig.4 Chromatograms of mineral oil for different food packaging paper1.printed corrugated paper(印刷瓦楞纸);2.brown wrapping paper(牛皮外包装纸);3.gray wrapping paper(灰色外包装纸) 尽管矿物油的检测技术多种多样,但其检测仍存在较大的局限性和挑战。首先,由于矿物油本身成分复杂,干扰物质多,除来自于食品或包装材料的基质干扰之外,不同来源的矿物油会在色谱图上呈现不同的形态,峰形各异[7,49-50]。如图4,不同纸制品中矿物油成分不同,需要对样品进行逐一分析。而对矿物油进行准确的定量和污染源的分析,需要掌握不同生产工艺下矿物油副产物的碳链范围、性质特征等情况,并针对全供应链上可能存在的风险点进行排查和分析,这对研究机构提出了极高的要求。 其次,尽管使用了净化手段,但矿物油中仍然存在很多无法去除的干扰物,如食品植物油中的不可皂化物(高级脂肪醇、甾醇、蜡酯、色素、维生素等),来自于包装材料的添加剂和原料(如油墨使用的松香、色料、湿润剂、干燥剂、稳定剂等),均属于烃类有机化合物,无法与目标成分进行有效分离,也无法通过质谱识别一一剔除。另外,采用手动积分的方法进行定量时,无法避免由主观因素所带来的误差和结果差异。 最后,目前除SN/T 3495-2017针对纸制品的迁移量建立了检测标准外,国内对于不同基质中矿物油的检测方法尚缺乏统一的操作标准,如定量内标物质的选择、加入量、碳链的分段等。目前大部分检测机构的检测方法是依据德国联邦风险评估研究所(Bundesinstitut fur Risikobewertung,BfR)推荐的方法及已报道的测试方法[11,17]而建立,因此对于样品的测试结果,实验室间存在较大的差异和争议。 食品和食品接触材料是消费者烃类矿物油暴露的重要来源,烃类矿物油能够通过直接接触或间接传质方式污染食品,其引发的食品安全问题亟需关注。烃类矿物油成分复杂,分析难度较大,对现有检测技术仍然存在较大的挑战。针对烃类矿物油分析的分离和净化技术,色谱峰的积分定量技术,矿物油来源鉴定技术等还需进一步的优化和完善。为完善对烃类矿物油的科学风险评估和风险管理,需进一步改进和规范烃类矿物油的检测技术。这将为我国食品和食品接触材料中烃类矿物油的安全标准制定和行业风险管理工作提供科学依据。3.2 食品接触材料中矿物油的检测
4 存在的问题及挑战
4.1 矿物油的定义与毒理评估
4.2 矿物油的分析方法
5 总结与展望
