保健食品逢泰胶囊中大黄素和大黄酚的含量测定
2019-11-21汤丽昌北海市食品药品检验所
□ 汤丽昌 北海市食品药品检验所
逢泰胶囊是以泽泻、生何首乌、荷叶、绞股蓝、红曲、糊精、硬脂酸镁为主要成分加工而成的胶囊剂,其中,泽泻、何首乌是辅助降血脂的主要功效来源,使该胶囊作为保健食品具有降血脂的辅助功效。目前有文献显示,泽泻含有大黄素,何首乌含有大黄素和大黄酚,而大黄素、大黄酚的含量对于临床用药的安全性和活性有较大的指导意义[1-3]。2015年版《中国药典》将何首乌中的大黄素作为质量控制成分[4],然而保健食品的大多数产品标准并无其含量测定项。本研究采用高效液相色谱法对逢泰胶囊中的大黄素和大黄酚进行含量测定,以期为逢泰胶囊产品质量标准的制定提供依据。
1 材料与试剂
1.1 仪器
LC-2010A HT型高效液相色谱仪(岛津);S1-T256涡旋混合器;CPX5800H-C超声波清洗机(美国必能信上海科导仪器有限公司);XA205DU万分之一电子天平(上海梅特勒-托利多仪器有限公司)。
1.2 试药
大黄素对照品(批号:110756-200110),中国药品生物制品检定所提供;大黄酚对照品(批号:110796-201319),中国食品药品检定研究所提供;逢泰胶囊,武汉市元大生物科技有限公司提供;甲醇为色谱纯(Thermo),磷酸为色谱纯(Tedia),超纯水(Milipore制备)。
2 方法与结果
2.1 色谱条件
Shim-pack VP-ODS色谱柱(4.6×250mm,5μm),以十八烷基硅烷键合硅胶为填充剂。流动相:甲醇-0.5%磷酸水溶液(80∶20),流速为1.0mL/min,紫外检测波长为254nm。柱温:30℃,进样量10μL,理论板数按大黄素计算不低于2000,大黄素和大黄酚的分离度>1.5。
2.2 溶液的配制
2.2.1 对照品溶液的制备
精准称取9.14mg大黄素对照品,置于50mL棕色容量瓶中,加入少量甲醇超声溶解后继续用甲醇定容至刻度。摇匀,即得每1mL含有大黄素182.8μg的标准溶液,备用。精准称取10.02mg大黄酚对照品,置于250mL棕色容量瓶中,加入少量甲醇超声溶解后继续用甲醇定容至刻度。摇匀,即得每1mL含有大黄素40.08μg的标准溶液,备用。
2.2.2 供试品溶液的制备
取批次为20180401的逢泰胶囊10粒,取其内容物混合,精密称取0.2g置于10mL棕色容量瓶中,加入适量甲醇溶解,超声提取(300W,250KHZ)处理30min,静置冷却,用色谱纯甲醇定容至容量瓶的刻度,摇匀后用0.22μm微孔滤膜过滤,取滤液即得标准的供试品溶液,备用。
2.2.3 阴性样品溶液的制备
取不含大黄素、大黄酚的阴性样品,同法制备阴性样品溶液。
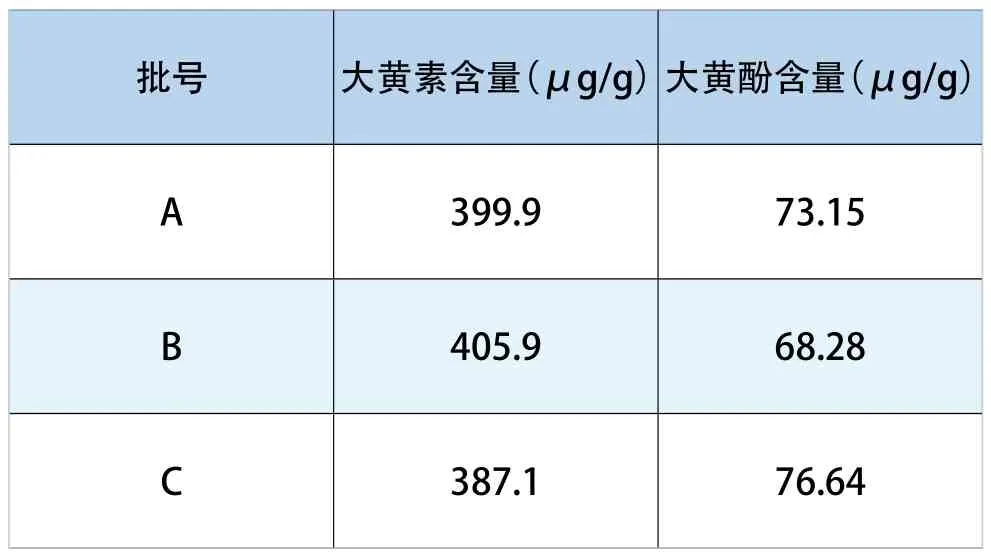
表1 大黄素含量测定结果
2.3 方法学考察
2.3.1 专属性试验
取制备好的对照品溶液、阴性样品溶液、样品溶液分别注入液相色谱仪,记录。结果表明,阴性溶液在大黄素、大黄酚保留时间处并没有出现相应峰,对照品溶液和样品溶液理论板数均大于2000,大黄素和大黄酚的分离度为7.6。
2.3.2 线性关系考察试验
吸取对照品溶液(大黄素质量浓度为182.8μg/mL,大黄酚质量浓度为100.2μg/mL)1.00、2.00、5.00、10.00、20.00mL,分别置于100mL棕色容量瓶中,然后加入甲醇并稀释至刻度,经0.22μm微孔滤膜过滤,按“2.1”步骤选定的色谱条件注入对照品待测液,记录峰面积。以峰面积Y与对照品待测液浓度X进行线性回归,得到回归方程Y=19904X-1776.5(r=0.9999),大黄素在1.828~36.56μg/mL线性关系良好;Y=17692X-577.7(r=0.9999),大黄酚在0.4008~8.016μg/mL线性关系良好。
2.3.3 精密度试验
精密吸取“2.3.2”步骤下所得大黄素和大黄酚对照品混合液线性中第3个浓度5μL,重复进样6次,分别测其峰面积,大黄素的RSD为0.93%,大黄酚的RSD为1.42%。结果表明,仪器和分析方法的可重复性均良好,即精密度较好。
2.3.4 稳定性试验
取同一批次供试品(批号:20180401)按“2.2.2”步骤下的制样方法制备1份供试品溶液,按“2.1”选定的色谱条件分别在供试品溶液制备后0、4、8、12、16、20、24h进样5μL,测定大黄素、大黄酚峰面积,RSD分别为1.46%、1.24%,该结果表明试验溶液在24h内稳定。
2.3.5 重复性试验
精密称取6份批号为20180401的样品,按“2.2.2”步骤的制样方法制备6份供试品溶液,按“2.1”选定的色谱条件下测定大黄素、大黄酚峰面积。结果显示,大黄素和大黄酚峰面积分别为RSD=0.97%、RSD=1.69%,表明该分析方法重复性良好。
2.3.6 加样回收率试验
精密称取批号为20180401的样品6份,分别精密加入0.5mL大黄素、大黄酚对照品溶液。按“2.2.2”步骤的制样方法制备,按“2.1”选定的色谱条件下,测定大黄素、大黄酚峰面积,按照样品含量方法操作并计算,大黄素回收率为101.1%,RSD为1.21;大黄酚回收率为96.7%,RSD为1.53。
2.4 样品测定
精密称取供试品3批,按“2.2.2”步骤的制样方法制备供试品溶液,然后按“2.1”选定的色谱条件,注入高效液相色谱仪进行测定,将所测得的大黄素和大黄酚峰面积代入标准曲线中,各样品两组分含量见表1。
3 结论
本研究与文献报道方法对比发现[4-5],样品用加热回流和超声提取大黄素、大黄酚的提取完全程度基本一致。本研究采用的方法简单便捷、精密度、重现性、稳定性良好,试验操作简单且回收率高,可为保健食品逢泰胶囊质量控制提供依据。
