生物工程角膜移植治疗感染性角膜炎
2019-10-12林莉
林 莉
0引言
感染性角膜炎是我国主要的致盲性眼病之一。严重者可继发角膜穿孔、眼内感染甚至失明。对于药物治疗无效,或角膜濒临穿孔的患者,往往需要手术干预[1]。以往多采取穿透性角膜移植手术,但术后炎症反应较重,排斥机率高[2]。选择结膜瓣遮盖术也是一种治疗手段,但愈后患者角膜瘢痕形成,影响视力恢复[3]。在感染尚未累及后弹力层时,施行深板层角膜移植术,可以尽可能地切除病灶,同时降低了术后免疫排斥的风险。而由于在我国未对器官捐献进行立法,导致角膜供体严重匮乏。在这种情况下,通过我国角膜病学组多位专家的共同努力,成功研发了生物工程角膜(脱细胞角膜基质)。生物工程角膜没有内皮细胞,仅能实施板层角膜移植手术,在一定程度上替代人角膜,缓解供体匮乏的局面。我院自2016-12/2019-02期间收治的感染性角膜炎患者采用生物工程角膜移植治疗,取得较好的疗效,现报道如下。
1对象和方法
1.1对象本组病例为2016-12/2019-02我院眼科收治的感染性角膜炎患者35例35眼。其中真菌性角膜炎14眼,细菌性角膜炎13眼(包括因细菌感染导致的角膜小穿孔1眼),病毒性角膜炎8眼(表1)。男21例,女14例,年龄42~87(平均61.66±13.23)岁。上述病例均经过1wk以上的常规药物治疗,自觉症状没有减轻,眼部感染未能控制,眼表溃疡无明显修复或有穿孔风险。观察组使用生物工程角膜材料施行板层角膜移植手术,共15例15眼。对照1组使用保存人角膜材料施行板层角膜移植手术,共10例10眼。观察组与对照1组为随机分组。对于角膜病灶位于角膜边缘,溃疡面积较大,或者拒绝施行角膜移植手术者,纳入对照2组。对照2组采用自体结膜瓣遮盖的手术方式,共10例10眼。纳入标准:(1)感染性角膜炎,角膜浸润局限于角膜基质层,尚未穿透角膜全层者;(2)角膜穿孔位于角膜周边,穿孔直接小于2mm者。排除标准:(1)真菌性角膜炎有明显内皮斑和前房积脓者;(2)视力高于0.1者不纳入观察组与对照1组;(3)有明显的眼表疾病如重度干眼、神经麻痹性角膜炎、睑裂闭合不全等不纳入观察组和对照1组。本研究经医院伦理委员会批准,所有需要手术的患者,经充分沟通,并告知术中使用材料,包括使用生物角膜的患者,告知生物角膜的来源,取得患者的充分理解和配合的情况下,签署手术知情同意书及特殊耗材使用同意书后进行手术。
1.2方法
1.2.1材料准备观察组使用的生物工程角膜为脱细胞猪角膜基质。对照1组使用的材料为-80℃冰箱冷冻保存的人角膜供体。对照2组使用的材料为自体结膜瓣组织。
1.2.2术前药物保守治疗方法手术治疗前,给予常规的药物保守治疗。术前通过角膜刮片镜检确诊为真菌性角膜炎的患者,局部滴用50g/L那他霉素滴眼液或滴用自配的10g/L伏立康唑滴眼液抗真菌治疗。通过病史及临床表现诊断为细菌性角膜炎的患者,根据临床经验选择针对性的抗生素滴眼液局部点眼治疗,必要时配合全身用药。治疗后根据患者临床表现及药敏培养结果调整药物治疗方案。通过病史及临床表现术前诊断为病毒性角膜炎的患者,同时合并角膜溃疡、细菌感染或坏死性角膜基质炎的情况,予以局部滴用更昔洛韦凝胶,静滴阿昔洛韦抗病毒治疗的同时,给予抗感染、促进角膜修复对症治疗。上述药物保守治疗1wk无效,角膜溃疡未见修复,角膜濒临穿孔或已出现小穿孔的情况下,采取手术治疗的方式。
1.2.3手术方法观察组:术中均采用20g/L利多卡因3mL加7.5g/L布比卡因2mL行球后阻滞麻醉。使用角膜环钻钻切植床,角膜板层刀剖切角膜致完全切除角膜病灶。将生物工程角膜放置于平衡液中复水30s左右,以等大的角膜环钻钻切相应大小的生物工程角膜植片。常规临床上行人板层角膜移植是植床的环钻直径比植片的环钻直径小0.25mm,但生物工程角膜应使用等大的环钻。如植片比植床大,很难完成缝合,即使勉强完成缝合,也将影响切口的愈合。置生物工程角膜植片于角膜植床上,以10-0尼龙线间断对位缝合植片与植床,使植片与植床完全贴合,用无损伤有齿镊对合植床与植片,使植床边缘覆盖于植片之上,以利于角膜上皮移行覆盖在整个植片之上。

表1 三组病例情况 眼
对照1组:术中均采用20g/L利多卡因3mL加7.5g/L布比卡因2mL行球后阻滞麻醉。使用角膜环钻钻切植床,角膜板层刀剖切角膜致完全切除角膜病灶。取出冷冻保存的眼球,平衡液中复水解冻以后,用角膜剪剪下带巩膜的角巩膜植片,以大于角膜植床0.25mm的角膜环钻钻切相应大小的角膜植片,去除植片内皮及后弹力层。置角膜植片于角膜植床上,以10-0尼龙线间断对位缝合植片与植床,使植片与植床对合整齐。
对照2组:术中使用盐酸丙美卡因滴眼液表面麻醉联合20g/L利多卡因结膜下浸润麻醉的方法。冲洗结膜囊后,尽可能完全剔除角膜病灶及坏死组织,保持角膜创面平整,根据角膜病灶范围采取全结膜瓣遮盖或结膜瓣搭桥的方式覆盖角膜病灶,10-0尼龙线间断缝合固定结膜瓣。为保持结膜瓣不过早滑脱,术毕以5-0黑丝线作临时性睑裂缝合1wk。
1.2.4术后用药患者术后继续术前抗感染治疗。真菌性角膜炎患者,使用50g/L那他霉素滴眼液或滴用自配的10g/L伏立康唑滴眼液每天4次点眼。诊断为病毒性角膜炎患者,术后继续阿昔洛韦注射液静滴,连续使用5~7d后改为口服阿昔洛韦片0.4g/次,3次/d,持续口服3mo。口服药物期间,需定期监测肝功能。局部滴用更昔洛韦凝胶每天4次点眼,逐渐减量至每天1次或隔日1次,持续使用6mo[4]。除真菌性角膜炎患者外,角膜植片上皮修复后,加用妥布霉素地塞米松滴眼液每天4次点眼,持续滴用2wk后改为氟米龙滴眼液点眼,逐渐减量,维持治疗6mo。所有角膜移植患者术后均滴用他克莫司滴眼液每天3次预防排斥反应,逐渐减量,维持使用6~12mo。
1.2.5术后随访及观察指标术后患者观察1wk出院,所有出院患者均定期在门诊随访复查。观察组及对照1组患者术后前3mo,平均2wk门诊复查一次,超过术后3mo者,平均1~2mo门诊复查1次。1例最短随访时间为3mo,2例最长随访时间为20mo。对照2组门诊随访时间约3mo。通过裂隙灯观察角膜感染控制情况及角膜溃疡愈合程度;通过裂隙灯观察角膜及角膜植片透明度,有无新生血管生成及移植排斥反应发生;术前术后最佳矫正视力的比较;术后术眼与健眼眼压对比;自觉症状的改善程度。
2结果
2.1术后角膜感染控制情况及角膜溃疡愈合程度术后3~6d,观察组及对照1组行角膜移植手术的病例,无论采用保存人角膜材料或生物工程角膜材料,通过角膜荧光染色,均可见角膜上皮完全覆盖角膜植片。眼表炎症减轻,前房未见明显炎症。随访3~20mo,观察组中15例15眼角膜感染均得到控制,无感染复发情况。除1眼在随访过程中发生植片混浊,其余角膜植片均保持基本透明。该例患者在术后3mo内感染控制,无复发征象,角膜维持透明,随访中,最佳矫正视力0.3。术后4mo,患者角膜植片缝线松动,但未及时复诊拆除缝线,植片边缘糜烂,植片发生混浊。拆除缝线后,予以促进角膜修复治疗,角膜植片再次愈合,但植片未能恢复透明性。术后1wk拆除睑裂缝线,对照2组结膜瓣均覆盖角膜病灶区域,缝线在位,无结膜瓣滑脱情况。除1眼因真菌感染严重,但术前患者拒绝施行角膜移植手术,选择行结膜瓣遮盖姑息治疗,术后15d,结膜瓣逐渐滑脱,角膜溃疡未见修复,真菌感染加重,出现前房积脓,患者疼痛症状明显,选择眼内容物剜除手术。其余病例,术后1mo左右,结膜瓣逐渐退缩,变薄,角膜感染得到控制,角膜溃疡瘢痕愈合,可见新生血管长入病灶区域,角膜上皮完整。

图1 病例1,患者男性,54岁,因左眼疼痛伴视力下降15d就诊,诊断:左眼真菌性角膜炎、2型糖尿病,使用生物工程角膜施行板层角膜移植手术治疗 A:术前视力手动/眼前,左眼裂隙灯照相,角膜中央区域混浊水肿,溃疡形成,基质灰白色浸润,化脓性改变;B:术后即时,生物角膜呈灰白色混浊,与植床贴附好;C:术后7mo,已拆除部分缝线,颞侧有新生血管自角膜缘长入角膜植片,角膜植片基本透明,无感染复发;D:术后18mo,术眼矫正视力0.4,角膜植片基本透明,新生血管未完全消退。
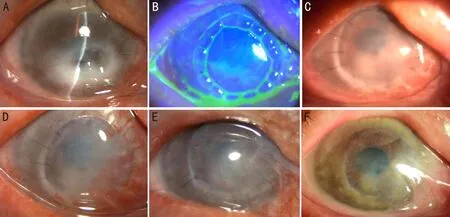
图2 病例2,患者男性,79岁,因右眼疼痛、发红15d就诊,诊断:右眼角膜溃疡、双眼慢性泪囊炎、双眼角膜白斑、双眼年龄相关性白内障。行右眼泪囊摘除术后2d,结膜囊干净,无明显分泌物,泪囊区无红肿,使用生物工程角膜施行板层角膜移植手术治疗 A:术前视力数指/眼前,裂隙灯照相情况,右眼角膜中央偏下方灰白色全层混浊伴溃疡形成;B:术后4d,角膜荧光素钠染色无明显着染,上皮覆盖角膜植片;C:术后12d,因患者全层角膜混浊,植床中下方不透明,但瞳孔区无明显遮挡,植片轻度水肿;D:术后18d,鼻侧大量新生血管长入角膜,角膜植片混浊,使用他克莫司、泼尼松龙滴眼液抗炎、抗排斥治疗;E:术后2mo,炎症逐渐减轻,角膜水肿及新生血管逐渐消退,已拆除部分缝线,鼻侧有胬肉组织长入;F:术后20mo,术眼矫正视力0.05,角膜植片较前明显透明,新生血管大部分消退,鼻侧可见翼状胬肉,晶状体核性混浊,拟行白内障手术。
2.2术后角膜及角膜植片透明度,有无新生血管生成及移植排斥反应发生随访3~20mo,观察组中14眼角膜植片维持基本透明,角膜上皮完整,患者角膜在裂隙灯下的宏观形态见病例1~3(图1~3)。1眼角膜植片混浊。其中2眼因植片靠近角膜缘,术后15d左右即发现有新生血管自角膜缘长入角膜植片与植床层间(病例1、2),经过局部点他克莫司、泼尼松龙滴眼液抗排斥、抗炎治疗后,新生血管逐渐萎缩,炎症反应减轻,持续随访1a,见新生血管未完全消退,但对角膜透明度及视功能没有造成较大影响。对照1组中9眼角膜植片维持透明,角膜上皮完整,未见新生血管长入。1眼因病毒感染复发,新生血管长入,角膜混浊。对照2组9眼角膜溃疡瘢痕修复,角膜不透明,新生血管长入,角膜上皮完整。1眼因真菌感染加重,疼痛症状明显,行眼内容物剜除术。
2.3治疗前后视力对比以最后一次随访复查的视力为术后视力。本研究中,患者以老年居多,大多合并年龄相关性白内障。观察组15例15眼术后最佳矫正视力均较术前提高,无1眼视力下降。其中1眼因细菌感染所致的周边角膜小穿孔,术后最佳矫正视力由术前0.2提高到0.8(7%)。对照1组9例9眼术后最佳矫正视力均较术前提高,1眼视力无改变,术后最佳矫正视力0.3及以上者2眼(20%)。对照2组6眼术后最佳矫正视力较术前提高1~2行,3眼视力无改变。1眼因行眼内容物剜除,由术前视力光感下降为无光感(表2)。
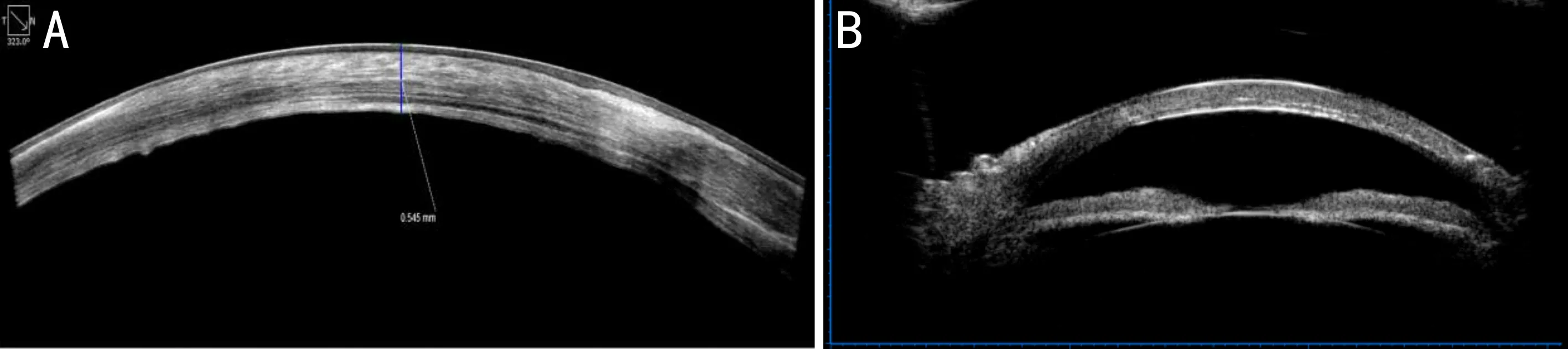
图4 患者术后前节OCT图片和UBM图片 A:前节OCT显示术后18mo角膜情况;B:UBM显示术后18mo角膜情况。
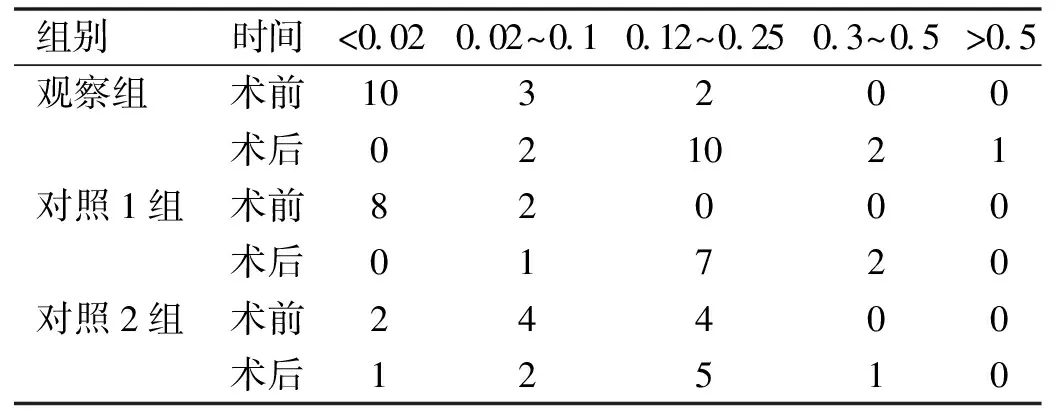
表2 三组术前术后最佳矫正视力对比 眼
2.4术后术眼与健眼眼压对比术后患者于门诊随访,监测眼压情况,根据随访结果发现观察组中术眼较对侧健眼眼压普遍偏低3~6mmHg。术后18mo,前节OCT测量术眼与对侧健眼的角膜厚度无明显差异(图4A)。UBM显示,术后角膜保持正常弧度及表面光滑度(图4B)。而对照组中,术眼与对侧健眼眼压对比无明显差异。
2.5自觉症状改善程度术后1~2wk,观察组患者眼部疼痛、畏光流泪症状均不同程度减轻或消失,1眼于术后4mo因角膜缝线松动致角膜植片边缘溶解,出现眼部异物感等不适症状,予以拆除松动的角膜缝线,配戴角膜绷带镜,促进角膜修复对症治疗后,角膜植片与植床愈合,眼部不适症状消失。对照1组于术后1~2wk眼部疼痛、畏光流泪症状均不同程度的减轻或消失,1眼于术后2.5mo发生病毒感染复发,经药物保守治疗控制后,症状逐渐改善。对照2组除1眼真菌感染加重外,其余9眼于术后1~2wk眼部疼痛、畏光流泪症状逐渐减轻或消失,于术后3wk左右拆除结膜瓣缝线后,眼部刺激症状完全缓解。
3讨论
角膜病是我国的第二大致盲性眼病,角膜盲患者占盲人总数的1/4[1]。面对我国现有的角膜盲患者与逐年增长的角膜盲患者的需求,我国的角膜供体严重不足,绝大多数患者在黑暗中排队等待,有的甚至错过了最佳治疗时机。早在2001年美国加利福尼亚州和中国台湾2个研究小组,则分别报道了通过植入实验室培植的角膜给盲人带来光明的事例,预示着生物角膜将使患者重见光明[5]。张燕等[6]曾对在北京同仁眼科中心实施了角膜移植手术,以及在北京同仁眼库登记拟实施角膜移植手术的患者进行了一个问卷调查,以此来了解角膜盲患者对异种角膜的接受度。结论是大多数角膜移植患者能接受动物角膜的移植,他们主要在意的是使用动物角膜移植的结果。所以,除了因为个人信仰等原因,不论是利用生物角膜还是人角膜供体进行角膜移植手术,只要能带来好的治疗效果,患者普遍是可以接受的。通过前期的开发和临床试验,由我国科学家自主研发的脱细胞角膜基质,全球首个生物工程角膜于2015年获得了上市批准。生物工程角膜是脱细胞猪角膜基质,取材于猪眼角膜,经病毒灭活与脱细胞等工艺制备而成,其主要成分为胶原纤维骨架结构,保留了天然角膜的前弹力层和部分基质层,移植于受体角膜植床以后,由受体的角膜细胞附着、移行、增生到生物角膜基质中去,促进组织再生和修复。其作用机制是在手术切除角膜病灶后,使用生物角膜覆盖于角膜病灶缺损区域,保护角膜创面,引导基质胶原合成及上皮再生,可逐渐被机体细胞所改建,形成与正常角膜相似的结构,恢复角膜的透明性[7]。
生物工程角膜中去除了生物细胞和其他抗原性物质,故术后发生炎症反应和免疫排斥反应的机率较低。张明昌教授等在中国率先开展了生物角膜应用于人体的临床研究,并报道了使用生物角膜移植治疗真菌性角膜感染的病例。最终得出结论,应用脱细胞猪角膜基质进行板层角膜移植治疗真菌性角膜溃疡安全有效,并且还有治疗其他临床疾病的潜力[8]。在本研究中,不论是使用生物角膜或人角膜行板层角膜移植的患者,术后均局部滴用他克莫司滴眼液6mo左右,预防移植排斥反应,在随访的20mo内,生物角膜未见发生严重的排斥反应。作为板层角膜移植的供体,生物角膜主要应用于感染性角膜炎,通过与人角膜供体对比,其透明度接近于人角膜,在植床角膜内皮细胞正常,感染得到控制后,可以维持角膜基本透明。术后上皮完全覆盖角膜植片的愈合时间为3~6d,与人角膜供体移植的愈合时间基本一致。而观察中发现,与人角膜供体不同的是,术后早期生物角膜是一种灰白色不透明的形态,但随着炎症的控制和时间的推移,在术后1mo左右,生物角膜植片逐渐变得透明,水肿完全消失。需要注意的是,术中取材为与植床相等大小的植片,缝合角膜后,对合植片与植床,需要让植床完全覆盖植片边缘,否则上皮难以覆盖角膜植片,植片与植床愈合困难,严重者将出现角膜植片溶解,而导致移植失败。同时我们发现生物角膜术后更早出现缝线松动,需要根据情况,在术后3~7mo即拆除所有角膜缝线。如角膜缝线松动,但未能及时拆除缝线,则有可能形成植片溃疡,进而导致植片的溶解坏死。
病毒性角膜炎的患者因为病毒感染易复发而出现角膜溶解的风险,术后长期、规律的口服及局部使用抗病毒药物对于防止病毒感染复发非常重要。目前生物角膜投入使用的时间尚短,移植术后部分患者可能因为植片愈合不良或感染复发等情况,而出现角膜植片溶解。故确保患者的规律随访复查及依从性可以提高手术成功率以及植片的存活率。对于术后发生病毒感染复发的情况,必要时可以联合羊膜移植或结膜瓣遮盖,促进植片溃疡的愈合,避免植片溶解。
本研究观察组中15例使用生物角膜移植的患者,术中缝合时发现生物角膜植片较人角膜植片偏软,弹性略低于人角膜供体。故术后监测眼压发现术眼眼压普遍低于对侧健眼,考虑与生物角膜的硬度与弹性有关[9]。术中缝合时注意不要过度的牵拉植片,否则将导致植片严重变形,而影响植片与植床的愈合。通过术后前节OCT及UBM检查发现,观察组中所有生物角膜植片愈合后均保持了正常的角膜厚度及弧度,与人角膜供体无明显差异。
Akanda等[10]通过研究发现穿透性角膜移植手术相对于板层角膜移植手术来说,有更高的移植排斥风险和移植失败率。而深板层角膜移植排斥反应较少,且植片存活率增加[11-12]。我们知道,当角膜处于炎性反应活动期时,若行穿透性角膜移植手术,属于高危角膜移植范围,术后免疫排斥反应发生率高,长期预后差,易导致移植失败。对于面积较大,位于角膜周边部的溃疡,药物保守治疗经久不愈的,也可以实施结膜瓣遮盖手术,通过与角膜病变区域的密切接触将结膜的营养物质运送到角膜表面,从而达到抗感染,促进角膜炎症消退和溃疡愈合的目的。同时,结膜瓣遮盖也起到机械性保护创面的作用,减轻局部炎症刺激,加速溃疡修复的过程[13]。结膜瓣遮盖术因为不需要角膜供体,取材于自身,手术过程相对简单,可操作性强,使一些药物治疗无效的复杂性角膜溃疡能尽快愈合,达到控制炎症、挽救眼球的目的,并为患者进一步施行其他手术治疗创造条件。但因角膜溃疡瘢痕愈合,新生血管长入,视力难以恢复。且术后遗留结膜瘢痕,部分患者可能出现睑球粘连等情况,影响外观。所以在感染性角膜炎中,选择病灶未累及角膜全层的病例,通过施行板层角膜移植手术,可及时去除角膜病灶,达到控制感染,提高视力的目的。对于细菌性角膜炎,即使有反应性的前房积脓,术中仍可施行深板层角膜移植,去除角膜坏死组织后,通过角膜侧切口行前房冲洗,清除前房脓液,术后继续抗感染治疗,不影响治疗效果。这种情况下,对于急需手术控制感染,却没有人角膜供体时,使用生物工程角膜是非常好的人角膜供体的替代品。生物工程角膜属于标准化的生产,干燥保存,且有不同厚度,可以满足临床上各类的板层角膜移植需求。在人角膜供体极为匮乏的情况下,为解决逐年增长的角膜病患者与短缺的角膜供体材料之间的矛盾,使用生物工程角膜移植最大程度地替代人角膜供体施行板层角膜移植术,为患者保住眼球,带来复明的希望。
在本研究中,生物角膜的透明度接近于人角膜,在角膜炎症和感染控制、角膜水肿消退以后,可以恢复到基本透明的状态。如植床靠近角膜缘处,容易有新生血管长入植片内,从而引发排斥反应。一般术后5mo左右才开始发现角膜植片上皮下有少量神经纤维长入[14],所以即使移植成功,上皮完全覆盖的角膜植片,后期仍可能出现植片与植床交界处的上皮反复脱落,严重者将发生角膜植片的自溶,需要长期的随访观察,不能掉以轻心。总之,生物工程角膜是一种新型的角膜供体材料,目前尚未得到临床上广泛的应用。对于其临床价值和意义还值得进一步的研究和深入的探讨,以发现生物工程角膜的价值,从而拓宽角膜植片供体的来源,解决角膜供体稀缺的问题,造福越来越多的角膜盲患者。
