宝藿苷Ⅰ减轻链脲佐菌素诱导大鼠海马神经元结构损伤的作用机制研究
2019-09-30尹彩霞陈晶张珏
尹彩霞 陈晶 张珏
【摘 要】 目的:探索宝藿苷I(Baohuoside I)对链脲佐菌素(STZ)所致大鼠神经元结构损伤的影响及其可能的机制。方法:HE、Nissl染色分别观察海马神经元结构损伤情况及存活情况,Western blot检测海马过氧化物酶体增殖物激活受体α(PPARα)和PPARγ的蛋白表达。结果:Baohuoside I高剂量组能减轻大鼠海马神经元结构损伤,阻遏存活神经元数目的减少,上调海马PPARα、PPARγ蛋白表达。结论:Baohuoside I具有改善STZ所致大鼠海马神经元结构损伤的作用,其作用机制可能与上调PPARα、PPARγ的蛋白表达有关。
【关键词】 宝藿苷I;链脲佐菌素;过氧化物酶体增殖物激活受体
【中图分类号】R965 【文献标志码】 A【文章编号】1007-8517(2019)10-0012-05
Study on the Effect and Mechanism of Baohuoside I in Attenuating Streptozotocin-Induced Hippocampal Neuronal Injury in Rats
YIN Caixia CHEN Jing ZHANG Jue*
Zunyi Medical And Pharmaceutical College, Zunyi 563003, China
Abstract: Objective To explore the effect and possible mechanisms of Baohuoside I on neuronal injury induced by streptozotocin(STZ)in rats. Methods HE staining and Nissl staining were used to detect neuronal injury and neuronal survival of hippocampus, respectively; Western blot was used to examine the protein expression of peroxisome-proliferator-activated receptor α(PPARα)and PPARγ. Results Baohuoside I high dose group could attenuate the neuronal injury, inhibit the decrease of the number of surviving neurons, and up-regulate the protein expression of PPARα and PPARγ. Conclusion Baohuoside I has an improvement effect on STZ-induced neuronal injury of hippocampus in rats, and the underlying molecular mechanism may be related to the up-regulation of PPARα and PPARγ.
Key words:Baohuoside I; Streptozotocin; Pperoxisome-Proliferator-Activated Receptor
阿爾茨海默病(Alzheimers Disease, AD)又名阿尔采末病,是老年性痴呆最常见的类型,主要临床表现为持续性记忆丢失和渐进性认知功能障碍[1]。其神经病理学特征主要包括海马和皮质部位神经元的缺失、细胞外β-淀粉样蛋白(β-amyloid,Aβ)沉积形成的Aβ斑(老年斑)、细胞内tau蛋白异常磷酸化形成的神经原纤维缠结[1-2]。其中,Aβ沉积是导致海马神经元病变、引发AD最主要的原因[3],而且研究已经证实过氧化物酶体增殖物激活受体(Peroxisome-Proliferator-Activated receptors,PPARs)可参与调节这一过程[4]。链脲佐菌素(Streptozotocin,STZ)化学名为2-脱氧-2-{(甲基-亚硝基氨基)羰基-氨基}-D-吡喃葡萄糖,是一种具有毒性的氨基葡萄糖-亚硝基脲化合物,可选择性地摧毁胰岛β细胞,使得胰岛素信号途径受阻[5-6] 。除此之外,侧脑室内注射STZ可引发皮质与海马的葡萄糖代谢减慢,导致突触丢失、神经元结构损伤,促进Aβ的异常增加,最终诱导学习记忆功能障碍[7]。目前,应用STZ诱导海马神经元结构损伤建立AD动物模型已被广泛用于体内实验研究[8-10]。迄今为止,临床用于抗AD的药物(如胆碱酯酶抑制剂加兰他敏、NMDA受体拮抗剂美金刚)只能延缓AD的病程及发生,又因其毒副作用大,使得疗效受限。因此,基于AD的发病机制探索新型AD治疗药物迫在眉睫。
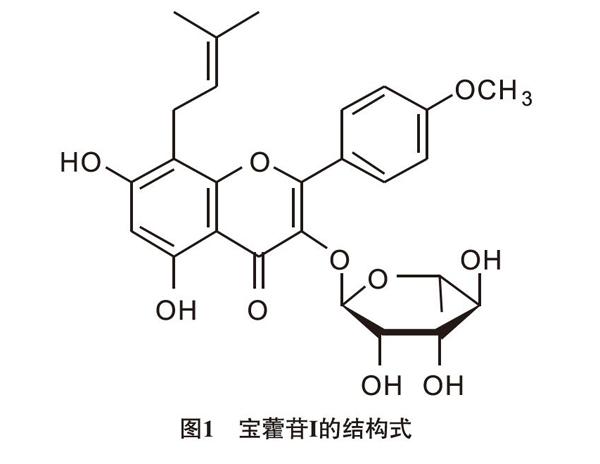
宝藿苷Ⅰ(Baohuoside I)又称淫羊藿次苷II,是我国传统中草药淫羊藿(Herba Epimedii)的基本药用活性成分之一,属于天然黄酮醇苷类化合物,具有抗炎、减轻缺血性脑损伤、抗肿瘤、改善性功能障碍等多种药理学作用,其分子量为514.53,结构式如图1所示[11-14]。而且,新近研究发现Baohuoside I减轻缺血性脑损伤的机制与PPARα、PPARγ的上调有关[13]。值得注意的是,已有研究证实Baohuoside I 可通过增加PPARγ的蛋白表达,从而抑制BACE1的转录,促进Aβ代谢,最终减轻APP/PS1转基因小鼠的学习记忆下降及海马神经元结构损伤,起到抗AD的作用[15]。此外,本课题组研究发现Baohuoside I能改善侧脑室内注射STZ所致的AD大鼠认知功能减退及海马神经元结构损伤,其机制与阻遏Aβ的异常增加有关[8],同时综合上述的前期研究我们推测PPARα、PPARγ参与了这一过程。因此,本研究继续采用STZ诱导的类AD样大鼠模型,探索Baohuoside I减轻该模型大鼠神经元结构损伤的机制是否与PPARα、PPARγ有关,为Baohuoside I用于AD的防治提供新的药理学依据。
1 材料与方法
1.1 实验材料
1.1.1 实验动物 本研究所用的40只成年雄性SD大鼠购买于重庆第三军医大学实验动物中心,均为SPF级,体重260g~270g,许可证号为SCXK-(军)2012-0011。大鼠以每笼5只适应性饲养一周后进行实验。
1.1.2 主要药品、试剂、仪器设备 链脲佐菌素(货号S0130)购自美国Sigma公司;宝藿苷I(纯度≥98%,批号140701)购于南京泽朗医药有限公司;甲苯胺蓝购于北京索莱宝科技有限公司;PPARα兔多克隆抗体及PPARγ兔多克隆抗体均购于英国Abcam有限公司;β-actin小鼠单克隆抗体购自江苏碧云天生物技术有限公司;SR-6N大鼠脑立体定位仪购自日本东京Setagaya.ku 公司;全波长酶标仪及Quantity One-全自动凝胶成像分析仪购自美国BIO-RAD公司;BX43正置显微镜购于日本Olympus 公司。
1.2 实验方法
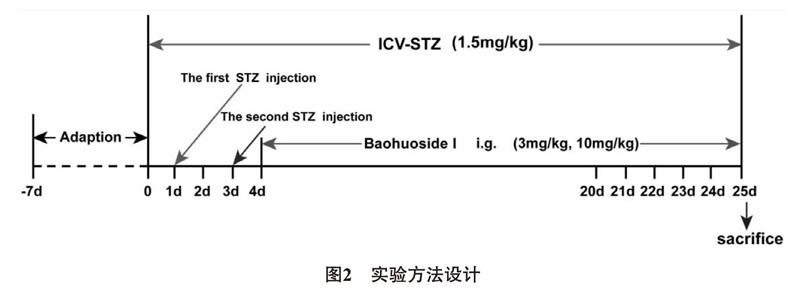
1.2.1 动物分组、造模及给药方法 将40只成年雄性SD大鼠随机均分为4组:假手术组、STZ组、Baohuoside I低剂量组、Baohuoside I高剂量组。用7%水合氯醛将大鼠麻醉(0.5 mL /100 g,i.p),然后再将其头部固定于大鼠脑立体定位装置上,沿头皮中间位置切一矢状切口,根据《大鼠脑立体定位图谱》确定大鼠侧脑室进针坐标(前囟后0.8mm,中线旁开1.5 mm,颅骨下3.6mm)进行模型的制备。STZ组和Baohuoside I低、高剂量组大鼠经微量注射器在第1天和第3天分别向双侧侧脑室匀速推注STZ(浓度为1.5mg/kg,用0.05mmol/L 柠檬酸缓冲液配置,并调节pH 值为 4.2,需现配现用,冰上操作)5μL,同法向假手术组大鼠双侧侧脑室推注等体积溶媒(柠檬酸缓冲液)。第3天手术结束后次日开始给药,Baohuoside I经双蒸水溶解,低剂量组每日灌胃Baohuoside I 3mg/kg,高剂量组每日灌胃Baohuoside I 10mg/kg,连续给药21d,假手术组和STZ组同法灌胃等体积双蒸水,同时监测大鼠体重的变化。实验方法设计如图2所示。
1.2.2 HE染色、Nissl染色 大鼠经Baohuoside I给药结束后,各组随机抽取3只,用4%多聚甲醛进行透灌,透灌结束后立即断头取脑,取下的全脑用4%多聚甲醛溶液固定5d,进行常规石蜡包埋,最后将蜡块切片(厚度为5μm),置于60℃烘箱中粘片,分别进行HE染色(主要用苏木素、伊红染色)和Nissl染色(主要用甲苯胺蓝染色),BX43正置显微镜观察海马神经元结构损伤情况及海马神经元的存活情况。
1.2.3 Western blot檢测蛋白表达 Baohuoside I给药结束后,处死大鼠,冰上分离双侧海马,置于-80℃低温冰箱保存备用。称取海马组织50mg,用RIPA裂解液提取总蛋白,蛋白浓度用BCA试剂盒进行检测。制备含20μg蛋白的上样样本,用10% SDS-聚丙烯酰胺凝胶电泳将蛋白进行分离。电泳结束后,用电转的方式将蛋白转至PVDF膜上,5%的脱脂牛奶封闭120 min,加入一抗(PPARα,1∶1000;PPARγ,1∶1 000;βactin,1∶5000)于 4℃孵育过夜,再加入二抗(1∶2000)于常温孵育60min。二抗反应结束后,相应的条带用ECL发光剂显影,并置于全自动凝胶成像分析仪中测定泳带的吸光度积分值。
1.3 统计学分析 所有数据均用SPSS 16.0统计软件进行单因素方差分析,并用均数加减标准差(x±s)表示。P<0.05为差异有统计学意义。
2 结果
2.1 Baohuoside I对STZ诱导的大鼠海马神经元结构损伤的影响 HE染色观察大鼠海马神经元结构损伤情况。如图3所示,假手术组大鼠海马神经元结构清晰完整,无明显损伤;STZ组大鼠海马神经元萎缩,核出现深染甚至消失,损伤严重;Baohuoside I高剂量治疗后,大鼠海马神经元结构较为清晰完整,损伤明显减轻。
2.2 Baohuoside I对STZ诱导的大鼠海马存活神经元数目减少的影响 尼氏染色观察大鼠海马存活神经元情况。如表1及图4所示,假手术组大鼠海马神经元形态正常,结构清晰完整;STZ组大鼠海马神经元萎缩,存活神经元数量显著减少;Baohuoside I高剂量治疗后,大鼠海马神经元少有萎缩,存活神经元数量明显增加。
2.3 Baohuoside I对大鼠海马PPARα蛋白表达的影响 Western blot检测大鼠海马PPARα蛋白表达。如表2及图5所示,与假手术组比较,STZ组PPARα 蛋白表达增加;Baohuoside I高剂量连续给药21 d后,显著增加了STZ 大鼠海马PPARα的蛋白表达。
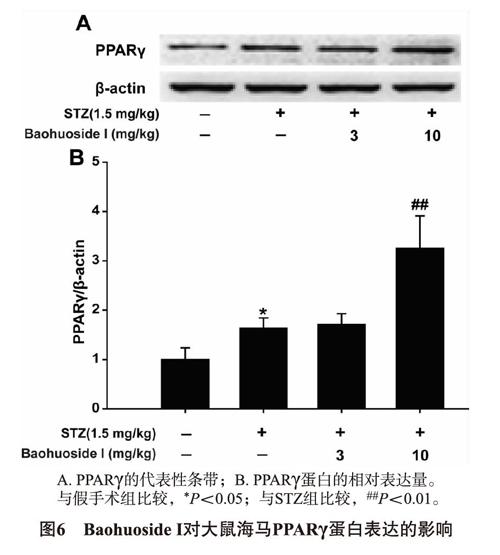
2.4 Baohuoside I对大鼠海马PPARγ蛋白表达的影响 Western blot检测大鼠海马PPARγ蛋白表达。如表3及图6所示,与假手术组比较,STZ组PPARγ 蛋白表达增加;Baohuoside I高剂量连续给药21d后,显著增加了STZ 大鼠海马PPARγ的蛋白表达。
3 讨论
AD是一种由多因素导致的中枢神经系统退行性疾病,其初始阶段主要表现为脑内胰岛素抵抗引起的胰岛素信号障碍和葡萄糖摄入不足引起的葡萄糖代谢减慢[1, 16]。STZ作为一个有毒的烷基化氨基葡萄糖-亚硝基脲化合物,可激活聚腺苷酸二磷酸核糖转移酶[poly (ADP-ribose) polymerase,PARP],使DNA发生烷基化,进而导致细胞坏死[6]。近年来,大量研究表明双侧侧脑室内注射STZ可引起胰岛素受体功能障碍、葡萄糖代谢率降低,最终表现出Aβ异常增加、tau蛋白异常磷酸化、海马神经元受损缺失、突触丢失等类似于AD的病理学特征[7, 17]。因此,本研究采用STZ双侧侧脑室注射诱导类AD样大鼠模型,探索Baohuoside I能否减轻该模型大鼠的神经元结构损伤及初探其可能的机制。众所周知,海马和皮质部位的胆碱能神经元缺失变性是AD的特征性病理学变化之一[18]。本研究采用HE染色观察大鼠海马CA2区神经元的形态,结果显示STZ组大鼠海马神经元变性且核固缩,结构明显受损,与Rostami等的研究一致[17],提示大鼠经双侧侧脑室注射STZ后可引起海马神经元结构损伤。与此同时,大鼠经Baohuoside I 10mg/kg治疗后神经元结构损伤得到明显缓解。由此可见,Baohuoside I 10 mg/kg可阻遏STZ组大鼠的海马神经元受损缺失。值得注意的是,Baohuoside I 3mg/kg连续给药不能减轻STZ诱导的大鼠海马神经元损伤,提示Baohuoside I在本实验条件下的阈剂量大于3 mg/kg。神经元的功能状态主要由尼氏小体反映,尼氏小体数量多且体积大,说明神经元合成蛋白质的功能较强。然而,一旦神经元受到损伤,尼氏小体就会溶解甚至消失。因此,本研究采用尼氏染色法对海马神经元存活情况进行检测,结果表明STZ组大鼠尼氏小体的数目明显减少,与前期研究一致[8]。长期给予Baohuoside I 10mg/kg治疗后大鼠尼氏小体的数量显著增多。由此可见,Baohuoside I 10 mg/kg可阻遏STZ诱导的大鼠海马存活神经元数目的减少,进而维持海马存活神经元的数量。
实际上,本课题组前期研究已经证实,Baohuoside I可通过减少淀粉樣前体蛋白APP(amyloid precursor protein,APP)、β-分泌酶(β-site APP cleavage enzyme,BACE1)的蛋白表达抑制Aβ的生成,同时还能增加脑啡肽酶(neprilysin,NEP)的蛋白表达促进Aβ的代谢,最终减少Aβ的异常增加,改善STZ诱导的大鼠学习记忆功能障碍,起到抗AD的作用。而且,越来越多的研究表明在AD动物模型脑内Aβ的减少与PPARα、PPARγ密切相关[4]。PPARα、PPARγ均属于核转录因子,在激活状态下,能与视黄素x受体形成异质二聚体,形成的异质二聚体可与过氧化物酶体增殖物反应元件结合,调控基因的表达[4-19]。其中,PPARα激活后可上调α-分泌酶(a disintegrin and metalloproteinase domain 10, ADAM10)的基因表达,使APP降解,从而减少Aβ的生成。而PPARγ激活后能抑制BACE1的转录,调控APP的进程,从而影响Aβ的生成。此外,PPARγ对Aβ的清除具有促进作用[4]。由此可见,PPARα和PPARγ在Aβ的生成、代谢过程中均起着至关重要的作用。综上所述,笔者推测本课题组前期研究发现的Baohuoside I减少STZ大鼠脑内Aβ异常增加的机制与PPARα和PPARγ的激活有关。因此,本研究采用Western blot法检测大鼠海马PPARα和PPARγ的蛋白表达。本实验结果发现STZ组大鼠海马PPARα和PPARγ的蛋白表达高于假手术组,同时Baohuoside I 10mg/kg给药组PPARα和PPARγ的蛋白表达明显高于STZ组,与Li等的研究结果类似[20]。此结果提示,Baohuoside I 10 mg/kg可通过激活PPARα和PPARγ,减少STZ诱导的Aβ异常增加。然而,为什么STZ组PPARα和PPARγ的蛋白表达高于假手术组,可能与STZ制模时的时间点有关,这是本课题组后续研究的重点。
总之,本研究证实了PPARα和PPARγ参与了侧脑室内注射STZ诱导的大鼠海马神经元结构损伤的调控过程,加深了课题组对AD脑内Aβ异常增加机制的认识。Baohuoside I可减轻STZ诱导的大鼠海马CA2区神经元结构的损伤,其机制与PPARα和PPARγ的激活有关。
参考文献
[1]Bazazzadegan N, Dehghan Shasaltaneh M, Saliminejad K, et al. Effects of Ectoine on Behavior and Candidate Genes Expression in ICV-STZ Rat Model of Sporadic Alzheimers Disease [J]. Adv Pharm Bull, 2017, 7(4):629-636.
[2]Dos Santos JPA, Vizuete A, Hansen F, et al. Early and Persistent O-GlcNAc Protein Modification in the Streptozotocin Model of Alzheimers Disease [J]. J Alzheimers Dis, 2018, 61(1):237-249.
[3]Jiao C, Gao F, Ou L, et al. Tetrahydroxy stilbene glycoside (TSG) antagonizes Abeta-induced hippocampal neuron injury by suppressing mitochondrial dysfunction via Nrf2-dependent HO-1 pathway [J]. Biomed Pharmacother, 2017(96) :222-228.
[4]Vallee A, Lecarpentier Y. Alzheimer Disease:Crosstalk between the Canonical Wnt/Beta-Catenin Pathway and PPARs Alpha and Gamma [J]. Front Neurosci, 2016(10):459.
[5]Shingo AS, Kanabayashi T, Murase T, et al. Cognitive decline in STZ-3V rats is largely due to dysfunctional insulin signalling through the dentate gyrus [J]. Behav Brain Res, 2012, 229(2):378-383.
[6]Grieb P. Intracerebroventricular Streptozotocin Injections as a Model of Alzheimers Disease:in Search of a Relevant Mechanism [J]. Mol Neurobiol, 2016, 53(3):1741-1752.
[7]Knezovic A, Osmanovic Barilar J, Babic A, et al. Glucagon-like peptide-1 mediates effects of oral galactose in streptozotocin-induced rat model of sporadic Alzheimers disease [J]. Neuropharmacology, 2018(135):48-62.
