烟气脱硫中间产物CaSO3无氧热分解的研究
2019-09-07袁晓东杨忠董林齐誉乔秀文洪成林李洪玲王金但建明
袁晓东,杨忠,董林,齐誉,乔秀文,洪成林,李洪玲,王金Ⅰ,但建明*
(1 石河子大学化学化工学院/省部共建国家重点实验室培育基地/新疆兵团化工绿色过程重点实验室/材料化工新疆维吾尔自治区重点实验室,新疆 石河子832003; 2 新疆天业集团,新疆 石河子832003;3 南京大学化学化工学院江苏省机动车尾气污染控制重点实验室,江苏 南京210000)
我国能源消费以煤为主,2017年煤炭产35.2 亿吨,其中电煤消耗约19.43 亿吨[1]。我国煤炭磷、硫含量较高[2],因此其造成了SO2的大量排放[3],约占SO2排放总量的80%-90%[4-5],因此我国政府规定燃煤电厂必须安装脱硫装置进行脱硫减排[6]。目前燃煤烟气脱硫的主流工艺是石灰石/ 石灰- 石膏湿法脱硫技术[7],约占脱硫技术的90%左右,该方法最终产物为脱硫石膏。脱硫石膏在我国的综合循环利⒚率较低[8],大部分以填埋的方式处理,既占⒚大量的土地资源,污染了环境,同时又浪费了钙硫资源[9-10]。国内外研究者提出将脱硫石膏还原分解为SO2和CaO,实现进行钙硫资源的循环回收利⒚[11]。但该法还原分解温度较高,需加还原剂,导致工艺复杂,成本较高,限制了其推广[12],故需开发烟气脱硫副产物循环利⒚的绿色新途径[13-14]。
烟气脱硫主要包括SO2吸收生成CaSO3·0.5H2O(以下简称 CaSO3)和CaSO3氧化两个过程[15]。其中CaSO3需要在大量氧气的作⒚下被氧化生成CaSO4·2H2O,即通过大功率的罗茨风机对脱硫塔中的CaSO3浆液进行曝气处理,增加浆液中的溶解氧含量以促进CaSO3氧化成CaSO4·2H2O。CaSO3的氧化过程速度慢,反应时间长,是脱硫工程的控制过程[16],需要耗费大量的电能和时间[17],据统计,烟气脱硫电耗约占燃煤电厂自身发电能力的10%左右,导致脱硫运行费⒚较高。故有必要简化脱硫工艺,降低脱硫的运行费⒚。
本文提出将烟气脱硫过程控制在生成CaSO3阶段,对该段产物CaSO3进行热分解,将CaO 应⒚于循环脱硫,回收SO2制备化工产品[17]。㈦脱硫石膏的还原分解相比,CaSO3的热分解具有分解温度低、且无需还原剂的特点[18-19],同时简化了现有的脱硫工艺,降低脱硫运行费⒚[20],还提供脱硫资源[21]。基于此,本文以分析纯CaSO3模拟脱硫中间产物CaSO3,研究热分解条件对CaSO3热分解影响的规律,以期为烟气脱硫中间产物CaSO3的循环利⒚提供理论和实际指导。
1 实验部分
1.1 实验试剂和仪器
1.1.1 实验试剂
CaSO3购自上海晶纯生化科技股份有限公司,分析纯;蔗糖、氢氧化钠、碳酸钠购自天津市致远化学试剂有限公司,分析纯; 盐酸购自石河子北生物商贸有限公司,分析纯;酚酞、甲基橙购自天津市福晨化学试剂厂,分析纯;氮气、氩气、氧气购自石河子宏晟供气站,工业纯度。
1.1.2 仪器设备
DYT-270D 烘箱,东莞市鼎耀机械设备科技有限公司;FA2004-200G-0.0001G 精密电子分析天平,北京梓航浩海商贸有限公司;TL1200-S Mini 管式炉,广州儒瑞科技有限公司;DF-101S 磁力搅拌器集热式恒温加热水油浴锅搅拌机,郑州泰洪升仪器有限公司;BRUKER-D8-ADVANCE X 射线衍射仪。
1.2 实验方法
1.2.1 实验步骤
首先检验管式炉密闭性㈦通气性; ⒚电子天平准确称取经105 ℃干燥的CaSO32.0000g,将装CaSO3坩埚放入高温管式炉刚Ⅰ管中间; 缓慢打开气体罐通入N2至排尽炉膛内空气;接通管式炉电源并设置热分解温度、 热分解时间、 热分解升温速率及N2流量实验参数;反应时将热分解产生的SO2混合气体通入碱液安全瓶内;热分解结束后,在N2气氛下待炉内温度冷却至室温,取出样品; 称量热分解产物质量,测试产品中CaO 的含量;记录实验数据,计算CaO 产率并对样品进行XRD 物相分析。
1.2.2 热分解产物CaO 的测定及计算
根据HG/T 4120-2009 标准分析热分解产物,按照下式计算CaO 含量。
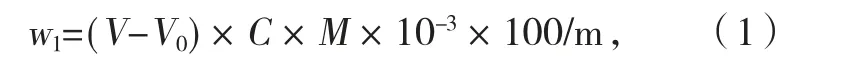
式中:w1是氧化钙(CaO)的质量分数,以%表示;V是滴定试验溶液所消耗的盐酸标准滴定溶液体积的数值,单位为毫升(mL);V0是滴定空白试验溶液所消耗的盐酸标准溶液体积的数值,单位为毫升(mL);C是盐酸标准滴定溶液浓度的准确数值,单位为摩尔每升(mol/L);m是产品质量的数值,单位为克(g);M是氧化钙(1/2CaO)摩尔质量的数值,单位为克每摩尔(g/mol)(M=28.04)。
2 实验结果㈦讨论
2.1 热分解气氛对热分解产物CaO 含量的影响
在热分解温度1100 ℃,热分解时间2 h,热分解升温速率6 ℃/min,气流量200 mL/min,进行CaSO3热分解,并对热分解产物CaO 的含量进行测试。热分解气氛对CaO 含量的影响如图1所示。
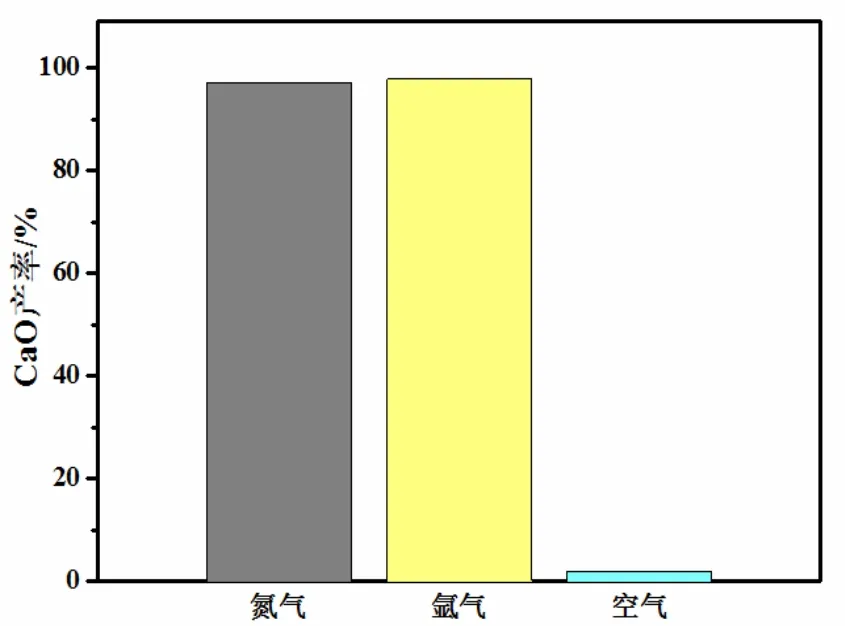
图1 热分解气氛对CaO 含量的影响Fig.1 Effect of thermal decomposition atmosphere on CaO content
由图1可知: 在N2和Ar 惰性气体气氛下,CaSO3热分解产物CaO 含量分别为85.33% 和85.94%,空气气氛下CaO 含量为2.03%,因此在有氧的条件下不利于CaSO3热分解产物CaO 和SO2的生成,隔绝空气即在无氧环境(N2和Ar 惰性气体)保护下有利于CaSO3热分解产物CaO 的生成。
为验证气氛中O2对热分解的影响,相同热分解条件下,实验了N2氛围下不同O2含量对热分解产物中CaO 含量的影响,结果见图2。由图2可知:随着N2气氛中O2含量的增加,CaSO3热分解产物CaO含量逐降低;在N2气氛下CaSO3热分解产物CaO 含量为85.94%,在空气氛下CaSO3热分解产物CaO 含量最低,为2.03%。
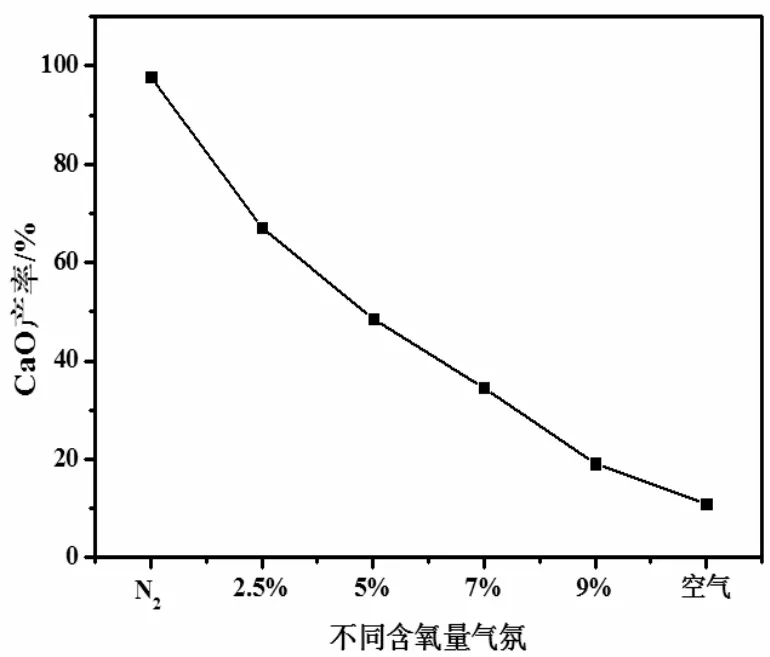
图2 热分解气氛中含氧量对CaO 含量的影响Fig.2 Effect of oxygen content in thermal decomposition atmosphere on CaO content
热分解气氛对 CaSO3热分解产物CaO 含量的影响主要㈦O2对CaSO3的氧化有关。在无氧热分解气氛下,CaSO3可完全热分解为CaO; 在含氧热分解气氛下,热分解产物CaO 含量降低,主要是因为在有O2存在的热分解气氛中,CaSO3会被氧化为CaSO4[22],O2含量越高,被氧化为CaSO4的量越大,从而产物中CaO 含量越低。
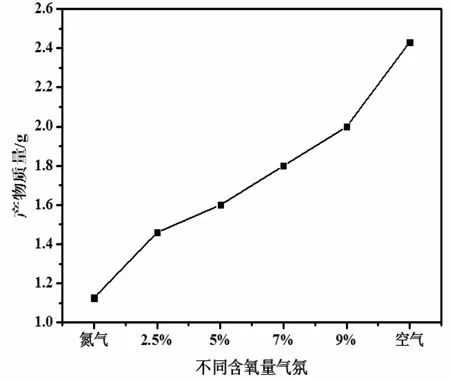
图3 O2 含量对产物质量的影响Fig.3 Effect of O2 content on product quality
这也可从热分解气氛O2含量㈦热分解产物质量的关系图3中得到确认,CaSO3热分解产物质量随热分解气氛O2含量提高而增加。因此选择热分解气氛为无氧气氛,以防止高温情况下CaSO3被氧化为CaSO4,从而降低产物中CaO 含量和SO2收率。另外,从经济角度相比于氮气和氩气价格,应⒚氮气为保护气氛较好。
以下实验均在氮气气氛下进行热分解。
2.2 热分解温度对热分解产物CaO 含量的影响
在N2气氛,热分解时间2 h,热分解升温速率6℃/min ,N2流量200 mL /min,进行CaSO3热分解,并对热分解产物CaO 的含量进行测试。热分解温度对CaO 含量的影响如图4所示。由图4可知:随着热分解温度的升高,CaSO3热分解产物中CaO 含量逐渐上升,热分解温度低于1000 ℃,CaO 含量提高比较缓慢,1000 ℃时热分解产物CaO 含量仅为16.97%; 热分解温度高于1000 ℃,CaSO3热分解产物CaO 含量提高迅速,最终CaSO3热分解产物CaO含量高达97.87%,几乎完全分解。
这表明CaSO3在N2保护的无氧热分解气氛中,主要受热力学控制,升高热分解温度能加快反应速率。对样品进行整体加热,使其热分解速率增加,促进CaSO3热分解为CaO 和SO2。因为CaSO3热分解为强吸热过程,根据计算ΔH>0,随着热分解温度的升高,将促进该反应的进行,且该反应在热分解温度高于1000 ℃时,ΔG<0,反应开始自发进行,因此热分解温度升高促进CaSO3热分解为CaO 和SO2。

图4 热分解温度对CaO 含量的影响Fig.4 Effect of thermal decomposition temperature on CaO content
2.3 热分解时间对热分解产物CaO 含量的影响
在N2气氛,热分解温度1150 ℃,热分解升温速率6 ℃/min,N2流量200 mL /min,进行CaSO3热分解,并对热分解产物CaO 的含量进行测试。热分解时间对CaO 含量的影响如图5所示。由图5可知:随着热分解时间的延长增加,CaSO3热分解产物CaO含量逐渐上升,热分解时间低于0.5 h 时,CaSO3热分解产物CaO 含量增长较快,当热分解时间从0.5 h 增至2 h 时,CaSO3热分解产物CaO 含量增长变缓,最终CaSO3热分解产物CaO 含量高达99.58%,几乎完全分解。
这表明CaSO3热分解产物为CaO 和SO2时,热量由外向内传递,外部生成的CaO 包覆在CaSO3表面,由于CaO 导热能力较差,使该过程热量的传递缓慢,需要较长的时间,所以延长热分解时间有利于CaSO3热分解产物为CaO 和SO2。
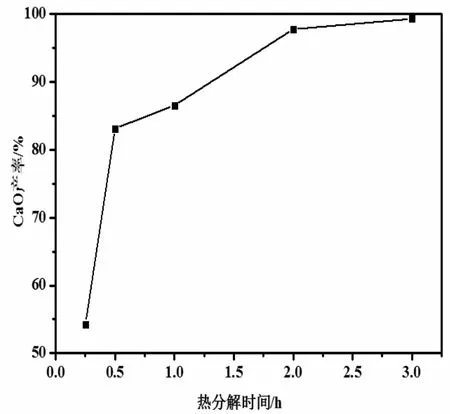
图5 热分解时间对CaO 含量的影响Fig.5 Effect of thermal decomposition time on CaO content
2.4 热分解升温速率对热分解产物CaO 含量的影响
在N2气氛,热分解温度1150 ℃,热分解时间2 h,N2流量200 mL /min,进行CaSO3热分解,并对热分解产物CaO 的含量进行测试。热分解升温速率对CaO 含量的影响如表1所示。由表1可知:随着热分解升温速率的增加,CaSO3热分解产物CaO 含量逐渐出现小幅度下降,热分解升温速率在3-6 ℃/min之间,CaSO3热分解产物CaO 含量基本保持在99%左右,热分解升温速率在6-9 ℃/min 之间,CaSO3热分解产物CaO 含量出现小幅度下降,但是整体变化不大,最终CaSO3热分解产品CaO 含量高达99.77%,几乎完全分解。
以上结果说明CaSO3热分解产物为CaO 和SO2时,当热分解升温速率提高,但热传导和热分解温度滞后,这是因为试样内部存在一定的热度梯度,热分解升温速率较快时,热分解的程度并不完全,所以产生了相对的温度滞后现象; 另外,不同热分解升温速率将造成热分解反应时间的差异从而造成传递的热量减少,进而造成反应不彻底,CaO 含量出现小幅度降低。

表1 热分解升温速率对CaO 含量的影响Tab.1 Effect of heating rate of pyrolysis on CaO content
2.5 N2 流量对热分解产物CaO 含量的影响
在N2气氛,热分解温度1150 ℃,热分解时间2 h,热分解升温速率6 ℃/min,进行CaSO3热分解,并对热分解产物CaO 的含量进行测试,N2流量对CaO含量的影响如图6所示。由图6可知:随着N2流量的增加,CaSO3热分解产物CaO 含量先增加后基本不变然后逐渐出现小幅度下降,N2流量在25-80 mL/min 之间,CaSO3热分解产物CaO 含量逐渐增加,N2流量在80-200 mL/min 之间,CaSO3热分解产物CaO 含量出现小幅度下降,但是整体变化不大,N2流量在200-300 mL/min 之间,CaSO3热分解产物CaO 含量下降变快。
上述结果说明CaSO3热分解产物为CaO 和SO2时,随N2流量增加时,另外一个热分解产物SO2被带走,从而促进平衡向正向进行,从而CaO 含量上升,但是当N2气流量增加时,相当于大量冷气体进入,从而吸收大量的热量,将大量的热量带出反应体系之外,造成在一定热分解时间内反应体系热量减少,从而热分解产物CaO 和SO2含量降低。
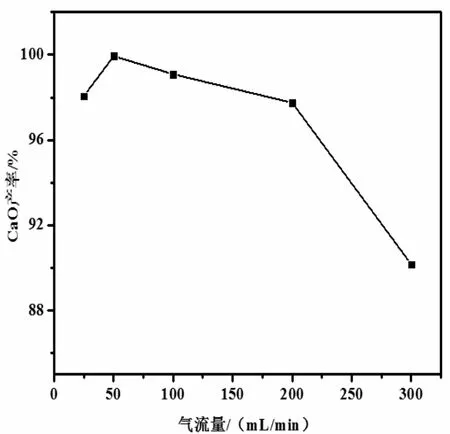
图6 N2 流量对CaO 含量的影响Fig.6 Effect of N2 flow rate on CaO content
2.6 CaSO3 热分解产物XRD 分析
由以上实验结果可知,热分解温度对CaSO3热分解产物CaO 含量影响最为显著,于是对不同热分解分解温度下,CaSO3热分解产物进行XRD 分析,结果如图7所示。由图7可知: 热分解温度700 ℃-900,CaSO3热分解产物为较多CaSO4、CaS,少量的CaO,分解温度为1000 ℃,CaSO3热分解产物为较多CaSO4、CaS、CaO,热分解温度为1100 ℃,CaSO3热分解产物为较少CaSO4、CaS,较多CaO,热分解温度为1150 ℃,CaSO3热分解产物为较多CaO,微量CaSO4、CaS。因此在热分解温度1150 ℃,CaSO3热分解产物几乎完全为CaO。
以上结果说明在无氧氛围热分解温度较低的情况下,CaSO3热分解反应主要为自身歧化反应,从而产生较多的CaSO4、CaS,在无氧氛围热分解温度较高的情况下,CaSO3热分解反应主要为热分解反应,从而产生较多的CaO 和SO2。

图7 CaSO3 热分解产物X- 射线衍射图谱Fig.7 X-ray diffraction patterns of thermal decomposition products of CaSO3
2.7 CaSO3 热分解正交实验分析
由正交优化试验结果(表2)可知:在热分解温度、热分解时间、N2流量、热分解升温速率四因素中,热分解温度在正交优化实验直观分析中极差最大。这表明热分解温度对CaSO3热分解产物CaO 含量影响最为显著,热分解时间次之,其次是热分解升温速率,N2流量对CaSO3热分解产物CaO 含量影响最小。
由正交优化实验方差分析结果(表3)可知:在热分解温度、热分解时间、N2流量、热分解升温速率四因素中,热分解温度的F比大于F临界值,所以在此⒚数学的方法的得出热分解温度对CaSO3热分解产物CaO 含量影响最为显著,且各因素在影响效率上依次为:热分解温度>热分解时间>热分解升温速率>N2流量,从而得出优化条件为:热分解温度1150 ℃、 热分解时间2 h、 热分解升温速率6 ℃/min、N2流量80 mL/min。
在优化条件下,经过3 次验证实验,CaO 含量分别为99.62%,99.62%,98.73%,最终得出CaSO3热分解产物CaO 平均含量为99.32%,继而证明CaSO3在优化条件下几乎完全分解为CaO 和SO2。
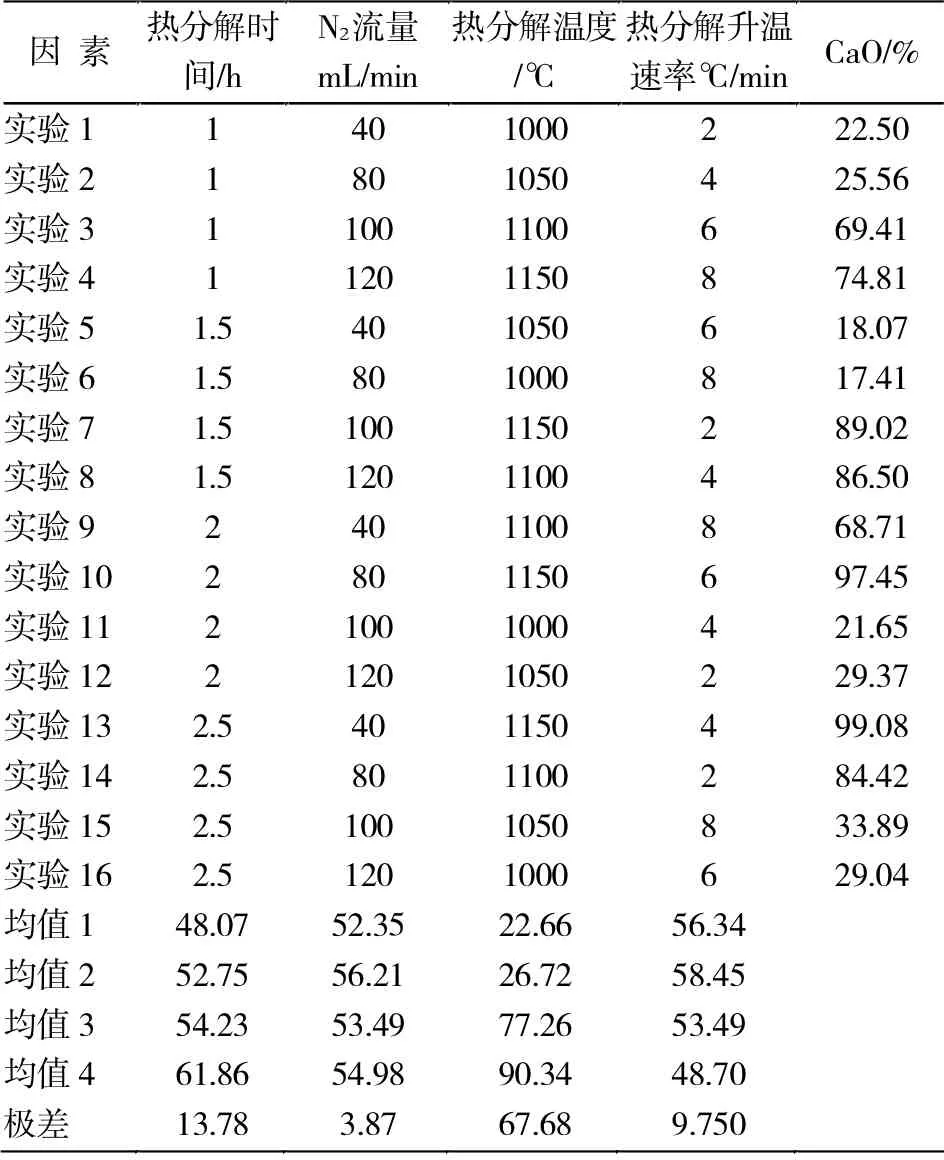
表2 正交优化实验Tab.2 orthogonal optimization experiment
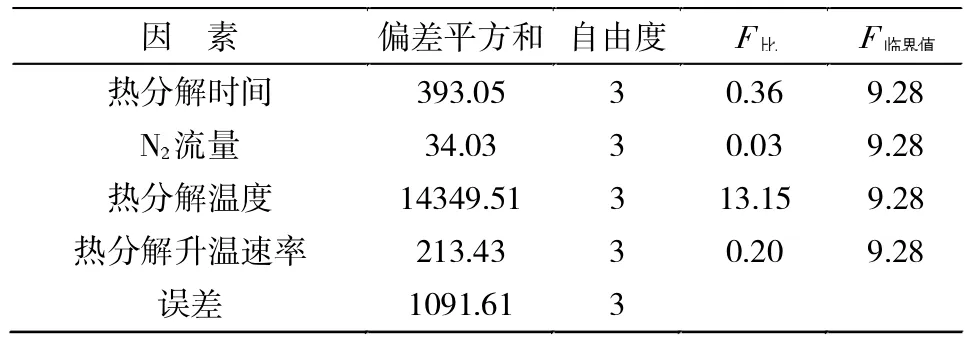
表3 正交优化实验方差分析Tab.3 Analysis of variance of orthogonal optimization experiment
3 结论
(1)在相同的热分解温度下,无氧氛围条件下比有氧氛围下CaSO3热分解产物CaO 含量高。在热分解温度、热分解时间、N2流量、热分解升温速率四因素中,热分解温度对CaSO3热分解产物CaO 含量影响最为显著,为主要因素,4 种影响因素对CaSO3热分解产物CaO 含量影响的顺序为: 热分解温度>热分解时间>热分解升温速率>N2流量。
(2) 在热分解温度为700-1000 ℃时,CaSO3热分解产物CaO 含量较低,CaO 含量为16.71%,其热分解产物多为歧化产生的CaSO4、CaS; 在热分解温度为1100-1150 ℃时,CaSO3分解得到热分解产物CaO 含量较高,其CaO 含量为99.32%,几乎完全分解为CaO 和SO2。
(3)CaSO3热分解得到热分解产物CaO 和SO2的优化条件为: 热分解温度1150 ℃、 热分解时间2 h、热分解升温速率6 ℃/min、N2流量80 mL/min。在该优化条件下进行三次验证分析,最终CaSO3热分解产物CaO 含量平均值为99.32%。
