美罗培南与亚胺培南/西司他丁在治疗重症感染患者中的安全性Meta分析
2019-09-02罗少华罗骞
罗少华 罗骞
(1 广东省医学科学院,广东省人民医院,广州 510055;2 广州医科大学附属第五医院,广州 510799)
碳青霉烯类抗生素(carbapenems)是20世纪70年代发展起来的一类抗菌谱最广、抗菌活性最强的,具有新型结构的β-内酰胺类抗生素,亚胺培南/西司他丁和美罗培南是其中最常用的两种。在过去约20年中,国内外均进行了多项比较美罗培南与亚胺培南/西司他丁治疗重症感染疗效差异的试验,近年来也陆续报道了碳青霉烯类药物在临床上的使用,对其进行疗效观察、不良反应监测等。然而即使是在试验患者临床特征相似且干预特征相同的情况下,各个试验研究所得的结果仍存在不太一致的情况,且各个研究纳入的病例数量有限[1]。Meta分析是将研究目的相同的多个研究结果进行加权合并和综合评价的一种方法,它能够提高统计检验效能,解决研究结果间的不一致性,使研究结论更加适合于人群总体[2]。 按照Cochrane系统评价的要求,本文收集自1990年以来国内外发表的关于两药治疗重症感染的研究文献,运用Meta分析方法对MEPM和IPM/CST治疗重症感染的安全性进行比较,旨在为临床提供安全合理使用的依据。
1 材料与方法
1.1 检索策略
在CNKI、维普、万方、CBM、PubMed等数据库,检索年限均从1990年—2018年2月。英文检索词包括:meropenem、imipenem、imipenem plus cilastatin和carbapenems。中文检索词包括:美罗培南、亚胺培南、亚胺培南/西司他丁、碳青霉烯和重症感染。
1.2 纳入标准
1.2.1 研究类型
国内、外的随机对照试验(RCTs);原始文献为国内外已公开发表的全文文献,不限制是否使用盲法,提供MEPM组、IPM/CST组不良反应(ADR)例数;语种限制为中文和英文。
1.2.2 研究对象
患者(种族和性别不限,年龄≥16岁)有明确的细菌性感染指征,经临床诊断或实验室检查确诊为以下重症感染中的一种或几种感染合并存在:下呼吸道感染;腹腔感染;泌尿道感染或者脓毒症等。
1.2.3 干预措施
两个随机试验组治疗干预措施为美罗培南和亚胺培南/西司他丁,治疗条件具有可比性。
1.2.4 结局指标
原始文献须有明确的不良反应发生率及不良反应的症状描述等。
1.3 排除标准
(1)文献未及不良反应的;(2)文献类型为个案报道、硕、博士学位论文、综述、评价性文章;(3)重复研究或发表的文献;(4)两药与其他抗生素配对试验的RCTs。
1.4 统计学处理
统计分析使用Rev-Man 5.3软件对本系统评价关注的指标进行合并效应量分析,二分类变量资料采用比值比(OR)及其95%可信区间(95%CI)为Meta分析统计量。首先检验异质性,检验标准设为0.10,试验间异质性采用χ2检验,P>0.1,I2<25%时为研究间无统计学异质性;若无异质性,采用固定效应模型(fixed effect model,FEM)进行数据合并分析;如存在异质性,可采用随机效应模型(random effect model,REM)进行合并分析。
2 结果
2.1 文献筛选结果
初步检索得到英文文献257篇(有3篇英文文献无法追溯,1篇为意大利文,剩余英文文献253篇),中文文献225篇。通过Endnote去重和手工去重后剩余中文文献135篇,英文文献253篇;通过阅读排除入选41篇文献,其中英文文献12篇[3-14],中文文献29篇[15-43]。
2.2 美罗培南和亚胺培南/西司他丁治疗重症感染的不良反应发生率比较
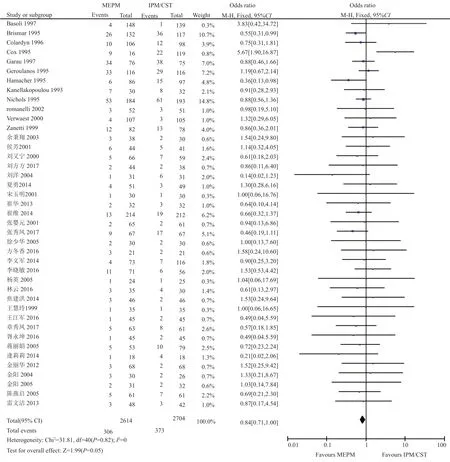
图1 MEPM和IPM/CST治疗重症感染不良反应发生率的Meta分析—森林图Fig.1 Meta analysis of adverse effects rate for MEPM compared with IPM/CST in the treatment of severe infections (forest)
合并分析,森林图结果见图1。同质性检验:χ2=31.81,df=40,P=0.82>0.10,I2=0<25%,可认为各研究是同质的,可以采用FEM进行分析。分析结果显示合并效应量OR=0.84,95%CI=0.71~1.00,森林图中其对应横线与无效竖线相交,且该横线基本全都在无效竖线左侧,合并效应量的检验结果Z=1.99,P=0.05近似临界值,表明差异具有临界的统计学意义,但是证据尚不足以证明MEPM在治疗重症感染时的不良反应发生率比IPM/CST低。对于MEPM在治疗重症感染时的不良反应发生率是否低于IPM/CST,需要更多的文献支持。
针对两组的不良反应发生率进行发表偏倚分析,结果见图2,从漏斗图中可以看出,大部分研究处于“倒漏斗”的上部,而基底部研究少,图形左右基本对称,SE(logRR)范围为0.25~1.4左右,可认为所纳入文献无明显偏倚。
2.3 不良反应发生率亚组分析
在所纳入文献中,提取关于不良反应发生率的数据涉及下呼吸道感染、腹腔感染两个不同病种,故根据不同病种做亚组分析,探究重症感染中不同疾病的不良反应发生率情况。
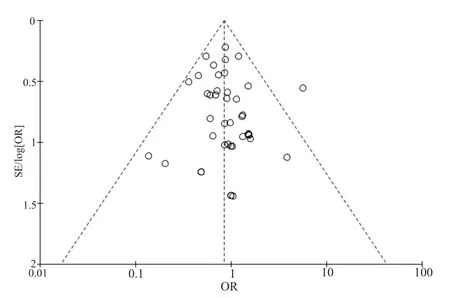
图2 MEPM和IPM/CST治疗重症感染不良反应发生率的Meta分析—漏斗图Fig.2 Meta analysis of adverse effects rate for MEPM compared with IPM/CST in the treatment of severe infections (funnel)
(1)在下呼吸道感染亚组中,共纳入19个研究,经合并分析,森林图详见图3。同质性检验:χ2=7.67,df=18,P=0.98>0.10,I2=0<25%,可认为各研究间是同质的,可以采用FEM进行分析。分析结果显示合并效应量OR=0.65,95%CI=0.46~0.91,森林图中其对应横线与无效竖线不相交,且该横线在无效竖线左侧,差异有统计学意义(Z=2.54,P=0.01<0.05),故可认为MEPM在治疗下呼吸道感染时的不良反应发生率低于IPM/CST。

图3 MEPM和IPM/CST治疗重症感染不良反应发生率的亚组分析—森林图Fig.3 Subgroup analysis of the incidence of adverse reactions rate for MEPM and IPM/CST in the treatment of severe infections (forest)
(2)在腹腔感染亚组中,共纳入5个研究,经合并分析,森林图详见图3。同质性检验:χ2=5.23,df=4,P=0.26>0.10,I2=23%<25%,表明所纳入文献的同质性较好,该研究的异质性可忽略,可以采用FEM进行分析。分析结果显示合并效应量OR=0.87,95%CI=0.62~1.23,森林图中其对应横线与无效竖线相交,差异无显著统计学意义(Z=0.79,P=0.43>0.05),MEPM与IPM/CST在治疗腹腔感染的不良反应发生率无显著性差异。
针对两个亚组的不良反应发生率进行发表偏倚分析,结果见图4,从漏斗图中可以看出,其图形左右基本对称,大部分研究处于“倒漏斗”的上部而基底部研究少,提示该研究无明显发表偏倚。
2.4 美罗培南和亚胺培南/西司他丁治疗重症感染的不良反应症状比较(表1)
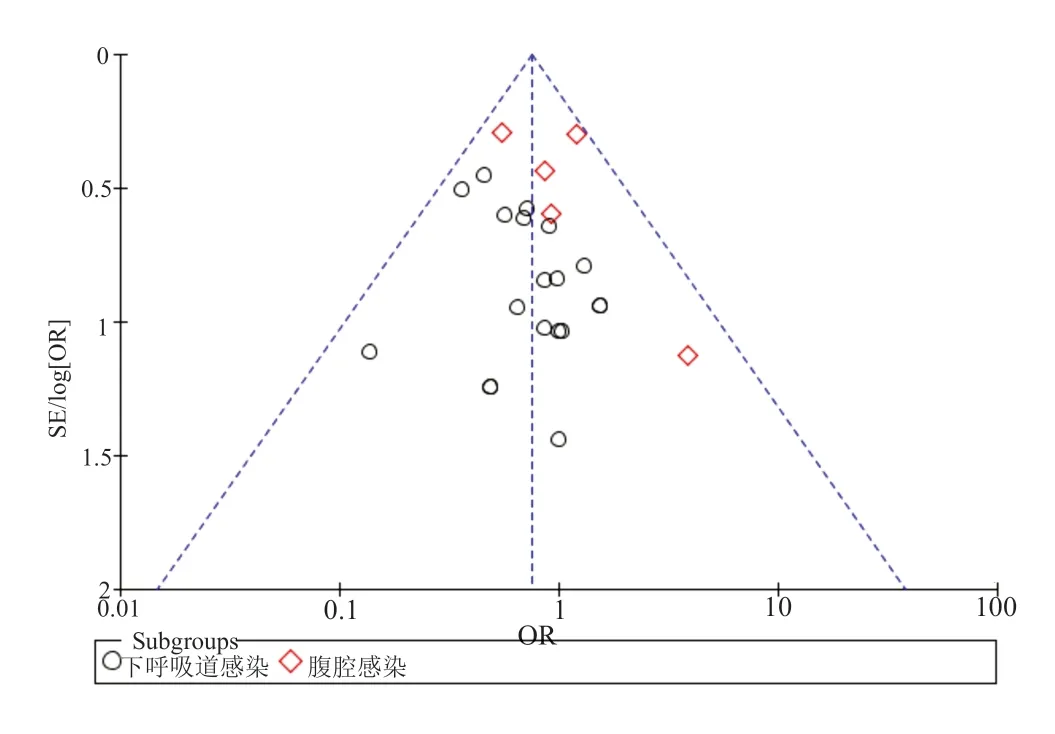
图4 MEPM和IPM/CST治疗重症感染不良反应发生率的亚组分析—漏斗图Fig.4 Subgroup analysis of the incidence of adverse reactions rate for MEPM and IPM/CST in the treatment of severe infections (funnel)
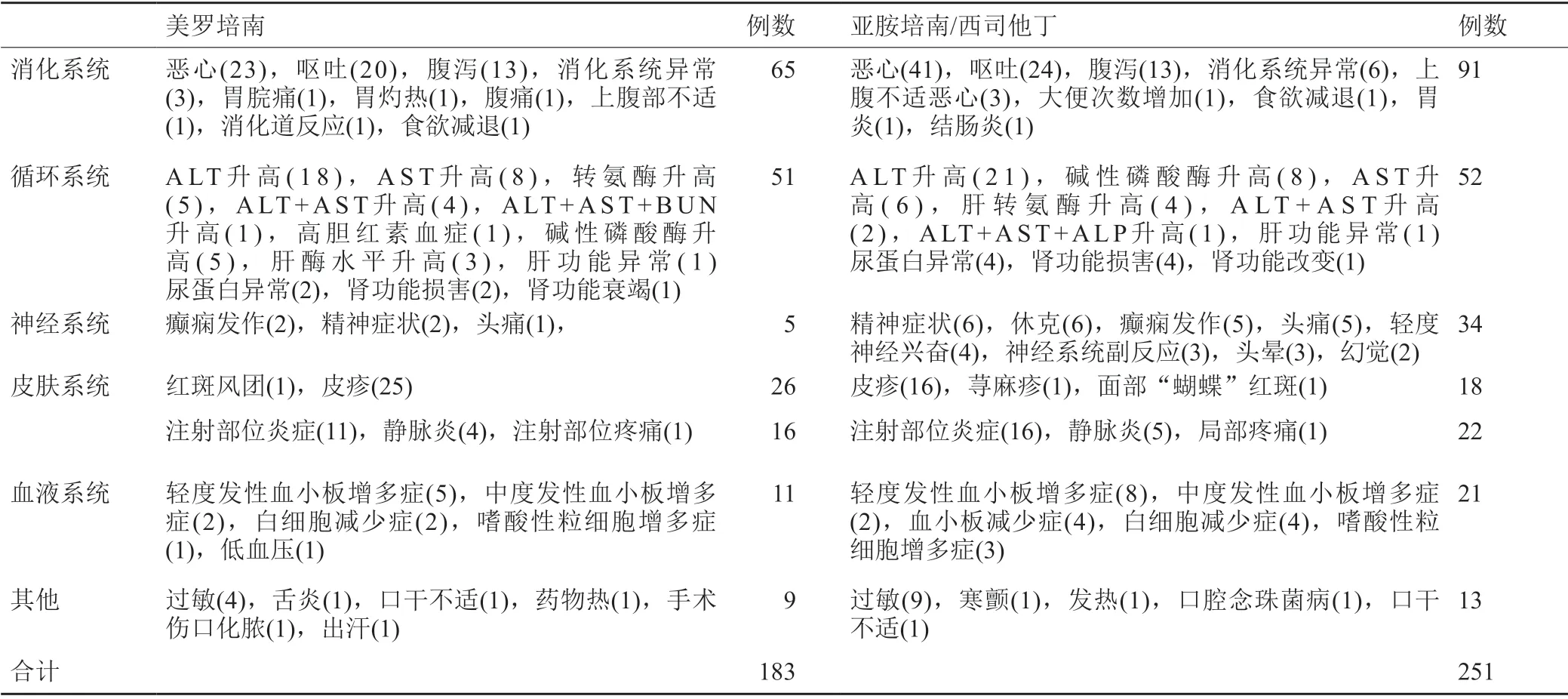
表1 美罗培南和亚胺培南/西司他丁治疗重症感染的不良反应症状Tab.1 Symptoms of adverse reactions of meropenem and imipenem/cilastatin in the treatment of severe infections
将文献中不良反应的症状进行列举分析,总体看亚胺培南/西司他丁的不良反应的多过美罗培南的。从不良反应的症状显示,消化系统的不良反应最多,循环系统、皮肤及注射部分次之。两者之间进行比较,亚胺培南/西司他丁在消化系统、静脉炎或注射部位炎症、神经系统及血液系统中发生的例数高于美罗培南。引起皮疹的例数后者多于前者。其他症状的例数相差不大。
3 讨论
目前,国内外均进行了多项比较MEPM与IPM/CST治疗重症感染疗效及安全性差异的试验,但各个试验研究的结果仍存在不太一致的情况[1]。本文收集自1990年以来国内外发表关于两药治疗重症感染的文献,采用Meta分析方法及对美罗培南与亚胺培南/西司他丁的安全性方面进行了比较。
本次研究结果整体上看不能说明美罗培南的不良反应发生率比亚胺培南/西司他丁低(P=0.05)。在重症下呼吸道感染的亚组结果中,美罗培南的不良反应发生率低(P=0.01)。在治疗腹腔感染的亚组中,所得结果无统计学意义(P=0.43)。从症状上看两者消化系统的不良反应最多,循环系统、皮肤及注射部分次之。美罗培南引起皮疹多于亚胺培南;两者对肝肾功能的影响相当;而亚胺培南/西司他丁在其他系统中发生的不良反应例数都高于美罗培南。尤其神经系统的影响亚胺培南/西司他丁大于美罗培南。亚胺培南/西司他丁[44]不适用于有癫痫或精神病史及严重中枢神经系统疾患的患者。美罗培南[45]与中枢神经系统γ-氨基丁酸受体亲和力较亚胺培南低,因此癫痫等中枢神经系统不良反发生率比后者显著为低[46]。有研究对于有癫痫的患者,在足够的抗癫痫药治疗的情况下,使用亚胺培南剂量≤2g/d和美罗培南并不会增加癫痫发生率[47]。
本研究存在一定不足:①由于各研究中疾病的严重程度差异及其他基础疾病的存在,或者文献质量低造成偏倚过大。②各研究治疗方案用药剂量区间为1.0~4.0g/d,用药方法为bid或tid,用药时间也不尽相同,可能会对研究的结果产生影响。③亚组分析中对于腹腔感染目前可纳入文献有限,此处结果有一定的局限性。
综上亚胺培南/西司他丁不良反应发生例数多于美罗培南,发生率总体上相当。不同的患者要个体化给药,如用药易引起皮疹的患者选用亚胺培南。胃肠道疾病、中枢神经系统疾病的选用美罗培南。
