聚偏氟乙烯微孔滤膜-聚多巴胺-氧化石墨烯固相萃取结合离子迁移谱快速检测尿液中的麻黄碱
2019-07-27柴常伟崔毅轩管宇珊王子晗
柴常伟,刘 迪,崔毅轩,管宇珊,庞 羽,王子晗,蒋 晔
(河北医科大学 药学院,河北 石家庄 050017)
随着经济的发展,机动车给人带来方便的同时,交通事故也给驾驶人及路人造成不可逆伤害[1]。目前,因饮酒、非法药物使用及药物滥用后驾车已成为交通事故的主要原因[2-6]。药驾(Driving under the inference of drugs,DUID)[7-8]指在药物的影响下驾驶,易诱发交通事故。影响驾驶能力的药物根据标准有不同的分类结果[9-11]。依据药效作用分类,主要包括毒品类、中枢神经系统兴奋剂、中枢神经系统抑制药、三环类抗抑郁药物、抗糖尿病药物、抗高血压药物、抗组胺药等[11]。当今,交通管理部门对于禁止酒驾的宣传及检查已相对完善,但对于药驾方面的交通安全宣传和整治却迫在眉睫。同时,高空驾驶人员(如飞机驾驶员)的不合理用药而引起的药物不良反应也给飞行人员健康和飞行安全带来危害和隐患[12-14]。为进一步规范驾驶行为并保证交通、飞行安全,建立药驾在线检测和现场监察的方法刻不容缓。
麻黄碱(Ephedrine,EPH)作为生物碱类的中枢神经系统兴奋剂,通过人体代谢,主要经肾脏以原形从尿液中排泄[15],具有发汗、平喘、利尿、抗炎、抗过敏、镇咳、祛痰、解热、抗菌、抗病毒等药用功效,被广泛应用于医药领域[16]。然而,由于EPH引发的神经过敏、耳鸣、失眠、血压升高、头痛、头晕、心慌、血糖升高、心前区疼痛、心动过速、心动过缓、心律失常等不良反应[17-19],会严重影响驾驶安全,因此建立尿液中EPH的快速检测尤为重要。目前,已报道的关于麻黄碱的检测手段很多[16],主要包括光谱法、色谱法[20-26]、电泳法[27-29]、联用技术[22-24,26]等,其中光谱法[16]主要用于制剂中EPH的检测;色谱法、电泳法、联用技术广泛应用于尿液中的EPH检测,但这些实验室检测手段由于仪器体积及分析时间的限制,不适合现场快检。对于尿液中EPH的前处理方法主要包括液液萃取(Liquid-liquid extraction,LLE)[20-21,25-26,28-29]和固相萃取(Solid phase extraction,SPE)[22-24]。但LLE萃取和溶剂转换过程需消耗大量时间;SPE需活化、淋洗、洗脱等繁琐步骤,且吸附不具有特异性。由此可见,已有的前处理方法和检测手段均不适用于尿液中EPH的现场快速检测。
氧化石墨烯(GO)是一种由单层碳原子构成的呈蜂窝状的二维平面薄膜,主要由碳原子和极性含氧官能团组成,位于表面的羟基和环氧基,以及处于边缘的羧基使其具有极强的亲水性[30]。GO作为一种新型吸附剂,被广泛应用于固相萃取[31-34]。便携式高分辨离子迁移谱(Portable high resolution ion mobility spectrometry,PHR-IMS)作为一种大气压下对带电物质进行分离的检测技术,具有灵敏度高、分析速度快、体积小、便携等优点,因此广泛应用于爆炸物的检测。随着离子迁移谱(IMS)的发展,其在药物分析方面的应用崭露头角[35-37]。基于此,本文首次采用聚偏氟乙烯微孔滤膜(PVDF)为支撑载体,GO为萃取剂,聚多巴胺为交联剂,交联GO与PVDF,建立了聚偏氟乙烯微孔滤膜-聚多巴胺-氧化石墨烯固相萃取(Polyvinylidene fluoride microporous membrane-polydopamine-graphene oxide solid phase extraction,PVDF-PD-GO-SPE)结合PHR-IMS快速检测尿液中EPH的分析方法,PVDF膜几分钟即可完成吸附过程,相比于搅拌棒[33],显著节省了吸附时间,可为药驾在线检测和现场监察提供有效手段。
1 实验部分
1.1 仪器与试剂
Excellims GA2100高效离子迁移谱仪,电喷雾离子源,进样方式为直接进样。VisIon Analysis分析软件(Analysis_2_3_1_23);Sartorius BP 211D(十万分之一,上海耀壮检测仪器设备有限公司)电子天平;Milli-Q 50超纯水系统;T1901 双光束紫外可见分光光度计(北京谱析通用仪器有限公司);FTIR-8400S 红外光谱仪(日本岛津公司);S-3500扫描电子显微镜(日本日立公司);DF-101S集热式恒温加热磁力搅拌水浴锅(巩义市科华仪器设备有限公司)。
聚偏氟乙烯微孔滤膜(F型)(上海兴亚净化材料厂,规格Φ50 mm);甲醇(色谱纯,Fisher公司);盐酸麻黄碱(纯度>98%,中国药品生物制品检定所,批号:714-8501);氧化石墨烯为实验室自制,经紫外光谱、傅立叶红外光谱、扫描电镜表征;盐酸多巴胺(纯度>99%,山东西亚化学工业有限公司);三羟甲基氨基甲烷(Tris试剂纯度>99%,天津光复精细化工研究所);急支糖浆(太极集团重庆涪陵制药厂有限公司);所用其它试剂均为分析纯。健康受试者尿样于-20 ℃冰箱中保存。
1.2 溶液的配制
1.2.1 聚多巴胺-Tris-HCl缓冲溶液的制备称取Tris试剂约0.363 g于300 mL水中溶解,用浓盐酸调节pH值至8.5,得10 mmol/L的Tris-HCl溶液;称取约0.6 g的盐酸多巴胺于10 mmol/L的Tris-HCl溶液中溶解,超声搅拌至溶液呈棕黑色,即得2 mg/L的聚多巴胺-Tris-HCl缓冲溶液。
1.2.2 盐酸麻黄碱对照品的制备精确称取盐酸麻黄碱对照品25.82 mg于25 mL容量瓶中,加甲醇稀释至刻度,制得质量浓度为1.033 mg/mL的盐酸麻黄碱甲醇对照品储备溶液。取甲醇储备液制备1.033 μg/mL的麻黄碱甲醇溶液。
精确称取盐酸麻黄碱对照品12.37 mg于100 mL容量瓶中,加水稀释至刻度,得质量浓度为123.7 μg/mL的盐酸麻黄碱水溶液储备液。
1.2.3 加标样品溶液的制备取近期未服用含有麻黄碱药品的健康成年人尿液作为空白样品进行测定。分别取123.7 μg/mL的盐酸麻黄碱水溶液储备液0.25、1.0、5.0 mL于100 mL容量瓶中,用空白尿样进行稀释,得0.309、1.237、6.185 μg/mL 3个质量浓度水平的加标样品溶液。
1.3 PVDF-PD-GO-SPE的制备
参考文献[33-34]制备氧化石墨烯,并采用紫外光谱、傅立叶红外光谱、扫描电镜表征,结果与文献报道一致。取20 mg氧化石墨烯超声分散于20 mL水中,即得1 mg/mL氧化石墨烯溶液,于4 ℃保存备用。首先将聚偏氟乙烯微孔滤膜用甲醇清洗,干燥。然后将干燥好的滤膜放入聚多巴胺-Tris-HCl缓冲溶液中,于30 ℃水浴中搅拌12 h。待反应完成后,将滤膜干燥,即得聚多巴胺涂层的滤膜。然后将其放入氧化石墨烯溶液(1 mg/mL)中,于65 ℃水浴中反应10 h后取出,干燥。重复以上步骤2次,即得具有一定厚度的氧化石墨烯镀层滤膜(PVDF-PD-GO-SPE)。再将该膜用甲醇超声清洗10 min,干燥,待用。
1.4 样品前处理
吸附过程:将萃取膜卷成管状置于10 mL离心管中,加入加标尿样溶液10 mL,涡旋吸附5 min,弃去样品溶液;去基质过程:用5 mL超纯水清洗萃取膜及离心管,弃去洗涤水,重复3次;洗脱过程:加入甲醇1 mL,涡旋洗脱10 min,洗脱液待测。操作流程见图1。
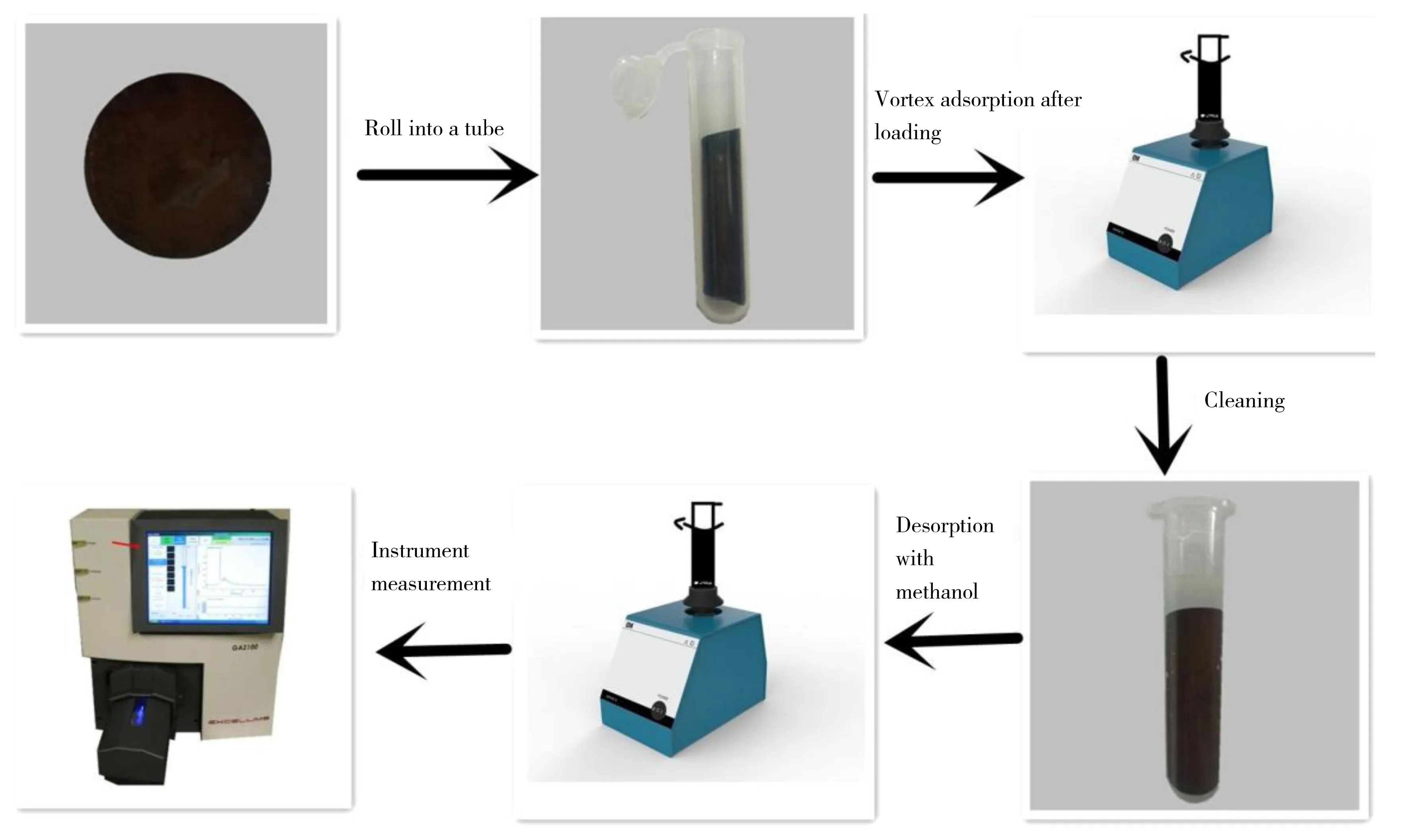
图1 样品处理过程示意图Fig.1 Schematic of the experimentation
1.5 IMS分析
进样前,取校正溶液对仪器进行校正,校正完成后,取样品溶液30~40 μL,进行IMS分析。IMS工作模式为正离子模式,源电压2 800 V,迁移管电压8 400 V,气体进样温度170 ℃,迁移管温度170 ℃,门电压宽度120 μs,门电压50 V,谱图时长26 ms;溶剂延迟0 ms,谱图叠加10次,采集运行时长10 s,采集速率200 K Samples/Sec;排气泵速率1.25 L·min-1,迁移气速率1.00 L·min-1;直接喷雾进样流速1.0 μL·min-1,进样针直径1.46 mm。
2 结果与讨论
2.1 IMS操作参数优化
为提高EPH在离子迁移谱上的响应强度,从而进一步提高检测灵敏度,实验取1.033 μg/mL麻黄碱甲醇溶液进样,对离子迁移谱的主要检测参数如迁移管电压(7 500~8 500 V)、迁移管温度(140~180 ℃)、门电压(40~90 V)、门宽度(80~130 μs)进行了优化,优化范围上限依据仪器所允许的最大值界定。
迁移管电压和迁移管温度是影响待测物响应强度及分辨率的重要参数,因此实验考察了迁移管电压和迁移管温度对响应强度及迁移时间的影响。结果显示,迁移时间与迁移管电压呈现负相关(r2=0.998);响应强度在7 500~8 400 V范围内与迁移管电压呈正相关(r2=0.991),且在8 400V时响应强度最大,因此迁移管电压以最优值8 400 V为仪器使用条件。在优化范围内,迁移管温度与迁移时间呈现负相关(r2=0.980);而迁移管温度与响应强度无相关性,但在170 ℃时的响应强度最大。迁移管电压与温度对迁移时间负相关的依赖性,表明带电离子在迁移管内的迁移行为的改变不可忽略。
离子化物质具有一定的能量才能克服门电压的限制进入迁移管,同时门电压限制了其他弱电物质进入迁移管,增大待测物的响应强度,但若门电压过高,待测物能量过低则进入迁移管的量降低,降低了待测物响应强度,通过实验优化,发现门电压为50 V是最适条件。另外,门宽度越大,进入迁移管的待测物响应越高,但同时基线波动越大,灵敏度越低,因此选择门宽度为120 μs。
2.2 PVDF-PD-GO-SPE镀膜次数的优化
考察了聚多巴胺-氧化石墨烯镀膜次数(0、1、2、3次)对PVDF-PD-GO-SPE吸附性能的影响(图2),结果显示,未镀膜的空白PVDF膜(曲线E)对EPH有少量吸附,吸附率为1.6%,而镀膜之后(曲线B、C、D)的PVDF-PD-GO-SPE对EPH萃取效率显著提高,因此空白膜的少量吸附可以忽略,且镀膜2次(曲线C)与3次(曲线B)的萃取效率无明显差异,为了节约时间成本,本研究选择PVDF-PD-GO-SPE镀膜2次。

图2 PVDF-PD-GO-SPE镀膜次数的优化Fig.2 The optimization of coating times on PVDF-PD-GO-SPEA.ephedrine control peak,B.coating three times,C.coating two times,D.coating one time,E.blank film
2.3 萃取过程的优化
2.3.1 样品溶液及洗脱溶剂体积的优化实验考察了吸附过程中,样品溶液体积(2、5、10 mL)对EPH响应强度的影响。结果显示,当样品溶液体积为2、5 mL时,涡旋顺利进行,响应强度为0.541~0.607 V;当样品溶液体积为10 mL时,样品溶液处于震荡状态,涡旋操作受限,响应强度为0.781~0.868 V。推测该现象的可能原因为:吸附过程是一个动态结合-解吸过程,当涡旋顺利进行时,涡旋作用力较大,待测组分与氧化石墨烯之间的吸附力不足以克服涡旋作用力,造成已吸附的待测物又回到溶液中;当离心管中加入的样品溶液过多时,若再进行涡旋操作,操作受阻,已吸附的待测物可以相对稳定地吸附于萃取膜上,而涡旋提供的震荡作用力足以减小吸附剂附近的浓差极化,使得吸附过程顺利进行。因此选择样品溶液体积为10 mL。
考察洗脱过程中解吸溶液体积(1、2、5 mL)对EPH响应强度的影响,结果发现洗脱溶液体积为1 mL时,响应强度最大,因此选择洗脱剂体积为1 mL。
2.3.2 吸附过程、洗脱过程时间的优化实验分别考察了吸附时间(2、5、8、10 min)和洗脱时间(2、5、8、10、12 min)对结果的影响。发现当吸附5 min,洗脱10 min时,响应强度最高,因此选择吸附时间5 min、洗脱时间10 min为实验最优条件。
2.3.3 PVDF-PD-GO-SPE使用次数取“1.2.2”制备的EPH储备溶液配成1.237 μg/mL质量浓度的溶液,在优化条件下测定,记录IMS图谱,然后使用甲醇和水各洗涤2次,重复操作。结果显示,该PVDF-PD-GO-SPE至少可以重复使用14次,第14次测定之后的萃取效率为初始值的96.9%~102%,其萃取效率无明显变化,说明该镀层在萃取过程中具有良好的耐受性和稳定性。
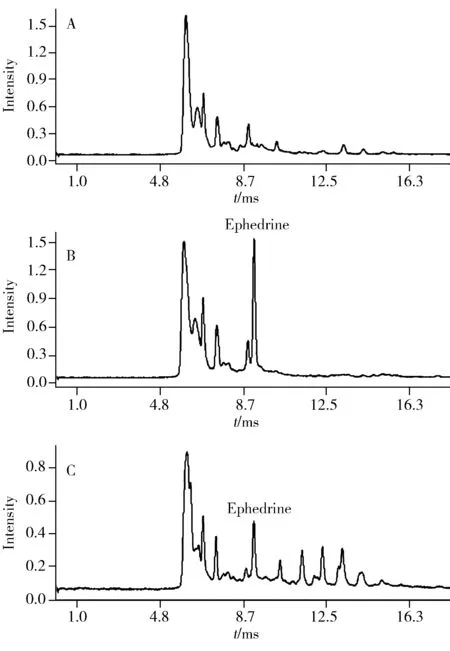
图3 专属性考察Fig.3 The results of specificity testA:blank urine sample,B:1.033 μg/mL standard solution,C:spiked 0.309 μg/mL sample solution
2.4 方法学验证
2.4.1 专属性空白样品溶液及0.309 μg/mL加标样品溶液按照“1.4”方法处理,进样,采集谱图信息。如图3所示,麻黄碱在(9.18±0.013)ms出峰。对比图3A、B、C可知尿液基质不干扰EPH的测定,分离良好,方法具有较强的专属性。
2.4.2 线性关系、检出限与定量下限取空白尿液,准确配制成系列浓度的质控样品溶液,在优化条件下测定并记录IMS图谱,以响应强度(E)对其质量浓度(C)绘制标准曲线。结果显示,EPH在0.124~6.129 μg/mL质量浓度范围与响应强度呈良好的线性关系,线性方程为E=0.581C+0.225(r2=0.988)。取最低点质控样品逐级稀释,依次进样分析,以S/N=3和S/N=10时对应的质量浓度分别记为检出限、定量下限,计算得麻黄碱的检出限为9.60 ng/mL,定量下限为32.0 ng/mL。
2.4.3 回收率与相对标准偏差取“1.2.3”制备的低(0.309 μg/mL)、中(1.273 μg/mL)、高(6.185 μg/mL) 3个浓度加标样品各3份,按照“1.4”方法处理后进样,以IMS中的峰面积计算回收率,得回收率为91.0%~113%,RSD为4.6%~8.5%。
2.4.4 实际样品检测健康受试者3人,一次性服用急支糖浆5 mL,服药后5 h采集尿样,在优化条件下处理后进样测定,采集谱图信息,得麻黄碱的质量浓度分别为1.240(曲线1)、1.052(曲线2)、0.490(曲线3) mg/L,结果见图4。

图4 实际样品检测谱图Fig.4 The spectra of real samples
2.5 与已有方法的比较
尿液中EPH的前处理方法主要包括液液萃取和固相萃取(表1),但液液萃取需长时间的萃取相平衡过程,且萃取剂与检测手段不相符的还要进行溶剂转换,操作繁琐耗时;传统的固相萃取要经活化、淋洗、洗脱、溶剂转换等繁琐步骤,也不适用于EPH的快速检测。本文建立的新型PVDF-PD-GO-SPE膜萃取方法,操作简单省时,氧化石墨烯吸附剂可以特异性吸附EPH,且不需要长时间的吸附过程,无需溶剂转换,洗脱液可直接测定。
对比可知,PHR-IMS法的检测灵敏度与色谱-质谱联用法相当,相较于色谱法可以提高2~3个数量级。PHR-IMS操作简单、大气压下即可操作、体积小便于携带、分析测定可在数秒内完成的优点为药驾的快速现场检测,提供了可行性,奠定了基础。

表1 前处理方法比较Table 1 The comparison of pretreatment methods
3 结 论
本文首次以聚偏氟乙烯为支撑载体,通过聚多巴胺结合氧化石墨烯吸附剂制成新型固相萃取模式,增大了吸附表面积,进一步缩短了吸附时间、洗脱时间,操作简单、省时;将其与PHR-IMS结合可实现尿液中麻黄碱的快速检测,该方法操作简单、灵敏度高、重现性好,为药驾在线检测和现场监察提供了一种有效手段。
