QuEChERS法结合液相色谱-串联质谱测定保健食品中50种非食用添加物
2019-06-24胡胜杰伊雄海邓晓军徐敦明上海大学生命科学学院食品工程系上海00上海出入境检验检疫局动植物与食品检验检疫技术中心上海005上海杉达学院上海009厦门出入境检验检疫局检验检疫技术中心福建厦门60
胡胜杰, 李 优, 周 莹, 伊雄海, 邓晓军,陈 沁, 徐敦明, 钮 冰(.上海大学生命科学学院食品工程系,上海 00;.上海出入境检验检疫局动植物与食品检验检疫技术中心,上海 005;.上海杉达学院,上海 009;.厦门出入境检验检疫局检验检疫技术中心,福建 厦门 60)
保健食品是一种适于特定人群食用,不以治疗为目的,且能够调节人体生理机能的食品种类[1-4]。2001年,欧盟对保健食品中的化学物质进行安全性评估,建立了肯定列表,规定保健食品中不得含有药物成分[5]。我国《食品安全法》第三十四条明文规定,保健食品中禁止添加任何非食用添加物[6]。近年来,由于相关产业竞争激烈,部分不法商贩为牟取暴利、肆意增强产品的疗效,无视相关法规,在保健食品中大量添加药物甚至违禁药物。消费者若长期服用此类产品会对健康造成巨大隐患。目前我国已发布的检测标准包括减肥[7]、降糖[8]、抗疲劳[9]类药物的测定,基质与化合物考察范围的局限性较强。因此,建立跨基质类别、跨药品类别的检测方法,对打击违法添加行为、保障消费者安全具有重要意义。
目前国内外报道的检测保健食品中非食用添加物的方法主要有毛细管电泳法(CE)[10]、气相色谱-串联质谱法(GC-MS/MS)[11,12]、液相色谱-串联质谱法(LC-MS/MS)[13-15]、高效液相色谱法(HPLC)[16]、液相色谱-四极杆飞行时间质谱法(LC-QTOF-MS)[17,18]等。其中,LC-MS/MS因灵敏度高、特异性强,已广泛应用于食品、药物检测[19]。李丹等[20]采用该技术检测了胶囊类保健食品中36种解热镇痛、抗炎类药物[20];黄芳等[15]使用该技术测定了片剂、胶囊类保健食品中17种壮阳类药物;祝伟霞等[21]使用UPLC-MS/MS测定了片剂、颗粒、口服液类保健食品中26种非食用添加物,涉及减肥类、壮阳类等8类药物。同时检测口服液、片剂、胶囊、丸剂、膏剂中减肥、安眠、降血糖、降血压、降血脂、消炎镇痛、抗疲劳类药物的方法未见报道。
本研究以口服液、片剂、丸剂、膏剂、胶囊剂类保健食品为研究对象,采用QuEChERS方法与LC-MS/MS技术,通过优化前处理步骤与仪器参数,建立了同时检测保健食品中50种减肥、安眠、降血糖、降血压、降血脂、消炎镇痛、抗疲劳类非食用添加药物的快速分析方法。该法前处理简便、重现性好、适用性强,为打击保健品行业的非法添加行为,填补检测技术空白以及保健食品突破国际贸易壁垒提供了可靠的技术储备。
1 实验部分
1.1 仪器、试剂与材料
1290 Infinity II液相色谱-6495三重四极杆质谱联用仪(美国Agilent公司),配备有ESI源;Allegra X-22R Centrifuge离心机(美国Beckman Coulter公司);CM-1000高速振荡器(日本EYELA公司);CPX5800H-C超声清洗机(美国Branson公司);Milli-Q超纯水系统(美国Millipore公司)。
甲醇、乙腈(色谱纯,美国Thermo Fisher公司);甲酸(纯度≥99%,美国Fluka公司);实验所用50种药物标准品(纯度≥95%,天津阿尔塔科技有限公司);尼龙针式过滤器(0.22 μm,上海安谱实验科技股份有限公司);硫酸镁(MgSO4)、氯化钠(NaCl)、柠檬酸钠(TSCD)、柠檬酸氢二钠(DHS)均为分析纯(国药集团化学试剂有限公司);N-丙基乙二胺(PSA)、十八烷基键合硅胶吸附剂(C18)、石墨化炭黑(GCB)均购自北京迪马科技有限公司;实验用水由Milli-Q超纯水系统制得。
口服液、片剂、丸剂、膏剂、胶囊样品均随机购买于上海市的药店、超市,密封,标识,置于4 ℃冰箱封存。
1.2 标准溶液配制
称取适量标准品,加入甲醇溶解,定容至10 mL,配制成1 g/L的储备液密封,于-20 ℃下保存。分别移取上述50种单标准储备液适量,用甲醇稀释,分别制备成1 mg/L的单一标准溶液和10 mg/L、1 mg/L的混合标准工作液,于-20 ℃贮存。
1.3 样品前处理
1.3.1固体、半固体样品
片剂和丸剂:以研钵磨碎;胶囊:将壳与内容物用研钵磨碎,混匀;膏剂:混匀。准确称取1 g代表性样品于50 mL具塞离心管中,加入10 mL甲醇,涡旋5 min,超声提取30 min,加入4 g MgSO4、1 g NaCl、1 g TSCD、0.5 g DHS,迅速振荡5 min,于4 000 r/min下离心5 min,取1 mL上清液于2 mL离心管,加入50 mg PSA、50 mg C18、7.5 mg CARB、150 mg MgSO4,涡旋2 min,于12 000 r/min下离心5 min,取500 μL上清液,以甲醇定容至1 mL,过0.22 μm滤膜,供LC-MS/MS测定。
1.3.2口服液
准确称取0.5 g于10 mL容量瓶中,以甲醇定容至10 mL,转移至50 mL离心管中,于12 000 r/min下离心5 min,取适量上清液,过0.22 μm滤膜,供LC-MS/MS测定。
1.4 仪器条件
色谱条件:Phoroshell SB C18色谱柱(150 mm×3.0 mm,2.7 μm;美国Agilent公司);流动相A:0.1%(v/v)甲酸水溶液,B:乙腈;洗脱程序:0~1.0 min,5%B;1.0~1.5 min,5%B~10%B;1.5~20.0 min,10%B~100%B,20.0~25.0 min,100%B;25.0~30.0 min,100%B~5%B;流速:0.30 mL/min;柱温:30 ℃;进样量:1 μL。
质谱条件:电喷雾离子源(ESI),正离子模式、负离子模式同时扫描,MRM检测模式,50种非食用添加物的保留时间、定性离子、定量离子、碰撞能量(CE)等质谱参数见表1。
2 结果与讨论
2.1 质谱条件的优化
取1 mg/L单一标准溶液,分别于正离子模式和负离子模式进行母离子全扫描,得到各化合物的准分子离子([M+H]+或[M-H]-),选取响应值高的离子为母离子。再对母离子进行二级质谱分析,选择干扰较小、丰度较强的两对子离子分别作为定量、定性离子。最后通过优化碰撞能量,使每种化合物的特征碎片离子对强度达到最大。
2.2 样品前处理条件的优化
2.2.1样品提取溶剂的选择
根据50种非食用添加物的化学特性,分别以甲醇、乙腈和水对添加浓度为1 mg/kg的片剂、膏剂、丸剂和胶囊剂进行提取,计算回收率。结果表明,上述3种溶剂对37种非食用添加物的提取率接近,均符合检测要求(>60.0%);对于剩余13种化合物,甲醇的提取率(>54.6%)比乙腈(<53.1%)和水(<45.1%)的提取率高。因此,选择甲醇作提取剂。
2.2.2QuEChERS净化剂的选择与优化
目前文献报道的净化方法主要有固相萃取法(SPE)[21]和QuEChERS法[22]。SPE法净化效果好,但优化步骤繁琐、耗时较长,不适于多类化合物检测。QuEChERS法快速、简便、适用性广,在非食用添加物的检测方法及标准中得到运用[19]。商品化的QuEChERS法主要为萃取盐与净化剂的组合,缓冲体系主要有果蔬农残检测方法AOAC 2007.10的醋酸盐体系[23]和EN 15662的柠檬酸盐体系[24]。
本实验考虑到药物稳定性,选择酸性较弱的柠檬酸盐体系作为QuEChERS缓冲体系,并以不同配方的吸附剂组合(MgSO4、MgSO4+PSA、MgSO4+PSA+C18、MgSO4+PSA+C18+GCB)对添加浓度为1 mg/kg的片剂、胶囊剂、膏剂和丸剂提取液净化,计算回收率。结果(见图1)表明,MgSO4可以除去部分水溶性杂质[25],但由于净化能力有限,主要干扰物未净化完全,因此整体回收率无显著变化;加入PSA后,各基质中超过76%的药物回收率得到提升,这与糖类、有机酸等主要干扰物质被去除有关[26];加入C18后,整体回收率略有提升,可能与样品含脂量低有关,除去了部分脂质等非极性干扰物;加入GCB后,整体回收率最好(74.9%~113.0%),色素被进一步净化,本底的干扰降至最低。因此,本实验最终采用MgSO4+PSA+C18+GCB协同净化的方式,增强杂质的净化能力,降低离子抑制作用,提高方法的准确度。
2.2.3基质效应
取口服液、片剂、胶囊、膏剂、丸剂代表性样品,配制成0~100 μg/L的基质匹配标准溶液与试剂标准溶液,按下列公式计算基质效应(ME):ME=基质匹配标准曲线的斜率/试剂标准曲线的斜率×100%[27]。若ME在80%~120%范围内,表明基质效应不明显;若ME>120%,表明基质增强效应显著;若ME<80%,表明基质抑制效应显著[28]。计算结果如表2所示,5种基质的ME为56.6%~88.0%,74.4%的化合物基质抑制效应显著。

表1 50种非食用添加物的分子式、保留时间及质谱参数Table 1 Formula,retention times and MS/MS parameters of the 50 non-edible additives
CE:collision energy;* quantitative ion.

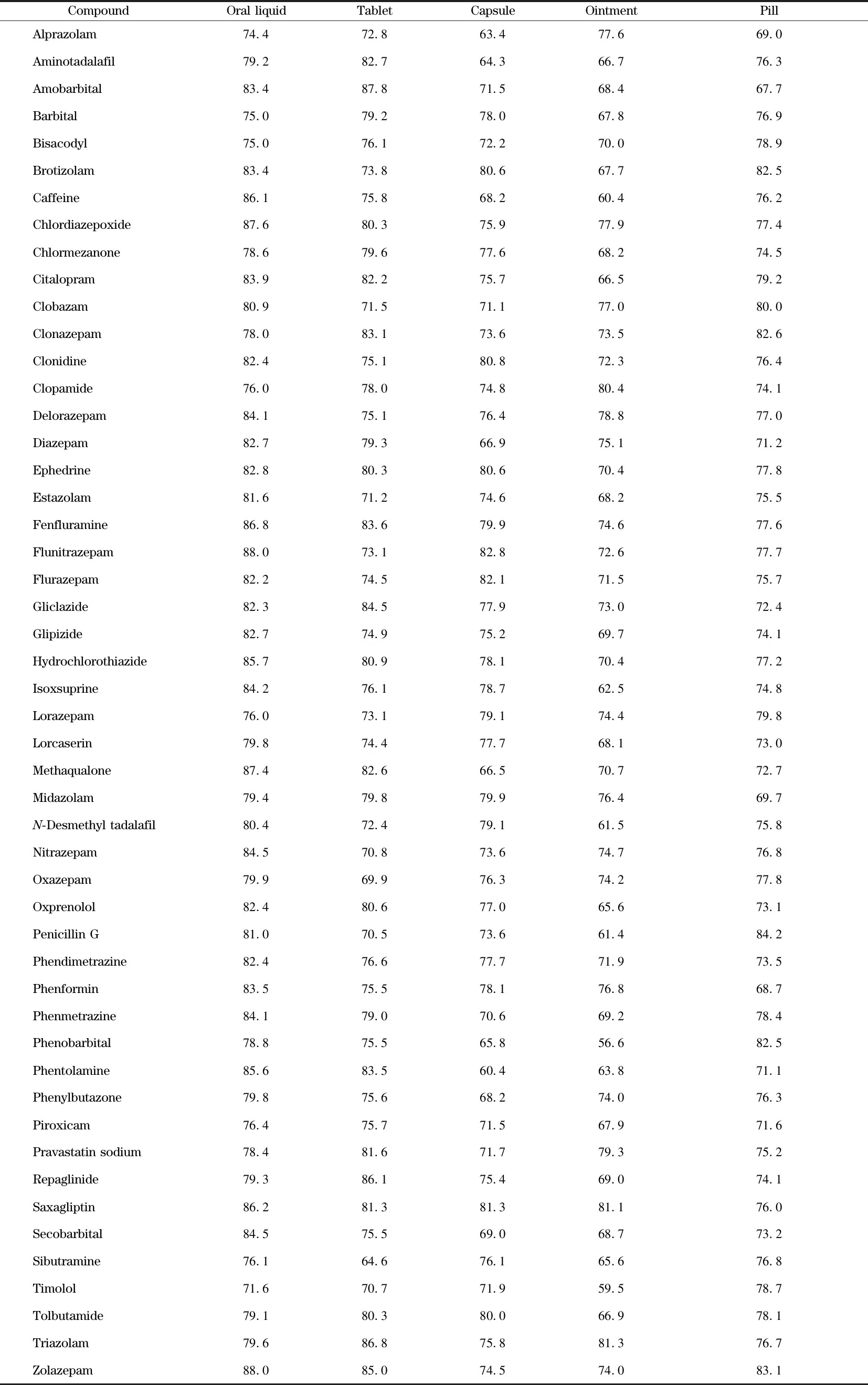
表2 50种非食用添加物在不同基质中的基质效应 Table 2 Matrix effects of the 50 non-edible additives in different matrices %
因此,本方法采用基质匹配标准溶液进行校正,可消除离子抑制,改善回收率。
2.3 线性范围和检出限
在5种样品中添加目标化合物,以50种化合物的质量浓度(X,μg/L)为横坐标,峰面积(Y)为纵坐标,绘制标准曲线。以S/N≥3与S/N≥10分别确定方法的检出限与定量限。其中巴比妥、苯巴比妥、异戊巴比妥、氯美扎酮、司可巴比妥、普伐他汀钠和格列齐特在0~1 000 μg/L范围内线性良好,苯巴比妥的检出限为1 mg/kg,定量限为2 mg/kg,其他6种药物的检出限为500 μg/kg,定量限为1 mg/kg;其余43种化合物在0~10 μg/L内线性关系良好,检出限为10 μg/kg,定量限为20 μg/kg;以上所有化合物的线性相关系数(r2)均大于0.99。
2.4 准确度与精密度
在上述5种空白基质中分别添加终浓度相当于1、2、10倍LOQ的混合标准溶液进行加标回收率试验,每个水平重复6次,在优化的条件下测定,结果见表3。可以看出,口服液的平均回收率为82.8%~113.9%,RSD为0.7%~6.1%;片剂的平均回收率为65.4%~111.5%,RSD为1.6%~8.6%;胶囊剂的平均回收率为67.6%~115.5%,RSD为1.3%~8.9%;丸剂的平均回收率为71.0%~115.7%,RSD为1.5%~6.1%;膏剂的平均回收率为63.1%~111.7%,RSD为1.2%~7.5%,满足检测要求。
2.5 实际样品检验
应用本方法对市售100份保健食品,包括褪黑素片、海狗人参丸、左旋肉碱胶囊、功能饮料等进行测定。其中,3份功能饮料中检出西布曲明,其定性、定量离子对的比例与空白基质匹配标准溶液、空白添加回收样品匹配(偏差范围<15%),定量结果分别为64.2 μg/kg、110.7 μg/kg、160.7 μg/kg ,其余样品均未检出50种非食用添加物。相关谱图见图2。

表3 50种非食用添加物在5种保健食品基质中的平均加标回收率和精密度Table 3 Average recoveries and relative standard deviations (RSDs)of the 50 non-edible additives spiked in five kinds of health food matrices
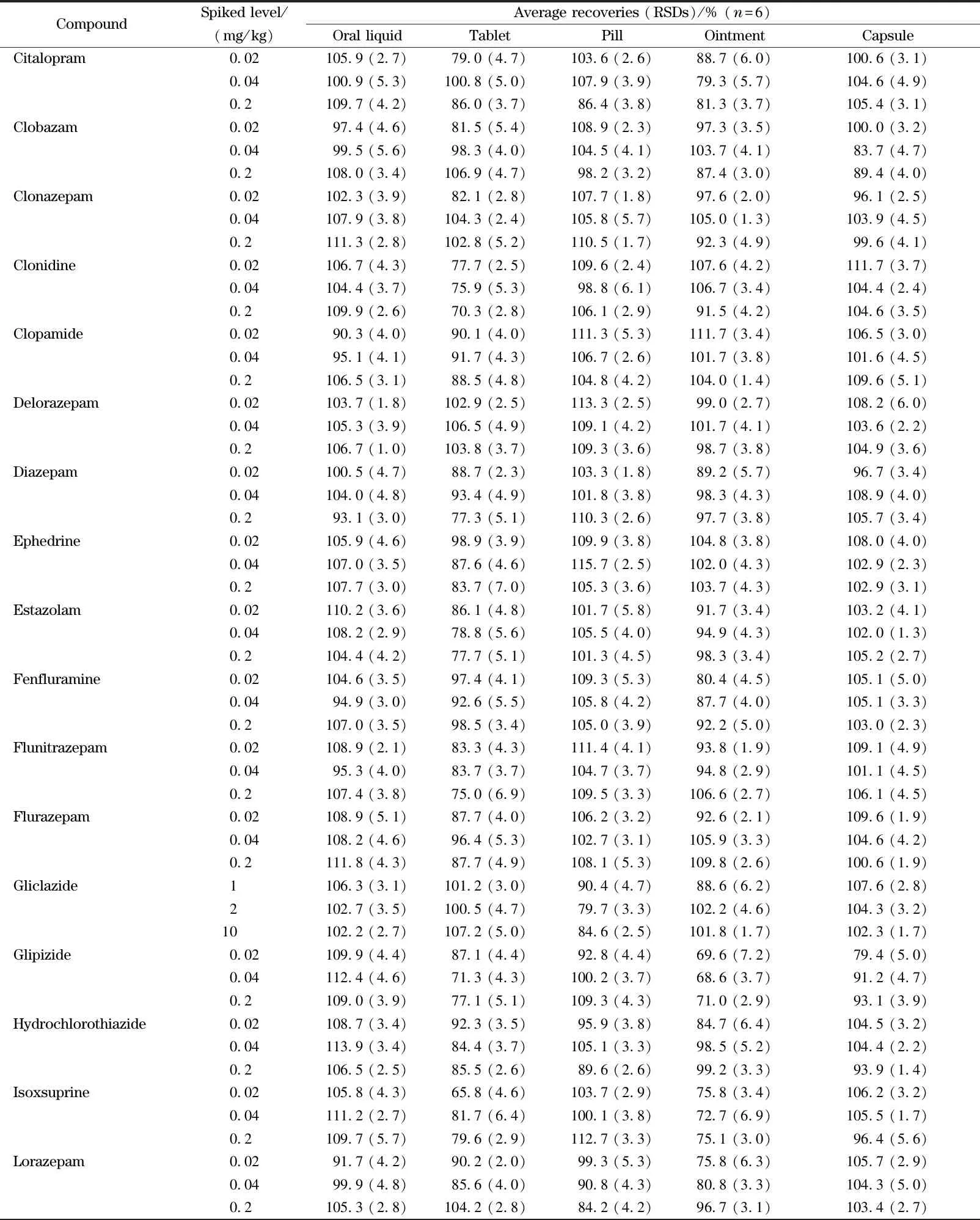
表3 (续)Table 3 (Continued)

表3 (续)Table 3 (Continued)

表3 (续)Table 3 (Continued)

图2 空白口服液的基质匹配标准溶液(20 μg/L)、加标样品(400 μg/kg)与阳性样品(160.7 μg/kg)中西布曲明的MRM色谱图与质谱图Fig.2 MRM chromatograms and MS spectra of sibutramine in oral liquid matrix-matched standard solution (20 μg/kg),spiked sample (400 μg/kg),and actual sample (160.7 μg/kg)
3 结论
本实验建立了针对保健食品中可能违法添加的50种化合物的LC-MS/MS筛查与确证方法,同时对质谱条件、提取溶剂、净化剂组合等进行了考察与优化,并对基质效应进行了评价。实际检测结果表明,该法的前处理简单、灵敏度高且实用性强,为监督保健品行业违法违规现象提供了有力的技术支持。
