包埋法制备替米考星淀粉微球工艺的优化
2019-06-11王丽陈洪轩常杰等
王丽 陈洪轩 常杰等

摘要 [目的]研究替米考星淀粉微球的制备工艺。[方法]以可溶性淀粉为原料,以N,N-亚甲基双丙烯酰胺为交联剂,以过硫酸钾和亚硫酸氢钠为引发剂,采用包埋法制备替米考星淀粉微球。以载药量和包封率为指标,通过正交试验,采用综合平衡法对替米考星淀粉微球的制备工艺进行优化,在扫描电子显微镜下观察替米考星交联微球的形貌及表面形态。[结果]替米考星淀粉微球的最佳制备工艺如下:替米考星0.02 g,可溶性淀粉4 g,交联剂(N,N-亚甲基双丙烯酰胺)0.95 g,乳化剂(mSpan80:mTween80=2∶1)0.75 g,反应时间1.5 h,在优化工艺参数下制得的替米考星淀粉微球载药量为1.63%,包封率为81.4%;微球大小分布均匀,外观圆整,表面粗糙多孔。[結论]该制备工艺可行,扩大了替米考星的应用,为替米考星的剂型改进提供了参考。
关键词 替米考星;可溶性淀粉;包埋法;微球制备工艺
中图分类号 S859.79+6文献标识码 A
文章编号 0517-6611(2019)04-0110-04
Abstract [Objective] To study the preparation process of tilmicosin starch microspheres.[Method] With soluble starch as materials,N,Nmethylenebisacrylamide as crosslinking agent and potassium persulfate with sodiun bisulflte as initiator,tilmicosin starch microsphere was synthesized by using embedding method.The preparation process of tilmicosin starch microsphere was optimized by integrated balance method through the orthogonal experiment,with the drug loading and encapsulation rate as indicators.The morphology features and surface topography of tilmicosin starch microsphere were characterized by Quanta 250FEG scanning electron microscope.[Result]The optimum preparation process was as follows:the quantity of tilmicosin 0.02 g,soluble starch 4.0 g,N,Nmethylenebisacrylamide 0.95 g,surfactant (mSpan80∶mTween80=2∶1)0.75 g, and the reaction time was 1.5 h.Under these optimized technology parameters,the drug loading and embedding ratio of tilmicosin starch microsphere were 1.63% and 81.4% respectively.The size of microspheres was uniform,the appearance was round and the surface was rough and porous.[Conclusion] The preparation process was feasible,which expanded the application of tilmicosin.Therefore this research provided references for the improvement of tilmicosins dosage forms .
Key words Tilmicosin;Soluble starch; Embedding method;Preparation process of microspheres
替米考星是一种以泰乐菌素为前体药物半合成而来的畜禽专用抗生素[1],20世纪80年代由英国Elanco公司开发。替米考星具有很强的抗菌活性,抗菌谱广,耐药性低,对所有的革兰氏阳性菌和部分革兰氏阴性菌、霉形体、螺旋体等均有抑制作用,临床上主要用于预防和治疗猪、鸡、牛、羊等由细菌和支原体感染引起的疾病,如猪喘气病、乳房炎、鸡慢性呼吸道病、胸膜炎等[2]。目前,替米考星已在许多国家批准上市,我国现有剂型主要有预混剂、注射液、饮水剂,但现有剂型给药后会表现出明显的峰谷现象,且产生心脏毒性和肾脏毒性的可能性较大,使不良反应率大大增加[3-4]。微球具有缓释与长效性、掩盖药物不良气味、提高药物稳定性、低毒、无免疫原性等特点[5-6]。以无毒、安全、原料廉价易得的可溶性淀粉为原料制备的微球是一种理想的新型药物载体,具有较好的生物可降解性、生物相容性、生物稳定性和较低的毒性[7-8]。笔者以可溶性淀粉为原料,采用包埋法[9]制备替米考星淀粉微球,并对其制备工艺进行优化,以期获得最佳制备工艺,扩大其临床应用范围。
1 材料与方法
1.1 试剂和药物 替米考星(辽宁大连鑫辉生物科技有限公司,批号为20140402)、可溶性淀粉(天津市科密欧化学试剂有限公司,批号为20160922)、环己烷(天津市永大化学试剂有限公司,批号为20140308)、司班80(上海化学试剂有限公司,批号为20140812)、吐温80(天津市富宇精细化工有限公司,批号为20120720)、N,N-亚甲基双丙烯酰胺(天津市科密欧化学试剂有限公司,批号为20171012)、无水乙醇(天津市永大化学试剂有限公司,批号为20160801)、乙酸乙酯(天津市永大化学试剂有限公司,批号为20161001)、过硫酸钾(天津市科密欧化学试剂有限公司,批号为20150710)、亚硫酸氢钠(天津市科密欧化学试剂有限公司,批号为20161210)、氢氧化钠(天津市凯通化学试剂有限公司,批号为20081018)。试验所用试剂均为分析纯。
1.2 仪器 紫外分光光度计(TU-1810,北京普析通用仪器有限责任公司)、场发射扫描电镜(Quanta 250FEG,美国FEI)、集热式恒温加热磁力搅拌器(DF-101S,郑州长盛实验设备器有限公司)、循环水式多用真空泵(SHB-ⅢA,郑州长城科工贸有限公司)、超声波清洗器(KQ2200E,昆山市超声仪器有限公司)、电子天平(WT5003CH,常州万泰天平仪器有限公司)。
1.3 淀粉微球的制备
1.3.1 空白淀粉微球的制备。
1.3.1.1 油相的制备。将80 mL环己烷置于250 mL锥形瓶中,加入司班80和吐温80(按质量比2∶1加入),在50 ℃水浴條件下,搅拌溶解,备用。
1.3.1.2 水相的制备。将4 g可溶性淀粉置于100 mL烧杯中,加入30 mL纯化水,在80 ℃水浴条件下,使其溶解;用氢氧化钠溶液调节pH 9~10;转移至60 ℃恒温水浴锅中,加入0.6 g N,N-亚甲基双丙烯酰胺和0.6 g过硫酸钾,搅拌溶解,备用。
1.3.1.3 空白微球的制备。将油相加入到水相中,置于集热式恒温加热磁力搅拌器中,50 ℃下搅拌使其乳化0.5 h,加入0.6 g亚硫酸氢钠,升温至60 ℃,引发交联反应,搅拌反应2 h,静置,取下层沉淀,用适量乙酸乙酯洗涤多次,再用适量无水乙醇洗涤多次,抽滤,干燥,得到空白淀粉微球。
1.3.2 替米考星淀粉微球的制备。使用以下成分制备替米考量淀粉微球:替米考星0.02 g、环己烷80 mL、 司班80∶吐温80(质量比为2∶1)0.75 g、可溶性淀粉4 g、N,N-亚甲基双丙烯酰胺0.95 g、过硫酸钾0.6 g、亚硫酸氢钠0.6 g、蒸馏水30 mL。
1.3.2.1 油相的制备。将80 mL环己烷置于250 mL锥形瓶中,加入司班80和吐温80(按质量比2∶1加入),在50 ℃水浴条件下,搅拌溶解,待用。
1.3.2.2 水相的制备。将4 g可溶性淀粉置于100 mL烧杯中,加入30 mL纯化水,在80 ℃水浴条件下,使其溶解;降温至60 ℃,加入0.02 g替米考星、0.95 g N,N-亚甲基双丙烯酰胺和0.6 g过硫酸钾,搅拌溶解,备用。
1.3.2.3 替米考星淀粉微球的制备。将油相加入到水相中,置于集热式恒温加热磁力搅拌器中,50 ℃下搅拌使其乳化0.5 h,加入0.6 g亚硫酸氢钠,升温至60 ℃,引发交联反应,搅拌反应2 h,静置后取下层沉淀,用适量乙酸乙酯洗涤多次,再用适量无水乙醇洗涤多次,抽滤并干燥,得到替米考星淀粉微球。
1.4 替米考星标准曲线的绘制
称取替米考星0.011 3 g置于25 mL容量瓶中,加入无水乙醇定容,为储备液。分别从上述储备液中一起移取0.1、0.2、0.3、0.4、0.5、0.6、0.7、0.8、0.9、1.0 mL置于10 mL容量瓶中,用无水乙醇定容,摇匀。在紫外可见分光光度计下于最大吸收波长282 nm[10]处测定吸光度,绘制替米考星的标准曲线。
1.5 单因素试验
为了考察影响替米考星淀粉微球的载药量和包封率的因素,根据替米考星淀粉微球的制备方法,控制其他因素和条件不变,分别以替米考星的用量、反应时间、交联剂的用量、乳化剂的用量为研究对象进行单因素试验。
1.6 正交试验
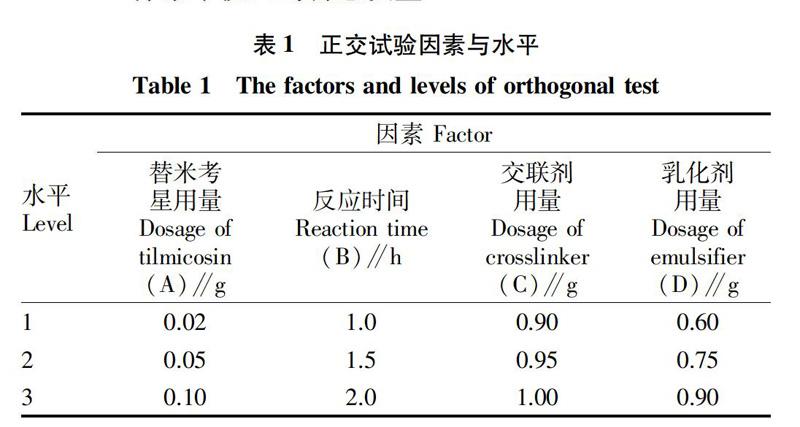
为了确定替米考星淀粉微球的最佳制备工艺,在单因素试验结果及有关报道的基础上[11],选定替米考星用量(A)、反应时间(B)、交联剂用量(C)、乳化剂用量(D)为影响因素,每个因素选取3个水平(表1),进行正交试验设计。
1.7 评价指标
每次取0.1 g替米考星淀粉微球,加入定量的无水乙醇,超声一定时间,过滤后取滤液,用无水乙醇定容至50 mL,在紫外分光光度计下测其吸光度,带入标准曲线计算替米考星浓度,最后计算其载药量(Y1)和包封率(Y2)。
1.8 替米考星交联淀粉微球的表征
取一定量的替米考星淀粉微球真空冷冻干燥后喷金制样,在Quanta 250FEG扫描电子显微镜下观察其形貌及表面形态[12]。
2 结果与分析
2.1 替米考星的标准曲线
由图1可知,替米考星的标准曲线回归方程为:y=0.036 2x+0.000 2(R2=0.999 9),在浓度0.005~0.050 mg/mL范围内有良好的线性关系。
2.2 单因素试验结果
2.2.1 替米考星用量对替米考星淀粉微球载药量和包封率的影响。按照“1.3”的试验方法,控制处方及制备工艺中其他条件不变,分别考察替米考星用量为0.02、0.05、0.10和0.15 g 时对替米考星淀粉微球载药量和包封率的影响,结果见图2。
2.2.2 反应时间对替米考星淀粉微球载药量和包封率的影响。按照“1.3”中试验方法,控制处方及制备工艺中其他条件不变,分别考察反应时间为1.0、1.5、2.0、2.5 h时对替米考星淀粉微球载药量和包封率的影响,结果见图3。
2.2.3 交联剂用量对替米考星淀粉微球载药量和包封率的影响。按照“1.3”中试验方法,控制处方及制备工艺中其他条件不变,分别考察交联剂用量为0.85、0.90、0.95、1.00 g时对替米考星淀粉微球载药量和包封率的影响,结果见图4。
2.2.4 乳化剂用量对替米考星淀粉微球载药量和包封率的影响。按照“1.3”中试验方法,控制处方及制备工艺中其他条件不变,分别考察乳化剂用量为0.60、0.75、0.90和1.05 g时对替米考星淀粉微球载药量和包封率的影响,结果见图5。
2.3 正交试验结果
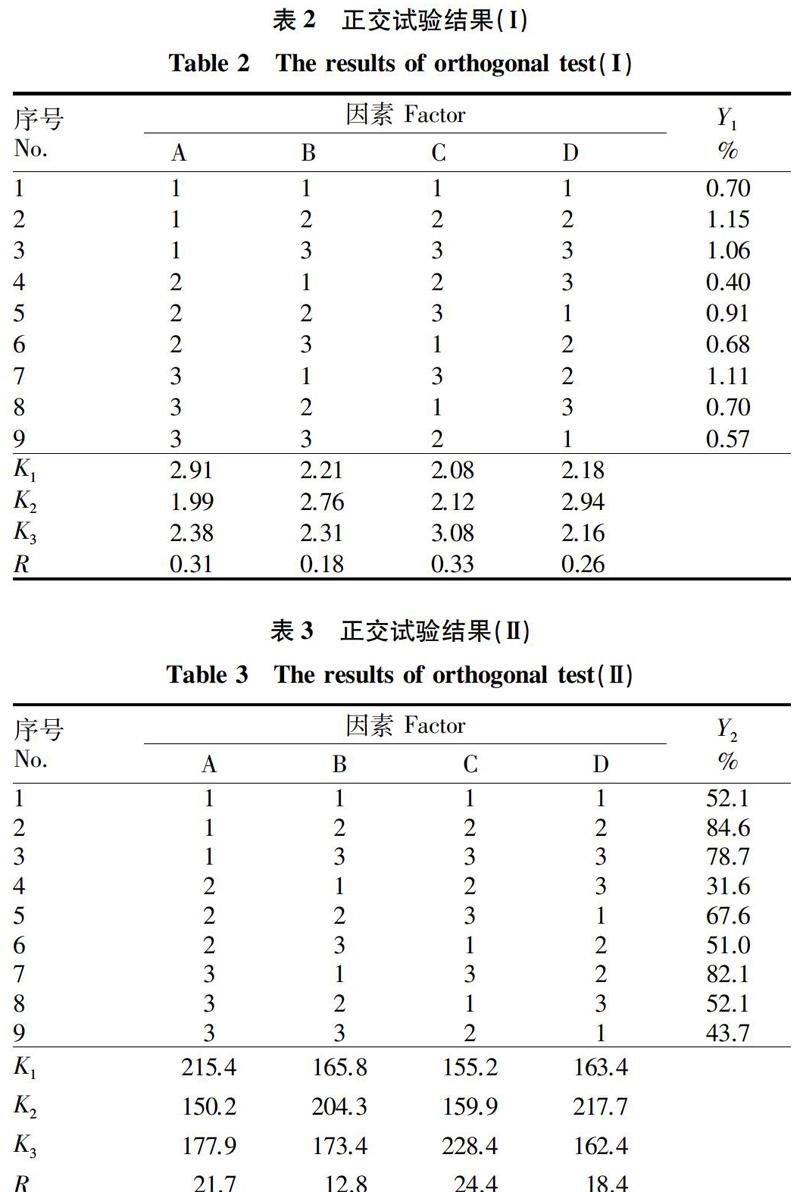
根据正交试验因素与水平表(表1),以载药量(Y1)和包封率(Y2)为考察指标进行正交试验,结果见表2~3。
以载药量(Y1)和包封率(Y2)为考察指标,在正交试验结果分析时使每个指标尽可能达到最优。采用综合平衡法[13]的统计学分析方法,先对每个指标分别进行单指标的直观分析,得到每个指标的影响因素主次顺序和最佳水平组合:①以载药量为考察指标时,影响因素从大到小依次为交联剂用量、替米考星用量、乳化剂用量、反应时间,最佳制备工艺条件为A1B2C3D2(表2)。②以包封率为考察指标时,影响因素从大到小依次为交联剂用量、替米考星用量、乳化剂用量、反应时间,最佳制备工艺条件为A1B2C3D2(表3)。
根据理论知识和实际经验,交联剂用量要适当,当交联剂用量为1.00 g时,虽然载药量和包封率较高,但通过扫描电镜的观测发现微球少,且大量粘连,因此选择的交联剂用量为0.95 g,即C2。
综合考虑Y1和Y2 2个指标后,确定各影响因素从大到小依次为交联剂用量、替米考星用量、乳化剂用量、反应时间;最佳制备工艺条件为A1B2C2D2,即替米考星0.02 g,交联剂0.95 g,乳化剂0.75 g,反应时间1.5 h,按照优化工艺参数制得的替米考星淀粉微球的载药量为1.63%,包封率为81.4%。
2.4 替米考星交联淀粉微球的表面形态分析 由图6可知,微球形貌较圆整规则,大小比较均一。微球表面粗糙多孔,无粘连。这说明反应过程中交联乳化效果较好,体系较为稳定。
3 讨论
(1)制备过程中应注意集热式恒温加热磁力搅拌器的搅拌速度。搅拌速度过小,水相易粘连成块状,交联效果差;搅拌速度过大,油相易飞溅,影响反应的进行。因此,在反应过程中需要适当控制搅拌速度,且用锥形瓶作为反应器,以减少油相的飞溅。
(2)采用适当的两相加入的方法。文献中均采用水相加入油相的制备方法,但经过多次预试验发现,由于水相为可溶性淀粉溶液,较为黏稠,在制备过程中损失较大,因此该研究采用油相加入水相的方法,易于操作,减少了药物损失,提高了包封率和载药量。
(3)洗涤微球应充分。用适量乙酸乙酯洗涤多次,再用适量无水乙醇洗涤多次;否则,抽滤后的微球粘成块状,不易干燥,且不易破坏,影响含量的测定。
4 结论
采用单因素试验和正交试验优化替米考星淀粉微球的制备工艺,各影响因素从大到小依次为交联剂用量、替米考星用量、乳化剂用量、反应时间;最佳制备工艺条件如下:替米考星0.02 g,交联剂0.95 g,乳化剂0.75 g,反应时间1.5 h,按照此优化工艺参数制得的替米考星淀粉微球载药量为1.63%,包封率为81.4%;制得的微球形貌较为圆整规则,大小较为均一。该研究为替米考星剂型的改进和创新提供了新思路,扩大了替米考星的应用范围,也为兽药新剂型和新技术的研究与发展提供了重要参考。
参考文献
[1] NORCIA L J L,SILVIA A M,HAYASHI S F.Studies on timekillkinetics of different classes of antibiotics against veterinary pathogenic bacteria including Pasteurella,Actinobacillus and Escherichia coli[J].The journal of antibiotics,1999,52(1):52-60.
[2] 郭腾,吴连勇,张家祥.兽用抗菌新药替米考星研究进展[J].中国兽药杂志,2002,36(7):38-39,43.
[3] MAIN B W,MEANS J R,RINKEMA L E,et al.Cardiovascular effects of the macrolide antibiotic tilmicosin,administered alone and in combination with propranolol or dobutamine,in conscious unrestrained dogs[J].Journal of veterinary pharmacology & therapeutics,1996,19(3):225-232.
[4] 远立国,鲍杰,李成明,等.替米考星肺靶向微球的研制[J].中国兽医科学,2008,38(12):1093-1097.
[5] 方亮.药剂学[M].北京:人民卫生出版社,2016:319.
[6] 徐军,陈子扬,单鹏,等.明胶微球的制备[J].中国生物制品学杂志,2012,25(2):230-232.
[7] DA FONSECA C O,LANDEIRO J A,CLARK S S,et al.Recent advances in the molecular genetics of malignant gliomas disclose targets for antitumor agent perillyl alcohol[J].Surgical neurology,2005,65(S1):52-58.
[8] PERESWETOFFMORATH L.Microspheres as nasal drug delivery systems[J].Advanced drug delivery reviews,1998,29(1):185-194.
[9] 李仲謹,杨威,刘艳,等.替米考星淀粉微球的制备及缓释性能的研究[J].中国畜牧兽医,2010,37(11):230-234.
[10] 刘亚.硅胶表面替米考星分子印迹聚合物的制备及性能研究[D].北京:北京化工大学,2006.
[11] 杨黎燕,余丽丽,牛秀明.替米考星交联淀粉载药微球的制备研究[J].应用化工,2012,41(2):217-220.
[12] 李艳平,申宇,唐洪波.交联淀粉微球的制备及表征[J].粮油加工,2015(1):44-46,50.
[13] 苑玉凤.多指标正交试验分析[J].湖北汽车工业学院学报,2005,19(4):53-56.
