PVAT免疫微环境与血管疾病①
2019-06-10李育林赵明升张利宁
李育林 赵明升 张利宁
(山东大学基础医学院免疫学系,济南250012)
脂肪组织不仅分布于皮下和内脏器官周围,也存在于血管周围。除脑血管外,全身的各处血管,特别是冠状动脉和主动脉,都被血管周围脂肪组织(Perivascular adipose tissue,PVAT)所包被[1]。PVAT贴近血管外膜层,占全身脂肪总量的3%左右,主要由脂肪细胞、成纤维细胞、干细胞、免疫细胞以及神经细胞等构成[2]。在正常情况下,PVAT不仅对血管起机械支撑作用,还能释放多种细胞因子和脂肪因子用以维持血管张力和调节血管功能。早在2005年,发表于《Lancet》上的一篇文章就指出,PVAT是联系内脏脂肪、胰岛素抵抗以及血管疾病的重要枢纽,在肥胖相关疾病中起到重要作用[3]。近年来,由于PVAT所处部位的特殊性,它的免疫微环境紊乱在血管疾病中的作用正越来越得到关注。
现有的研究结果表明,在一些心血管疾病的发病过程中,管周脂肪中的免疫细胞与其分泌的细胞因子相互作用构成的免疫微环境受到影响,其中保护性因子(ADRF等)和抗炎因子的释放减少,而许多旁分泌因子如脂肪因子(抵抗素、瘦素和内脏脂肪素)、细胞因子(IL-6和TNF-α)以及趋化因子(RANTES和MCP-1)的释放增加,这些因子都可以直接作用于内皮细胞和血管平滑肌细胞(Vascular smooth muscle cell,VSMC),启动血管炎症反应。这种抑炎因子和促炎因子产生和释放的不平衡,被称作PVAT 的功能紊乱[4]。功能紊乱的PVAT在动脉粥样硬化、高血压、糖尿病血管病变和肥胖症等诸多血管疾病中均有报道[5]。虽然不同情况下PVAT功能紊乱的机制可能不同,但其免疫微环境的改变对血管内皮细胞以及平滑肌的影响在许多血管病变的发生过程中有着共同特征,这也是目前该领域研究的主要焦点[6]。
1 PVAT是不属于白色脂肪和棕色脂肪的特殊脂肪组织
脂肪组织按细胞来源通常可分为白色脂肪(White adipose tissue,WAT)和棕色脂肪(Brown adipose tissue,BAT),主要的区别是线粒体的功能特征和解偶联蛋白1(Uncoupling protein 1,UCP-1)的含量。棕色脂肪具有强大的产热能力,而白色脂肪的作用是储存脂质,代谢水平相对较低[7]。
PVAT与其他脂肪在部位和功能特征上均有所区别(表1)。在小鼠体内,围绕胸主动脉的PVAT主要是棕色脂肪,但紧邻血管外膜有一条白色脂肪带,而腹主动脉则被棕色和白色脂肪所混合包裹,肠系膜动脉周围主要是棕色脂肪[13]。在人类中,PVAT更倾向于白色脂肪的组织学特性。然而,PVAT与典型的白色脂肪也有区别,在一些容易发生动脉粥样硬化的大血管中,PVAT与WAT相比,脂肪细胞体积较小且分化程度较低,脂质储存能力较弱[14],一些WAT的特异性分子标记物表达水平较低[15],这些特点与BAT类似。在基因水平上,PVAT中脂肪分化相关因子以及一些脂肪细胞特征性因子,如:过氧化物酶体增殖物激活受体γ(PPAR-γ)、脂肪酸结合蛋白4(FABP4)、增强子结合蛋白(C/EBP-α)、脂肪酸合成酶(FAS)、甘油3-磷酸脱氨酶1(GPDH)等表达水平明显低于皮下及内脏脂肪[15],其分化程度较低,更接近于前脂肪细胞,有释放促炎因子和生长因子的特性。病理情况下产生的血管紧张素Ⅱ(AngⅡ)或促动脉粥样硬化因子可诱导PVAT脂肪细胞去分化[16,17]。正是由于其独特的特征,PVAT被认为是一种不同于传统WAT和BAT的“新的”脂肪组织,对其的研究也日益增加。
2 PVAT免疫微环境与血管功能
免疫细胞与其分泌的细胞因子相互作用共同构成免疫微环境。生理状态下,PVAT具有促进血管平滑肌舒张、促进内皮细胞增生和诱导新生血管形成等功能。而在多种血管疾病中,功能紊乱的PVAT可以导致血管平滑肌舒缩障碍和内皮细胞功能紊乱。该过程由脂肪因子和PVAT中活化的炎症细胞释放的细胞因子所共同介导,其中瘦素、脂联素、IFN-γ、IL-17、IL-6和TNF-α等在此过程中发挥关键作用[19]。
2.1PVAT免疫微环境与血管内皮细胞的功能 γ干扰素(IFN-γ)由T细胞、NK细胞等产生,可以活化单核/巨噬细胞系统并促进免疫细胞向促炎表型的转化。除此之外,体外研究及IFN-γ-/-小鼠体内实验均证实,IFN-γ会损害内皮依赖性舒张反应[20]。而在趋化因子RANTES敲除的高血压动物模型中,T细胞和NK细胞等在PVAT中的浸润降低,使内皮依赖性舒张反应下降,而对内皮非依赖性舒张反应无影响[6]。
IL-6可由巨噬细胞、T细胞、DC细胞和管周脂肪细胞产生,能够直接作用于内皮细胞[21]。其通过NO-cGMP信号通路增加超氧化物的产生,诱导内皮功能紊乱[22],而IL-6基因敲除能够明显减轻继发性血管功能紊乱[23]。另外,IL-6对Th17细胞分化也是必需的[24],后者是另一种对内皮和VSMC具有强烈促炎作用的T细胞亚群。
IL-17是内皮细胞的激活因子之一,可以促进黏附分子的表达[25]。内皮细胞产生的一氧化氮(NO)在调节血管扩张及内皮细胞功能中发挥重要作用。IL-17A 激活RhoA/Rho 激酶,并促进内皮细胞NO合成酶(eNOS)抑制位点Thr495的磷酸化,导致NO产生减少,内皮功能受损[26]。IL-17A与TNF-α具有协同作用,上调许多靶基因,特别是IL-6的表达,共同调节炎症反应[27]。
表1 白色脂肪、棕色脂肪和管周脂肪的主要区别
Tab.1 Key differences between WAT,BAT and PVAT
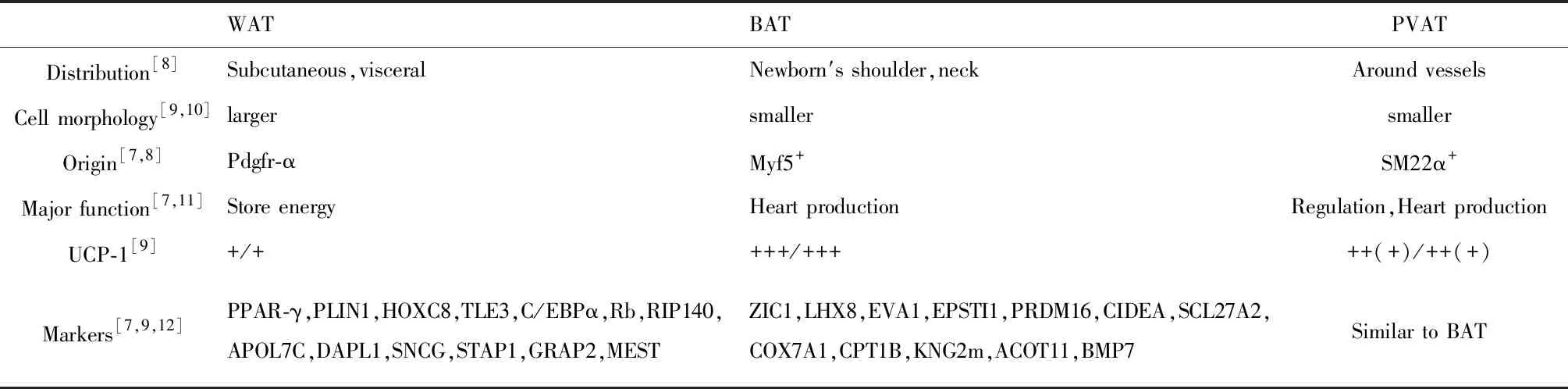
WATBATPVATDistribution[8]Subcutaneous,visceralNewborn′s shoulder,neckAround vesselsCell morphology[9,10]largersmallersmallerOrigin[7,8]Pdgfr-α Myf5+SM22α+Major function[7,11]Store energyHeart productionRegulation,Heart production UCP-1[9]+/++++/+++++(+)/++(+)Markers[7,9,12]PPAR-γ,PLIN1,HOXC8,TLE3,C/EBPα,Rb,RIP140,APOL7C,DAPL1,SNCG,STAP1,GRAP2,MESTZIC1,LHX8,EVA1,EPSTI1,PRDM16,CIDEA,SCL27A2,COX7A1,CPT1B,KNG2m,ACOT11,BMP7Similar to BAT
2.2PVAT免疫微环境与血管平滑肌的功能 管周脂肪释放的炎症细胞因子参与调节平滑肌细胞收缩、增殖和迁移等过程[28]。
与其在内皮细胞中的作用类似,IL-6通过AngⅡ介导的途径显著增加VSMC中ROS的产生[29]。对C57BL6小鼠的IL-6体内干预实验表明其可以增加血管AT1受体的表达并介导内膜肥大[23]。此外,IL-6还在VSMC迁移和增殖过程中发挥作用[30]。
IL-17受体也存在于VSMC上[31]。IL-17A通过p38 MAPK依赖性途径诱导胶原蛋白Ⅰ、Ⅲ和Ⅴ的mRNA表达,导致胶原沉积和主动脉顺应性丧失[32]。经AngⅡ处理的IL-17A-/-小鼠血管通过合成超氧化物和纤维化维持血管正常功能[33]。IL-17A还可与TNF-α协同作用,增加人主动脉平滑肌细胞中趋化因子CCL8、CSF3、CXCL2和CCL7的表达[33]。IFN-γ也可以直接诱导VSMC增殖以及细胞凋亡[34,35]。此外IFN-γ也通过上调人主动脉平滑肌细胞中NOXs的表达和活性而影响超氧化物的产生[36]。
在马来西亚施工,部分工作必须是取得了政府部门许可的资格证书的人员才可从事的。HSSE部门先后组织了多次起重工(Rigger Signalman)、起重监督员(Lifting Supervisor)、急救员(First Aid,CPR & AED)、受限空间作业员(Authorised Entrant & Standby Person)、油气安全施工证(Oil and Gas Safety Passport)的取证培训。
如前所述,PVAT对血管功能的影响也依赖于脂肪因子的表达和释放。其中脂联素具有广泛的抗炎作用,而瘦素有促炎作用[37],二者的动态平衡对调节血管免疫微环境至关重要。研究发现,TNF-α、IL-6和IL-17A等促炎细胞因子可以抑制脂联素的合成[38],同时IL-17A和TNF-α可以增加瘦素的合成[39]。一方面,瘦素可以直接作用于VSMC与内皮细胞,促进NO的产生,使血管扩张;另一方面瘦素可以通过影响白细胞趋化性、氧自由基的释放、VSMC增生以及黏附分子在内皮细胞和VSMC上的表达来发挥间接的调节作用。此外,PVAT的抵抗素表达水平也相对较高,抵抗素上调黏附分子VCAM-1和ICAM的表达,诱导内皮细胞合成并分泌CCL2以及内皮素-1,从而导致内皮免疫微环境紊乱[40]。IL-1β、IL-6和TNF-α等炎症细胞因子可以上调抵抗素基因的表达[41]。此外,PVAT中免疫微环境紊乱的脂肪细胞可以产生高水平的趋化因子MCP-1、IL-8和IL-6,进一步激活PVAT的炎症反应。
3 PVAT免疫微环境改变与血管疾病
3.1PVAT免疫微环境改变与动脉粥样硬化 冠状动脉粥样硬化性心脏病(冠心病)对人类健康的危害极大,2017年发表在《Lancet》上的研究指出,2016年全球冠心病死亡人数超过940万,在264个单病种死因中排首位[42]。我国学者周脉耕在《Lancet》发表的临床流行病学研究也表明冠心病是目前中国人群第二位死亡原因[43]。而动脉粥样硬化(Atherosclerosis,AS)是导致冠心病发生、发展的主要原因,对PVAT的研究有助于更好地阐明动脉粥样硬化的发生机制,以期控制疾病的进展。
血管炎症在AS发生和进展中的作用已经得到了广泛印证[44],特别是炎症与内膜增生和动脉粥样硬化斑块形成之间的相互作用。但是,对于动脉粥样硬化,只关注动脉本身的炎症显然有失偏颇。由于PVAT与血管外膜联系密切,而且从解剖学的角度二者没有明确的边界,因此PVAT的作用也十分重要。
已有研究表明,管周脂肪的炎症反应在AS的不同时期均发挥着重要作用[45]。在动脉粥样硬化模型小鼠(ApoE-/-或LDL-R-/-)中,管周炎症发生的时间早于粥样斑块形成,甚至早于内皮的损伤[45]。在管周炎症过程中,ApoE-/-小鼠PVAT促炎细胞因子如IL-1和IL-6的释放增加[46],此外,血管周围炎症也与某些趋化因子的增加相关,如MCP-1、巨噬细胞炎症蛋白1-α(MIP-1α)和调节活化正常T细胞表达与分泌的趋化因子(Regulated upon-activation normal T cell expressed and secreted,RANTES)等[47-49]。而且,颈动脉管周脂肪移植可以通过外膜炎症反应和血管再生诱导LDL-R-/-动物的血管重构[47]。而血管内皮损伤也可以显著上调PVAT内MCP-1、TNF-α、IL-6和纤溶酶原激活物抑制剂-1(PAI-1)等促炎因子的表达并下调抗炎脂肪因子如脂联素的表达[50]。
同时,免疫细胞也在发挥着不同的作用。在ApoE-/-小鼠的AS过程中,巨噬细胞、T细胞和树突状细胞迁移进入血管外膜和脂肪组织[51],并且其浸润程度与炎症持续时间和病变面积相关[48]。在动脉硬化的早期阶段,外膜内就出现T细胞的浸润,但此时细胞分布较为分散[51],而在后期,浸润的细胞聚集、成团,形成结构复杂的外膜三级淋巴器官(Tertiary lymphoid organ,TLO)[52]。TLO是由于慢性炎症导致免疫细胞聚集成团形成的异位淋巴样结构。据报道,它们可以存在于慢性同种异体移植排斥、动脉粥样硬化、肺动脉高压和慢性阻塞性肺疾病患者的血管周围[52]。而且,TLO的形成是可逆的,当施加干预治疗或炎症消退后即消失[53]。
最近有研究发现,该过程中平滑肌细胞来源的IL-17C通过促进管周Th17细胞浸润发挥促动脉粥样硬化的功能。IL-17C-/-ApoE-/-小鼠主动脉免疫细胞浸润减少[54]。另外,外膜中的部分T细胞能够产生促炎因子IL-17A,IL-17A表达下调可导致巨噬细胞浸润下降和动脉粥样硬化程度的减轻。
免疫组化也显示,与高胆固醇喂养的野生小鼠相比,ApoE-/-小鼠和LDL-R-/-小鼠PVAT巨噬细胞和T细胞浸润均明显增加[55]。与此一致,Yamashita等[56]发现外膜中的巨噬细胞通过作用于基质和平滑肌细胞参与动脉粥样硬化的血管重构过程,但内膜无此现象。除此之外,在人类的AS中,人们还发现血管病灶周围的巨噬细胞向M2型极化[57],但其具体功能仍有待进一步研究。
除了巨噬细胞和T细胞,另一重要组分——肥大细胞也发挥其重要功能[58]。在斑块进展期,活化的肥大细胞在动脉外膜募集并促进巨噬细胞凋亡和微血管通透性增加[59]。此外,管周肥大细胞活化也促进单核细胞以CXCR2和VCAM1依赖性方式黏附[60]。
动脉粥样硬化中PVAT炎症的分子机制尚不清楚。有研究报道信号传导和转录激活因子4(STAT4)在脂肪细胞和免疫细胞中都有表达,并可能参与PVAT炎症。有研究表明在ApoE-/-小鼠和胰岛素抵抗的肥胖大鼠中STAT4基因的敲除可抑制动脉粥样硬化的进展过程和PVAT的炎症反应[61,62]。与ApoE-/-STAT4-/-小鼠相比,ApoE-/-小鼠PVAT中有较多的CD45+细胞和CD8+T细胞,而内脏脂肪无此差异。在ApoE-/-STAT4-/-小鼠中,PVAT炎症水平的降低亦与趋化因子CCL5、CXCL10、CX3CL1和TNF-α的表达下降相关。此外,STAT4-/-会导致AS模型小鼠PVAT中的巨噬细胞向产生IL-10和IL-4等的抗炎型分化,而总数目保持不变[61]。另外,使用四氢生物喋呤可经内皮细胞信号转导通路显著降低AS斑块和血管外膜白细胞的浸润[63]。而相关机制的探索也印证了上述研究,如血管保护性化合物Mas受体激动剂通过降低PVAT中趋化因子的表达和免疫细胞的募集来预防AS[45]。
3.2PVAT免疫微环境改变与高血压 高血压的发病与肾素-血管紧张素-醛固酮系统(Renin-angiotensin-aldosterone system,RAAS)的活化和血管氧化应激的增加有关。血管紧张素Ⅱ(AngⅡ)和活性氧(Reactive oxygen species,ROS)在血管炎症的发生和进展中都起着至关重要的作用[64]。高血压血管炎症最早发生于PVAT和PVAT/外膜边界内[65]。除肾素外,几乎所有的RAS系统成分都在PVAT中表达[66],并在调节高血压血管周围炎症中起关键作用。其中AngⅡ增加循环中活化的T细胞百分比,活化的T细胞随后聚集在病变部位的PVAT,诱发炎症并促进血管功能紊乱。AngⅡ还可诱导T细胞向Th1表型的转化,产生IFN-γ[67]。还有研究发现AngⅡ诱导的高血压与PVAT中B细胞的活化增加相关,该过程还与血清和主动脉外膜IgG2b与IgG3抗体沉积升高相关,并且降低B细胞的数量可以控制高血压[68]。
慢性氧化应激促进高血压血管炎症。高血压中,PVAT内ROS信号通路较为复杂,包括NADPH、内皮型一氧化氮合酶(eNOS)和抗氧化酶等多个关键组分[69]。PVAT来源的ROS可以通过清除eNOS或通过管周炎症来诱导内皮功能障碍[70]。而在PVAT和外膜浸润的巨噬细胞通过NOX2 NADPH氧化酶释放自由基[71]。巨噬细胞产生多种细胞因子,如IL-6、IFN-γ和TNF-α,改变血管平滑肌和PVAT的生物学功能。另一方面,p47phox、NOX1和NOX4等NADPH氧化酶组分敲除的小鼠内皮损伤和高血压严重程度明显降低[72],而平滑肌靶向过表达p22phox(NADPH催化亚基)小鼠的血管超氧化物产生增加,使PVAT中白细胞总数升高,并促进了血管功能障碍的发生[73]。
研究发现,对高血压小鼠模型,外源调节性T细胞(Tregs)可以减轻单核/巨噬细胞和T淋巴细胞在管周脂肪的浸润,改善血管功能紊乱,降低血压[74]。Treg细胞在PVAT 中占比较少,但功能非常重要。其以高表达CD25为特征,并表达叉头转录因子(FOXP3),通过释放抑炎细胞因子(IL-10和TGF-β等)维持免疫稳态,防止过度的免疫应答[75]。
研究还发现,在肥胖诱导的高血压中,免疫细胞主要浸润在大血管和阻力血管的PVAT内,如主动脉和肠系膜动脉。而且在非肥胖诱导的高血压中,相同部位免疫细胞的浸润要轻得多[76]。
3.3PVAT免疫微环境改变与动脉瘤 腹主动脉瘤(Abdominal aortic aneurysm,AAA)是一种炎症性疾病,与主动脉壁和PVAT的细胞组成发生显著变化有关。 动脉瘤常常形成在动脉粥样硬化的基础上。研究发现,许多炎症细胞,例如嗜中性粒细胞、巨噬细胞、T细胞、B细胞和肥大细胞参与AAA的形成[77,78],且在PVAT、管壁和腔内血栓中均可观察到[79],它们明显增加了AAA形成的易感性[80]。另外,TLR4或髓系分化因子88(MyD88)表达下调可减少血管周围炎症和AAA形成[81]。除了促进全身炎症外,PVAT中的白细胞能产生多种蛋白酶,包括促进主动脉壁平滑肌细胞降解的组织蛋白酶[82],从而导致动脉壁破坏以及动脉瘤的发生。
总之,PVAT炎症是血管病变的一个重要特征,其在不同疾病间存在着许多相似之处,但也存在重要差异。在动脉粥样硬化中,血管周围的免疫细胞浸润相对迅速,而且形成独特的外膜三级淋巴器官,在高血压中T细胞和B细胞浸润分布则更加分散。而巨噬细胞浸润PVAT在动脉粥样硬化中比在高血压中更为明显。动脉瘤是迄今为止唯一在PVAT明确观察到的外膜ATLO结构的人类疾病,这可能与动脉瘤发生时通常已经存在晚期动脉粥样硬化有关。
4 结语
管周脂肪是血管炎症发生的地点,是血管疾病进展的前哨站,赋予了其在血管功能调节中重要的作用,而且这种作用是双重的。一方面,PVAT维持管周免疫微环境稳态的作用已被证实,这也诠释了一个理念,那就是“fat is not always bad”;然而另一方面,PVAT也在某些情况下发生以保护性功能丧失为特征的功能紊乱,这不仅与脂肪因子相关,后来普遍认为炎症反应是该过程的主导。在炎症反应中,血管周围脂肪细胞去分化,不再主要行使脂质储存功能,而是成为代谢活跃的分泌器官,产生促炎细胞因子和趋化因子,参与心血管疾病的炎症进程。该过程与许多疾病,如高血压、动脉粥样硬化、动脉瘤和糖尿病等密切相关。更为重要的是,PVAT表型变化所导致的脂滴包被蛋白的丢失会引起原发性高血压和血管功能紊乱,亦伴有显著的炎性细胞浸润[83]。种种研究表明,PVAT对管周免疫微环境的调节在血管功能紊乱的进展中起着关键作用,是血管疾病恶性循环中的关键一环。然而,这一领域的研究还有很长的路要走,很多关键的问题仍待解决,比如管周炎症怎样影响血管的功能和重构?PVAT仅仅是外膜炎症的始发点,还是说它也调节血管内膜和中膜层?现在可以看到的是,PVAT参与调节管周免疫微环境,PVAT炎症是一个紧密调节的过程,它发生在血管疾病的早期,也是未来治疗的一个关键靶点。
