锰氧化物负极材料的制备及储锂性能研究
2019-04-08汪燕鸣
汪燕鸣,陈 盛,王 飞
(淮北师范大学信息学院,安徽淮北235000)
锂离子电池由于具有高能量密度和高功率密度的优点,可用作大型电子设备和电动汽车的电源。然而,高的能量密度需要高容量的电极材料。目前商业化的石墨类负极材料理论容量仅372 mAh g-1,难以满足大型动力电池的需求。金属氧化物类负极材料,如 Fe3O4、Co3O4、MnxOy,由于具有几乎三倍于石墨的理论容量而受到广泛的关注[1-3]。尤其锰氧化物(MnxOy)具有资源丰富、成本低、环境友好等优点显示出巨大的应用潜力。MnO2、Mn2O3、Mn3O4和MnO的理论容量分别达到1250、1018、936和750 mAh g-1;而且具有较低的充放电电压(0.5~1.25 V vs.Li/Li+)[4-7]。然而,MnxOy较低的电子导电性和转换反应过程中较大的体积变化导致其大电流可逆容量不高和快的容量衰减。为了进一步提高MnxOy的电化学性能,近年来研究者设计构筑纳米结构(纳米片、纳米棒、纳米球等)和多孔结构[8-10],以加快Li+的固相扩散和提高材料结构稳定性,取得较好的效果。
研究表明,电极材料形貌和微结构对其电化学性能具有显著的影响,由纳米粒子组装的多孔微米球能够有效缓冲电极反应过程中体积变化引起的机械应力,并能减小界面接触阻抗,获得好的电化学活性和循环稳定性[11-12]。本文采用简便的沉淀反应制备了球形碳酸锰前驱体,在不同条件下热分解获得四种锰氧化物,研究了它们的形貌微结构和电化学性能。
1 实验
1.1 材料制备
将1.69 g MnSO4·H2O(AR)溶解于200 mL去离子水和400 mL乙二醇(AR)的混合液中,然后加入4.2 g NaHCO3(AR)沉淀剂,在室温下磁力搅拌反应6 h。将沉淀过滤、洗涤、干燥后得到MnCO3前驱体。将两份前驱体粉末分别置于管式炉内空气氛中热分解,在400oC下处理5 h合成MnO2材料;在600oC下处理5h合成Mn2O3材料。将两份制得的MnO2分别置于管式炉内在H2/Ar(5:95,v/v)混合气中还原,在280oC下处理3h合成Mn3O4材料;在400oC下处理6h合成MnO材料。
1.2 材料表征
使用Bruker D8/ADVANCE型粉末X-射线衍射仪(XRD)分析样品的晶体结构。采用Phenom ProX台式扫描电子显微镜(SEM)和JEM-2100透射电子显微镜(TEM)观察样品形貌和微结构。
1.3 电化学性能测试
按质量比70:20:10的比例将锰氧化物(MnO2、Mn2O3、MnO2和Mn3O4)负极材料、Super P导电碳和聚偏氟乙烯粘结剂在5 mL小烧杯中混合均匀,加入适量N-甲基吡咯烷酮溶剂超声分散0.5 h后磁力搅拌4 h形成均匀的浆料。用湿膜制备器将浆料均匀刮涂在铜箔上,在鼓风干燥箱中60°C下烘干,剪切成直径12 mm的圆片,在80°C下真空干燥后转入充满Ar的手套箱中组装成CR2016型扣式电池。圆形锂片作为对电极,1 M LiPF6/EC+DMC(v/v,1:1)作为电解液。在室温下测试电池性能:在LANHE CT2001电池测试系统上进行恒流充放电测试,截止电压范围为0.01-3.0 V;在CHI 650C型电化学工作站上测试循环伏安(CV)曲线,扫速为0.1 mV s-1。
2 结果与讨论
图1是制备的四种锰氧化物材料的XRD图。图1a对应于P63/mmc空间群的MnO2(PDF No.30-0820)[4];图1b对应于Ia-3空间群的Mn2O3(PDF No.41-1442)[5];图1c对应于I41/amd空间群的Mn3O4(PDF No.24–0734)[3];图1d对应Fm-3m空间点群的MnO(PDF No.78–0424)[7]。四种锰氧化物的衍射峰清晰,没有检测到其它杂相物质,说明选择合适的热处理条件可将碳酸锰前驱体分解生成不同的纯相氧化物。

图1 四种锰氧化物的XRD谱图
图2为制备的四种锰氧化物材料的SEM和TEM图。SEM图显示,四种锰氧化物均具有单分散亚微米球形形貌,平均直径约400 nm。可见,MnCO3前驱体在不同条件下热处理后均能保持原有球形形貌。TEM图显示热分解时释放CO2,在球体内部形成丰富的孔隙;球体由相互连接的纳米粒子构成,形成稳定的三维多孔结构。然而,组成四种锰氧化物的纳米颗粒大小有差异,Mn2O3和Mn3O4纳米粒子约40 nm,且球体内部孔隙较大;MnO纳米粒子约10 nm,球体内部孔隙分布均匀;而MnO2纳米粒子最小,且球体内部较为密实。可见,MnCO3前驱体在不同温度和气氛下分解得到的产物微观形貌和组成粒子的大小存在一定差异。这种多孔微纳结构有利于电解液的渗透,促进材料和电解液的接触,有利于增大电极反应界面,提高材料的电化学活性[2-4]。同时,三维多孔结构能够有效缓冲材料充放电过程中的体积变化[5,9,12],提高材料的循环稳定性。
图3为四种锰氧化物材料前3次循环的CV曲线图。由图可见,首次负向扫描曲线中,MnO2、Mn2O3和Mn3O4位于大约1.2、1.3和1.5 V处的还原峰对应于Mn4+/3+还原为Mn2+;位于0.15 V附近的尖锐还原峰对应Mn2+还原为Mn[3-4]。在随后的正向扫描曲线中,位于1.3 V的氧化峰对应Mn氧化为Mn2+/3+[5,7]。首次负扫在0.15 V的还原峰在随后的第2和3次循环扫描中正向移动到0.25 V附近,说明了固体电解质界面膜(SEI)的产生主要在第1次循环。第2和3次循环的扫描曲线基本重合,说明材料具有较好的电极反应可逆性。电极反应过程可表示为:MnOx+2x Li++2x e-↔Mn+x Li2O。

图2 SEM 图:MnO2(a1),Mn2O3(a2),Mn3O4(a3),MnO(a4);TEM图:MnO2(b1),Mn2O3(b2),Mn3O4(b3),MnO(b4)
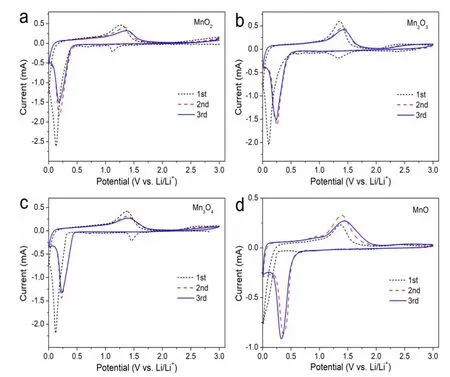
图3 四种锰氧化物的CV曲线
图4为四种锰氧化物材料在0.1 A g-1电流密度下前5次循环的充放电曲线。MnO2、Mn2O3、Mn3O4和MnO的首次放/充电容量分别为1850/1058、1545/1100、1705/1077和1198/913 mAh g-1,库仑效率分别为57%、71%、63%和76%。首次不可逆容量损失主要是在电极表面形成SEI层以及Mn的不完全氧化;从第2次循环开始,充放电曲线稳定。在第5次循环时,MnO2、Mn2O3、Mn3O4和MnO的库伦效率已分别上升到89%、94%、86%和97%,放电容量分别为 752、1012、1054 和 968 mAh g-1。可见,Mn3O4在0.1Ag-1电流密度下具有最高的可逆容量。

图4 四种锰氧化物的在0.1 A g−1下的充放电曲线
图5为四种锰氧化物的倍率性能曲线。由图可知,随着充放电电流增大,反应极化的程度加重,可逆放电容量逐渐减小。在1 A g-1电流密度下MnO2、Mn2O3、Mn3O4和 MnO 仍然具有 396、473、347和683 mAh g-1的平均放电容量,特别是MnO与Mn2O3在2 A g-1的高电流密度下还分别具有515和392 mAh g-1的可逆放电容量,仍然高于商业石墨负极的理论容量(372 mAh g-1)。四种锰氧化物表现出不同的倍率性能,与其多孔微纳结构密切相关。MnO虽然在0.1 A g-1的小电流密度下容量低于Mn2O3和Mn3O4,但其却具有最高的倍率性能,这主要由于其具有较小的一次纳米颗粒和均匀的孔隙结构,增大了电极反应界面,缩短了锂离子在材料固相中扩散路程[7,9,12]。尽管MnO2的一次纳米颗粒最小,首次放电容量最高,但密实的球形颗粒内部孔隙相对较小,不利于电解液的渗透,因此倍率性能最差。

图5 四种锰氧化物的倍率性能曲线
图6为四种锰氧化物材料在0.2Ag-1电流密度下的循环性能曲线。由图可见,在前20次循环中,四种锰氧化物的放电容量均呈现不同程度的下降趋势,这可归因于相转变反应引起的体积变化和部分颗粒的粉化[1,12];随着循环次数的增加,电极材料内部结构不断重组活化,引起可逆容量逐渐提升,这在很多多孔氧化物负极材料中是一个普遍现象[3-7]。循环 200 次后,MnO2、Mn2O3、Mn3O4和MnO的可逆放电容量分别为1206、1070、1147和917 mAh g-1,容量保持率分别为第2次放电的123%、110%、93%和89%;可见,在低电流密度下MnO2表现出最好的循环可逆性。另外,MnO2、Mn2O3、Mn3O4和MnO在200次循环后的可逆容量分别达到各自理论容量的96%、105%、122%和122%,因此本文采用简单的沉淀热解法制备的多孔锰氧化物均表现出较好的电化学活性。

图6 四种锰氧化物的循环性能曲线
3 结论
采用简便的沉淀-热解法成功制备了MnO2、Mn2O3、Mn3O4和MnO四种多孔球形锰氧化物负极材料。由纳米颗粒组装成的直径约400 nm的多孔球结构,提供较大的电极反应界面,利于Li+的快速传输;丰富的孔结构可缓解嵌脱锂时的体积变化,提高循环可逆性。电化学测试表明,MnO2、Mn2O3、Mn3O4和MnO循环200次后的可逆放电容量分别为1206、1070、1147和917 mAh g-1,达到各自理论容量的96%、105%、122%和122%,表现出较高的电化学活性和循环稳定性。其中MnO与Mn2O3在2 A g-1的高电流密度下放电容量达到515和392 mAh g-1,高于商业石墨负极的理论容量(372 mAh g-1),表现出较好的功率性能。
