新型评分系统在动脉瘤性蛛网膜下腔出血预后预测中的研究进展
2019-03-16冯宇轩姚声涛匡舒蔓方莎莎
冯宇轩,姚声涛,匡舒蔓,汪 峰,方莎莎
(遵义医学院附属医院脑血管病科,贵州 遵义 563000)
动脉瘤性蛛网膜下腔出血(aneurysmal subarachnoid hemorrhage,aSAH)是脑血管疾病中较为常见的一种类型,具有起病急骤、发病凶险、进展迅速等特点。据不完全统计,大约有50%的患者在发病后1年内死亡,然而即使侥幸存活也只有33.3%的患者能够不依靠他人独立生活,并且最终能够成功避免神经功能损害而达到完全康复的患者仅占其中的25%[1]。其原因主要与颅内压增高,脑积水形成,迟发性脑缺血(delayed cerebral ischemia,DCI)发生,微循环功能障碍,脑组织扩散性抑制样去极化以及神经系统自我调节功能受损等密切相关[2]。因此,需要早期识别具有不良预后风险的患者,从而加强对他们的监测并尽可能地采取更为先进的治疗策略。目前国内外专家学者根据疾病的临床表现和影像学特征研制出Hunt-Hess评分、Fisher分级以及世界神经外科医师联盟分级(World Federation of Neurological Surgeons,WFNS)等多个临床评分量表用于患者预后的评估[3-4]。但是随着时间的推移,它们已经无法满足临床医师的需求,故而多种新型评分系统被相继提出并得到广泛的认可。现对近年来由多位研究人员所创建的评分量表进行综述,以期为更加精确地预测aSAH预后提供理论基础。
1 马萨诸塞州总医院评分量表
1998年Ogilvy和Carter[5]为了更精确地对aSAH患者预后进行评估,将409例行显微夹闭术的患者资料进行多元Logistic回归分析,并归纳出5个相对危险度较高的因素进行组合,创建出第一个针对颅内动脉瘤夹闭患者预后的评分(表1)。该评分系统由Hunt-Hess分级、Fisher分级、年龄、动脉瘤大小以及后循环是否有大小>25 mm的动脉瘤5个评分项目组成,评分范围为0~5分。2006年Ogilvy等[6]将其命名为马萨诸塞州总医院(Massachusetts General Hospital,MGH)评分,并对行开颅动脉瘤夹闭和血管内介入栓塞的患者进行研究分析后发现,无论患者行何种治疗,MGH评分量表均能精确地对其预后进行预测。然而它不仅能提升对aSAH患者预后预测的准确率,还有多种用途。其中Sun等[7]研究发现,MGH评分量表能较好地对脊髓海绵状血管瘤患者病情进行评估。Rosenthal等[8]对aSAH患者进行MGH评分后发现,其能准确地预测DCI发生。

表1 MGH评分
MGH:马萨诸塞州总医院;后循环:大脑后动脉、基底动脉末端、小脑上动脉、基底动脉干、椎基底动脉连接处、小脑后下动脉
2 aSAH入院患者的预后评分量表
aSAH入院患者的预后(prognosis on admission of aneurysmal subarachnoid hemorrhage,PAASH)评分量表(表2)最早由Takagi等[9]于1999年提出,并在2008年由van Heuven等[10]命名。它是一种将格拉斯哥昏迷评分(Glasgow coma scale,GCS)分为5个不同等级的评分系统。其中van Heuven等[10]分别通过PAASH评分量表和WFNS评分量表对aSAH患者预后进行预测后发现受试者工作特征曲线下面积(area under curve,AUC)分别为0.81和0.82。但是由于PAASH评分量表中不同类别的比值比高于WFNS评分量表,认为PAASH评分量表与aSAH患者预后的关联性更强。但是在PAASH评分量表诞生前,Oshiro等[11]已经根据GCS评分的特点将其分成5个等级。随后使用该评分量表与Hunt-Hess评分量表以及WFNS评分量表一起进行一致性检验后发现Kappa值分别为0.46、0.41、0.27。之后St Julien等[12]对1 532例aSAH患者进行统计学分析后表达了对Oshiro等[11]提出方案的认可,并认为可以将其广泛应用于临床。因此如何将GCS评分进行划分才能更加精确地预测aSAH患者的预后值得进一步思考。
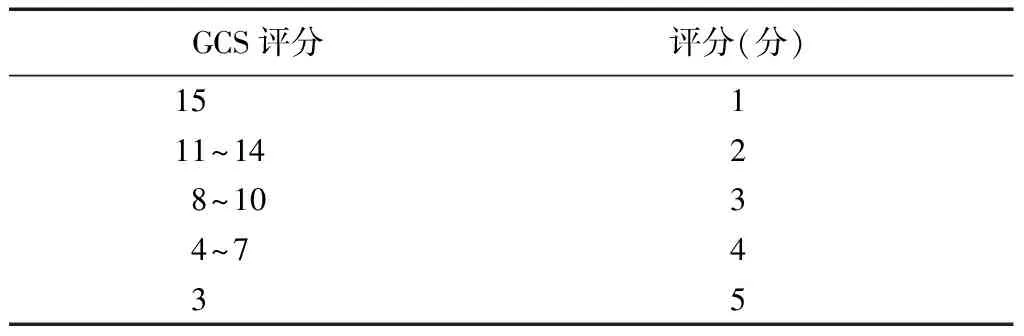
表2 PAASH评分
PAASH:动脉瘤性蛛网膜下腔出血入院患者的预后;GCS:格拉斯哥昏迷评分
3 Elwatidy评分
Elwatidy[13]通过收集哈立德国王大学附属医院行开颅动脉瘤夹闭的aSAH患者资料进行统计学分析建立了新的评分量表(表3)。该评分量表包括Hunt-Hess分级、蛛网膜下腔内积血厚度、是否有脑积水以及动脉瘤大小4个项目组成,评分范围为-8~9分。其中Elwatidy评分≤-2分为低危组,患者大多有较好的预后;-2分
4 Rosen评分
Rosen和Macdonald[14]将欧洲、澳大利亚、新西兰、南非以及北美等多个地区神经外科中心的3 567例aSAH患者进行随机对照试验,并依据既往研究得出的结论,将20个可能对预后造成影响的临床和放射学参数进行单变量和多变量分析后建立出一套全新的评分系统(表4)。该评分系统包括WFNS评级、年龄、是否有高血压史、入院收缩压、动脉瘤大小、动脉瘤部位、蛛网膜下腔内积血厚度以及是否入院时有脑血管痉挛发生8个项目组成,评分范围为1~15分。随后使用新量表与WFNS评级对预后进行预测后发现AUC分别为0.78和0.74[14]。然而虽然将多个危险因素与WFNS评级组合在一起能够提升预测效能,但是未能在临床上得到广泛应用。其原因可能与其评分项目过多,且无法对临床医师做出的决策产生影响有关。

表3 Elwatidy评分

表4 Rosen评分
WFNS:世界神经外科医师联盟分级;1 mmHg=0.133 kPa
5 全面无反应性评分
GCS评分是最早对昏迷患者预后进行评估的评分系统,并在临床上得到了广泛应用[15]。但随着时间的推移,GCS评分预测的准确性受到各种质疑。其原因包括GCS评分无法对带有气管插管的患者进行语言评定,并且缺乏对脑干反射、呼吸运动以及神经系统查体中一些细微改变的检测[16]。然而Wijdicks等[16]在充分认识GCS评分量表的缺点和不足的基础上创建出全面无反应性(full outline of unresponsiveness,FOUR)评分量表(表5)。该量表包括睁眼反应、语言反应、脑干反射以及呼吸运动4个评分项目,评分范围为0~16分。随后为了验证FOUR评分量表在aSAH预后预测中的适用性,Zeiler等[17]对aSAH患者入院当天、入院后第7天以及入院后第14天进行规范化评分后发现,入院后第1天以及第7天的FOUR评分与患者病死率,出院后1个月和出院后6个月患者的预后密切相关;入院后第14天的FOUR评分仅与出院后6个月患者的预后有关;脑干反射亚组评分与患者预后无关联。但目前FOUR评分多用于样本量小、入院病情较为平稳的患者。因此,还需要对入院病情危重的aSAH患者进行多中心临床试验进行验证。

表5 FOUR评分
FOUR:全面无反应性
6 Mocco评分
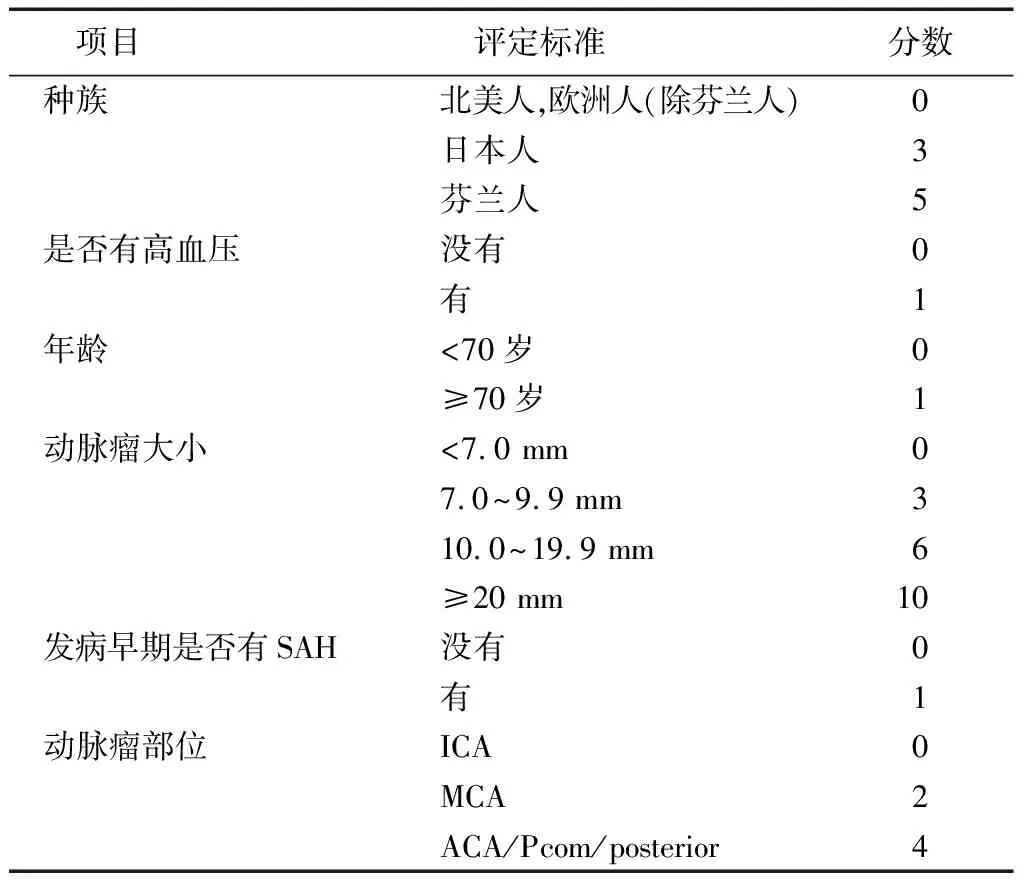
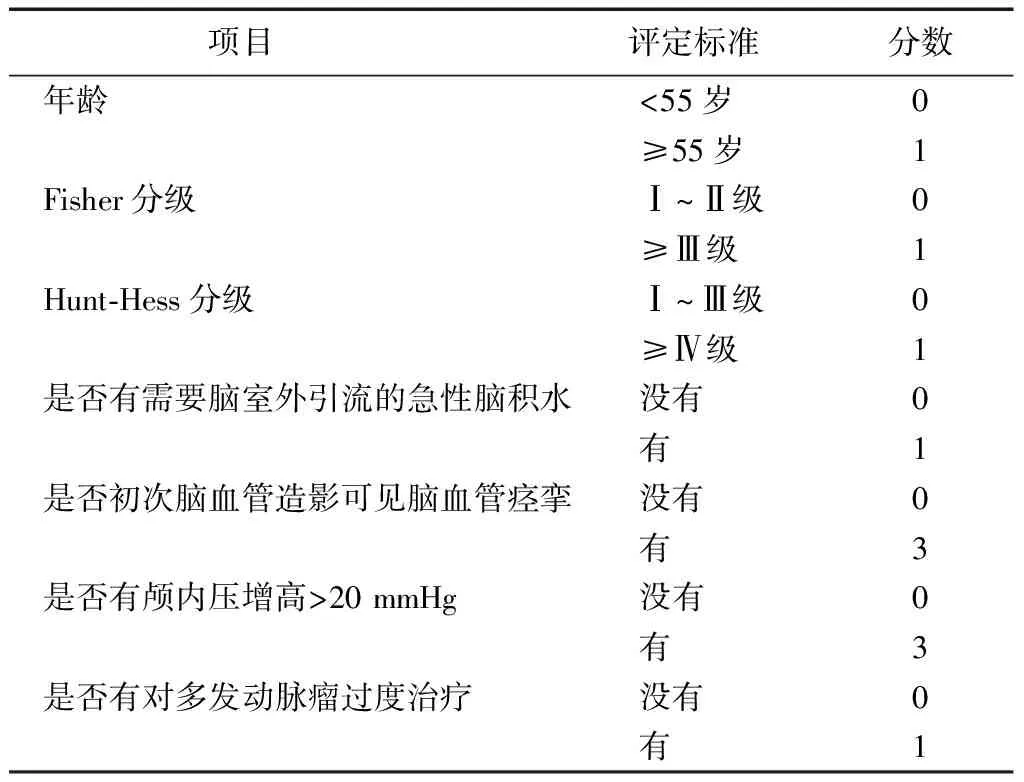
近年来,根据临床评分的特点将aSAH划分为多个等级。其中Hunt-Hess分级为Ⅳ、Ⅴ通常被定义为高级别,且预后一般较差[18-20]。但是在临床上却有部分高分级患者在进行相应的治疗后能获得较好的结局。因而对高级别aSAH患者的长期预后进行精确预测变得十分重要。Mocco等[21]将高级别aSAH患者根据是否行开颅夹闭或介入栓塞分为保守治疗组和外科干预组,通过对组内和组间差异性进行分析后建立了一套针对高级别aSAH的评分系统(表6)。该评分系统由年龄、Hunt-Hess分级、动脉瘤大小以及血糖浓度4个评分项目组成,评分范围为0~7分。其中Mocco评分≤1分为预后较好组,Mocco评分2分为预后中等组,2分 表6 Mocco评分 低级别GCS(poor grade GCS,PGS)评分量表(表7)由Starke等[22]研发。将它与PAASH评分量表进行对比后可以发现两者的评分方式大体一致,但是唯独缺少GCS评分为13~15分的患者。其主要原因是Starke等[22]只纳入Hunt-Hess分级为Ⅳ、Ⅴ级的高级别aSAH患者,然而在这些患者中GCS评分最高也只能达到12分。但是作者将他们进行前瞻性研究后发现PGS评分量表能更简便、更快速、更精确地对高级别aSAH患者的预后做出预测。 表7 PGS评分 PGS:低级别格拉斯哥昏迷评分;GCS:格拉斯哥昏迷评分 为了能够更加准确地预测aSAH介入栓塞术后患者的预后,Degos等[23]于2012年创建出入院生物临床评分(admission bioclinical score,ABC)(表8)。该评分量表由GCS评分、肌钙蛋白I以及中枢神经特异性蛋白3个评分项目组成,评分范围为0~6分。随后分别使用ABC评分、GCS评分、WFNS分评和Fisher分级对2003—2007年以及2008—2009年两个不同时间段行血管内治疗的患者1年病死率进行预测后发现ABC评分的AUC值分别为0.82和0.76,并且都明显高于其他评分量表。与此同时,还发现随着ABC评分的增加,量表的灵敏度在不断降低,然而其特异度以及1年病死率在不断提升。但目前通过ABC评分预测aSAH预后的研究仍较少,所以还需要更多的随机对照试验证实其有效性。 表8 ABC评分 ABC:入院生物临床评分;GCS:格拉斯哥昏迷评分 近年来随着对aSAH发病特点的深入研究,发现动脉瘤破裂出血后颅内血肿形成是影响患者预后极为重要的因素之一[24]。Shim等[25]为了能够更直观地进行评估,对行开颅动脉瘤夹闭和血肿清除的患者进行非参数秩和检验和χ2检验后构建出一套针对合并有颅内血肿的aSAH预后评分(表9)。该评分量表包括颅内血肿体积是否≥25 mL、中线移位是否≥5 mm以及是否蛛网膜下腔弥漫性出血3个评分项目组成,评分范围1~4分。之后Lee等[26]将大脑中动脉动脉瘤破裂伴脑血肿形成的患者根据血肿所在部位的不同分为外侧裂血肿组和脑实质内血肿组,并分别对两组进行评分后发现Shim评分与他们出院时的GCS预后评分密切相关。 表9 Shim评分 Fisher分级是最早通过判定头颅CT各个层面上蛛网膜下腔积血的程度来预测脑血管痉挛发生的评分量表。但近年来,随着CT扫描的各参数性能不断增加,Fisher分级的预测效能在逐渐降低。为了能够准确地对aSAH后症状性脑血管痉挛的发生做出预测,美国巴罗神经学研究所创建出巴罗神经学研究所(Barrow Neurological Institute,BNI)评分量表(表10)[27]。该量表主要根据脑池或侧裂池内血肿的厚度进行评分,评分范围为1~5分。此后随着研究的深入,BNI评分在其他方面的表现也得到了肯定。其中Diesing等[28]研究发现BNI评分的高低与aSAH后分流依赖性脑积水的发生密切相关。Dengler等[29]将BNI评分与Fisher评分进行对比后发现,BNI评分在预测造影性脑血管痉挛以及早期脑梗死发生方面更佳。Neidert等[30]对多个医疗中心进行外部检验分析后发现BNI评分与患者的不良预后以及DCI的发生紧密相关。 表10 BNI评分 BNI:巴罗神经学研究所 Naval等[31]通过回顾性分析aSAH患者院内死亡因素进行归纳分析后创作出一个新的评分量表(表11)。该量表由GCS评分、年龄以及是否有合并症3个评分项目组成,评分范围为0~9分。通过双盲试验对所有病患进行评分后发现评分范围为7~8分时阳性预测值为88.5%,然而评分范围为6~8分时阳性预测值下降为83%。但阴性预测值在0~2分和0~3分时相差不大,分别为94%与92%。其后使用Naval评分量表、WFNS评分量表以及Hunt-Hess评分量表进行预测后发现AUC分别为0.821、0.777和0.771。因此认为Naval评分可以更加精确地预测出aSAH院内病死率。 表11 Naval评分 GCS:格拉斯哥昏迷评分:合并症:高血压、使用可卡因、糖尿病、冠状动脉疾病、充血性心力衰竭、慢性阻塞性肺疾病、痴呆、脑卒中、慢性肾功能衰竭、癌症/肿瘤、肝硬化、获得性免疫缺乏综合征 2014年Lee等[32]创造出一套适合所有SAH患者院内死亡预后评分系统,并将其命名为HAIR评分[Hunt-Hess评分,年龄(Age),脑室内出血(IVH),24 h内再次出血](表12)。该评分量表包括Hunt-Hess分级、年龄、是否有脑室内出血以及是否有24 h内再次出血4个评分项目组成,评分范围为0~8分。其中HAIR评分≤2分为低危险组,3分≤HAIR评分≤5分为中危险组,6分≤HAIR评分≤8分为高危险组。此后为了验证HAIR评分系统的预测效能,Witsch等[33]分别对1 629例SAH患者进行评分后发现当评分区间在0~5分时能够明确地分辨出患者病死率的高低,但是当评分区间在6~7分时发现病死率与评分无相关性,而当评分为8分时患者病死率为100%。Dengler等[34]通过研究发现HAIR评分能够预测aSAH的预后以及脑梗死的发生情况。HAIR评分在Abulhasan等[35]的研究中也得到了验证。 Greving等[36]通过系统回顾和汇集分析构建了一套适用于颅内动脉瘤破裂风险的预测评分系统,并将其命名为PHASES[种族(Population),高血压(Hypertension),年龄(Age),动脉瘤体大小](表13)。该评分量表包括种族、是否有高血压、年龄、动脉瘤大小、发病早期是否有SAH以及动脉瘤部位6个评分项目组成,评分范围为0~22分。Backes等[37]通过Cox回归分析发现PHASES评分同样能用于动脉瘤生长风险的预测。Foreman等[38]通过研究发现较高的PHASES评分是造成aSAH患者预后不良的独立危险因素。 表12 HAIR评分 表13 PHASES评分 SAH:蛛网膜下腔出血;ICA:颈内动脉;MCA:大脑中动脉;ACA:大脑前动脉 DCI是导致aSAH患者病死率和病残率增加的主要因素,因而针对DCI早发现、早治疗十分重要。但是DCI高危患者难以识别,且潜在的危险因素也无法确定[39]。为了能够早期预测DCI的发生,de Oliveira Manoel等[40]将其发病风险进行分层创建出VASOGRADE评分量表(表14)。该评分量表根据WFNS分级和改良Fisher分级将aSAH患者分成绿色、黄色以及红色三个类别。其中绿色代表DCI发生风险较低,黄色代表DCI风险比率有增加的趋势,红色代表DCI的发生率比其他患者高3倍。有研究发现VASOGRADE评分同样能够预测aSAH患者的预后,但是预测效能与WFNS分级和Hunt-Hess评分基本一致[34]。 表14 VASOGRADE评分 Jabbarli等[41]为了能够早期识别出aSAH后脑梗死发生的高危人群,于2015年提出了BEHAVIOR评分量表。该评分量表由年龄、Fisher分级、Hunt-Hess分级、是否有需要脑室外引流的急性脑积水、是否初次脑血管造影可见脑血管痉挛、是否有颅内压增高>20 mmHg以及是否有对多发动脉瘤过度治疗7个评分项目组成,评分范围为0~11分。其中0分≤BEHAVIOR评分≤2分为低危险组,3分≤BEHAVIOR评分≤6分为中危险组,7分≤BEHAVIOR评分≤11分为高危险组。各组间脑梗死发生的平均风险率分别为23.6%,62.3%,93.2%。此外,通过分析还发现BEHAVIOR评分与患者短期预后也密切相关。 表15 BEHAVIOR评分 1 mmHg=0.133 kPa 2018年Ahn等[42]通过大量的观察,对aSAH患者早期头颅CT各个层面所发生的细微变化创建出蛛网膜下腔出血早期脑水肿评分(subarachnoid hemorrhage early brain edema score,SEBES)量表(表16)。该量表主要将岛叶皮质矢状层面和大脑半球半卵圆中心层面进行评定。其中脑沟消失或大脑白质与大脑灰质交界区被破坏均被评为1分,而两者均无异常则被评为0分,评分范围为0~4分。之后研究分析发现,SEBES能够当作早期脑损伤的替代标志物,并能准确地预测DCI的发生以及临床预后。Savarraj等[43]通过酶联免疫吸附试验测定aSAH患者血清中不同生物学标志物的表达水平后发现巨噬细胞炎性蛋白1β是高SEBES评分(评分≥3分)的独立危险因素。SEBES评分还被当作评分项目纳入mSWAI评分量表[44]。并且mSWAI评分也被认为能够反映早期脑损伤的发生情况,并能较好地预测SAH患者预后以及DCI的发生。 表16 SEBES评分 SEBES:蛛网膜下腔出血早期水肿评分 Maragkos等[45]对近年来提出的评分系统进行总结后发现大多数评分系统使用困难并且主观性较强。因而为了能够更加简便客观地对aSAH预后做出预测,他们构建出脑动脉瘤研究所(Brain Aneurysm Institute,BAI)评分量表(表17)。该评分由年龄、复苏后GCS评分、蛛网膜下腔积血的厚度、入院后是否使用抗血小板治疗4个评分项目组成,评分范围为0~5分。之后将BAI评分与Hunt-Hess评分、WFNS评分、改良Fisher评分、MGH评分以及BNI评分进行对比后发现其预测效能最高,并认为它有利于早期对aSAH患者病情做出评估从而促进医疗资源的合理分配。然而BAI评分作为目前对aSAH预后预测最精确的评分系统还需进一步得到外部验证才能广泛应用于临床。 表17 BAI评分 BAI:脑动脉瘤研究所;GCS:格拉斯哥昏迷评分 目前,神经科学领域的专家已经研制出大量的组合型评分量表用于预测aSAH患者的预后。然而通过对各个量表中的参数进行观察后可以发现几乎所有的量表都没有将术中相关因素纳入评分项目。但是是否需要对载瘤动脉或颈内动脉临时夹闭、是否动脉瘤再次破裂出血、是否因动脉瘤巨大而需要将其做旷置切除以及动脉瘤夹闭或栓塞过程中是否有粥样斑块脱落等术中不可预见因素也常影响患者预后[46]。因此,仍需要将这些危险因素纳入研究,从而降低预测的误差,提升精准度。
7 低级别GCS评分

8 入院生物临床评分

9 Shim评分

10 巴罗神经学研究所评分

11 Naval评分

12 HAIR评分
13 PHASES评分

14 VASOGRADE评分

15 BEHAVIOR评分
16 蛛网膜下腔出血早期脑水肿评分

17 脑动脉瘤研究所评分

18 小 结
