四数九里香中的咔唑类生物碱成分及其细胞毒活性研究
2019-03-08周永福陈鸿平刘友平
周永福,陈鸿平,陈 林,刘友平 ,李 应
1成都中医药大学药学院,成都 611137;2重庆工业职业技术学院化学与制药工程学院,重庆 401120
九里香属植物具有行气止痛、活血化瘀之功效[1];民族民间用于胃痛、风湿痹痛、外治牙痛、跌扑肿痛、虫蛇咬伤[2];主要含有咔巴唑生物碱、黄酮类、香豆素类等[3]。四数九里香(MurrayatetrameraHuang)主要分布于海南南部、广西、云南南部一带。在当地少数民族地区(彝族、壮族、苗族、傣族)以其干燥叶入药。临床上用于局部麻醉、降血糖[3]等。为了阐明其药效与化学成分的相关性,我们对该植物药做了系统研究。
我们采用冷浸渍法对采自于云南华宁的四数九里香进行冷浸、过滤、减压蒸馏、得浸膏;使用硅胶层析柱、凝胶柱色谱、重结晶等方法对浸膏的乙酸乙酯萃取部分进行分离纯化,运用1H NMR、13C NMR、HSQC、HMBC和ESI-MS等波谱方法和文献数据对比,鉴定化合物结构。结果:从四数九里香的叶子中鉴定得到7个咔唑类生物碱、1个甾体类化合物:分别为β-谷甾醇(1)、1-甲基-3-丙酰基咔唑(2)、1-甲氧基-3-乙基咔唑(3)、1-甲氧基-3-甲酰基咔唑(4)、1-甲氧基-3-甲基咔唑(5)、1-羧基甲酯-3-甲基咔唑(6)、1-羧基甲酯-3-乙基咔唑(7)、mananimbine(8)。除了化合物1、其他化合物为首次从该植物中分离得到,化合物2、3、4、5、7对SMMC-7721显现良好的细胞毒活性。
1 仪器及材料
核磁共振仪(TMS为内标、瑞士bruker公司、400 MHz型);柱色谱用硅胶GF254(200~300目、青岛海洋化工公司);Sephadex LH-20,ODS2A(50 μm,日本 日本YMC/维美希公司);旋转蒸发仪(河南省巩义市予华仪器有限公司);循环水式真空泵:SHZ-D(III)(河南省巩义市予华仪器有限公司);低温冷却循环泵(DLSB-5L/25、河南省巩义市予华仪器有限公司)UtraScan ESI-MS(瑞士bruker公司);二氧化碳培养箱(济南鑫贝西生物技术有限公司)、多功能酶标分析仪(MULTISKAN FC);乙醇、乙酸乙酯、石油醚、甲醇均为工业纯,减压蒸馏使用。
药材于2016年2月采自云南省华宁县,经成都中医药大学陈新博士鉴定为芸香科九里香属四数九里香MurrayatetrameraHuang的枝叶。植物标本(标本编号:20160122001)保存于重庆工业职业技术学院中医药物研究所;SMMC-7721细胞株购自于中国科学院昆明细胞库。
2 提取与分离
四数九里香叶35 kg,晾干、粉碎、60%的乙醇溶液浸提(5×10.0 L×3)、浓缩、合并,得浸膏2.8 kg,温水溶解、分别用石油醚、乙酸乙酯、正丁醇萃取、浓缩得石油醚萃取部分200 g;乙酸乙酯萃取部分680 g;正丁醇萃取部分460 g。
用硅胶色谱柱(200~300目、10 cm×150 cm)对乙酸乙酯萃取部分进行分离、分别用石油醚;乙酸乙酯(20∶1→18∶3→16∶5→14∶7→12∶9→10∶11→8∶13→6∶15→0∶21)为流动相进行洗脱,经TLC检测后合并得39个组分:A1→A39。A1(80 g)经过混合溶剂(乙酸乙酯和丙酮)溶解、自然放置得针状结晶、重结晶,得化合物1(45 g,展开剂为:石油醚:乙酸乙酯=20∶1,Rf=0.67);A1余下部分经过硅胶柱色谱、使用环己烷:乙酸乙酯(30∶1→25∶6→20∶11→15∶16→10∶21)和乙酸乙酯为混合溶剂进行淋洗,得5个馏分:A1-1、A1-2、A1-3、A1-4、A1-5;A1-1(2.0 g)上凝胶色谱柱(2 cm×150 cm),纯化得化合物2(30.8 mg,环己烷:乙酸乙酯=10∶1,Rf=0.62);A1-2(4.5 g)上正相硅胶柱子(2 cm×50 cm),用环己烷:乙酸乙酯为15∶1淋洗、合并相同部位,自然放置,得晶体,为化合物3(53.65 mg、环己烷:乙酸乙酯=6∶1,Rf=0.72);A1-3(5.0 g)上凝胶柱子(3 cm×120 cm),分成三段:F1-3;F1进行薄层层析刮板,制得化合物4(6.8 mg,石油醚:乙酸乙酯=5∶1,Rf=0.78)、F2进行薄层层析刮板,得化合物5(13.4 mg,石油醚:乙酸乙酯=5∶1,Rf=0.51)、F3进行薄层层析刮板,得化合物6(21.1 mg,石油醚:乙酸乙酯=2∶1,Rf=0.76);A1-4(7.0 g),重复上正相,分为4馏分,各馏分上凝胶、合并相同部分,重结晶得化合物7、8。
3 结构鉴定
化合物1无色针晶(CHCl3);1H NMR(400 MHz,CDCl3) δ:7.26(1H,s,-OH),5.35(3H,d,H-6),3.52(1H,dd,H-3),2.17(7H,s,H-8),1.84(7H,m,H-9),1.00(3H,s,H-19),0.92(3H,d,J=6.5 Hz,H-21),0.85(3H,d,J=7.0 Hz),0.83(3H,d,J=6.9 Hz),0.81(3H,d,J=6.8 Hz),0.68(3H,s,H-18);13C NMR(CDCl3,100 MHz) δ:12.01(C-18),12.11(C-26),18.90(C-19),19.04(C-29),19.41(C-21),19.83(C-28),21.09(C-25),23.07(C-15),24.31(C-22),26.07(C-12),27.23(C-27),28.26(C-8),29.16(C-7),31.67(C-2),31.92(C-1),33.95(C-23),36.16(C-20),36.51(C-10),37.26(C-16),39.78(C-4),42.32(C-24),45.84(C-13),50.14(C-9),56.06(C-17),56.78(C-14),71.79(C-3),121.72(C-6),140.77(C-5)。以上数据与文献[4]报道一致,确定化合物为β-谷甾醇。
化合物2油状(CHCl3);1H NMR( 400 MHz,CDCl3) δ:8.03(1H,d,J=7.6 Hz,H-5),7.48(1H,d,J=7.6 Hz,H-8),7.36(1H,m,J=7.6 Hz,H-7),7.20(1H,dd,J=7.6 Hz,H-6),6.73(1H,s,H-2),2.15(3H,s,-CH3),1.25(2H,dd,-CH2-);13C NMR(CDCl3,100 MHz) δ:15.46(-CH3),27.06(-CH2-),29.72(-CH3),103.74(C-2),110.74(C-4),111.38(C-1),114.29(C-4a),116.68(C-8),117.85(C-4b),119.60(C-6),124.01(C-3),124.29(C-7),131.01(C-8b),138.87(C-8a),143.77(C-5),154.05(-C=O)。以上数据与文献[5]一致,鉴定化合物为1-甲基-3-丙酰基咔唑。
化合物3油状(CHCl3);1H NMR( 400 MHz,CDCl3) δ:8.00(1H,d,J=8.00 Hz,H-5),7.44(1H,d,J=8.05 Hz,H-8),7.21(t,J=8.00 Hz,J=8.00 Hz,H-7),7.195(t,J=8.00 Hz,J=8.00 Hz,H-6),3.995(3H,s,-OCH3),1.529(3H,s,-CH3);13C NMR(CDCl3,100 MHz) δ:21.95(-CH3),29.72(-CH2-),55.48(-OCH3),107.65(C-7),110.90(C-8),112.50(C-4),119.14(C-6),120.46(C-5),123.51(C-3),124.29(C-4a),125.49(C-2),127.96(C-8a),129.45(C-4b),139.44(C-8b),145.32(C-1)。以上数据与文献[6]一致,鉴定化合物为1-甲氧基-3-乙基咔唑。
化合物4油状(CHCl3);1H NMR( 400 MHz,CDCl3) δ:10.01(1H,s,-CHO),8.71(1H,s,H-N),8.17(1H,s,H-4),8.10(1H,d,J=8.0 Hz,H-5),7.51(1H,d,J=6.8 Hz,.H-8),7.477(1H,t,J=6.9 Hz,H-7),7.451(1H,s,H-2),7.33(1H,t,J=6.9 Hz,H-6),4.041(3H,s,H-OCH3);13C NMR(CDCl3,100 MHz) δ:146.26(C-1),139.61(C-8b),130.13(C-3),123.83(C-4a),123.78(C-4b),139.64(C-8a),103.67(C-2),111.71(C-8),120.62(C-4),120.68(C-5),120.86(C-6),126.79(C-7),192.15(1-CHO),55.942(-OCH3)。以上数据与文献[7]报道一致,故鉴定化合物为1-甲氧基-3-甲酰基咔唑。
化合物5油状(CHCl3);1H NMR(400 MHz,CDCl3) δ:8.00(1H,d,J=8.00 Hz,H-5),7.44(1H,d,J=8.05 Hz,H-8),7.21(t,J=8.05 Hz,H-7),7.19(t,J=8.00 Hz,H-6),3.99(3H,s,-OCH3),1.53(3H,s,-CH3);13C NMR(CDCl3,100 MHz) δ:22.17(-CH3),55.57(-OCH3),107.92(C-7),111.20(C-8),112.86(C-4),119.66(C-6),120.65(C-5),123.59(C-3),124.57(C-4a),125.76(C-2),128.30(C-8a),129.68(C-4b),139.73(C-8b),145.54(C-1)。以上数据与文献[8]一致,鉴定化合物为1-甲氧基-3-甲基咔唑。
化合物6油状(CHCl3);1H NMR(400 MHz,CDCl3) δ:8.06(1H,d,J=7.6 Hz,H-5),7.58(1H,d,J=8.0 Hz,H-8),7.52(1H,s,H-2),7.38(1H,t,J=7.6 Hz,J=7.2 Hz,H-6),7.17(1H,t,J=8.0 Hz,J=7.2 Hz,H-7),6.85(1H,s,H-4),4.01(3H,s,-OCH3),2.52(3H,s,-CH3);13C NMR(CDCl3,100 MHz) δ:22.68(-CH3),56.53(-OCH3),109.21(C-7),112.83(d,C-8),113.85(m,C-4),120.17(m,C-6),121.65(m,C-5),124.82(d,C-3),125.75(C-4a),126.78(C-2),129.90(C-8a),130.31(C-4b),141.72(C-8b),147.32(C-1),178.98(C-1-C=O)。以上数据与文献[9]一致,鉴定化合物为1-甲酸甲酯-3甲基咔唑。
化合物7油状(CHCl3);1H NMR(400 MHz,CDCl3) δ:8.17(1H,d,J=7.6 Hz,H-5),8.13(1H,s,H-8),7.59(2H,m,J=8.0 Hz,J=8.4 Hz,H-2),7.35(2H,m,J=7.6 Hz,J=8.0 Hz,H-6,H-7),7.29(1H,d,J=7.6 Hz,J=8.0 Hz,H-3),4.62(2H,s,-OCH2-),4.21(3H,s,-OCH3),3.39(3H,s,-OCH3);13C NMR(CDCl3,100 MHz) δ:58.75(-OCH3),65.18(N-OCH3),76.36(-O-CH2-),109.99(C-7),110.27(C-8),121.63(C-4),121.68(C-6),121.87(C-5),122.04(C-3),122.31(C-4a),128.11(C-2),128.36(C-8a),132.60(C-4b),139.23(C-8b),140.01(C-1).低分辨质谱显示分子离子峰为m/z:241.012;分子式为:C15H15NO2,以上数据与文献[10]一致,鉴定化合物为1-甲醚-9-甲氧基咔唑。
化合物8油状(CHCl3);1H NMR(400 MHz,CDCl3) δ:7.94(1H,d,J=7.50 Hz),7.68(1H,s,H-4),7.41(3H,d,J=8.00 Hz,H-5),7.32(t,J=8.10 Hz),6.67(d,J=8.00 Hz,H-8),5.68(1H,d,J=9.8 Hz),4.02(2H,s,H-13),3.52(2H,s),2.55(1H,s),2.36(3H,s),2.20(3H,t),1.48(3H,s);13C NMR(CDCl3,100MHz) δ:14.15(3-CH3),16.10(10-CH3),22.76(C-13),40.78(C-12),55.48(C-11),104.20(C-1),110.37(C-8),112.50(C-4a),116.61(C-9),117.54(C-3),118.43(C-5),119.20(C-6),121.25(C-4),123.93(C-5a),124.19(C-7),124.19(C-14),125.64(C-15),128.54(C-10),131.70(C-1a),139.45(C-8a),149.91(C-2)。低分辨质谱显示m/z=307.26,[M+H]+,提示化合物分子式为:C21H25NO。以上数据与文献[11]报道的数据基本一致,鉴定化合物为mananimbine。
4 细胞毒活性研究
用含10%胎牛血清的RMPI1640培养液配成单个细胞悬液,以每孔5 000 个细胞接种到96孔板,每孔体积100 μL,细胞提前12~24 h接种培养;化合物用DMSO溶解,以100、20、4、0.8、0.16 μg/mL浓度筛选肝癌细胞株SMMC-7721,每孔终体积200 μL,每种处理均设3个复孔。37 ℃条件下培养48 h后,弃孔内培养液;每孔加MTS溶液20 μL和培养液100 μL;设3个空白复孔(MTS溶液20 μL和培养液100 μL的混合液),继续孵育3 h,使反应充分进行;选择492 nm波长,采用多功能酶标仪(MULTISKAN FC)读取各孔光吸收值(A),应用两点法(Reed and Muench法)计算各化合物的IC50值[12]。
细胞抑制率=(A对照-A样品)/(A对照-A空白)
每次实验均设顺铂(DDP)和紫杉醇(Taxol)两个阳性对照化合物,以浓度为横坐标,细胞存活率为纵坐标绘制细胞生长曲线,应用两点法(Reed and Muench法)计算化合物的IC50值。初步筛查结果见表1;结合初步筛查结果,以化合物编号为横坐标,细胞抑制率为纵坐标,制得图1。化合物的IC50值见表2。
表1化合物1~8的肝癌细胞株(SMMC-7721)毒活性初步测试结果
Table 1 The cytotoxic activity of compound1-8(Preliminary test result)
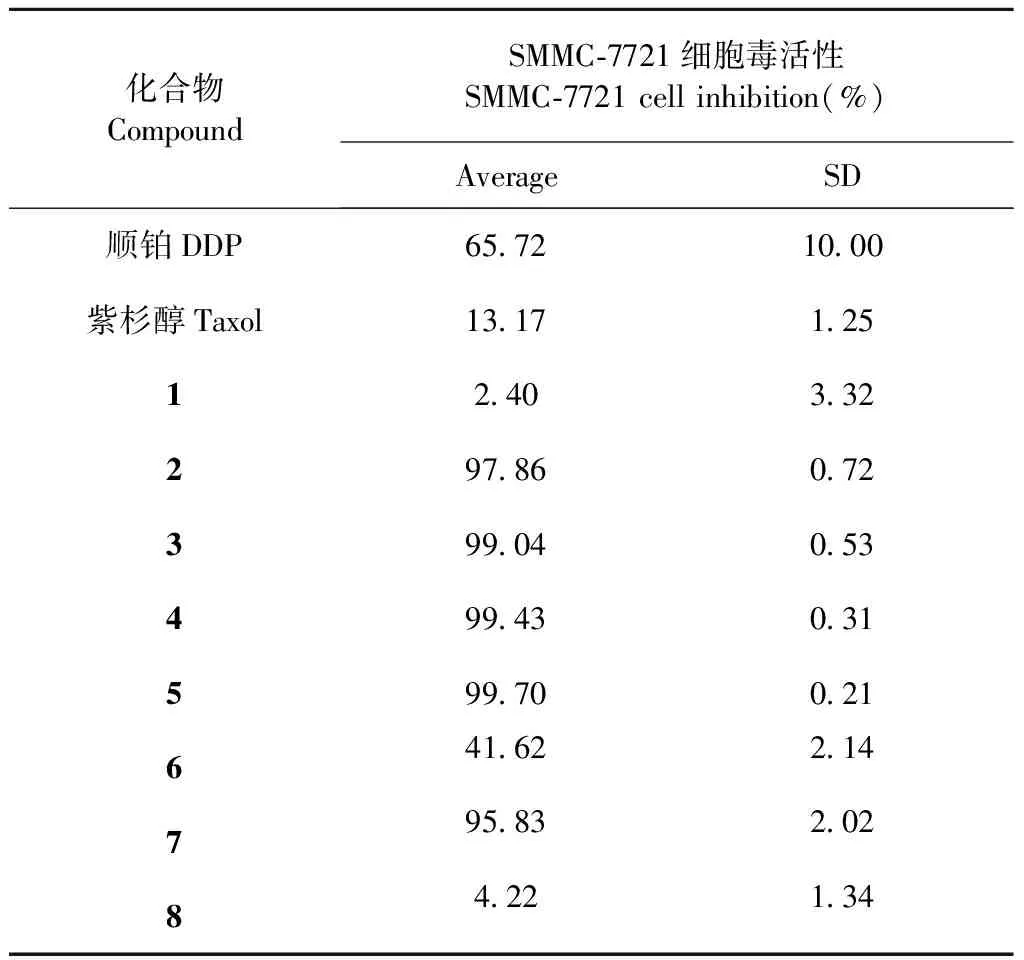
化合物CompoundSMMC-7721细胞毒活性SMMC-7721 cell inhibition(%)AverageSD顺铂DDP65.72 10.00 紫杉醇Taxol13.17 1.25 12.40 3.32 297.86 0.72 399.04 0.53 499.43 0.31 599.70 0.21 641.62 2.14 795.83 2.02 84.22 1.34
注:与顺铂(DDP)和紫杉醇(Taxol)两个阳性化合物比较。
Note:Compare with DDP and Taxol.
在100 μg/mL浓度下,单体化合物对肝癌细胞株毒活性初步测试结果见表1;从表1中明显看到:与阳性化合物对比,化合物2~5、7对肝癌SMMC-7721的体外肿瘤生长有半数抑制活性。
以化合物对SMMC-7721细胞的体外肿瘤生长有半数抑制活性为筛选基础,进一步分析测试化合物2~5、7的细胞毒活性IC50值。测试结果见表2。
化合物2~5、7的IC50值表明:与阳性对照物比较,化合物2~5、7对肝癌细胞株SMMC-7721显现了很好的细胞毒活性。
5 结论
九里香属植物四数九里香MurrayatetrameraHuang具有抗炎症,抗生育、抗甲状腺等作用。本实验通过色谱技术从中分离制得8个单体化合物,采用现代波谱分析方法鉴定了它们的结构,分别为7个咔唑类生物碱和1个甾体化合物;并以肝癌细胞株(SMMC-7721)为细胞模型,分别对这8个化合物做了细胞毒实验初步筛选和复选,研究表明:化合物2~5、7对肝癌细胞株SMMC-7721显现了很好的细胞毒活性。该研究结果为四数九里香抗肝癌活性提供了数据和理论支持,为进一步研究开发民族民间药物四数九里香和相关的抗肝癌新药提供了坚实的基础。
表2化合物2~5、7的肝癌细胞株毒活性测试结果(IC50)
Table 2 The SMMC-7721 cytotoxic activity of compound2-5,7(IC50)
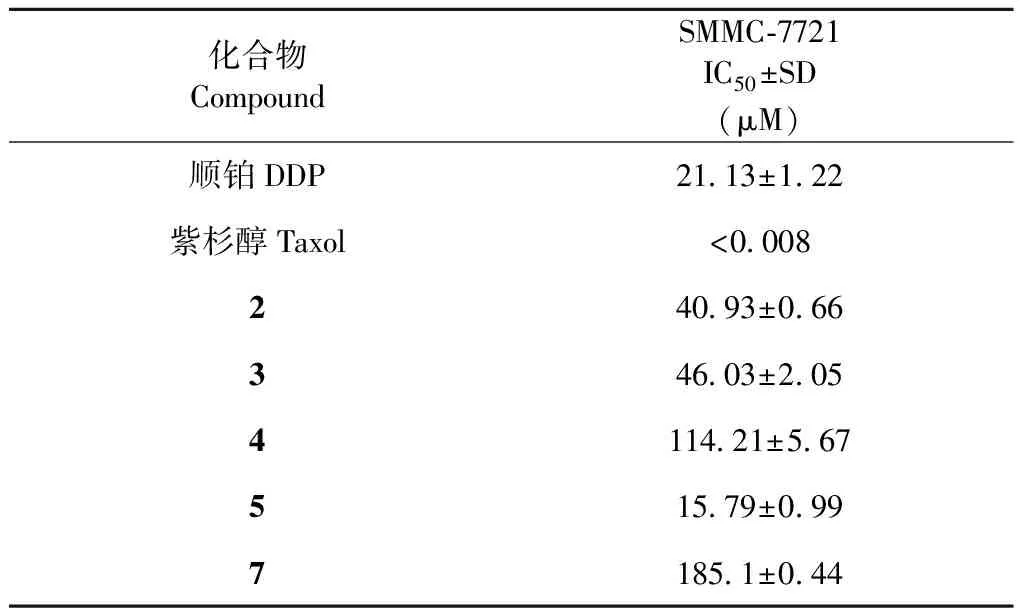
化合物CompoundSMMC-7721IC50±SD(μM)顺铂DDP21.13±1.22紫杉醇Taxol<0.008240.93±0.66346.03±2.054114.21±5.67515.79±0.997185.1±0.44
