碳纳米管改性g-C3N4提升可见光催化降解性能
2019-02-27鹏李2周颖梅徐艳朱捷王士凡蔡可迎堵锡华杨朋举
王 鹏李 昭,2周颖梅徐 艳朱 捷王士凡蔡可迎 李 靖 堵锡华 杨朋举
(1徐州工程学院化学化工学院,徐州 221018)
(2中国矿业大学化工学院,徐州 221116)
(3福州大学化学学院,能源与环境光催化国家重点实验室,福州 350116)
0 引 言
光催化技术是一项能够缓解能源短缺和改善环境污染问题的前沿技术。设计研制具有可见光响应、量子效率高、稳定性好的光催化剂是当前光催化领域的研究热点和难点。近年来,以石墨相氮化碳(g-C3N4)为代表的聚合物半导体,由于其能带、光吸收及物化性质等易调控,已经成为光催化领域、特别是光催化材料领域的研究热点[1-3]。
g-C3N4具备良好的化学稳定性,廉价易得,环境友好,且具有独特的电子能带结构。g-C3N4导带位置和价带值分别是-0.89和1.81 V[4-5],从热力学上观察,其能带结构可应 用于光解水[6]、CO2还原反应[7]、氧还原反应[8]、选择性有机合成[9]、污染物降解[10]等领域。然而,体相g-C3N4通常具有较小的比表面积和较低的可见光利用率,且激子结合能高和光生载流子难以分离,因而光催化效率较低,仍不能满足实际应用需求,故必须对其进行改性。多壁碳纳米管具有独特的管腔结构,优异的限域效应,被作为载体广泛应用于金属催化领域[11]。它还具有优异的电子效应,能够接受、转移及储存电子,能够延迟及阻碍g-C3N4内光生电子-空穴的复合[12]。除此之外,CNT还具有较大的比表面积可适当调控g-C3N4的形貌及结构特点[13],以获得更多的光催化活性位点。
本文采用CNT与g-C3N4进行复合,借助CNT与g-C3N4的间的协同作用,优化光催化剂的电子能带结构和纳米结构,增强可见光吸收,提高电子转移能力。以尿素为前驱体制备出一系列CNT/g-C3N4催化剂。并以RhB水溶液模拟废水,系统考察了不同CNT含量对催化剂在可见光下催化降解性能的影响。 并通过 XRD,SEM,FT-IR,N2吸附-脱附,XPS,UV-Vis-NIR Spectrophotometer,PL 等表征,深入探讨了CNT复合对g-C3N4的形貌结构和光学性质的影响,并分析其降解机理。
1 实验部分
1.1 试剂与仪器
尿素,无水乙醇,均为分析纯,国药集团化学试剂有限公司;RhB,分析纯,天津市化学试剂研究所;CNT,分析纯,中国科学院成都有机所。
X射线粉末衍射仪(XRD,UltimaⅣ型)日本理学公司,Cu Kα靶,波长为0.154 06 nm,工作电压为40 kV,工作电流为 40 mA,扫描范围为 5°~85°,扫描速度为10°·min-1;紫外-可见-近红外分光光度计(UV-Vis-NIR Spectrophotometer,Lambda 750 型),美国 PE 公司;荧光光谱仪(PL,Hitachi F-2700型),日本日立公司,激发波长为380 nm;傅里叶红外光谱仪(FT-IR,ALPHA型),德国布鲁克公司;扫描电镜(SEM,Apreo型),捷克 FEI公司,在 600或 1 kV 下操作拍摄;透射电镜(TEM,JEM-2100F),日本 JEOL公司,在200 kV下操作,晶格分辨率0.14 nm;物理吸附仪(Tristar 3000型),美国Micromeritics公司,77 K N2吸附;X射线光电子能谱仪(XPS,AXISULTRA DLD 型), 日本岛津公司,Al Kα 射线(hν=1 486.6 eV);光化学反应仪(YM-GHX-Ⅶ),上海豫明仪器有限公司;超声波清洗器(KQ-250DB),昆山市超声仪器有限公司;集热式恒温加热磁力搅拌器(DF-101S),巩义市予华仪器有限责任公司;管式炉(OTF-1200X-80),合肥科晶材料技术有限公司;台式高速离心机(TG16MW),湖南赫西仪器装备有限公司。
1.2 催化剂制备
1.2.1 g-C3N4的制备
采用一步热缩合法制备g-C3N4光催化剂。以尿素为原料,称取20 g尿素至玛瑙研钵中研磨至均匀后装入40 mL的小坩埚内,再将小坩埚放置于瓷方舟上,放入管式炉中,通N2。以5℃·min-1升温速率升温到550℃后,保温3 h,最后在N2气氛下冷却至室温,得到的浅黄色固体,即为g-C3N4。称量所得产物约为1 g(产率为5%)。所得样品记为CN。
1.2.2 CNT预处理
与直接使用CNT不进行预处理[14]或将CNT置于水热釜中简单处理使其表面官能团化不同[13,15],本文采取的处理方法如下:将CNT置于盛有浓HNO3(68%(w/w))的三口烧瓶内,在140℃条件下回流14 h对CNT进行纯化、切割,使CNT开口及引入表面官能团。接着将混合液用去离子水进行过滤及洗涤,直至pH值为7,然后放入烘箱中于60℃干燥10 h,研磨为粉末。这种开放体系下的充分回流使得CNT不仅表面富含羟基、羧基官能团,同时HNO3中的氮使得CNT微量氮掺杂[16-17]。此外,还使CNT被有效切割,具有较多缺陷位。
1.2.3 g-C3N4与CNT复合催化剂的制备
称取20 g尿素与适量处理后的CNT,将两者混合放入烧杯中加入50 mL水使尿素完全溶解。再将其置于超声仪中,超声1 h使CNT完全分散。超声后将烧杯放入油浴锅内,设置温度为100℃,使其缓慢蒸干水分。之后,产品在烘箱中于60℃下干燥24 h,最后在N2氛围下焙烧。焙烧条件与上述制备g-C3N4保持一致。得到一系列CNT/g-C3N4光催化剂。将CNT在催化剂中的质量百分数为0.05%,0.1%、0.3%和0.5%的催化剂样品分别记为CN-CNT0.05,CN-CNT0.1,CN-CNT0.3,CN-CNT0.5。 其 颜 色 随 着CNT含量的增加,逐渐加深至灰色。
1.3 光催化性能测试
选取RhB作为光催化降解反应的目标污染物。具体步骤如下:首先称取0.03 g催化剂样品于试管中,加入50 mL浓度为10μg·mL-1的RhB溶液。加入磁子搅拌使催化剂均匀分散在RhB溶液中。以氙灯作为光源,480 W功率,电压、电流分别为80 V、6 A。在循环水中加入亚硝酸钠溶液使得只有可见光作为入射光。光照前需要避光搅拌1 h,使光催化剂充分分散于RhB溶液中,以达到吸附平衡。实验过程中,光照每隔1 h取一次样,每次取4 mL,放入8 000 r·min-1的高速离心机中离心得澄清液体。在紫外可见分光光度计上测定RhB的吸光度,取定波长λ=553 nm。以最初配置的10μg·mL-1的RhB溶液为原液,分别配置 2、4、6、8、10 μg·mL-1的 RhB 溶液。测定吸光度,得到关于浓度与吸光度的标准曲线。 以 10 μg·mL-1为初始浓度,记为 C0′,暗反应后的初始浓度为C0,不同时间段测得的浓度记为Ct。以Ct/C0′作为RhB的光降解率。以Ct/C0′为纵坐标,反应时间为横坐标,得到样品对RhB的降解反应活性图,从而对样品的光催化性能进行分析。动力学曲线拟合时取暗反应后的浓度为初始浓度C0,即可拟合得到过原点的动力学曲线。
2 结果与讨论
2.1 催化剂的形貌分析

图1 g-C3N4与CNT改性g-C3N4样品的SEM表征Fig.1 SEM images of the bulk and CNT modified g-C3N4 samples
为了研究所制备样品的形貌特征,采用扫描电子显微镜对其进行表征。由图1(a,b)可知,g-C3N4具有典型的石墨层状结构,由许多带有褶皱的银耳状块体相互堆叠而成,其块体的大小约为几微米至几十微米不等。掺杂0.1%的CNT使g-C3N4的团聚现象有所加强,如图1d所示,银耳状块体间空隙变小,彼此连接紧密。而与CN-CNT0.1样品相比,0.5%CNT的掺杂在一定程度上又增强了样品的分散性,如图1(e,f)所示,其片状结构明显增多,彼此间隙变大。可见CNT的添加量对体相g-C3N4的形貌特点产生影响,并有可能改变其织构参数。
由于SEM表征未能发现样品中的CNT,为了证明CNT的存在,对CN-CNT0.5样品进行了TEM表征。如图2所示,CNT高分散于g-C3N4内部,且无明显团聚现象,CNT两端开口,内径小于8 nm,且管长为0.5~2μm,这主要归因于采用浓硝酸预处理,将CNT有效切割,说明该方法可有效制备CNT与g-C3N4复合催化剂,易实现CNT和g-C3N4的均匀复合。
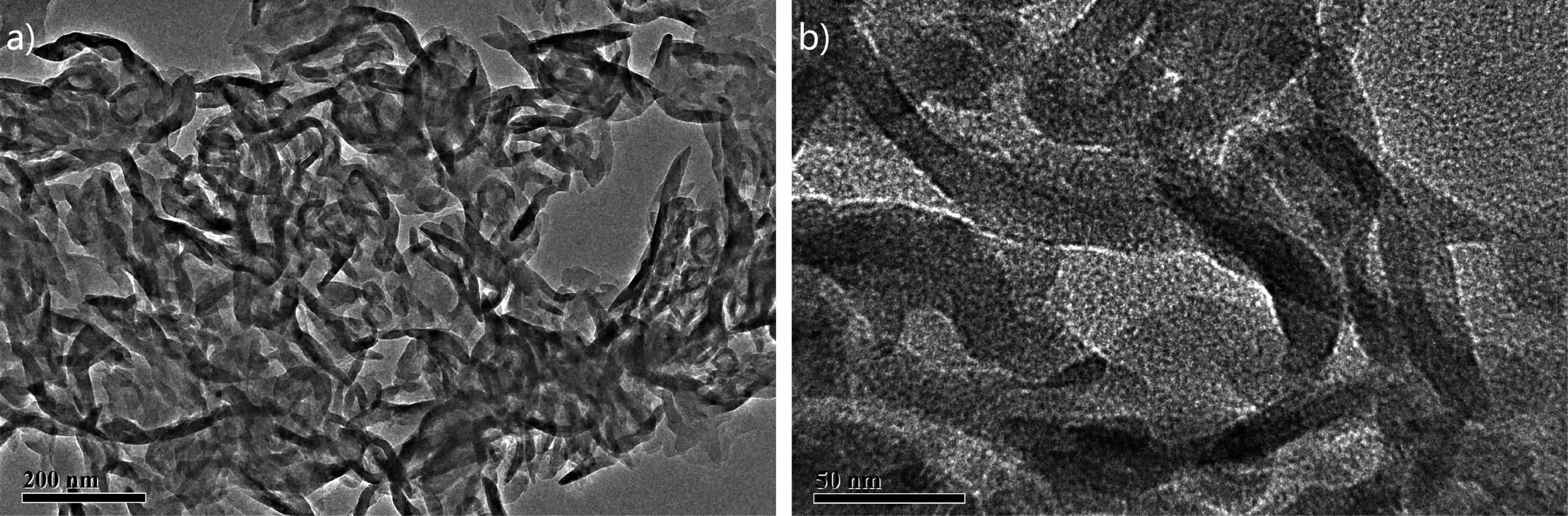
图2 CN-CNT0.5样品的TEM图Fig.2 TEM images of the CN-CNT0.5 sample
2.2 催化剂的结构与组成分析
体相g-C3N4与系列CNT/g-C3N4复合催化剂的XRD图如图3所示。其中27.5°的衍射峰强度最高,为共轭芳香物层间堆积特征峰,对应g-C3N4的(002)晶面。13.0°处的衍射峰代表的是平面层的七嗪结构单元,对应的是 g-C3N4的(100)晶面[18-19]。 可发现随CNT含量的降低,复合样品中g-C3N4衍射峰的强度不断减弱。碳的加入会调控氮化碳的聚合过程,而0.1%的添加量对氮化碳的生长调控最为明显,其(002)晶面的衍射峰最弱,说明其氮化碳的尺寸较小。而当碳的添加量增加,纳米管很可能存在一定的团聚,而这样的团聚体可能会作为氮化碳聚合的位点(可能起到模板作用)从而促进其生长。图中10°附近的衍射峰很可能是由插层效应引发的,随着CNT复合量的增多,该峰强度逐渐升高。且图中样品并未发现CNT的特征衍射峰,说明CNT分散于g-C3N4内,与SEM表征结果一致。
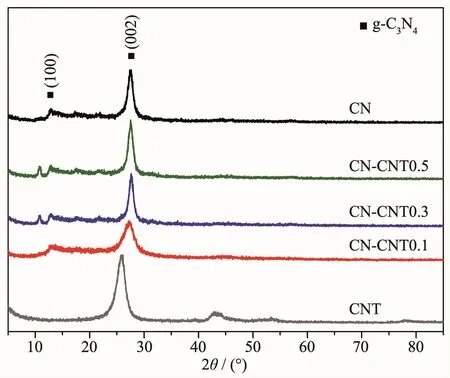
图3 g-C3N4与CNT/g-C3N4系列光催化剂的XRD图Fig.3 XRD patterns of the g-C3N4 and CNT/g-C3N4 photocatalysts
g-C3N4与CNT/g-C3N4复合催化剂的红外谱图如图4所示,复合样品所有吸收峰与g-C3N4样品的FT-IR光谱特征峰几乎完全相同,说明催化剂制备过程中CNT的复合并没有改变g-C3N4的成键结构,所有样品具有相似的化学组成。图中吸收峰主要集中在3个区域:3 000~3 500 cm-1处的宽吸收峰对应的是N-H的伸缩振,且复合之后出现宽化,说明复合体系存在氢键。1537,1462,1 408,1 318 和 1 238 cm-1处的吸收峰源于典型的CN杂环伸缩振动模式;810 cm-1处尖锐的吸收峰,主要是由于三嗪环状化合物的弯曲震动吸收所引起的[20-21]。
XPS常用于分析催化剂表面元素组成及价态变化。图5为CN及CN-CNT0.1样品中的C1s和N1s等元素XPS谱图。如图5a所示,2个样品的C1s XPS谱图的2个主要特征峰分别位于283.5 eV和287.1,283.5 eV分别代表外来碳、石墨碳(C-C/C=C键),287.1 eV处的峰归属于嗪环中sp2杂化的碳(NC=N键),而292.7 eV归属于嗪环内的π电子离域效应[22-23]。 通过 XPS分析软件 Thermo Avantage分峰计算发现,在CN样品中283.5 eV处峰面积与287.1 eV处峰面积比值为0.85,而在CN-CNT0.1样品中二者比值高达1.84。CNT内以C-C/C=C键为主,与氮化碳复合后样品内石墨碳比例大幅提升,说明CNT有效复合于体相g-C3N4内,即微量CNT的加入改变了复合催化剂表面碳物种的分布。在N1s XPS谱图中(图5b)1个主峰可分为3个特征峰,位于397.5,398.3,400.0 eV,分别归属于sp2杂化的N原子C=N-C,连接环状结构的N原子N-(C)3及氨基中的 N 原子-NH 或-NH2[14,24]。 由图可知,CNT 的加入也改变了复合样品表面氮物种的分布比例。
2.3 催化剂织构特点、能带结构及光生电荷性质
催化剂详细的织构信息表明0.1%CNT加入使体相g-C3N4的比表面积下降,孔容亦减小(表1)。说明微量CNT的加入造成氮化碳轻微团聚。而随着加入CNT量的提升,样品的比表面积又有所回升,孔容也进一步扩大,结合SEM表征,可推断CNT含量的增多有利于g-C3N4的剥离,导致其结构特点发生改变。
为了研究光催化剂样品的光学性质,在室温下采用紫外-可见-近红外分光光度计和PL荧光光谱仪对所有样品进行检测。样品对可见光的响应吸收以及根据其转换得到的能带间隙是光催化剂特性的重要参数。
图6为所制备样品的UV-Vis漫反射谱图。N2中焙烧所得的CN样品于452 nm附近出现了明显的吸收边,0.1%CNT的添加使吸收边发生“红移”至465 nm,而随着CNT添加量的提高,0.3%和0.5%CNT的添加使光催化剂在460~800 nm区间内对可见光的吸收增强。吸收强度的增强归因于CNT的加入降低了光线的反射,且CNT良好的导电性加速了电子的转移[24]。 由半导体禁带求导公式:αhν=A(hν-Eg)2以 hν为横坐标,以(αhν)1/2为纵坐标作图。其中 α为光学吸收系数,hν为光子能量,A为比例常数,Eg为带隙。对该图做切线得到样品的禁带宽度Eg(图7)。CN的禁带宽度为2.78 eV,CNT的复合降低了其带隙能,提高了可见光的利用率,其中CN-CNT0.1的禁带宽度最低为2.74 eV。综上所述CNT/g-C3N4复合光催化剂与体相g-C3N4相比,其对可见光的吸收性能显著增强,利用率有所提高,可能有助于g-C3N4光催化活性的提升。

表1 CN和CN-CNT系列催化剂的织构参数Table 1 Textural properties of the CNand CN-CNT catalysts
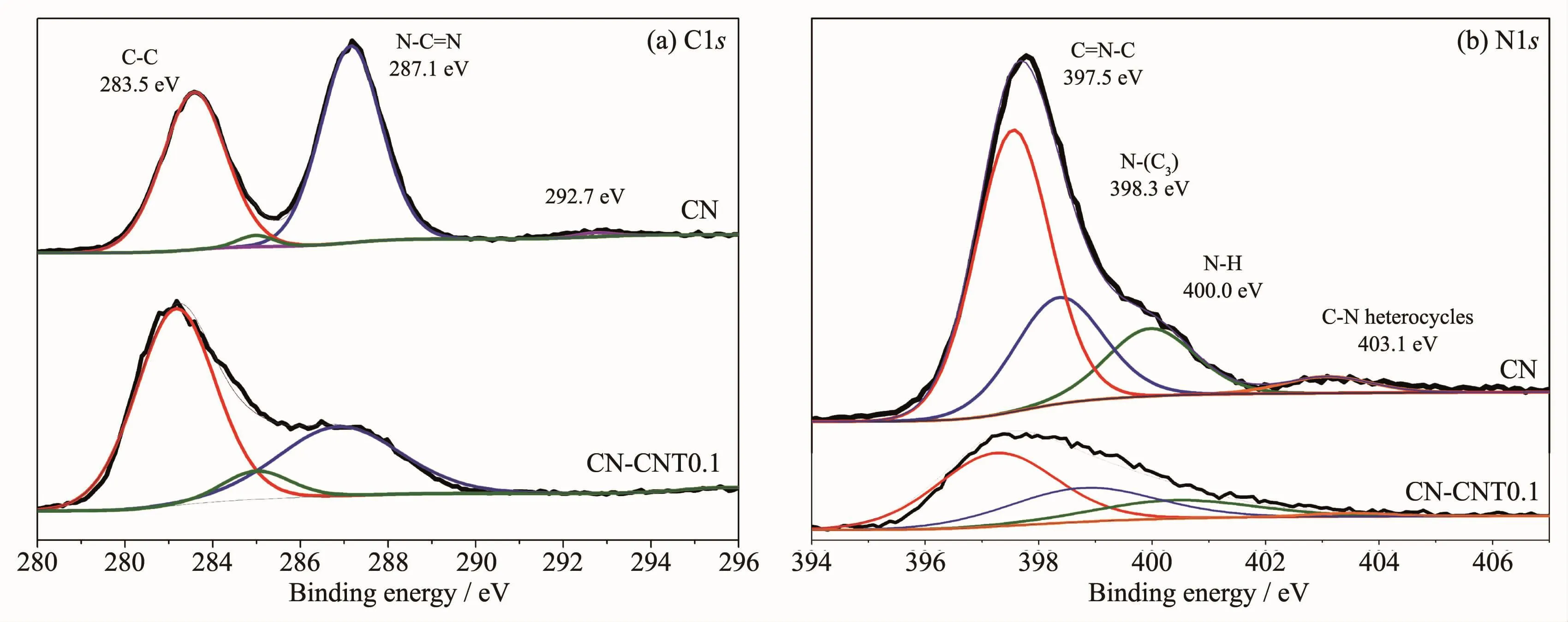
图5 CN和CN-CNT0.1样品的XPS谱图:(a)C1s及(b)N1sFig.5 XPSspectra of the C1s(a)and N1s(b)of the CN and CN-CNT0.1 samples
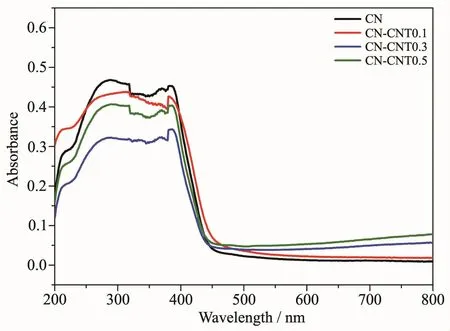
图6 g-C3N4和CNT/g-C3N4系列光催化剂的UV-Vis漫反射谱图Fig.6 UV-Vis diffuse reflection spectra of g-C3N4 and CNT/g-C3N4 photocatalysts

图7 g-C3N4和CNT/g-C3N4系列光催化剂的能带间隙图Fig.7 Energy bandgap spectra of g-C3N4 and CNT/g-C3N4 samples
PL光谱用于测定g-C3N4和CNT/g-C3N4光催化剂样品中光生电子-空穴对的复合程度。图8为激发波长为380 nm下所测荧光发射光谱图。通常来说,样品发射峰的强度越低,表明该样品内光激发电子-空穴对的复合率就越小[25-27]。由图可知,CN样品在450 nm附近有很强的荧光发射峰,而CN-CNT样品的荧光光谱发生明显的猝灭现象,并且随着CNT含量的降低,其PL信号强度逐渐减弱。其中,CNCNT0.1发射峰的强度最低,且发生偏移。偏移可能是由于微量CNT的引入提升了氮化碳的π电子体系,形成了更大的π键所致。结果表明,随着CNT的加入,CNT/g-C3N4催化剂内更多的光生电子可被迅速转移,CNT的复合可有效阻止光生载流子的复合,且发现CNT含量不宜过高,CN-CNT0.1的效果最佳。
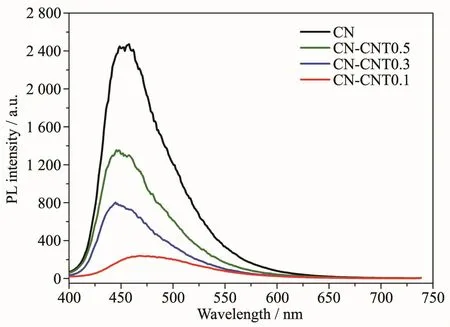
图8 g-C3N4和CNT/g-C3N4系列光催化剂的PL发射谱图Fig.8 PL emission spectra of g-C3N4 and CNT/g-C3N4 photocatalysts
2.4 光催化降解性能分析及机理探究
图9 为光催化剂随光照时间变化降解RhB的活性曲线。如图所示,暗吸附阶段CN-CNT0.1吸附能力欠佳与其较小比表面相关,而在可见光下CNCNT0.1的催化活性明显优于CN,随着CNT含量的增加,催化剂的光催化性能逐渐减弱。当CNT含量达到0.5%时,其光催化性能与CN相比已无明显差别。将CNT含量降低至0.05%时,发现其催化性能与CN-CNT0.1相似,反应速率略小,说明0.1%的CNT添加量是最佳值。CN-CNT0.1样品较高的光催化降解性能与其微观形貌、能带结构及可见光吸收能力和光生载流子分离效率相吻合。微量CNT的加入,会使CNT/g-C3N4样品轻微团聚、二者紧密接触,彼此间具有更好的协同作用,更有利于光生电子的转移。

图9 g-C3N4和CNT/g-C3N4系列催化剂在可见光下的催化性能评价Fig.9 Photocatalytic performances of g-C3N4 and CNT/g-C3N4 catalysts under visible light irradiation
g-C3N4和CNT/g-C3N4样品降解RhB的反应过程符合准一级动力学模型。图10为降解RhB的一级反应动力学曲线图。其直线的斜率即为速率常数k。 由 图 可 知 ,CN、CN-CNT0.5、CN-CNT0.3、CNCNT0.05 和 CN-CNT0.1 分别为 0.13、0.12、0.24、0.34和0.40 h-1。其中CN-CNT0.1样品具有最大的反应速率,其速率常数是g-C3N4的3.1倍。对CN-CNT0.1样品进行3次重复试验(图11),发现催化剂重复利用过程中并无明显失活现象,说明复合催化剂具有较为稳定的结构。
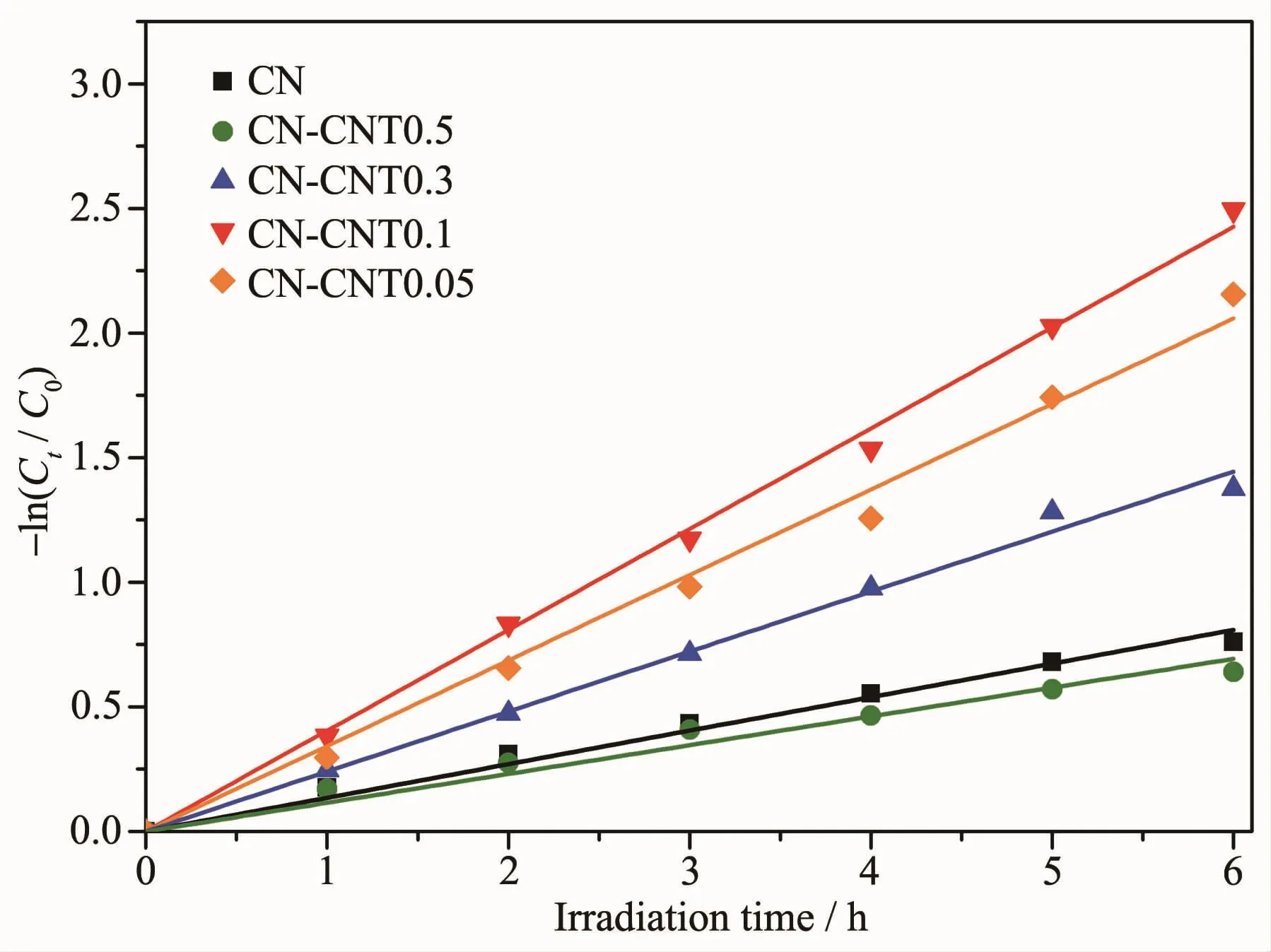
图10 g-C3N4和CNT/g-C3N4系列催化剂降解RhB的一级反应动力学曲线Fig.10 First-order kinetics curves of RhB degradation forg-C3N4 and CNT/g-C3N4 catalysts
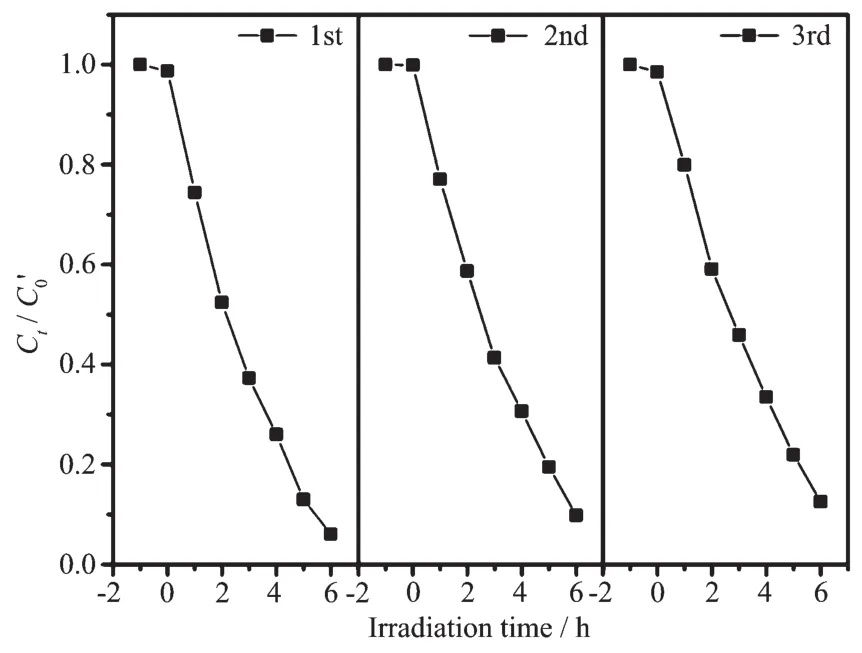
图11 CN-CNT0.1催化剂重复性实验Fig.11 Reusability of CN-CNT0.1 catalyst
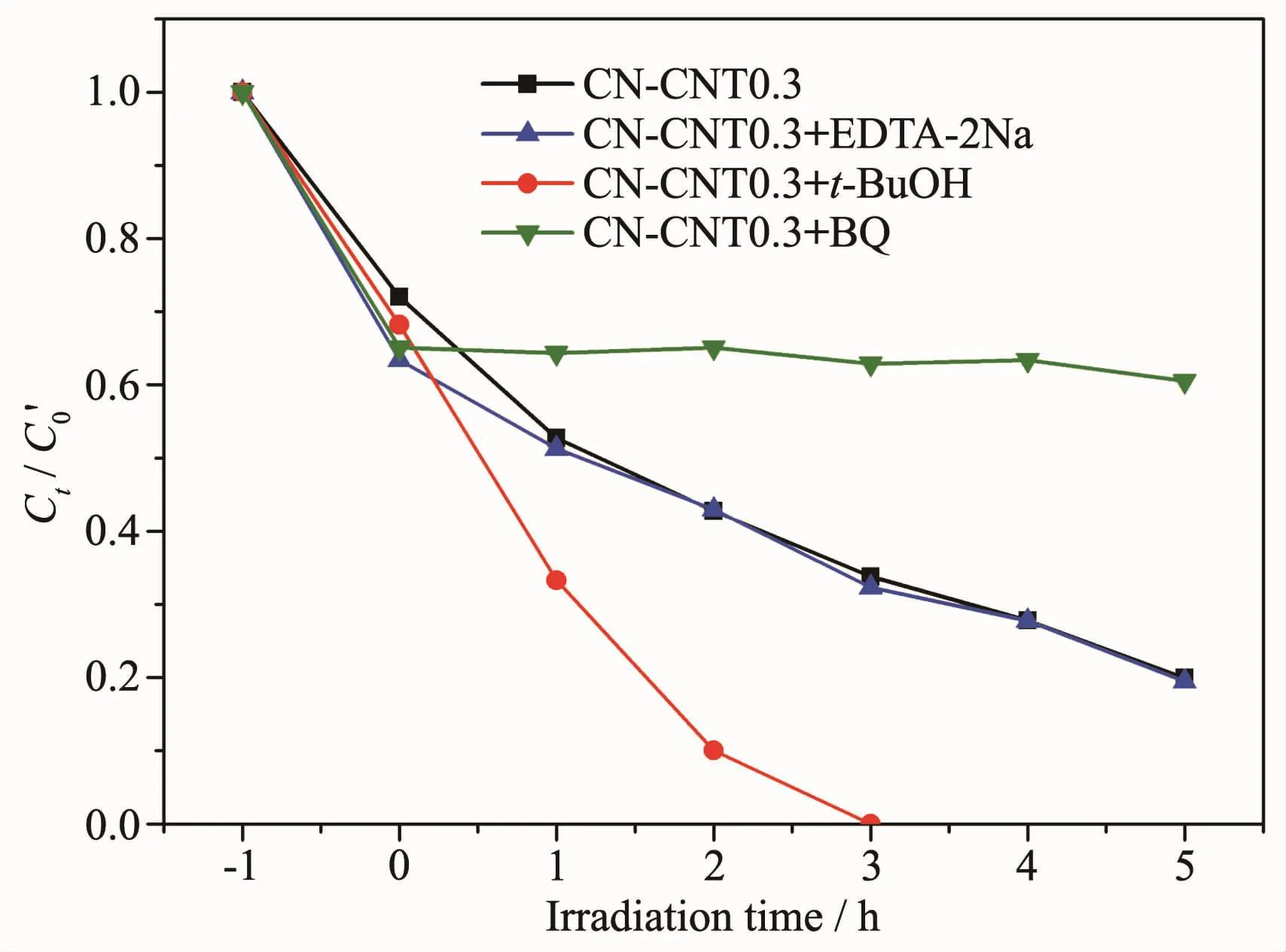
图12 不同牺牲剂对CN-CNT0.3样品在可见光下催化降解RhB的影响Fig.12 Influence of various scavengers on the visiblelight photocatalytic activity of CN-CNT0.3 for the degradation of RhB
为探究反应机理,在CN-CNT0.3样品催化降解RhB反应体系中,分别加入对苯醌(BQ)、乙二胺四乙酸二钠(EDTA-2Na)及叔丁醇(t-BuOH),三者可相应捕获反应过程中产生的超氧自由基(·O2-)、空穴(h+VB)和羟基自由基(·OH)[28]。 由图 12 可知,于 CN-CNT0.3 反应体系中加入BQ后,其降解率急剧下降,几乎不进行光降解,BQ的加入抑制了催化降解过程;而于该体系下加入EDTA-2Na后,其降解曲线几乎不变,EDTA-2Na的加入并未对降解过程带来影响。因此推测,·O2-为该反应体系的主要活性物种,而h+VB并不是此体系主要的活性物种。t-BuOH的加入却使得降解速率大幅提升,说明反应体系内存在·OH物种,对它的捕获给降解过程带来变化。·OH是一种活性物种,无论是在吸附相还是在溶液相都能引起物质的化学氧化反应,然而g-C3N4的价带电位低于·OH/OH-的氧化还原电位,价带h+VB不能将OH-氧化为·OH,但是氮化碳的导带位置很高,热力学上满足O2还原路径产生羟基自由基。具体过程如下:e-cb+O2(ads)→·O2-,·O2-+H+→·HO2,2·HO2→O2+H2O2,H2O2+·O2-→·OH+OH-+O2。而·OH的捕获使质子化反应向右移动,促进了第一步电子还原氧气反应,使体系内生成更多的·O2-,进而促使反应速率大幅提升。
由此推测,在光降解反应过程中,光化学反应仪内的风扇鼓风及反应管中的磁子搅拌,使空气与液面充分接触,为反应体系提供了充足的氧气氛围。催化剂经可见光照射,产生电子-空穴对,CNT的引入提升了光生载流子的分离效率,大量光生电子可经CNT与氧气反应,将氧气还原为超氧自由基,进而将RhB氧化降解,使复合催化剂光降解性能大幅提升。机理示意图如图13所示。
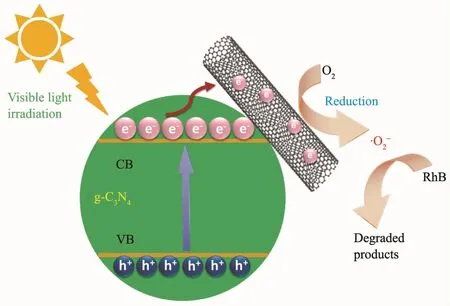
图13 可见光下CNT/g-C3N4催化体系降解RhB过程中光生载流子分离与转移路径Fig.13 Schematic of photo-generated charge carrier′s separation and transfer in the CNT/g-C3N4 system for degradation of RhB under visible light irradiation
3 结 论
以尿素为前驱体,复合不同质量的CNT,制备出一系列不同CNT含量的CNT/g-C3N4催化剂。通过系列表征,明确光催化剂的结构与性质。结果表明,CNT的复合可有效增强g-C3N4对可见光的吸收性能,降低其带隙能,提高其对可见光的利用率。CNT与g-C3N4存在协同作用,催化剂中CNT能有效转移光生电子,提升光生电子-空穴对的分离效率,可使更多的光生电子与氧气反应,所生成的超氧自由基为此降解过程的主要活性物种。微量CNT的复合利于催化活性的提升,其中CN-CNT0.1的催化活性最高,其在可见光下的降解速率是g-C3N4的3.1倍。
