腹腔镜非解剖性肝切除术治疗原发性肝癌的临床疗效分析
2019-02-26赵云张光亚别玉坤夏杰杨成林
赵云,张光亚,别玉坤,夏杰,杨成林
(安康市中心医院肝胆外科,陕西 安康 725000)
肝切除术是目前治疗肝癌的最主要方法[1]。早期的肝切除术是在开腹下实施,手术对病人的创伤大,不利于术后机体的恢复。1991年由美国医生Reich[2]应用腹腔镜开展了世界首例肝脏良性肿瘤切除术,1994年周伟平等[3]完成国内首例腹腔镜下肝癌切除术。随着腹腔镜技术的成熟和设备的更新,腹腔镜在肝胆外科的应用越来越广泛。然而,由于术中止血困难等难点未彻底解决,腹腔镜非解剖性肝切除术仍颇受争议。笔者结合我院肝胆外科开展的72例原发性肝癌病人的临床资料,比较腹腔镜非解剖性肝切除术与开腹手术的疗效,探讨腹腔镜非解剖性肝切除术在原发性肝癌治疗中的临床价值。
资料与方法
一、病例资料
选取2013年2月至2017年5月安康市中心医院收治的72例原发性肝癌病人作为研究对象,进行回顾性研究分析。其中,腹腔镜下非解剖性肝切除术组(腹腔镜组)34例,男性23例,女性11例;年龄34~68岁;病程4~21年;肿瘤直径3.6~8.5 cm。开腹非解剖性肝切除术组(开腹组)38例,男性25例,女性13例;年龄36~65岁;病程5~20年;肿瘤直径3.8~10.2 cm。两组病人术前一般资料比较,差异均无统计学意义(均P>0.05,表1)。术前完善腹部彩超、上腹部增强CT、腹部MRI、肿瘤标志物、乙型肝炎病毒标志物、肝纤维化指标等检查,符合原发性肝癌的诊断。术前所有病人的肝功能Child-Pugh分级均为A级,预留肝脏功能性体积≥标准肝脏体积(SLV)的40%,吲哚菁绿15 min滞留率(ICG R15 )<10%。所有病人均无手术禁忌证,无严重心脑血管等基础疾病。两组病人术后病理诊断均为肝细胞癌。
手术方法均获得病人本人或授权委托人知情同意,并经过医院医学伦理委员会批准。
二、病例纳入标准和排除标准
纳入标准:原发性肝癌病人,肿瘤位于肝脏2段(S2)、S3、S4b、S5、S6的单一肿瘤;两处肿瘤位于上述肝段肝脏边缘或表面,不影响肝门解剖;无腹部手术史;肝功能Child-Pugh分级均为A级;单一肿瘤直径≤10 cm。排除标准:肝脏良性肿瘤或转移性肝癌病人;有腹部手术史或腹腔严重粘连;腹腔镜中转开腹病人;肝功能Child-Pugh分级为B级或C级;肿瘤位于S4a、S7、S8;多发病灶(≥3处);单一肿瘤直径>10 cm;严重肝硬化、门静脉高压、大量腹水的病人;心肺脑等脏器功能障碍,无法耐受麻醉及手术。
对于腹腔镜手术的病例入组,主要依据病人的意愿、经济状况等采取病人自愿原则,严格按照腹腔镜手术的适应证,如既往无腹部手术史,无结核性腹膜炎等严重腹腔粘连,病人能忍受气腹等。
三、手术方法
手术均同一位主任医师带领的团队协作,按常规操作完成。
1.腹腔镜非解剖性肝切除术 气管内插管麻醉,取头高脚底“剪刀”体位,脐上2 cm穿刺CO2气腹,并置入10 mm Trocar,腹腔镜观察病变部位及腹腔探查。根据肝脏病变位置,取4~5孔法,适当调整体位。视肝脏切除部位,用强生超声刀分离肝圆韧带、镰状韧带、左右三角韧带、左右冠状韧带,充分游离肝脏,暴露术野。常规第一肝门Pringle法预置肝门阻断带,根据术中情况必要时适当行肝血流阻断。按恶性肿瘤边缘2 cm切除原则,用电凝钩沿肝脏表面画出拟切线,在吸引器、无损伤钳的协助下,超声刀切开肝组织。根据显露血管、胆管粗细选择电凝处理、钳夹、Hem-o-lok夹闭,必要时用Endo-GIA离断肝实质。将切除的肝组织装入标本袋,经上腹部小切口取出。电凝棒喷洒烧灼肝断面,生理盐水冲洗创面,吸净冲洗水并用干纱布蘸净,仔细确认无活动性出血及胆漏后,于肝断面喷洒止血胶,放置双套管引流管,全层缝合切口。
2.开腹非解剖性肝切除术 取右侧肋缘下或腹直旁切口,采用传统的非解剖性肝切除术,依据肝肿瘤的位置、大小和质地来决定断肝方式及器械选择,根据情况游离肝周韧带,必要时行肝门血流阻断,应用超声刀、钳夹法或一次性切割闭合器等离断肝脏。基本步骤同腹腔镜非解剖性肝切除术。

表1 两组病人术前一般资料的比较
四、观察指标
记录并比较两组病人的手术指标(手术时间、术中出血量),术后恢复指标(胃肠道恢复时间、术后拔除引流管时间),住院时间,住院费用,术后并发症情况及处理,术后1年的疗效、生存率及累积生存率。
五、随访情况
所有病人均获得随访,采取电话或微信群联系,门诊随访方式,随访时间1~2年,平均随访时间为1年,随访率为100%。门诊行腹部彩超、CT增强及肿瘤标志物检查。
六、统计学处理
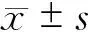
结 果
一、两组病人的手术指标、术后恢复指标、住院时间及住院费用的比较
腹腔镜组病人的手术时间、术中出血量、胃肠道恢复时间、术后拔除引流管时间及住院时间低于开腹组,而住院费用略高于开腹组(均P<0.05,表2)。
二、两组病人的术后并发症及处理
病人术后常见并发症包括出血、胆漏、切口感染、腹腔脓肿、胸腔积液及肝功能不良。两组病人在总的并发症发生率、肝功能不良发生率方面的比较(表3),差异均具有统计学意义(均P<0.05)。2例术后出血病人,其中1例,因肝硬化严重导致术中出血量大,术后凝血机制差,考虑肝断面渗血,给予输注新鲜血浆、冷沉淀、血小板、止血药物后出血自行停止;另外1例考虑肝右动脉小分支出血,行介入栓塞止血,手术顺利,术后出血停止,病人恢复良好。3例胆漏病人,其中2例经腹腔引流管充分引流自行停止,1例因引流管引流不畅,行腹腔穿刺置管引流术后愈合。3例切口感染病人均为开腹组,其中1例病人营养状况差,术后腹水,合并慢性支气管炎急性发作并肺部感染,咳嗽剧烈;2例合并2型糖尿病;经改善营养状况、控制肺部感染及血糖,定期换药后病人切口愈合。2例腹腔脓肿,其中1例考虑胆漏后胆汁等渗液局部包裹形成,行腹腔穿刺置管引流后脓肿吸收;另外1例经抗感染治疗后吸收好转。7例胸腔积液病人均为反应性,5例少量胸腔积液病人经保守治疗后自行吸收,2例中等量积液行胸腔穿刺抽液。术后1周9例肝功能Child-Pugh分级为B级病人,均经过保肝、营养支持、利尿等治疗后转为A级。所有病人的并发症经及时发现、及时治疗,无严重后遗症发生。
三、两组病人术后1年的疗效比较
术后1年两组病人在肝内转移、肝外转移、腹壁及戳孔种植转移,以及总的复发或转移率方面比较,差异均无统计学意义(均P>0.05,表4)。
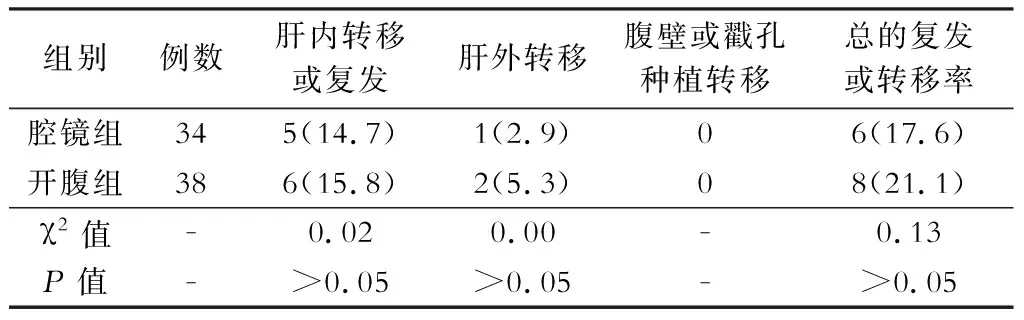
表4 两组病人远期疗效的比较[例(%)]
四、两组病人的生存率方面比较
术后随访1~2年,腹腔镜组与开腹组病人的1年生存率(91.2%比89.5%)比较,差异无统计学意义(P>0.05),两组病人的累积生存率结果分析显示,差异无统计学意义(P>0.05),见图1。

图1 腹腔镜组与开腹组的生存曲线
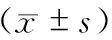
表2 两组病人手术指标、术后恢复指标、住院时间及费用的比较

表3 两组病人的术后并发症情况比较[例(%)]
讨 论
相关数据统计,我国肝癌的死亡人数及新增病人占全世界的一半以上,因此肝癌对病人的生存造成了重大威胁[4-5]。腹腔镜非解剖性肝切除术是一种比较安全的微创手术,具有手术时间短、术中出血量少,术后康复快的优点[6-7]。国外资料表明,腹腔镜肝切除术在各类肝切除术的比例高于75%[8]。
边缘性肝段系手术病灶位于S2、S3、S4b、S5、S6的肝前下段,且肿瘤直径一般小于5 cm[9];所谓中心肝段的S1、S4a、S7、S8,位于肝后上段,且肿瘤直径大于5 cm[10]。我们认为对位于边缘性肝脏肿瘤病人,完全腹腔镜非解剖性肝切除术是最佳手术方式,而且完全腹腔镜肝左外叶切除术是治疗该段疾病的金标准[11]。靳斌等[12]认为,腹腔镜右肝切除术较左肝切除术困难,主要表现在手术时间长、术中出血多、术后肝损害重,但通过改良肝门阻断技术及术野暴露技巧,腹腔镜肝切除术是相对安全的。但如何处理术中出血和止血是腹腔镜肝切除术的关键所在,也是争论的焦点之一。然而,对于边缘性肝癌病人,一般只需适当地游离肝脏,预置肝门阻断带,应用超声刀联合钛夹、Hem-o-lok夹闭,必要时用Endo-GIA离断肝实质或根据术中情况必要时适当行肝血流阻断,可以完全解决肝脏组织的出血问题,保证良好的手术视野,顺利完成手术。
本研究中,腹腔镜组病人的手术时间、术中出血量、胃肠道恢复时间、术后拔除引流管时间及住院时间低于开腹组,而住院费用略高于开腹组,差异均有统计学意义(均P<0.05)。说明腹腔镜非解剖性肝切除术在治疗原发性肝癌中具有手术时间短、术中出血量少、术后恢复快的优点,体现出微创手术的优势。其次,两组病人在总的并发症发生率方面比较,差异具有统计学意义(P<0.05)。腹腔镜组病人术后总的并发症及肝功能不良发生率明显低于开腹组。Yin等[13]通过大量病例研究,发现腹腔镜非解剖性肝切除术的术中出血、术后并发症的发生率明显优于传统开腹组。这种术后并发症及肝功能不良发生率的差别,原因可能与机体承受的应激强度大小有关。腹腔镜非解剖性肝切除术对腹壁和肝脏的创伤更小,能让静脉和淋巴回流得到保护,避免出现大量腹腔积液,使得电解质紊乱、低蛋白血症等发生率更低,从而降低术后并发症的发生[14]。
经过随访,术后1年两组病人在肝内转移、肝外转移、腹壁及戳孔种植转移,以及总的复发或转移率、累积生存率方面比较,差异均无统计学意义(P>0.05)。说明术后1年内腹腔镜非解剖性肝切除术在肿瘤复发及转移方面能达到与开腹手术类似的效果。佟庆等[15]经Meta分析认为:腹腔镜肝切除术可以达到与开腹肝切除术同样的根治效果,两者在近、远期效果方面无明显差异,腹腔镜肝切除术围手术期疗效和安全更具有优势。术后1年两组病人均无腹壁或戳孔种植转移的发生。目前肿瘤播散种植转移的概率及原因仍存在争议[11]。也有学者认为,腹腔镜手术并不增加恶性肿瘤复发转移的概率,甚至肿瘤的复发转移率要低于开腹手术组[16-17]。本研究表明,术后1年左右两组病人的肿瘤复发及转移、累积生存率无明显差别,但仍需长期随访及增加样本量进一步研究。
综上所述,腹腔镜非解剖性肝切除术治疗原发性肝癌具有创伤小、术后恢复快及总的并发症低的优势,有利于病人术后的快速康复。尤其对于边缘性原发性肝癌病人,腹腔镜非解剖性肝切除术是一种较理想的手术方式,值得临床应用及推广。
