水氯镁石喷雾热解制备氧化镁
2019-01-05,,,,
,, ,,
(华东理工大学 化学工程联合国家重点实验室,上海 200237)
1 引 言
青海察尔汗盐湖资源丰富,富含钠、钾、镁、锂、硼等无机盐,其中氯化镁资源储量超过30亿吨[1]。自20世纪60年代以来,察尔汗盐湖钾资源的开发利用突飞猛进,极大地促进了我国钾肥工业的发展,但随着钾资源的开发与利用,副产了大量的氯化镁,每年排出含氯化镁33%的老卤多达6000多万立方米,含水氯镁石2000余万吨[2],这不仅造成了镁资源的极大浪费,同时也给生态环境带来了巨大的压力,并且已经严重影响了察尔汗盐湖的卤水成份平衡。利用盐湖氯化镁资源生产氢氧化镁、氧化镁和氯化镁等系列镁产品是盐湖镁资源开发利用的重要研究方向,也是盐湖资源综合开发利用的重要环节。
氧化镁是镁盐产品中一种具有重要工业用途的无机化工产品,广泛应用于冶金、工业催化、陶瓷、建筑、军工、医药、塑料和橡胶等领域[3-7]。目前我国传统制备氧化镁的方法主要是固体矿菱镁矿煅烧法[8],此法工艺简单,成本低,但产品杂质含量较高且难去除,并且会产生大量的二氧化碳,污染环境,在大力推进节能减排的资源节约型和环境友好型的21世纪,此法将面临较大的挑战。为此,结合我国储量丰富的盐湖镁资源,许多学者研究了利用盐湖卤水、海水等液态镁资源制备氧化镁的工艺[9-10],该工艺方法可概述为沉淀法,通过纯碱、氨、碳铵、石灰乳等沉淀剂,与浓缩后的卤水、海水中的镁离子发生反应形成碳酸镁、碳酸氢镁、氢氧化镁等沉淀型镁盐,再在一定条件下煅烧即可得到氧化镁产品,但沉淀法的工艺设备较为复杂,投资成本高。卤水直接热解法[11]是将卤水或水氯镁石置于空气中加热至高温发生热分解反应,生成氧化镁产品,但是由于热解产生的高温盐酸气体腐蚀性强,对设备要求很高,增加了设备投资,限制了该应用的推广,因此在国内很少被采用。不过,此法基本不需要消耗其它辅料,成本低,产品纯度高,容易实现镁的高值化和产业化,一直以来都是众多学者的研究热门之一。
本文以水氯镁石为原料,采用喷雾热解法制得了氧化镁产品,并且解决了盐酸气的腐蚀问题,具有较好的应用前景。
2 实 验
2.1 实验基本原理
喷雾热解是一种特殊的喷雾干燥过程,原料液经过喷嘴的雾化作用后分散成微米级的小液滴,比表面积急剧增加,反应活性大大提高,可以在反应器内快速发生热解、脱水等反应,生成干燥的产品,一般整个过程只需几秒即可完成,多用来制备金属氧化物粉体或薄膜,赵爱春等[12]以AlCl3·6H2O为原料利用喷雾热解法制备了纯度较高的Al2O3粉末。水氯镁石热解反应极为复杂,同时存在脱水、水解、热分解等反应,最后生成氧化镁的温度阶段一般发生500℃左右,但是大量的氯化镁分解需要更高的温度,王路明[13]研究过800~900℃条件下浓卤水的热分解过程。其热解过程的总反应:
MgCl2·6H2O→MgO+2HCl↑+5H2O
从反应中可以看出,此热解过程的反应物为水氯镁石,理想产物为氧化镁、盐酸和水。
2.2 热解装置
为保证热解反应的充分进行,同时考虑到系统的热损失,在反应器设计过程中,需选取稍高于水氯镁石起始分解温度500℃的条件,然后基于喷雾干燥反应器的设计准则及过程[14],对水氯镁石热解反应器进行了初步的结构设计,并对整个工艺系统进行设计、选型。

1-热解炉;11-出料口;12-进料口;13-温控仪表检测口;14-温度测量口;15-出气口;16-阀门;17-产品料仓;21-0-、42-空气压缩机;21-液化石油气罐;21-1、21-2、21-3-减压阀;22-电磁阀;24-混合管;25-火焰检测器;26-燃烧枪;27-控制器;28-高压电子点火器;29-温控器;31-原料贮槽;32-供料泵;33-雾化喷嘴;41-陶瓷过滤板;43-抽气管;44-吸收槽。图1 热解工艺流程图Fig.1 Flow chart of the pyrolysis experiment
完整的实验装置主要包括热解反应器、热风系统、供料系统,产品及尾气系统六大部分,如图1所示。其中热解反应器为热解反应的发生场所,具有一定的结构尺寸,由耐高温腐蚀的碳化硅材质制成;热风系统位于反应器靠近底部的位置,采用液化石油气直接燃烧供热方式,并加以控制系统,为保证反应器内温度的均匀分布,采用同一平面上三个燃烧枪对置排列的方式;供料系统主要承担料液的输送及雾化过程;反应器底部设置出料口,顶部设有尾气出口,尾气由抽气管吸入,经陶瓷过滤器滤掉粉尘后直接用饱和碱液吸收,对环境无污染。
2.3 实验过程
将水氯镁石(化学纯)加入青海盐湖卤水中配制成饱和溶液,置于贮槽中待用。另取工业级氢氧化钠加水配制成饱和溶液置于吸收槽,用以吸收盐酸尾气。
连接好实验装置的各部分,先打开空压机,检查实验系统的管路是否顺畅,确认无误后再开启液化石油气储罐阀门,启动燃烧控制系统,程序控制器控制液化石油气管路上的常闭电磁阀开启,在空气的引射作用下,液化石油气与空气在混合关内混合均匀后进入燃烧枪,在高压电子点火器作用下燃烧供热,热解反应器温度上升。
待热解反应器温度升至所需温度时,打开供料系统,饱和氯化镁溶液经供料泵由贮槽输送至反应器顶部的进料口,经喷嘴雾化后的饱和氯化镁溶液雾滴在反应器内快速发生脱水、热解反应,生成的产品颗粒经反应器底部的出料口收集至产品料仓,热解尾气经陶瓷过滤器过滤掉携带的粉尘后,由抽气管提至碱液吸收槽,吸收净化后排放。实验结束后,依次关闭供料系统、液化石油气储罐阀门、空气压缩机、控制系统,待冷却至室温后取样分析。
3 结果与讨论
3.1 热解反应器内温度分布
3.1.1反应器内温度的轴向分布 反应器升温达到预定温度后,在开始喷雾前测量了炉内的轴向温度分布,如图2所示,热解炉内温度的轴向分布自上而下逐渐降低,拟合成幂函数分布(函数关系式为t=1206.2h-0.247,其中t为所处位置平面的温度,℃;h为所处位置平面距火焰中心的距离,cm)。

图2 反应器内温度的轴向分布Fig.2 Axial distribution of temperature in the reactor
水氯镁石的热解反应比较复杂,脱水反应、水解反应、热分解反应均同时存在于喷雾热解过程中,众多学者对水氯镁石热解机理进行了大量研究[15-16]。结果均表明,水氯镁石热解过程中前4个结晶水的脱除较为简单,发生反应的起始温度较低,为100℃左右,因此当饱和氯化镁溶液经喷嘴雾化成小液滴从反应器顶部进入时,该区域宜保持100℃以上的温度范围,以便快速蒸发饱和溶液中携带的自由水,然后液滴继续沉降,进入更高的温度区,水氯镁石热解生成氧化镁的阶段一般发生在500℃左右,但是大量的氯化镁分解需要更高的温度,因此在下部高温区域温度应高于500℃,并且具有一定的空间范围,以保证反应充分进行。本实验的反应器内轴向温度分布表明该条件可以得到很好的满足。
3.1.2热解过程温度分布 在喷雾热解实验中,设置了两个温度监测点:一个位于反应器下部火焰上方处,另一个位于反应器中部区域,从实时温度分布图(如图3)可以看出,实验前期,反应器内升温迅速,可较快达到反应所需的温度,图示该次实验设定温度为750℃,随后按照一定的加料速率喷入饱和氯化镁溶液,此时反应器内温度骤降约100℃,然后基本保持恒定,直至实验结束,燃烧系统关闭后自然冷却降温。在降温阶段,反应器底部的高温区域由于燃烧的骤然停止而迅速降温,而中上部的区域内则降温较缓慢。

图3 热解过程中反应器不同位置的温度变化(1-下部;2-中部)Fig.3 Temperature changes in the reactor during pyrolysis (1-Bottom; 2-Middle)
饱和氯化镁溶液含约30%的氯化镁,70%的自由水,从饱和溶液形成MgCl2·6H2O时,需蒸发约40%的自由水,此过程属于水分蒸发与热空气发生的热、质交换过程,蒸发过程需吸收较大的热量,并且此过程是在短时间内完成的,因此在喷雾热解初期,反应器内温度骤降。
3.2 产品分析
3.2.1产品粒度分析 产品粒度可以用来衡量喷雾热解所得产品的质量。从图4(a)看出,该样品的粒度分布比较均匀,多集中在10~100μm的范围内,其d0.5为29μm,体积平均粒径D4,3为35μm,表明这些颗粒粒径较小,通过计算可知其沉降速度较小,当其沉降速度小于反应器内上升气流的流速时,便被气流裹带出反应器。而图4(b)则是反应器底部收集所得产品的粒度分布图,图中显示此样品粒度分布不均匀,在1~1000μm范围内均有测到,但多集中于50~300μm,其d0.5为75μm,体积平均粒径D4,3为139μm,与被气流携带出反应器的4(a)样品相比,此处样品粒径大,计算得到的沉降速度大于上升热气流流速,因此沉降至反应器底部的产品收集口。

图4 反应器不同位置产品的粒度分析(a-顶部;b-底部)Fig.4 Particle size distribution of samples from different parts of the reactor (a-top;b-bottom)
3.2.2热解温度对产品的影响 在不同温度下进行了喷雾热解实验,对炉底所收集的样品进行比较分析,获得其XRD图谱和SEM照片,如图5。

图5 不同温度条件下相同取样处产品的XRD图谱和SEM照片(a-550℃;b-650℃;c-730℃)Fig.5 XRD pattern & SEM image of samples from different experiments under various temperatures(a-550℃;b-650℃;c-730℃)

水氯镁石喷雾热解制备氧化镁,温度过低氯化镁溶液分解不充分,MgO产率低;热解温度越高,分解越完全,但过高的温度会消耗不必要的能量。在500~800℃范围内,考察了炉底产品的氧化镁含量,如图6所示。可以看出,温度低于600℃时,炉底产品中未检测到氧化镁;之后,随着热解温度的升高,炉底产品中的氧化镁含量显著增加;温度达到710℃时,氧化镁含量变化开始趋于平缓。
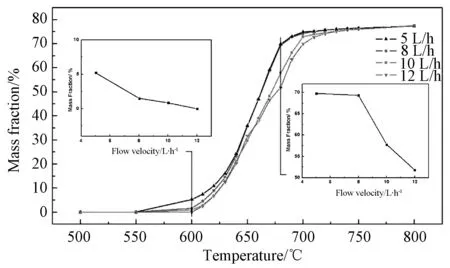
图6 热解温度和进料量对产品中氧化镁含量的影响Fig.6 Influence of thermal temperature and feed rate on MgO content in the product
3.2.3进料量对产品的影响 由热量衡算可知,溶液中所含水分的蒸发与水氯镁石热解所吸收的热量几乎占据了整个反应系统的能耗,根据溶液组成及反应过程计算,水分的蒸发相比于水氯镁石热解需要更多的热量(占比约为2∶1),因此溶液的进料量直接决定了所需求的热量,进而决定了反应器内的温度区间及分布,对热解过程会产生直接影响。本文对进料量的影响也进行了考察,实验中所用的喷嘴处理量分别为5L/h,8 L/h,10L/h,12L/h,不同进料量对产品中氧化镁含量的影响如图6。在较低温度(600℃)下,高流量(12L/h)的热解不能产生氧化镁;在较高温度(700~800℃)下,上述4种进料量的热解都能完成,氧化镁的含量趋于稳定。图中还标注了600℃和680℃时,4种进料量下热解生成的氧化镁含量,进料量越小,初始得到氧化镁的温度越低,分解完全所需的最低温度越低;反之,初始得到氧化镁的温度越高,分解完全所需的最低温度也越高。
3.2.4反应器不同高度处的产品分析 根据水氯镁石热解机理可知,在其热解过程中温度对其影响极为重要,由第2.1节的反应器内温度分布可知,反应器内不同高度处的温度不同,为了更好地研究反应器内水氯镁石的热解过程及对反应器进行优化设计,对同一实验条件下反应器内不同位置的产品进行取样分析,所得产品的XRD图谱和SEM照片如图7所示。
由图7(a)可见,反应器底部收集的样品为纯度较高的氧化镁,说明饱和氯化镁液滴从反应器顶部开始反应到沉降至底部过程中热解反应很充分,从SEM照片来看,样品形貌呈现疏松的团聚状。从图7(b)观察到晶须状的产物,颗粒最长的晶须可达30μm,XRD图谱表明此样品为高纯度的Mg2(OH)3Cl·4H2O中间产物,这主要是由于热解炉中部区域温度较低(约为400℃),水氯镁石热解不充分,在水蒸气和盐酸的混合气氛中,形成晶须状的中间产物,此后又因反应器内热气流的作用导致液滴本身的运动轨迹受到影响而发生粘壁行为,不能继续沉降至底部。图7(c)显示其主要成分是MgCl2·6H2O,伴有少量的MgO,这是由于反应器顶部出口处温度较低(约为200℃),经反应器顶部喷嘴雾化后的饱和氯化镁液滴析出水氯镁石晶体后被上升的热气流裹带出反应器,而反应器高温区域生成的部分颗粒较小的氧化镁也被携入之中。
上述结果展示了反应器内部不同位置处所发生的热解阶段,可以利用不同位置所对应的温度,实现水氯镁石的分步热解,进一步使能量消耗合理化,为反应器结构的优化设计提供了重要依据。
5 结 论
1.设计了一套水氯镁石热解反应系统,获得了反应器内的温度分布、产物粒度分布、产物形貌特征等基础数据,为中试扩大研究提供了基础;
2.温度、进料量和反应位置对热解产品有显著的影响。在燃烧区温度730℃,喷嘴进料量10L/h的条件下制得了粒度约为90μm的氧化镁颗粒产品,XRD图谱显示其纯度很高;在温度约为400℃的反应器中部区域获得了晶须状的中间产物Mg2(OH)3Cl·4H2O,其晶须长度达30μm。

图7 同一实验条件下反应器内不同高度处样品的XRD图谱和SEM照片(a-底部;b-中部;c-顶部)Fig.7 XRD pattern & SEM image of samples from different parts of the reactor in one experiment (a-bottom; b-middle; c-top)
[1] 马培华. 科学开发我国的盐湖资源[J]. 化学进展, 2009, 21(11): 2349~2357.
[2] Zhou Y, Li L, Wu Z, Li X. Exploitation and Comprehensive Utilization for Qinghai Salt Lakes [J]. Prog. Chem., 2013, 25(10): 1613~1624.
[3] Flemming J A, Vanner S J, Hookey L C. Split-dose Picosulfate, Magnesium Oxide, and Citric Acid Solution Markedly Enhances Colon Cleansing Before Colonoscopy: a Randomized, Controlled Trial [J]. Gastrointest. Endosc., 2011, 75(3): 537~544.
[4] Eckhardt B, Ortel E, Polte J, et al. Micelle-templated Mesoporous Films of Magnesium Carbonate and Magnesium Oxide [J]. Adv. Mater., 2012, 24(24): 3115~3119.
[5] Cao C Y, Qu J, Wei F, Liu H, Song W G. Superb Adsorption Capacity and Mechanism of Flowerlike Magnesium Oxide Nanostructures for Lead and Cadmium Ions [J]. Acs Applied Mater & Inter., 2012, 4(8): 4283~4287.
[6] Mao D S, Guo S Q, Meng T. Effect of Magnesium Oxide Modification on the Catalytic Performance of Nanoscale HZSM-5 Zeolite for the Conversion of Methanol to Propylene [J]. Acta Phy.-Chim. Sin., 2010, 26(8): 2242~2248.
[7] 李维维, 陈昌礼, 李良川, 冯义林. 外掺MgO水泥净浆和砂浆小尺寸试件的压蒸膨胀变形[J]. 材料科学与工程学报, 2016, 34(1): 160~165.
[8] Nogueira H, Lana S L B, Morato A G. Dead-burned Magnesia from Brazilian Magnesite [J]. ACS Bull., 1983, 62(9): 978~981.
[9] Yuan J J, Cui R, Zhang Y. Study on the Adsorption of Magnesium Hydroxide to Boron in Seawater and the Removal of Boron in Brine[J]. Sea-Lake Salt Chem. Ind., 2007, 12(2): 1054~1060.
[10] 杨雪梅, 胡珊, 文渊,郑谦, 周美珍. 利用硼泥制备氧化镁的工艺条件[J]. 材料科学与工程学报, 2014, 32(5): 727~731.
[11] Du Y, Sun Q, Huo Y, Han J, Li M. Study on Preparation of Magnesium Oxide by Spray Pyrolysis of Magnesium Chloride [J]. Inog. Chem. Ind., 2013, 45(4): 13~14.
[12] Zhao A C, Zhang T A, Lu G Z, Dou Z H. Preparation of Al2O3Powders by Spray Pyrolysis Deposition [J]. J Northeast. Univ., 2012, 33(3): 100~103.
[13] Wang L M. Experiment Process of the Preparation of High Pure and Superfine Magnesium Oxide by Lime-brine Method [J]. Sea-Lake Salt Chem. Ind., 2003, 32(6): 5~7.
[14] 杨庆贤. 气流式喷雾干燥器的设计[J]. 中国医药工业杂志, 1975, 15(2): 28~37.
[15] Sugimoto K, Dinnebier R E, Hanson J C. Structures of Three Dehydration Products of Bischofite from in situ Synchrotron Powder Diffraction Data (MgCl2·nH2O;n=1,2,4).[J]. Acta Crystal., 2007, 63(63): 235~242.
[16] Huang Q Z, Lu G M, Wang J, Yu J G. Mechanism and Kinetics of Thermal Decomposition of MgCl2·6H2O [J]. Metal. Mater. Trans. B, 2010, 41(5): 1059~1066.
[17] Peng H, Huang Q Z, Lu G M, Yu J G. Activity Research of Magnesia Formed on Calcination of Bischofite [J]. J Salt Chem. Ind., 2010, 39(6): 7~11.
