超声内镜与窄带放大内镜判断早期食管癌浸润深度的对比研究
2018-11-28朱建儒杨莹莹沈小春陈东风兰春慧
朱建儒,杨莹莹,沈小春,杨 婧,曹 燕,兰 丽,陈东风,兰春慧△
(1.中国人民解放军陆军军医大学大坪医院消化内科,重庆 400042; 2.中国人民解放军第一六三中心医院干部病房,长沙 410003)
早期食管癌的定义是指癌组织局限于黏膜内或黏膜下层,且伴或不伴淋巴结转移。当前,消化内镜下治疗早期食管癌或食管高级别上皮内瘤变(HGIN)的最重要的方式是黏膜下剥离术(ESD)[1-3]。我国《早期食管鳞状细胞癌及癌前病变筛查与诊治共识》认为食管高级别上皮内瘤变、癌组织限于黏膜上皮层(M1)或局限于黏膜固有层内(M2)是行ESD治疗的绝对适应证,不伴淋巴结转移的癌组织局限于黏膜肌层内(M3)或浸及黏膜下层上1/3(SM1)是ESD治疗的相对适应证,癌组织浸润至黏膜下层中层(SM2)或更深需要外科手术[4]。因此,术前评价早期食管癌浸润深度对指导手术方式具有重要意义。目前,用于判断早期食管癌浸润深度的主要技术是超声内镜(EUS),以及窄带成像技术(NBI)结合放大内镜技术[5-8]。本研究通过对52例食管HGIN或早期食管早癌患者分别行EUS及NBI检查,以探讨EUS与NBI放大内镜对判断早期食管癌浸润深度的价值。
1 资料与方法
1.1一般资料 收集2015年1月至2016年12月陆军军医大学大坪医院经内镜活检结果为早期食管癌或高级别上皮内瘤变的52例患者为研究对象,其中男38例,女14例;年龄42~78岁,平均年龄(61.8±8.2)岁。就诊时主要症状包括反酸、烧心、进食梗阻感等。
1.2器材及设备 NBI-ME内镜检查采用Olympus GIF-260Z型电子胃镜及其配套的NBI系统。超声内镜检查采用20 MHz小探头超声(Fujinon PL2226-15)。
1.3方法
1.3.1检查及治疗方法 在普通白光内镜下活检结果为食管高级别上皮内瘤变或早期食管癌的患者,分别由两位工作5年以上的内镜医师分别行NBI-ME检查和超声内镜检查,并记录食管黏膜上皮乳头内毛细血管襻(IPCL)及超声影像,并分别判断病变浸润深度,并规定两位内镜医生相互不能沟通。对于病灶局限于黏膜内或黏膜下层且无淋巴结转移且愿意接受内镜下治疗的患者行ESD治疗,不接受内镜治疗的患者行外科手术治疗。
1.3.2Inoue分型[9]对早期食管癌浸润深度的判定标准,根据NBI-ME内镜下观察食管黏膜微血管IPCL的形态,参照Inoue分型的标准:IPCLⅣ型表现为血管扩张、管径不规则,或迂曲、形态各异中的2~3个,见于高级别上皮内瘤变;IPCL V1型表现为Ⅳ型血管中所有的异常改变,见于原位癌;IPCL V2型表现为V1型血管的延伸,血管改变更明显,见考虑病变浸润至黏膜固有层;IPCL V3型表现为血管的进一步破坏,考虑浸润至黏膜肌层或SM1;IPCL Vn型血管表现为新生的肿瘤血管生成,见于病变浸润至SM2或更深,此时不具有内镜下ESD治疗的适应证。每一处病灶可能同时出现各种IPCL分型,记录考虑病变浸润深度最深的IPCL分型。
1.3.3EUS对早期食管癌浸润深度的判定标准 HGIN及M1、M2期癌表现为黏膜层回声减低或黏膜层和(或)黏膜肌层增厚,层间界限消失,黏膜下层及以下未见异常改变;M3期癌表现为黏膜层及黏膜肌层回声减低,界限消失或厚度增厚;SM期癌表现为前两层不均匀增厚,黏膜回声减低,黏膜肌层与黏膜下层间界限消失,黏膜下层内可见低回声影,第4、5层未见异常改变。
1.3.4观察指标 以术后病理为金标准,分别评价EUS及NBI-ME判断病变浸润深度与术后病理的一致性。
1.4统计学处理 采用SPSS19.0统计软件进行分析,计数资料以率表示,采用χ2检验及Kappa检验,以P<0.05为差异有统计学意义,K≥0.75一致性佳,0.4≤K<0.75中度一致,K<0.4一致性差。
2 结 果
2.1EUS判断早期食管癌或癌前病变浸润深度 52例早期食管癌或癌前病变,EUS判断为HGIN及M1、M2期癌共36例,M3、SM期癌共16例,总体准确率为84.6%(44/52)。EUS与术后病理结果一致性分析(K=0.630,P<0.05),EUS与术后病理结果一致性一般。将M3期和SM期合并为一组,HGIN、M1和M2合并为一组后,比较一致性分析为K=0.751,P<0.05,可以认为EUS与术后病理一致性较好,见表1。

表1 EUS判断早期食管癌或癌前病变浸润深度与病理结果的比较(n)
2.2NBI-ME判断早期食管癌或癌前病变浸润深度 NBI-ME判断为HGIN及M1、M2期癌共40例,M3、SM期癌共12例,总体准确率为92.3%(48/52)。NBI-ME与术后病理结果一致性分析,ME-NBI与术后病理结果一致性好(K=0.891,P<0.05)。将M3期和SM期合并为一组,HGIN、M1期和M2期合并为一组后,比较一致性分析为NBI-ME与术后病理结果一致性较好(K=0.783,P<0.05),见表2。
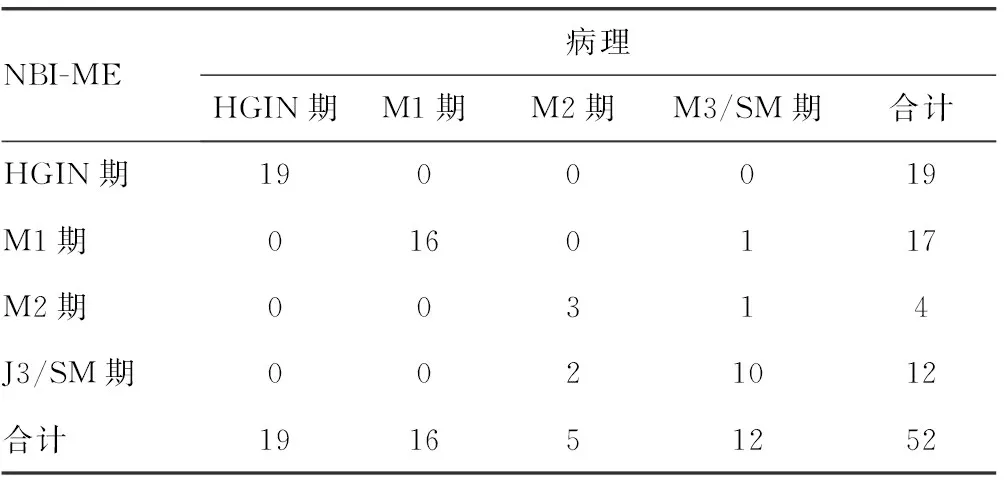
表2 NBI-ME判断早期食管癌或癌前病变浸润深度与病理结果的比较(n)
2.3两种方法对食管HGIN或早期食管癌浸润深度判断的对比 EUS和NBI-ME对判断早期食管癌浸润深度与病理结果均具有较好的一致性(K=0.630、0.891,P<0.05)。将M3期和SM期合并为一组,HGIN、M1期和M2期合并为一组后,两种方法判断早期食管癌浸润深度与病理结果的一致性相当(K=0.751、0.783,P<0.05);NBI-ME判断食管HGIN或早期食管癌浸润深度总体准确率(92.3%)高于EUS判断食管HGIN或早期食管癌浸润深度总体准确率(84.6%)。两种方法诊断准确率间差异无统计学意义(χ2=0.791,P>0.05)。
3 讨 论
随着EUS、NBI-ME,以及色素内镜等内镜技术的发展,早期食管癌及食管HGIN检出率显著提高。有研究显示,碘染与NBI放大内镜鉴别食管癌前病变或早期食管癌的敏感性与特异性上无明显差别,但是碘染无法判断病变深度,在这方面,EUS及NBI-ME有着突出的优势[9-13]。目前,ESD治疗技术其远期疗效与外科手术无明显差异,且损伤小、并发症少[14]。有研究显示,食管HGIN、M1期癌、M2期癌淋巴结转移率小于5%,是行ESD治疗的绝对适应证;M3期癌、SM1期癌淋巴结转移率为10%~20%,是行ESD治疗的相对适应证,SM2期癌、SM3期癌淋巴结转移率是30%~56%,需行外科手术[9-10]。故在适应证范围内选择内镜下治疗显得非常重要。高频(20 MHz)超声小探头使食管壁层次结构显示非常清楚,能够显示出食管壁9层结构,在判断早期食管癌的浸润深度方面有着非常重要的作用。
本研究显示,EUS对早期食管癌浸润深度判断的准确率达84.6%,一致性达到中度一致,本研究有6例判断过深,出现这种情况可能是部分患者反复多次深取活检后造成炎性反应或瘢痕形成,或病灶表面附有角化不全物质导致病灶黏膜层增厚,甚至层次结构消失。
本研究还发现,NBI-ME对食管癌前病变或早期癌进行深度判断时,HGIN及M1期癌的准确率远高于M2期癌及SM期癌的准确率。分析原因如下:(1)部分患者行外科手术治疗,病理切片可能未切病变浸润最深的部位,造成评估病变过浅;(2)本次纳入黏膜固有层病例数少,黏膜固有层癌诊断准确率特异性低。
将M3期和SM期合并为一组,HGIN、M1期和M2期合并为一组后,两种方法判断早期食管癌浸润深度与病理结果的一致性相当,由此推断在判断早期食管癌是否有ESD治疗绝对适应证时,两者之间无明显差异;本次纳入分析的M3、SM期癌仅12例,病例数相对较少,需要进一步扩大样本量才能确定NBI-ME和EUS对M3、SM期癌判断的特异性高低。并且NBI-ME放大内镜与超声内镜相比,可以根据血管形态能更细致地区分M3、SM1期癌与SM2、SM3期癌,从而更好地掌握ESD的相对适应证[15]。
综上所述,早期食管癌或食管高级别上皮内瘤变的患者行ESD前的术前评估显得尤为重要,NBI-ME与EUS对食管HGIN及早期食管癌浸润深度都具有一定的临床价值,两者在食管HGIN及早期食管癌ESD治疗的绝对适应证方面无明显差异,结合CT判断是否有淋巴结转移,对早期食管癌或癌前病变治疗策略的选择具有指导价值。
