纳米四方相二氧化锆的水热合成
2018-11-19李文芳宋继梅许子涵申岳新
李文芳,宋继梅,陈 波,许子涵,申岳新
(安徽大学 化学化工学院,安徽 合肥 230601)
自从20世纪80年代以来,随着电子和新材料工业的发展,纳米二氧化锆因其优异的物理和化学特性(如焰点高、硬度大、化学稳定性好、抗腐烛性强、耐磨性好和电化学性能优异等)而被广泛应用于催化、传感器、陶瓷和燃料电池等高科技领域,成为当今研究开发的热点之一[1].ZrO2有四方相(t-ZrO2)、单斜相(m-ZrO2)、立方相(c-ZrO2)等3种晶相结构,其中 t-ZrO2因具有高断裂韧性及良好的抗热震性能而被广泛地用于复合材料和先进陶瓷的增强增韧[2-3],然而,t-ZrO2为亚稳相,在制备过程中极易发生由t-ZrO2向m-ZrO2的转变.
为获得室温下稳定的t-ZrO2,研究者通过调控ZrO2的表面能、颗粒尺寸,增加氧空位缺陷或在ZrO2中掺杂与Zr4+半径相近、价态较低的稀土金属离子,如Er3+、Yb3+、Y3+等来实现对ZrO2物相的调控[4-5].Combemale 等[6]使用金属钇作为添加剂,在碱性环境下,微波处理后分别于 300,600,800,1 200 ℃等焙烧温度下制备出平均粒径为20 nm且分散均匀的四方相纳米二氧化锆晶体材料.Zhao 等[7]使用正丙醇锆和叔丁胺的混合溶液,通过添加油酸等阴离子表面活性剂,采用两相途径合成出四方相和单斜相共存的二氧化锆纳米晶体.王和义等[8]采用乙二醇为助剂,500~600 ℃煅烧下制得四方相为主的ZrO2粉体.Joo等[9]采用非水解溶胶凝胶法,以Zr[OCH(CH3)2]4·(CH3)2CHOH和25 mmol ZrCl4为锆源,在通入氩气且340 ℃煅烧下成功制得深绿色的 t-ZrO2纳米颗粒.
目前,合成t-ZrO2纳米颗粒的方法有很多,如溶胶-凝胶、微波、水热及共沉淀技术等[10],但是现在普遍存在的问题是:虽然也能得到分散性较好、颗粒尺寸较小的t-ZrO2纳米颗粒,但产物的纯度相对较低、成本相对较高、实验操作复杂且经常会使用一些有毒的有机化合物,对人体和环境有一定危害.因此,寻找简单有效、低成本的合成方法具有重大意义[11].
基于此,笔者以ZrOCl2·8H2O为原料,通过添加助剂(CH2(NH2)COOH/KCl)实现了高纯度t-ZrO2纳米微晶的水热合成,并进一步分析了纳米ZrO2晶相调控的影响因素,探讨了t-ZrO2纳米粉体的可能形成过程.
1 实验部分
1.1 试剂与仪器
八水合氯氧化锆(ZrOCl2·8H2O),分析纯,上海山浦化工有限公司;氢氧化钾、氯化钾、甘氨酸,分析纯,上海化学试剂有限公司;氨水,分析纯,上海远大过氧化物有限公司;无水乙醇,分析纯,上海润捷化学试剂有限公司;甲基橙,分析纯,上海试剂三厂;实验用水为去离子水.901-2型恒温磁力搅拌器,上海沪西仪器有限公司;电子天平(FA10554N),上海精密科学仪器有限公司;DZF-6030A型烘箱,上海一恒科技有限公司;XRD-6000型X射线衍射仪,日本岛津SHIMADZU公司;X-650型场发射扫描电镜,日本日立公司;UV-3600型紫外-可见分光光度计,日本岛津公司.
1.2 ZrO2的制备
以ZrOCl2·8H2O为原料,氨水为沉淀剂,氯化钾和甘氨酸为添加剂,在不同添加剂比例下合成二氧化锆样品.典型实验过程如下:称取12.5 mmol ZrOCl2·8H2O溶于20.0 mL去离子水,配制成溶液a;取2.0 mL氨水,加入不同摩尔比的CH2(NH2)COOH/KCl,搅拌均匀,配置成溶液b;将溶液a置于85 ℃恒温磁力搅拌器上,加入溶液b,调整反应液总体积至40.0 mL,混合均匀后,快速转移至50.0 mL反应釜中,在180 ℃下水热反应24 h,冷却,离心洗涤,直至上层清液用AgNO3溶液检测不出Cl-,80 ℃下真空干燥3 h,得到二氧化锆样品.
1.3 甲基橙吸附实验
采用甲基橙溶液模拟染料废水,用纳米二氧化锆粉体对甲基橙进行吸附实验.称取0.05 g纳米二氧化锆分散到50.0 mL甲基橙溶液(20.0 mg·mL-1)中,磁力搅拌,在黑暗条件下,每隔5 min取样5.0 mL,离心分离,取上清液,用UV-Vis分光光度计对甲基橙的吸附情况进行实时监控.
2 结果与讨论
2.1 物相表征
图1是140 ℃合成样品的XRD衍射花样.
a: 沉淀剂为KOH所得样品;b: 沉淀剂为NH3·H2O所得样品.图1 140 ℃下合成样品的XRD衍射花样
图1显示,样品a和b的所有衍射峰均与m-ZrO2标准卡片(JCPDS 37-1484)吻合,没有杂质峰出现,表明样品为纯m-ZrO2.从图1可以看出,用强碱KOH或弱碱NH3·H2O作为沉淀剂所得样品均为纯m-ZrO2,说明在一定范围内,改变沉淀剂对合成样品的晶相调控影响不大,可能是因为氯氧化锆和沉淀剂溶于水,会发生如下反应:
ZrOCl2+(x+1)H2OZrO2·xH2O+2HCl
(1)

(2)
NH3·H2O
(3)
由反应式(1)可知:氯氧化锆溶于水后溶液呈强酸性,大量的H+会与溶液中的OH—结合生成水,促使平衡式(3)向右移动,从而使弱碱NH3·H2O的解离度大大提高,几乎完全解离,故加入强碱亦或是弱碱对反应体系影响不大.
图2为180 ℃下合成样品的XRD衍射花样.

a:沉淀剂为KOH所得样品;b:沉淀剂为NH3·H2O所得样品.图2 180 ℃下合成样品的XRD衍射花样
图2显示,所有的衍射峰均与m-ZrO2标准卡片(JCPDS 37-1484)一致,进一步说明不管是加入强碱还是弱碱,所得样品均为m-ZrO2.
将图1与图2进行对比,发现温度的升高并没有改变纳米ZrO2的晶相,表明在该实验条件下,改变温度也不能达到调控纳米二氧化锆晶相的目的.
图3是180 ℃下添加剂(CH2(NH2)COOH/KCl)摩尔比例为1/2时所得样品的XRD衍射花样.

图3 180 ℃下添加剂(CH2(NH2)COOH/KCl)摩尔比例为1/2时样品的XRD衍射花样
图3显示,所有衍射峰均与t-ZrO2标准卡片(JCPDS 50-1089)一致,无杂质峰出现.在 2θ=30.2,34.8,35.3,50.7,59.6,60.2,63.0,73.5,82.5°出现的衍射峰分别对应于 t-ZrO2的 (011),(002),(110),(112),(013),(121),(202), (004),(031)晶面.值得注意的是,在 35.0°及60.0°左右,合成样品均发生了衍射峰分裂,分别出现2个不对称的衍射峰;而c-ZrO2没有衍射峰分裂,往往只有1个衍射峰出现.此特征恰好将 t-ZrO2和c-ZrO2很好地区分开来,充分说明在该条件下制得的样品确为t-ZrO2.由此可知,添加剂(CH2(NH2)COOH/KCl)在二氧化锆的晶相调控中起到了关键作用.
图4为180 ℃下添加剂(CH2(NH2)COOH/KCl)体系合成样品的XRD衍射花样.

添加剂摩尔比值Ma=2.5/1; Mb=2/1; Mc=1 /2; Md=1/6; Me=1/22; Mf=1/24; Mg=1/36; Mh=0+C2H5NO2; Mi=KCl+0; Mj=0/0.图4 添加剂(CH2(NH2)COOH/KCl)体系合成样品的XRD衍射花样
与标准卡片比对,图4中在30.2,34.8,35.3,50.7,59.6,60.2,63.0,73.5,82.5°处出现的衍射峰,分别对应于t-ZrO2的(011),(002),(110),(112),(013),(121) ,(202),(004),(031)晶面(JCPDS 50-1089);在28.2°和31.4°处出现的衍射峰分别对应于m-ZrO2的(-111)和(111)晶面(JCPDS 37-1484).不难推测, j为纯单斜相,c为纯四方相,而a、b、d、e、f、g、h、i均为混合相态.也就是说,当反应体系中无任何添加剂时,产物为纯m-ZrO2;只加入CH2(NH2)COOH或KCl时,产物均为混合相态(只加入CH2(NH2)COOH时,产物为偏向于四方相的混合状态,而只加入KCl时呈现的是偏向于单斜相的混合状态);当同时加入CH2(NH2)COOH和KCl且CH2(NH2)COOH/KCl的摩尔比值为1/2时产物为纯t-ZrO2.所以,四方相ZrO2的生成是CH2(NH2)COOH与KCl共同作用的结果.此外,当CH2(NH2)COOH/KCl的摩尔比值大于1/2或在1/6~1/36之间,产物均为混合相态(在比值大于1/2时,比值越大越倾向于单斜相;在1/6~1/36之间时,比值越小越有利于单斜相的生成),表明只有当CH2(NH2)COOH/KCl在一定的比值时才能形成纯的t-ZrO2.不同实验条件下合成样品的晶相分析结果如表1所示.

表1 不同实验条件下合成样品的晶相分析
为进一步研究纳米t-ZrO2粉体的可能形成过程,笔者做了一系列对比实验,结果如图5所示.

图5 不同条件下合成样品 的XRD衍射花样
在图5中,a代表的是以ZrOCl2·8H2O为锆源、KOH为沉淀剂、KCl为添加剂的体系;b代表的是ZrOCl2·8H2O为锆源、NH3·H2O为沉淀剂的体系;c代表的是以ZrOCl2·8H2O为锆源、KOH为沉淀剂、CH2(NH2)COOH/KCl为添加剂的体系;d代表的是以ZrOCl2·8H2O为锆源、NH3·H2O为沉淀剂、KCl为添加剂的体系;e代表的是以ZrOCl2·8H2O为锆源、NH3·H2O为沉淀剂、CH2(NH2)COOH/KCl为添加剂的体系.a、b均为单斜相,d是混合相态,对比a、b、d可知:d中少量四方相二氧化锆的出现可能是氨水与氯化钾共同作用的结果,单独的氯化钾或氨水都无法改变合成产物的晶相.Cao等[12]以Zr(NO3)4·5H2O和NaBH4为反应原料,采用水热法成功制备出t-ZrO2.笔者认为,在反应过程中NaBH4分解产生的氢气可以相互渗透形成较大的泡沫,这些氢气泡将保持反应体系处于持续的湍流状态,使附着在氢气泡表面的ZrO2晶核一次又一次地分散到反应体系中,并且聚结成热力学有利的ZrO2晶体,进而为ZrO2纳米晶体的生长提供具有高表面能的固体表面.因此,在目前含氢气泡的多相合成系统中,最初形成的ZrO2晶核的高表面能和气泡作用的动力扰动被认为是ZrO2纳米晶生长、组装及晶相控制的起源.在该实验中,氯化钾的加入提高了溶液的离子强度,较高的离子强度下,离子自由移动受到限制,实际浓度降低,这有利于反应体系中少量NH3的产生,从而形成一种较弱的气体湍流.这种较弱的气体湍流扰动[12]可能是影响纳米二氧化锆晶相的因素之一.另一方面,在图5中,c为混合相,a为单斜相,对比a、c可知:在相同实验条件下CH2(NH2)COOH是改变晶相的又一因素.CH2(NH2)COOH既具有羧基又含有氨基,容易与锆离子配位形成稳定的螯合物,可能正是由于这种络合作用而促使纳米二氧化锆发生了晶相转变.可能的络合过程如下:在成核阶段,Zr4+与小分子络合剂Y(CH2(NH2)COOH)和OH—同时连接,CH2(NH2)COOH与 OH—形成争夺 Zr4+的趋势,无机物和有机物在界面上发生由分子识别诱导的竞争反应,从而形成了 Ym-Zr-OHn晶核,从化学动力学上讲,这种竞争将减缓反应速率,使纳米粒子结构的各向异性充分发挥,从而对其晶相的调控产生一定的影响[13-15].再加上一定量KCl的加入,加大了溶液的离子强度,进一步调控了Zr4+的释放,使其有利于t-ZrO2的生成.另外,由表1知:仅当添加剂(甘氨酸/氯化钾)的摩尔比例为1∶2,Zr4+/甘氨酸的摩尔比值为1∶1时,产物才是纯t-ZrO2,这就更加说明单纯的分子络合无法达到物相控制的实验目的,必须结合溶液离子强度的共同作用,才能实现t-ZrO2的晶相控制合成.最后,对比样品e(四方相,NH3·H2O和CH2(NH2)COOH/KCl体系)、d(混合相,NH3·H2O和KCl体系)和c(混合相,KOH和CH2(NH2)COOH/KCl体系) 的XRD衍射花样,进一步表明纯t-ZrO2的形成是气体湍流的动力扰动和分子络合两种因素共同作用的结果.
2.2 吸附性质
利用甲基橙模拟染料废水,测试了不同相态纳米ZrO2的吸附性能,结果如图6所示.
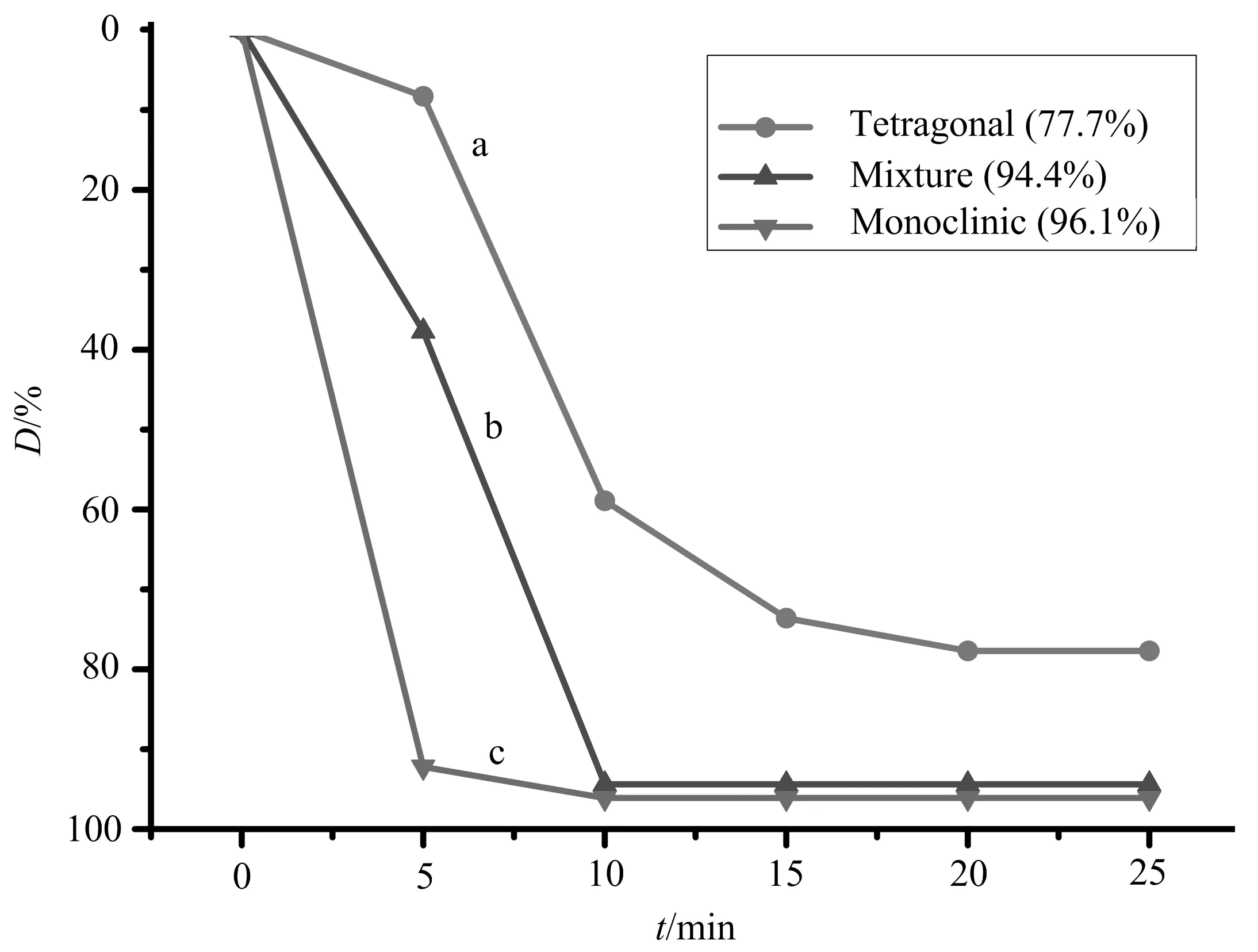
a:纯四方相;b:混合相;c:纯单斜相.图6 合成产物对甲基橙的去除率
图6显示,单斜相ZrO2去除甲基橙的效率最高,去除率达到96.1%,而在相同实验条件下,混合相与四方相ZrO2的去除率次之,分别为94.4%和77.7%.此外,单斜相ZrO2对甲基橙的吸附速度较快,在前5 min吸附去除率已达92.1%,10 min时达到吸附平衡.
图7为不同物相二氧化锆对甲基橙吸附的实时紫外吸收光谱图.

A:混合相;B:四方相;C:单斜相.图7 不同物相ZrO2对甲基橙吸附的紫外吸收光谱图
图7显示,纳米二氧化锆的物相不同,对甲基橙吸附性能也不同.
相对于四方相纳米ZrO2的XRD衍射峰(图3)而言,m-ZrO2的衍射峰(图2)弱而宽化.弱衍射峰的存在,说明m-ZrO2的结晶性较差,根据谢乐公式[16]L=kλ/βcosθ(式中:k=0.94;λ= 0.154 06 nm;θ为布拉格角(°);β为积分半高宽(rad);L为晶粒尺寸(nm))可知,m-ZrO2宽化的衍射峰表明其颗粒尺寸相对较小.
图8为纯m-ZrO2及t-ZrO2的SEM(扫描电子显微镜)扫描照片.

A: m-ZrO2;B: t-ZrO2.图8 纯m-ZrO2及t-ZrO2的SEM扫描照片
图8显示,t-ZrO2呈现出团聚的结构,颗粒尺寸在30 nm左右,而m-ZrO2的分散性相对较好,颗粒尺寸在10 nm左右,这与XRD分析结果相吻合.由此可知,可能是m-ZrO2的较小颗粒及相对较好的分散性使其比表面积较大,故在甲基橙吸附实验中展现出优异的吸附性能.
2.3 循环实验
在实际应用中,为达到循环使用的目的,需要考虑吸附剂的稳定性能.基于此,通过循环实验研究纳米二氧化锆(单斜相,180 ℃下水热制备)的稳定性.将吸附过后的样品充分洗涤干燥,再将其用作吸附剂进行重复实验,在相同实验条件下吸附甲基橙染料.结果如图9所示.

图9 纯m-ZrO2对甲基橙去除率循环实验
图9显示,吸附剂在使用5次后,去除率仍可达80%左右.总之,单斜相二氧化锆展示了较强的吸附能力和优良的稳定性,有望成为一种具有应用前景的吸附剂.
3 结束语
(1) 以ZrOCl2·8H2O为原料,在氨水或氢氧化钾的作用下,水热反应制得纳米ZrO2粉体.实验结果表明:溶液pH及水热温度对二氧化锆粉体晶相调控几乎没有影响.
(2) 在该实验条件下,CH2(NH2)COOH/KCl的加入调控了二氧化锆粉体的晶型,当其摩尔比值等于1∶2时,能够在180 ℃下实现从单斜相到四方相的转变而得到单一的四方相.当CH2(NH2)COOH/KCl的摩尔比值大于1/2或在1/6~1/36之间均为混合相态.由此可知,CH2(NH2)COOH/KCl在二氧化锆的晶相调控中具有关键作用.因此认为,纯t-ZrO2的形成是在一定离子强度下气体湍流的动力扰动和分子络合两种因素共同作用的结果.
(3) 在甲基橙吸附实验中,单斜相ZrO2的吸附性能较好,混合相及四方相次之,可见,纳米ZrO2的晶相可能是影响其吸附性能的主要因素.
