硫熏及不同硫熏程度对白术化学成分的影响△
2018-11-06徐春良付辉政赵雯戴冕任琦钟瑞建
徐春良,付辉政,赵雯,戴冕,任琦*,钟瑞建*
(1.江西中医药大学附属医院,江西 南昌 330006;2.江西江中中药饮片有限公司,江西 九江 332300;3.江西省药品检验检测研究院/江西省药品与医疗器械质量工程技术研究中心,江西 南昌 330029)
白术为菊科植物白术Atractylodes macrocephala Koidz.的干燥根茎,具有健脾益气,燥湿利水,止汗,安胎之功效。用于脾虚食少,腹胀泄泻,痰饮眩悸,水肿,自汗,胎动不安[1-4]。白术始载于 《神农本草经》,是常用大宗药材,俗有 “南术北参、十方九术”之说,为健脾补气第一要药,广泛应用于临床[5]。白术含有较多挥发性成分、内酯类成分、苷类及多糖类成分[6-7],储存不当容易发生 “走油变色”,且影响其外观和质量。白术在产地加工中,常采用硫磺熏蒸的方法进行干燥,经硫磺熏蒸后白术外观性状更加美观不易变色且更易保存[8]。《中华人民共和国药典》2015年版一部规定白术药材及饮片中二氧化硫残留量不得大于 400 mg·kg-1[1],笔者在2017年白术国家评价性抽验发现,部分白术饮片二氧化硫残留量超过规定限度1倍以上。硫熏不仅影响中药药效及安全性,还可能会破坏药材化学成分[9-11]。目前未见不同硫磺熏蒸程度对白术化学成分的影响研究。本实验首先采用薄层色谱法筛查硫熏对白术化学成分的变化,通过硅胶柱色谱分离制备和波谱技术分析确证发生变化的化学成分结构,其次采用离子色谱法和高效液相色谱法考察不同硫磺熏蒸程度白术与发生变化化学成分的相关性,为白术饮片的科学炮制、合理应用及质量评价提供参考。
1 仪器与试药
1.1 仪器
Thermo Fisher ScientificICS-1600离子色谱仪、淋洗液自动发生器、阴离子交换柱;CAMAG TLC Visualizer薄层色谱数码成像系统;Waters Xevo G2QTOF飞行时间质谱仪;SHIMADAU LC-20AD高效液相色谱仪,四元泵、自动进样器、柱温箱、PAD检测器、LC solution工作站;Sartorius BT 25 S十万分之一电子天平。
1.2 试药
东莨菪内酯对照品(中国食品药品检定研究院,批号:110768-200504,供含量测定用);硅胶G板(青岛海洋化工厂分厂);乙腈、甲醇为色谱纯,水为娃哈哈饮用纯净水,其他试剂均为分析纯。
白术(批号:20160901、170110、170209)购于浙江磐安药材市场,经江西省药品检验检测研究院付辉政副研究员鉴定为菊科植物白术 Atractylodes macrocephala Koidz.的干燥根茎。
2 方法与结果
2.1 硫磺熏蒸白术的制备
取白术饮片,采用有机玻璃材料自制熏箱进行硫磺熏蒸。熏箱内设一层网状隔板,将200 g白术饮片均匀摆放在隔板上,将定量硫磺(0.5、1、2、3 g)置于坩埚内并点燃形成蓝色火焰时放置于熏箱底部,熏至24 h后将白术饮片放置于恒温干燥箱80℃干燥。
2.2 硫磺熏蒸对白术化学成分的影响
2.2.1 薄层色谱定性筛选 取同一批硫熏与未硫熏白术样品粉末各4 g,加甲醇20 mL,超声处理45 min,滤过,滤液作为供试品溶液。吸取上述供试品溶液20μL,分别点于同一硅胶G薄层板上,以三氯甲烷-丙酮(19∶1)为展开剂,展开,取出,晾干,在紫外光灯(365 nm)下检视。结果见图1。

图1 白术样品中香豆素类成分薄层色谱图
由图1可知,白术经硫熏后,斑点1和2含量明显下降,说明硫熏会对白术化学成分产生影响。取不同批次的样品3批,同法实验,结果一致。为明确斑点1和2的结构,进一步对斑点1和2进行了制备及结构确证。
2.2.2 目标产物的制备 取白术(2.5 kg),粉碎,用10倍量80%乙醇回流提取3次,每次2 h。提取液浓缩至适量,用乙酸乙酯萃取4次,萃取液减压浓缩至干,得乙酸乙酯部分(105 g)。将乙酸乙酯部分与硅胶拌样,经正相硅胶柱色谱分离,以三氯甲烷-丙酮(50∶1~10∶1)梯度洗脱,经薄层色谱检视,合并相近的组分,得 10个组分(Fr.1~Fr.10)。Fr.6(8.6 g)以三氯甲烷-丙酮(15∶1)等度洗脱,得到目标产物1(斑点1)和2(斑点2)。
2.2.3 目标产物结构鉴定 目标产物1:淡黄色针状结晶(甲醇)。ESI-MS m/z:193[M+H]+,191[M-H]-。1H-NMR(600 MHz,CD3OD)δ:7.83(1H,d,J=9.4 Hz,H-4),7.08(1H,s,H-8),6.71(1H,s,H-5),6.18(1H,d,J=9.4 Hz,H-3),4.88(1H,s,-OH),3.88(3H,s,-OCH3);13C-NMR(150 MHz,CD3OD)δ:164.1(C-2),112.5(C-3),146.2(C-4),109.3(C-5),146.8(C-6),153.3(C-7),103.6(C-8),151.6(C-9),112.3(C-10),56.8(OCH3)。综合上述信息,将以上波谱数据与文献数据对照基本一致[12],鉴定为东莨菪内酯。
目标产物2:白色针状结晶(甲醇)。ESI-MS m/z:163[M+H]+,161[M-H]-。1H-NMR(600 MHz,CD3OD)δ:7.81(1H,d,J=9.4 Hz,H-4),7.41(1H,d,J=8.5 Hz,H-5),6.16(1H,d,J=9.4 Hz,H-3),6.75(1H,dd,J=8.5,2.2 Hz,H-6),6.70(1H,d,J=2.2 Hz,H-8);13C-NMR(150 MHz,CD3OD)δ:163.5(C-2),113.8(C-3),146.1(C-4),130.4(C-5),113.2(C-6),161.9(C-7),103.3(C-8),157.8(C-9),112.1(C-10)。综合上述信息,将以上波谱数据与文献数据对照基本一致[13],鉴定为伞形花内酯。
3 不同剂量硫磺熏蒸对白术中东莨菪内酯的影响
3.1 东莨菪内酯的HPLC含量测定
3.1.1 色谱条件 色谱柱为Inertsil ODS-SPC18(250 mm×4.6 mm,5μm),流动相为乙腈-水(8∶92),检测波长为344 nm,柱温为30℃,进样量为20μL。在上述色谱条件下,东莨菪内酯分离情况及峰形良好。色谱图见图2。
3.1.2 对照品溶液的制备 取东莨菪内酯对照品适量,精密称定,加甲醇制成每l mL含4μg的溶液,即得。
3.1.3 供试品溶液的制备 取本品粉末(过四号筛)约4 g,精密称定,置具塞锥形瓶中,精密加入甲醇20 mL,密塞,称定质量,超声处理(功率500 W,频率40 kHz)45 min,放冷,再称定质量,用甲醇补足减失的质量,摇匀,滤过,取续滤液,即得。
3.1.4 线性关系考察 精密称取东莨菪内酯对照品10.26 mg,置50 mL量瓶中,加甲醇溶解并稀释至刻度,摇匀,得东莨菪内酯对照品溶液。吸取东莨菪内酯对照品溶液,加甲醇分别稀释至质量浓度为1.026、2.052、4.104、6.146、8.208μg·mL-1,分别吸取20μL按上述色谱条件测定峰面积。以进样量(X)为横坐标,峰面积(Y)为纵坐标,绘制标准曲线,得回归方程为Y=3.693 1×106X-3.074 0×103(r=0.999 9),东莨菪内酯进样量在0.020 5~0.164 2μg与峰面积呈良好线性关系。
3.1.5 精密度试验 精密吸取按3.1.2制备的对照品溶液20μL,按3.1.1色谱条件连续进样6次,测定峰面积。结果东莨菪内酯峰面积的RSD=0.5%(n=6),表明仪器精密度良好。
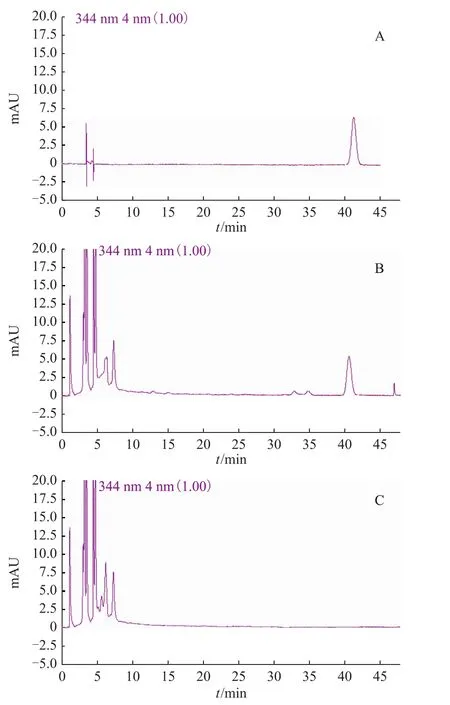
图2 白术及对照品HPLC图
3.1.6 重现性试验 取样品(批号:170110)6份,每份约4 g,精密称定,按3.1.3制备供试品溶液,按3.1.1色谱条件进行分析测定,东莨菪内酯含量的平均值为13.601 2 mg·kg-1,RSD=1.7%,表明该方法重现性良好。
3.1.7 稳定性试验 精密吸取供试品溶液(批号:170110)20μL,分别于 0、5、10、15、20、24 h进样测定,测得东莨菪内酯峰面积的RSD=1.6%(n=6),说明供试品溶液在24 h内稳定。
3.1.8 回收率试验 采用加样回收率法,精密称取已知含量(批号:170110)的样品 6份,每份约2.0 g,精密称定,置具塞锥形瓶中,每份精密加入含东莨菪内酯1.351 0μg·mL-1对照品溶液20 mL,按3.1.3制备供试品溶液,按3.1.1色谱条件进行分析测定,计算回收率。结果东莨菪内酯的平均回收率为100.6%(n=6),RSD=0.7%。见表1。
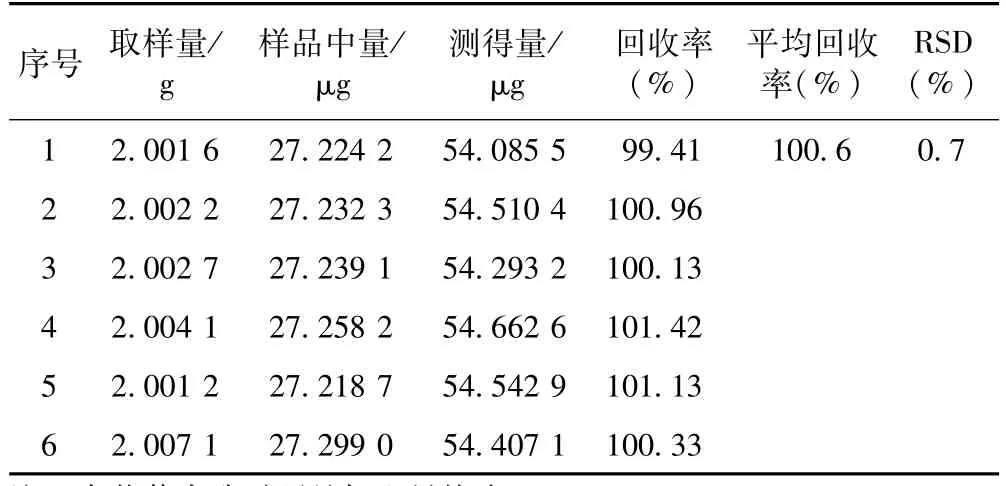
表1 白术中东莨菪内酯回收率试验结果(n=6)
3.1.9 耐用性试验 取样品按3.1.3制备供试品溶液,分别用 Inertsil ODS-SP C18(250 mm×4.6 mm,5μm)、Agilent XDB-C18(250 mm×4.6 mm,5μm)和Waters Sunfire C18(250 mm×4.6 mm,5μm)3种品牌的色谱柱按3.1.1色谱条件进行测定,含量测定结果无明显差别。
3.1.10 样品测定 取白术样品15批,每个样品取3份,按3.1.3制备供试品溶液。精密吸取供试品溶液20μL,按3.1.1色谱条件进样分析,测定峰面积,用外标法计算出东莨菪内酯的含量,测定结果见表2。
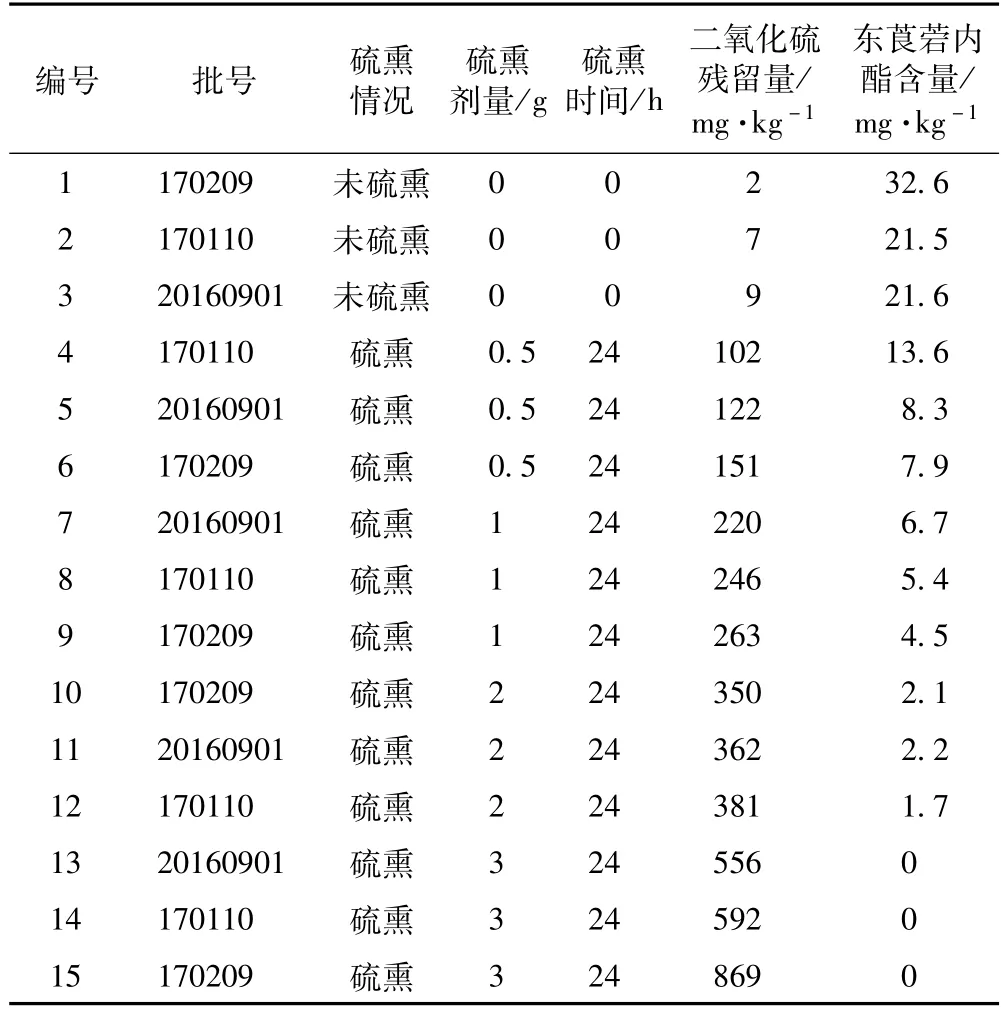
表2 白术中二氧化硫残留量及东莨菪内酯含量测定结果(n=3)
3.2 二氧化硫残留量测定
3.2.1 色谱条件 阴离子交换柱(AS11-HC,250 mm×4 mm),淋洗液为20 mmol·L-1氢氧化钾溶液,抑制电流为 50 mA,流速为 1.0 mL·min-1,柱温为30℃,进样量为25μL[14-15]。二氧化硫残留量测定离子色谱图见图3。
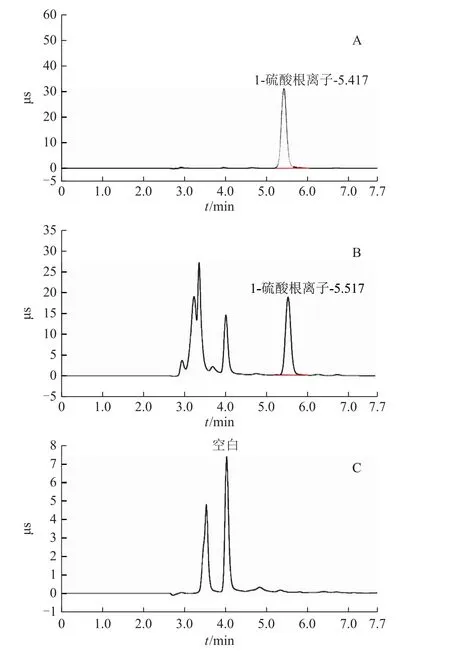
图3 白术中二氧化硫残留量测定离子色谱图
3.2.2 对照品溶液的制备 精密吸取硫酸根标准溶液(1000μg·mL-1),加水制成1、5、20、50、100、200μg·mL-1的溶液,绘制标准曲线。以进样量(X)为横坐标,峰面积积分值(Y)为纵坐标,绘制标准曲线,得回归方程为Y=0.237 8 X-0.036 1(r=0.999 9),硫酸根在 0.025~5.000μg与峰面积呈良好线性关系。
3.2.3 供试品溶液的制备 取白术粉末(过四号筛)约5 g,精密称定,置瓶 A(两颈烧瓶)中,加水50 mL,振摇,使分散均匀,接通水蒸气蒸馏瓶。吸收瓶B(100 mL量瓶)中加入3%过氧化氢溶液20 mL作为吸收液,吸收管下端插入吸收液液面以下。A瓶中沿瓶壁加入5 mL盐酸,迅速密塞,开始蒸馏,保持C瓶沸腾并调整蒸馏火力,使吸收管端的馏出液的流出速率约为2 mL·min-1。蒸馏至瓶B中溶液总体积约为95 mL,用水洗涤尾接管并将其转移至吸收瓶中,并稀释至刻度,摇匀,放置1 h后,以0.45μm微孔滤膜滤过,即得。
3.2.4 方法学考察 取对照品溶液测定6次,进行精密度考察;取供试品溶液,分别于0、5、10、15、20、24 h测定,进行稳定性考察;另取白术粉末(过四号筛)约5 g,共6份,按3.2.3制备并测定,进行重复性考察;再取白术粉末(过四号筛)约2.5 g,共6份,分别精密加入一定量的亚硫酸钠对照品,按3.2.3测定,进行加样回收率考察。结果表明,精密度、稳定性、重复性、加样回收率测定结果的RSD值均在2.0%以内;样品溶液二氧化硫残留量平均质量浓度为 220 mg·mL-1,24 h内测定稳定,平均加样回收率为97.52%。
3.2.5 样品测定 分别取白术粉末(过四号筛)15批,按3.2.3制备供试品溶液。精密吸取供试品溶液25μL,按3.2.1色谱条件进样,测定,计算样品中的硫酸根含量,按照(SO2/SO42-=0.666 9)计算样品中二氧化硫的含量。测定结果见表2。
4 讨论
本实验采用薄层色谱法对硫熏前后白术中化学成分进行定性筛选,并通过硅胶柱色谱分离制备和波谱数据分析确证硫熏对白术中产生影响的化学成分的结构。为了进一步考察硫黄熏蒸程度对白术中东莨菪内酯和伞形花内酯的相关性。由于白术中伞形花内酯含量非常低且液相色谱分离效果不佳,本次实验仅以东莨菪内酯为指标,采用离子色谱法和高效液相色谱法分别对白术中二氧化硫残留量和东莨菪内酯的含量进行测定,其结果重复性良好,方法可行。
实验结果表明,硫熏对白术中香豆素类成分东莨菪内酯和伞形花内酯有显著的影响,其中东莨菪内酯含量随着二氧化硫残留量增加,整体呈下降趋势直至为零。为了避免活性成分的下降,保证药材及饮片的质量,进而确保临床疗效,建议研究白术合理适量硫磺熏蒸的加工方法,并制定合理的二氧化硫残留量限度。
