电镀污泥和红土镍矿浸出液中镍的直接萃取分离研究
2018-08-23朱红斌韦志伟赵梦梦何嘉靖李勇宾李晓辉甘绍凤杨宏斌唐富顺张淑华
朱红斌, 韦志伟, 赵梦梦, 何嘉靖, 李勇宾, 李晓辉,甘绍凤, 杨宏斌, 唐富顺, 张淑华
(1.广西银亿新材料有限公司, 广西 玉林 537624;2.桂林理工大学化学与生物工程学院, 桂林理工大学广西有色金属隐伏矿床勘查及材料开发协同创新中心,广西 桂林 541004;3.广西壮族自治区固体废物管理中心, 广西 南宁 530028)
随着硫化镍矿资源的逐渐减少,从红土矿等氧化镍矿以及含镍钴冶炼渣中提取镍和钴已成为重要的生产途径。对于这些较低品位红土矿以及含镍冶炼渣的处理,近年来采用湿法冶金工艺较为经济有效[1-3]。典型的常压酸浸工艺,浸出液经黄钠铁矾法处理再提镍、钴,具有工艺简单、能耗低、不使用高压釜、投资费用少、操作条件易于控制等优点,但对不同来源和不同种类矿料的适应性不强,流程冗长且返料量大,浸出液杂质含量高,浸渣中镍含量较高,导致镍的回收率低且生产成本高[2-3]。为了分离镍钴获得最大效益,需要经过几个工序,但某些杂质的存在(如铁、镁和锰等)往往使分离复杂化。萃取剂P507对Ca有一定的共萃;Cyanex 301对Ni选择性优于Co,但化学稳定性差;LIX84-I萃取剂可以从氨性溶液中萃取镍,但需要预先将Co2+氧化成Co3+以避免镍萃取过程中钴的共萃[5-7]。广西银亿新材料有限公司的实际生产表明, P204萃取杂质和P507分离镍钴工艺存在的主要问题是金属回收率低,镍回收率仅为70%,钴回收率45%,该工艺只能处理铁、镁含量较低的原矿。开发新的镍萃取剂,提高Ni、Co的萃取选择性,如协同萃取剂等,是目前从浸出液中分离Ni、Co的技术挑战。HBL型系列萃取剂对于从镍矿加压浸出液以及高浓度硫酸钴溶液中萃取分离镍钴具有较好的效果[8-9]。本文对电镀污泥和红土镍矿进行硫酸浸出,采用特制的HBL型萃取剂- 磺化煤油体系萃取分离浸出液中的铜镍钴,探索从红土矿等氧化镍矿以及含镍钴冶炼渣中提取镍和钴的新工艺。
1 实验方法
1.1 实验材料
HBL型萃取剂主要由磺酸类有机物HA和脂类有机物B混合组成,稀释剂为磺化煤油,氢氧化钠为分析纯。实验所用电镀污泥和红土镍矿的浸出液由广西银亿新材料有限公司提供,采用电感耦合等离子体光谱仪(ICP)分析浸出液的成分,结果见表1。

表1 电镀污泥浸出液成分 g/L
表2 除铁铬后的红土镍矿浸出液成分 g/L
1.2 萃取方法
电镀污泥浸出液直接稀释一倍后作为实验萃原液使用,红土镍矿浸出液除铁铬后作为实验萃原液使用。按9∶11的比例取适量的HBL型萃取剂与磺化煤油,将两者混合用电动搅拌机搅拌30 min。用质量分数为17%的氢氧化钠溶液进行皂化,皂化率为51%。取适量浸出液,用质量分数为17%的氢氧化钠溶液将浸出液的pH调至一定值(即初始pH),并记录溶液体积扩大倍数。分别量
取一定体积的油相和浸出液加入到锥形瓶中,迅速放入一定温度下的恒温水浴震荡箱中震荡一定时间。取出锥形瓶,将混合液倒入梨型分液漏斗,静置分层以后进行分液操作。水相从下出口排出,记录水相的体积。水样采用ICP测定其中Cu、Ni、Co的浓度,计算Cu、Ni、Co萃取率。萃取率计算公式如下:
萃取率=(C初始浓度×V初始-C水相浓度×V水相)/(C初始浓度×V初始)×100%
(1)
1.3 萃取剂红外光谱表征(FT-IR)
采用赛默飞(Thermo Fisher)IS10傅里叶原位红外光谱仪,波数范围400~4 000 cm-1,扫描次数为15次,分辨率为4 cm-1,原位池窗片为KBr。
2 结果与讨论
2.1 萃取初始pH值对金属离子萃取率的影响
萃取相比O/A=1∶1,萃取时间5 min,萃取温度25 ℃,使用17%的NaOH调节浸出液初始pH值至所需酸度,实验结果如图1所示。

图1 萃取初始pH值对金属组分萃取率的影响
对于电镀污泥浸出液,随着萃取初始pH值的增大,Ni、Cu的萃取率逐渐增大,当萃取初始pH值达到2.0后,Ni、Cu离子的萃取率基本达到最大值, Ni的最大萃取率为37.85%,Cu的最大萃取率为92.56%;当萃取初始pH值为2.8时,Ni、Cu的萃取率略有降低。表明在电镀污泥浸出液中,HBL型萃取剂优先萃取Cu离子,从而导致Ni离子的萃取率偏低。随着萃取初始pH值的增大,Co的萃取率变化不大,仅当萃取初始pH为2.5时,Co的萃取率达到最大值3.65%。在Ni、Cu较高浓度的电镀污泥浸出液中,随着萃取初始pH的增大,Cu萃取率最大,其次是Ni,其他金属离子的萃取率相对较低,基本上很难被萃取。说明该萃取剂对Ni、Cu离子选择性高,可以实现镍铜与其他离子的分离,但Cu离子浓度较高时,会抑制Ni的萃取。综上,使用HBL型萃取剂萃取电镀污泥浸出液中的Ni、Cu离子,可考虑将萃取初始pH值设定在2.0~2.5之间。为使Ni的萃取率有效提高,可考虑先将Cu从电镀污泥浸出液中分离,再进行HBL型萃取剂萃取Ni。
从红土镍矿浸出液萃取结果看,随着萃取初始pH值的增大,各金属离子的萃取率逐渐增大。Ni、Cu在萃取初始pH值为1.0~2.0时,萃取率增大效果明显,pH值为2.0时趋于稳定,此时Ni的萃取率为96.91%,Cu的萃取率约为100%; pH值在2.0~3.0之间时,Ni、Cu的萃取率变化不大,pH值为3.0时,达到最大值,Ni的最大萃取率为98.08%,Cu的最大萃取率为100%。Co的萃取率随着萃取初始pH值的增大,逐渐增大,当初始pH值为2.0时,Co的萃取率68.63%;pH值为3.0时,Co的萃取率为77.84%。随着萃取初始pH值的增大, Fe、Cr元素的萃取率逐渐增大,pH值为1.5时,Fe的萃取率为8.4%、Cr的萃取率为1.14%;pH值为2.0时,Fe的萃取率大约为20%、Cr的萃取率为10%。随着萃取初始pH值的增大,Mg的萃取率变化不大,pH值在1.0~3.0时,Mg最大的萃取率为6.32%。综上,采用HBL型萃取剂萃取红土镍矿浸出液中的Ni、Cu离子时,可选择萃取初始pH值为2.0,这样既可获得Ni、Cu的高萃取率,又可降低杂质金属离子的萃取率。与电镀污泥浸出液的萃取结果相一致的是,该萃取剂对Ni、Cu离子具有较高的选择性。
另外,电镀污泥浸出液中Ni、Cu的萃取率均比红土镍矿浸出液中Ni、Cu的萃取率低。而从表1和表2可见,电镀污泥浸出液中Ni、Cu离子的浓度均比红土镍矿浸出液中的高。上述萃取实验采用的是单次萃取操作方式, 而HBL型萃取剂的单次萃取容量可能较易达到饱和状态,因此在萃取相比(O/A)相同的情况下,对于这两种浸出液,相同体积用量的萃取剂单次萃取出的Ni、Cu量相差不大,导致了实验中Ni、Cu离子浓度较高的电镀污泥浸出液单次Ni、Cu萃取率反而相对低;其次,电镀污泥成分比较复杂,浸出液中所含的杂质较多,这可能也影响了萃取剂单次萃取Ni、Cu的萃取效率。
2.2 萃取温度对金属离子萃取率的影响
萃取相比O/A=1∶1,萃取时间5 min,萃取初始pH值为2.0。用恒温反应震荡箱控制实验所需温度,实验结果如图2所示。
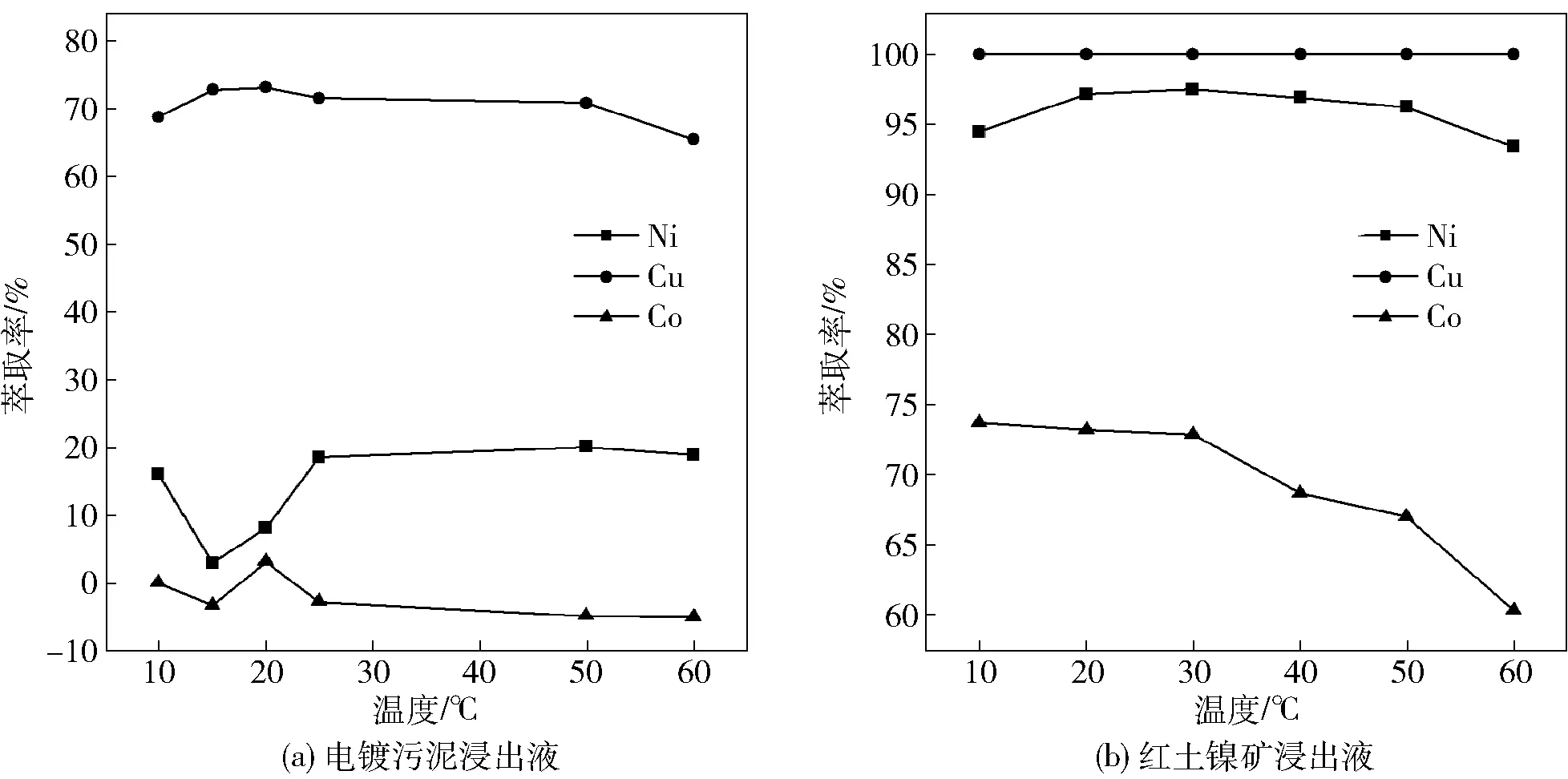
图2 萃取温度对Cu、Ni和Co萃取率的影响
由图2可见,萃取电镀污泥浸出液时,温度对萃取效率影响不大。无论是低温还是较高的温度条件,HBL型萃取剂对Ni2+、Co2+、Cu2+的萃取率基本无太大变化,只是萃取温度50 ℃以上时,Cu离子的萃取率略有下降,因此,萃取在常温下进行即可。对于红土镍矿浸出液,随着萃取温度的升高,Cu的萃取率几乎不变化,萃取初始pH值为2.0,萃原液中Cu浓度为0.083 g/L的情况下,Cu的萃取率已经可认为达到100%。而Ni的萃取率随着温度的升高,先升高后降低, 20 ℃时,Ni的萃取率达到最大,为97.46%;常温时,Ni的萃取率96.91%。在萃取初始pH值为2.0的条件下,随着萃取温度的升高,Co的萃取率逐渐降低。由此可见,该萃取剂对Ni、Cu的萃取热稳定性较好,而萃取Co时则受温度影响较大,因此可以适当选取较高的萃取温度,以提高对Ni离子的萃取选择性。
2.3 萃取时间对金属离子萃取率的影响
萃取相比O/A=1∶1,萃取温度25 ℃,萃取初始pH值2.0,萃取时间分别为(min):2、4、6、10,实验结果如图3所示。
由图3(a)可见,对于电镀污泥浸出液,萃取时间从2 min延长至4 min时,Cu萃取率从约20%增大到70%左右,Ni萃取率从约5%增大到20%左右,Cu、Ni萃取率增幅明显,但随着时间的进一步延长,萃取率变化不大,说明萃取达到饱和或平衡。由图3(b)可见,对于红土镍矿浸出液,萃取时间对金属离子的萃取率几乎没有影响,说明2 min后萃取即达到饱和或平衡。由此可见,HBL型萃取剂对Ni、Cu离子的萃取动力学速率较大。另可见,延长萃取反应时间,Co萃取率基本不变,维持较低,进一步说明该萃取剂对Ni、Cu离子具有较高的选择性。
2.4 萃取相比O/A对金属离子萃取率的影响
萃取温度25 ℃,萃取时间4 min,萃取初始pH值2.0,萃取相比O/A分别为:2∶1、1∶1、1∶2、1∶4,实验结果如图4所示。
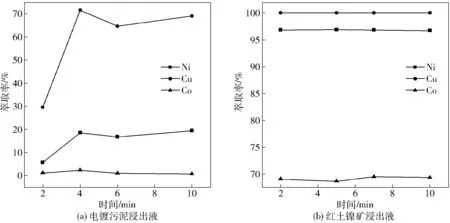
图3 萃取时间对Cu、Ni和Co萃取率的影响
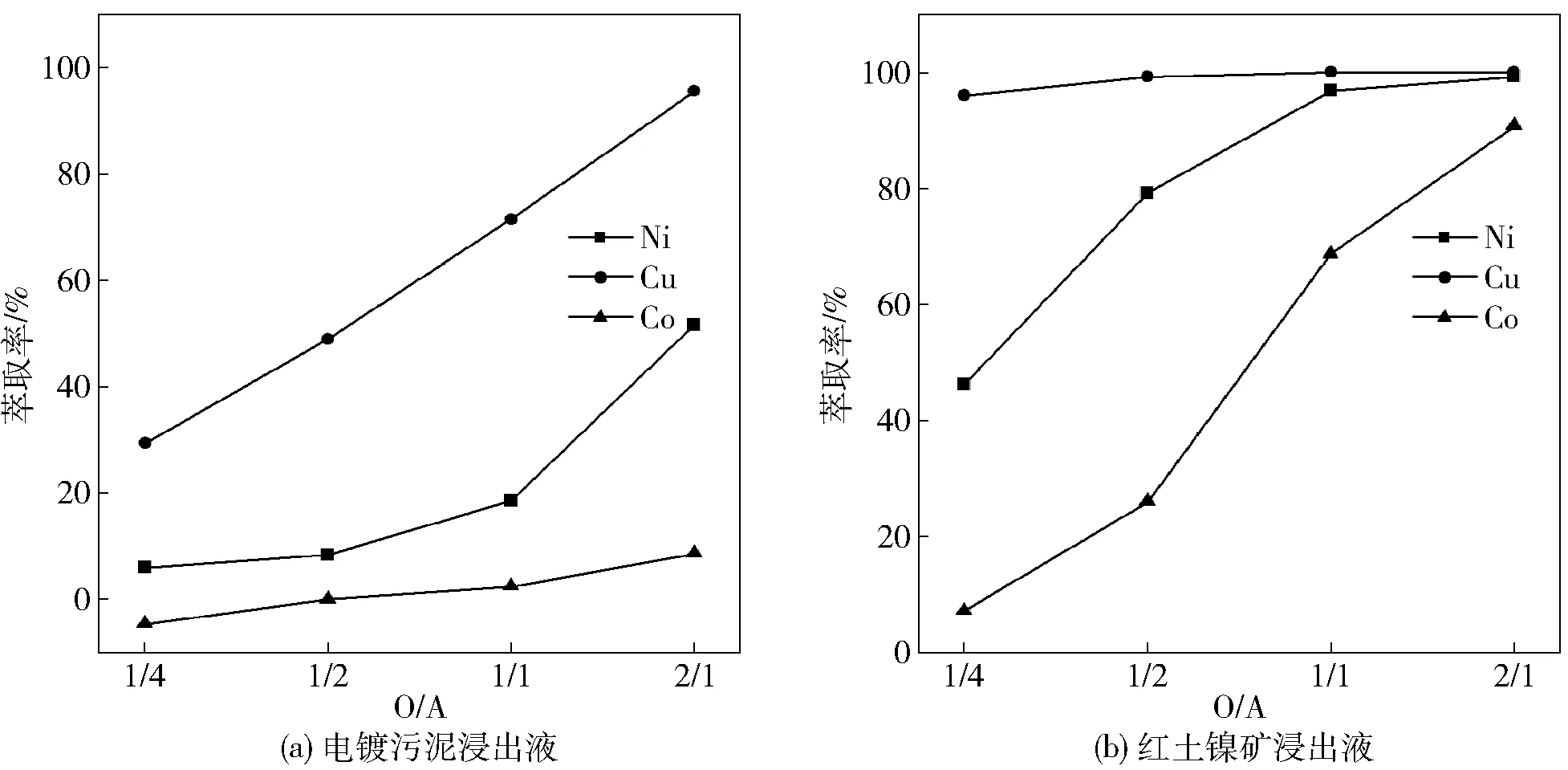
图4 萃取相比O/A对Cu、Ni和Co萃取率的影响
由图4可见,对于电镀污泥浸出液,相比O/A对Ni、Cu离子的萃取率影响较大,随着水相比例的减小,萃取率增大,也就是油相体积越大,萃取效率越高;而相比O/A对Co的萃取率影响较小。对于红土镍矿浸出液,随着萃取相比O/A的增大,Ni、Co的萃取率都呈现较大幅度的变化,而Cu的萃取率较高,随相比O/A变化不明显。当O/A=1∶1时,红土镍矿浸出液中Cu的萃取率达到100%,Ni的萃取率达到96.91%,Co的萃取率达到68.63%。若继续增大O/A到2∶1,则Co的萃取率将达到90.8%。
由此可见,各金属离子萃取率随萃取相比O/A的增大而增大,主要是由于随着有机相对水相的比例提高,HBL型萃取剂的相对含量增大,促使更多的金属离子进入有机相,萃取率提高。为获得较高的Ni、Cu萃取率,同时抑制Co的萃取,应选取合适的O/A。
2.5 萃取机理探讨
HBL型萃取剂是由磺酸类萃取剂HA与脂类中性萃取剂B组成的复配混合萃取剂,其基本结构单元如图5所示。
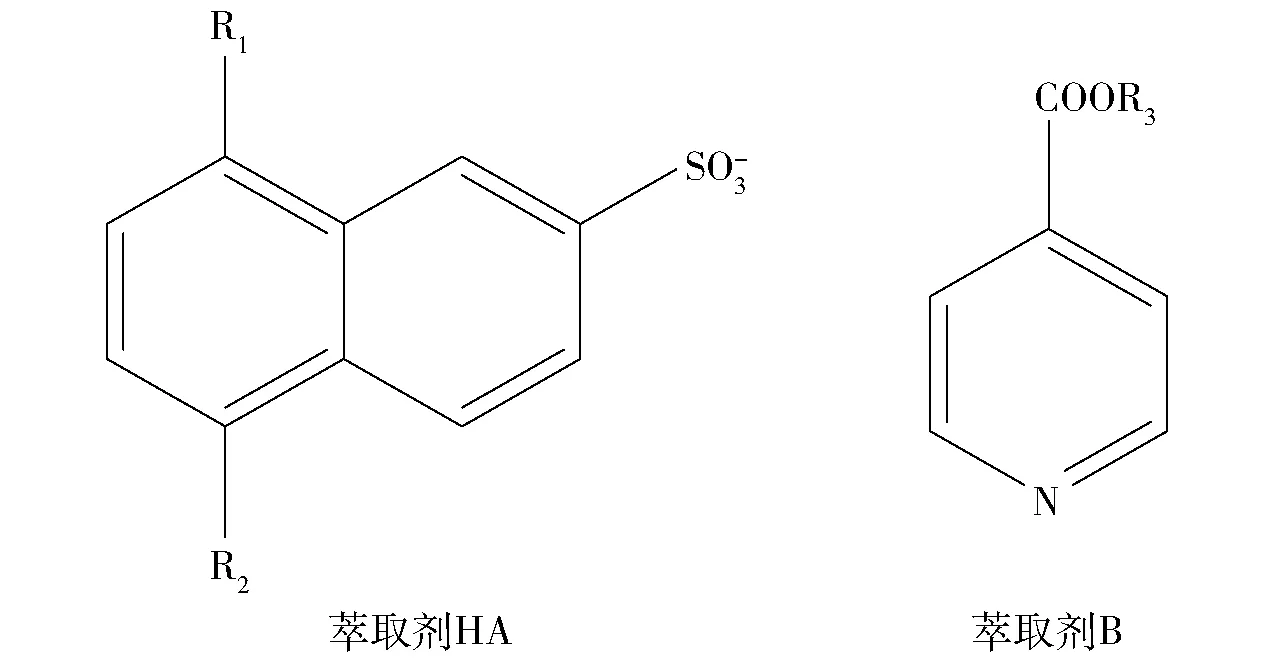
图5 HBL型萃取剂基本结构单元
HA为酸性萃取剂,萃取过程中与金属离子进行阳离子交换,实现萃合物的电荷平衡;B为中性萃取剂,为金属离子提供配位原子,满足配位数,实现金属离子与亲油的有机分子结合进入有机相。各种金属萃取率的高低与HBL型萃取剂金属的选择性有关,而金属离子和萃取剂生成的配合物的稳定性是决定其选择性最重要的因素。
图6为萃取前后的萃取剂红外光谱图。3 450 cm-1、1 629 cm-1可以认为是萃取剂配位水分子的振动吸收,又因3 450 cm-1处峰逐渐减弱,1 629 cm-1处峰消失,说明萃取剂上的部分配位水分子被金属离子替位,即金属离子和萃取剂键合。新增的1 164 cm-1处可以看作是成盐的-SO3-振动吸收,表明磺酸基与金属离子键合发生反应。677 cm-1处可以认为是肟酸上酰胺基O=C-N-的振动吸收,逐渐减弱甚至消失,表明酰胺基与金属离子螯合,从而减少或消失。HBL型萃取剂萃取主要是磺酸基和酰胺基与金属离子发生反应。红土镍矿浸出液中镍的直接萃取过程包括萃取、萃洗、反萃、反洗、皂化等步骤,反萃剂为含硫酸的溶液,皂化剂为氢氧化钠溶液。对于HBL型萃取剂而言,萃取过程的主要反应式为:
萃取: Ni2++2NaA=NiA2+2Na+
反萃: NiA2+2H+= Ni2++2HA
皂化:HA+Na+=H++NaA
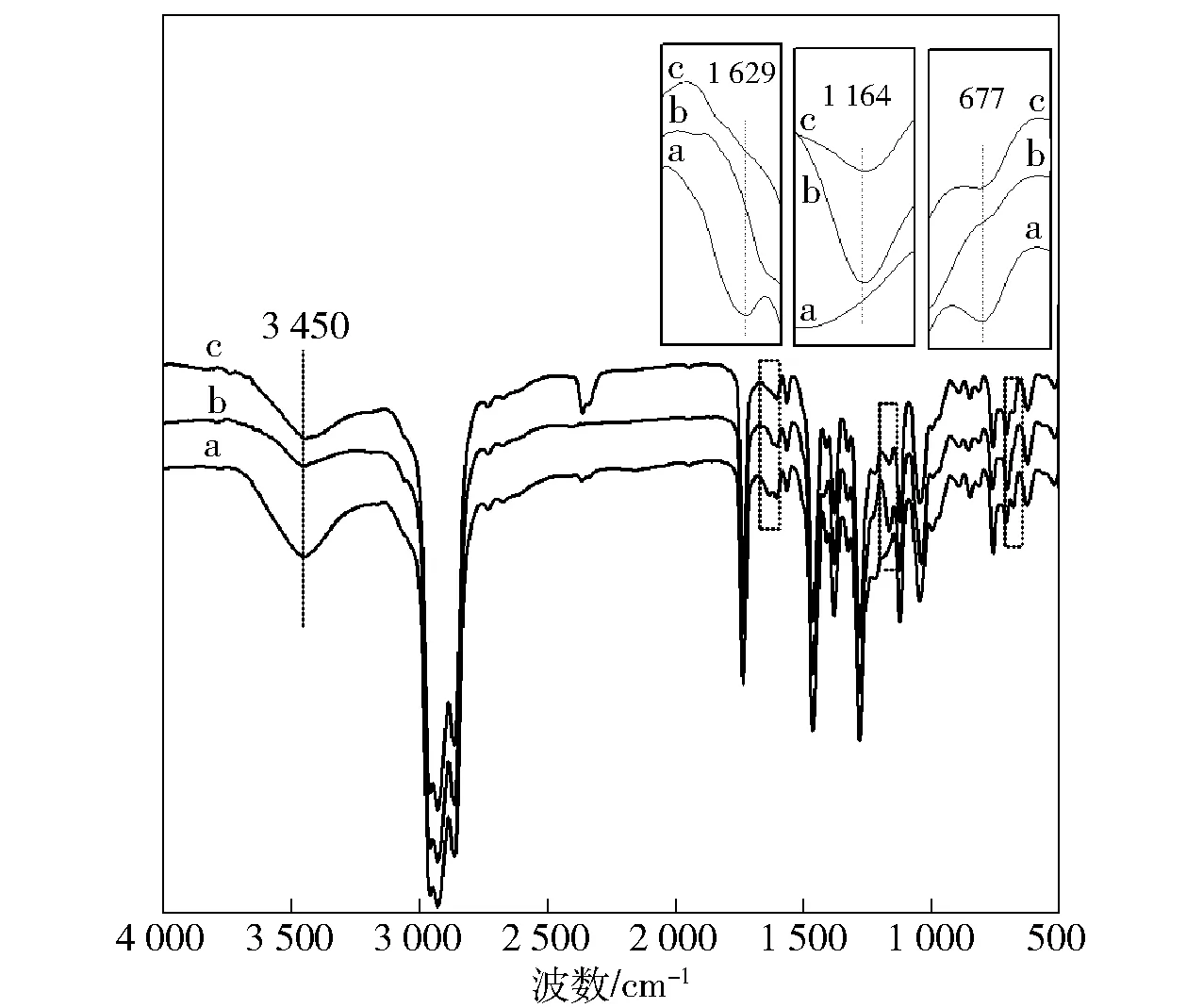
(a:反应前萃取剂;b:电镀污泥浸出液萃取后的萃取剂;c:红土镍矿浸出液萃取后的萃取剂)图6 萃取后的萃取剂红外光谱图
Cu2+的3d轨道有9个电子,还有1个空轨道,加上外面没有电子的4s、4p轨道,通过dsp2杂化,其倾向于生成平面四方形构型的配合物。这种构型具有一定的特殊性,导致铜与其他金属离子性质的一个重要差异,从而构成了铜的螯合萃取分离化学基础。朱萃等[10]对N902萃取铜的研究表明,铜是过渡离子,与N和O给体有较强的亲和力。萃取剂的给体原子是N或O,可以与Cu2+形成配合物,配位键强度极高。当两个萃取剂的原子与Cu2+生成螯合物时,构成了一个极其稳定的环境。同时,在萃取时,萃取剂中的H+与Cu2+交换,组成中性萃合物,且满足价态和配位数,构成最为理想的萃取螯合物,因此HBL型萃取剂对Cu的萃取率最高。
镍比较常见的配位数为4(sp3杂化)和6(sp3d2杂化)。配位数为6时,配体呈八面体型。由于配体之间的位置不同,5个轨道分裂为2组,电子与配体顶头接近的dz2和dx2-y2作用强烈,能量较高,为6Dq;而另外的dxy、dyz和dzx轨道作用力弱得多,能量较低,为-4Dq。配位数为4时,配体可以形成平面四方形或为正四面体构型。萃取剂的分子量较大,分子间存在较大的空间位阻,所以一般为正四面体构型。同样,四面体场亦发生分裂,但与八面体场完全相反,dxy、dyz和dzx轨道能量较高,为1.78Dq,而dz2和dx2-y2的轨道能量较低,为-2.67Dq。六配位的镍稳定性大于四配位的镍,所以溶液中的镍仅有六配位存在,如图7所示。由此,镍的萃取螯合物不在一个平面上,不利于在几何空间中的有效堆积,因此镍的萃取率小于铜。
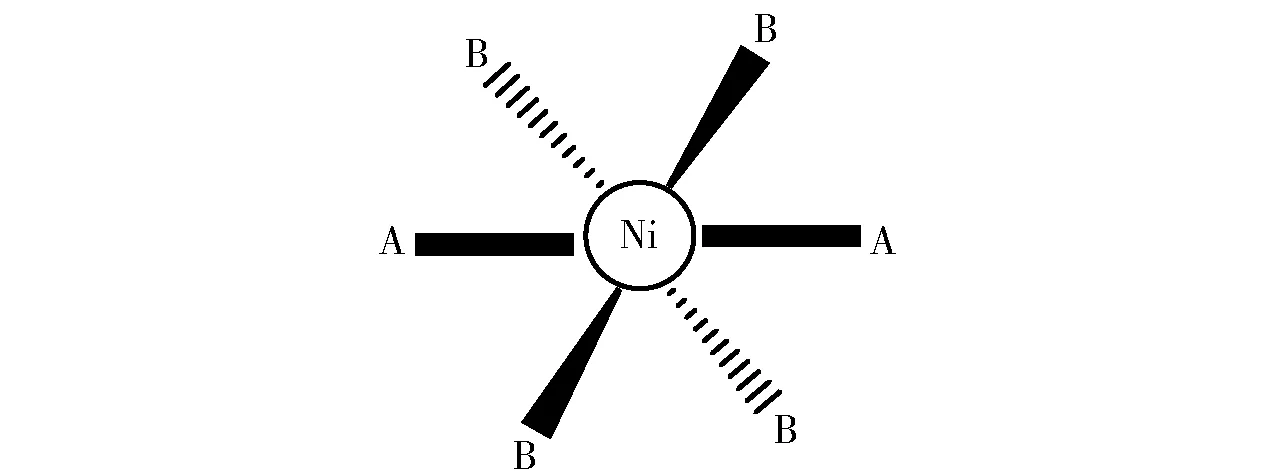
图7 Ni萃取螯合示意图
根据张健等[9]研究,萃取剂中的HA和B能优先与Ni2+形成稳定配合物,从而使镍优先进入有机相。王一乔等[11]人研究发现,HBL型萃取剂对镍离子的选择性大于对钴离子。同时,依据Irving-Williams序,第四周期离子形成的配合物稳定性如下:Mn2+ 基于上述实验结果,对红土镍矿浸出液直接萃镍进行放大试验,试验的主要设备为多级混合澄清萃取槽,5级一组,共3组,萃取槽混合室体积10 L,沉清室长度为混合室长度的3.6倍。采用新配的有机相,在稳定条件,通过萃取- 萃洗-反萃取- 反洗- 皂化一系列工艺过程处理酸浸液,反萃后的有机相重复使用,工艺连续运转。试验采用的镁质红土镍矿堆浸液镍离子浓度为3.48~4.07 g/L,平均3.75 g/L,总铁浓度平均为4.27 g/L,其中二价铁浓度1.35 g/L,镁浓度高达40 g/L以上,Cu浓度0.005 g/L,Co浓度0.057 g/L,萃原液pH值在1.99~2.19之间。试验操作温度为常温(22~27 ℃之间)。在优化条件下连续稳定运行,萃余液Ni浓度稳定小于0.1 g/L,萃余液Ni平均浓度为0.06 g/L,Ni平均萃取率为98.24%,Ni回收率远高于传统净化方法;反萃液中Ni浓度稳定在35 g/L以上,Ni浓度平均达39.14 g/L,反萃液中Ni浓度远比萃取原液中的Ni浓度(平均为3.75 g/L)高,镍的富集倍数大于10。由此说明,萃取过程能够实现高收率条件下镍离子浓度的高倍富集。在萃取—萃洗—反萃取平衡时,该过程Ni、Cu和Co的萃取率分别达98.24%、89.0%和42.10%,而杂质的除去率分别为Fe3+99.01%、Fe2+95.39%、Mg 99.94%、Mn 99.53%、Ca 99.88%、Zn 96.46%、Al 99.87%、Cr 99.7%和SiO299.65%,显示出HBL型萃取剂直接萃镍过程不仅镍收率高,而且具有优异的除Fe3+、Fe2+、Mg、Mn、Ca、Zn、Al、Cr和SiO2的能力。该萃取过程Cu萃取率高的主要原因是原料液中Cu的浓度低,仅为0.005 g/L。该萃取过程Co的收率为42.10%,HBL型萃取剂萃取Co2+的能力介于Ni2+和其它杂质之间,若提高Co的收率,必然会降低其它杂质的除去率。本试验镍的收率和杂质除去率为主要考察指标,没有特别控制Co的萃取率,因此,钴的收率偏低。若适当放宽对杂质除去率的要求,可使有价金属钴的收率进一步提高。 萃取剂的损失包括机械夹带损失、挥发损失、溶解损失以及操作不慎或设备问题导致的跑冒滴漏损失。跑冒滴漏损失在工业生产中通过加强管理可以避免,机械夹带损失可以通过加强水相沉清或其它油回收技术(超声波、树脂聚结等)予以回收。HBL型萃取剂合成时已经充分考虑了其挥发性,其挥发性极小,基本可以忽略不计。因此,重点考虑萃取剂在水相中的溶解损失。本次放大试验萃取过程中,吨镍的萃取剂溶解损失为15.45 kg(萃取剂损失率约为0.06‰),萃取剂损失小,完全在可接受的范围内。另外,取样测试比较了萃取中试连续运转前后有机相对镍的饱和萃取容量,结果表明新配的有机相饱和萃镍容量为7.32 g/L, 而连续运转15 d后的反萃有机相饱和萃镍容量为7.92 g/L, 饱和容量不降反升。该现象从另外一个侧面说明,萃取剂在使用过程中的溶解和挥发损失较小,至少比稀释剂磺化煤油的溶解和挥发损失小。表明HBL型萃取剂的可溶性很小。 目前工业上从红土镍矿浸出液中提取镍的传统工艺为沉淀除杂- 沉镍- 浸出- 深度净化- 电积,即首先在加温和较低pH值条件下除铁(铁矾法、针铁矿法和中和沉淀法),除铁后的浸出液调高pH值水解深度净化除铁、铝、硅等杂质,除杂后液采用沉淀剂沉淀镍获得镍中间产品,然后浸出镍中间产品,进一步深度净化浸出液后进行电解制取金属镍。上述方法存在流程长、镍损失大、能耗高、提镍成本较高等问题。而中试采用直接萃镍新工艺处理镁质红土镍矿堆浸液,吨镍消耗固体氢氧化钠1.58 t,浓硫酸2.36 t,相对于传统工艺,不仅大大简化了生产流,大幅度提高了镍回收率和直收率,而且降低了化学试剂消耗,经济效益明显。 采用HBL型萃取剂萃取分离电镀污泥浸出液和红土镍矿浸出液中的Ni离子时,Ni离子的萃取率受萃取初始pH值和萃取相比O/A的影响较大,受萃取温度和时间的影响较小。室温下(约20~25 ℃),萃取初始pH值为2.0,萃取相比O/A为1∶1时,萃取操作4 min,既可获得Ni、Cu的高萃取率,又可降低杂质金属的萃取率。HBL型萃取剂对Ni、Cu离子的萃取动力学速率较大,对浸出液中各金属组分的萃取选择性依次为:Cu2+>Ni2+>>Co2+及其他金属离子,这与各金属离子和萃取剂形成的螯合物稳定性相关。2.6 红土镍矿浸出液直接萃镍中试及工艺分析
3 结论
