2018年高考模拟试题
2018-07-26赵鑫光杨子毅
赵鑫光 杨子毅
吉林
可能用到的相对原子质量:H—1 C—12 N—14 O—16 S—32 Ca—40 Ga—70 As—75
第Ⅰ卷(选择题共42分)
一、选择题(本题共7小题,每小题6分,共42分。在每小题给出的四个选项中,只有一个选项符合题意)
7.化学与生活、社会发展息息相关,下列有关说法不正确的是
( )
A.唐代著名诗人刘禹锡诗句:“千淘万漉虽辛苦,吹尽狂沙始到金”,可以看出金性质稳定,可通过物理方法得到
B.范晔《后汉书》中写道:“时气错逆,霾雾蔽日”,说明雾所形成的气溶胶能产生丁达尔效应
C.葛洪《肘后备急方》中所述青蒿素的提取方法:“青蒿一握,以水二升渍,绞取汁”,该过程中发生了化学变化
D.南北朝时期炼丹家陶弘景在《陶隐居集》中描述对硝酸钾的鉴定过程:“外观如雪,强烧之,紫青烟起”。其原理是利用了焰色反应
8.设NA为阿伏加德罗常数的值,下列叙述正确的是
( )
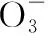
B.常温常压下4.4 g乙醛所含σ键数目为0.7NA
C.18 g D2O和18 g H2O中含有的质子数均为10NA
D.标准状况下,含有1 mol硫原子的SO2和SO3的混合物,其体积小于22.4 L
9.短周期主族元素W、X、Y、Z的原子序数依次增大,W、X、Y原子的最外层电子数之和为12,X、Y、Z位于同一周期,Y原子的最外层电子数既是W原子内层电子数的3倍又是X原子最外层电子数的3倍。下列说法正确的是
( )
A.元素W、Y的最简单氢化物溶于水都显酸性
B.元素X的单质能与W的最高价氧化物发生置换反应
C.元素X和Z能形成X2Z型的离子化合物
D.Z的单质常温下是气体,有毒,具有漂白性
10.分子式为C4H8ClI的有机物共有(不含立体异构)
( )
A.9种 B.10种
C.11种 D.12种

( )
A.充电时,该电池的负极应接电源的负极
B.电路中每转移0.1 mol e-,则负极质量减少3.25 g
D.回收该种废电池可减少重金属Ag+对环境的污染,又可将Ag回收利用
12.下列实验现象和解释正确的是
( )
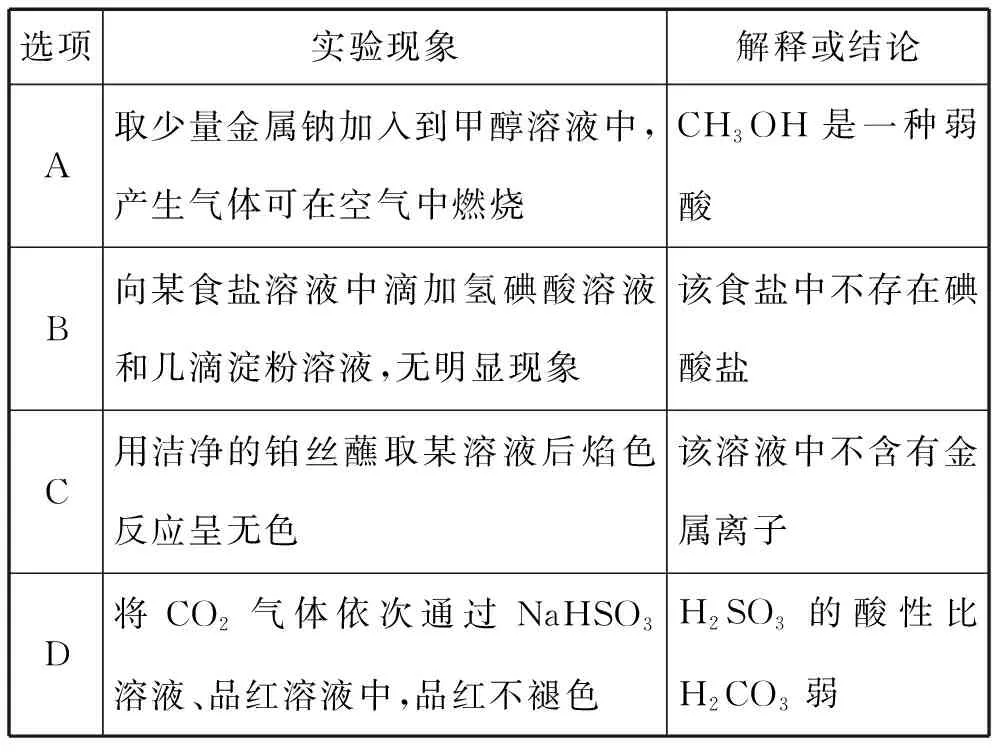
选项实验现象解释或结论A取少量金属钠加入到甲醇溶液中,产生气体可在空气中燃烧CH3OH是一种弱酸B向某食盐溶液中滴加氢碘酸溶液和几滴淀粉溶液,无明显现象该食盐中不存在碘酸盐C用洁净的铂丝蘸取某溶液后焰色反应呈无色该溶液中不含有金属离子D将CO2气体依次通过NaHSO3溶液、品红溶液中,品红不褪色H2SO3的酸性比H2CO3弱
13.常温下向某浓度的氯水中逐滴加入Na2SO3溶液,无气体逸出,溶液pH变化如图所示,下列关系错误的是
( )
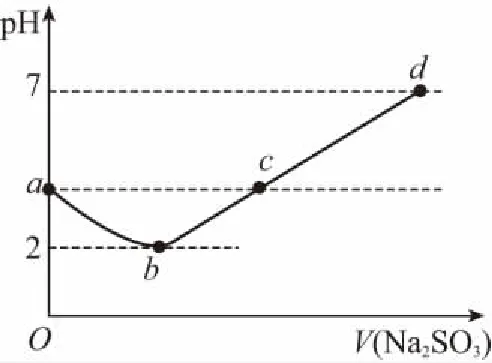
A.a点:c(H+)>c(Cl-)>c(ClO-)
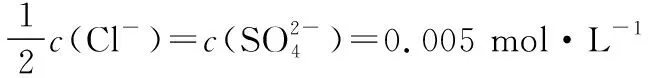
第一次测试:用户在8901下面进行激活,同时激活在SGSN3上,由8901->8902进行TAU测试,用户测试正常;
第Ⅱ卷(非选择题共58分)
二、必做题(本题共3小题,共43分)
26.(14分)氢能是一种清洁、高效的能源,氢燃料电池的效率可达普通化石燃料燃烧率的2倍以上,但氢气的使用面临着储存、运输等问题,目前解决办法之一是采用现制现用的方式,甲醇由于其含氢量高、易储存和运输等优点,可作为制氢原料。

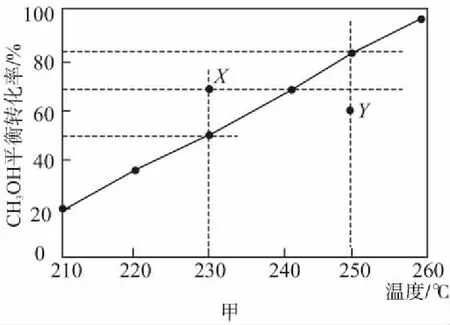
实验室模拟工业上甲醇制氢的反应,在1 L的恒容密闭容器中,充入10 mol甲醇气体和一定量的水蒸气,在不同温度下进行反应。
图甲为n(H2O)/n(CH3OH)=1时,不同温度下,甲醇的平衡转化率
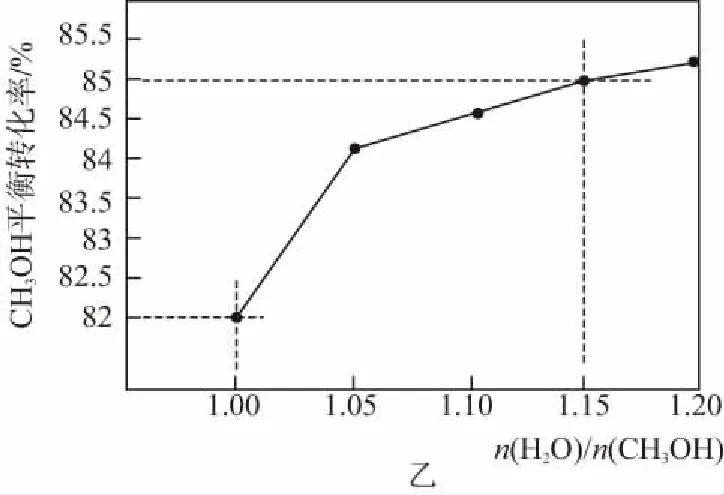
图乙为250℃时,不同n(H2O)/n(CH3OH)下,甲醇的平衡转化率


(3)某时刻若该反应处于图甲中X点的位置,如果想保持转化率不变应该进行的简单操作是________。
(4)某时刻若该反应处于图甲中Y点的位置,此时正逆反应速率的关系是v(正)________(填“>”“<”或“=”)v(逆)。
(5)图甲中,250℃反应达到平衡时容器中的压强为初始压强的________倍。
(6)试根据图乙确定n(H2O)/n(CH3OH)比例为多少较为适宜,并说明理由:__________________。
(7)反应过程中在其他条件不变的情况下,使用合适的催化剂可以提高反应的________。
A.转化率 B.选择性 C.产率 D.反应热
E.速率

(9)在反应过程中会产生少量的二甲醚(CH3OCH3),该物质可与空气在KOH溶液中组成碱性燃料电池,则二甲醚应在原电池的________(填“正”或“负”)极反应,电极反应式为__________________。
27.(15分)氮族元素包括氮(N)、磷(P)、砷(As)、锑(Sb)、铋(Bi)五种元素,具有丰富的化学性质。
(1)将NH3分子中的一个H原子用—OH取代可以得到一种化合物NH2OH,叫作羟胺。在羟胺中N元素的化合价是________;分子中共含有________个共价键。
(2)膦(PH3)是一种磷的氢化物,可由磷化钙水解得到,试写出生成PH3的化学方程式: _____________________;在反应过程中会产生少量的P2H4,一定温度下P2H4可以分解成PH3和某种磷的低氢化物(PxHy,其中x>y),试写出化学方程式:__________________。
(3)As2O3又叫砒霜,是一种剧毒物质,0.1 g可以致命,法医学上用马氏试砷法检验砷中毒,其过程是先将As2O3、Zn和盐酸混合,之后将生成的AsH3导入硬质玻璃管中加热可生成黑色的砷镜(单质砷),试写出相关的氧化还原反应方程式:___________________,_____________________;若某次检验中称取2.00 g的样品,测得砷镜的质量为1.50 mg,则整个检测过程中转移的电子数为________,样品中As2O3的质量分数为________(写百分数)。
(4)锑是氮族元素中从上到下的第一种金属,其在周期表中的位置是________。
(5)三甲基铋[(CH3)3Bi]是一种铋的金属有机化合物,它可由BiCl3和Al4C3在盐酸中反应制得,试写出相关的化学方程式: _____________________;该物质具有较强活性,在沸腾的酒精中,三甲基铋能与硫作用生成Bi2S3和一种气态烷烃,则这种烃的结构简式为________。
28.(14分)水泥生料由石灰石(主要成分为CaCO3和少量惰性杂质)、黏土(主要成分为SiO2和Al2O3)和钢渣(主要成分为Fe2O3)组成。水泥中钙的含量决定着水泥的强度,准确地测定出水泥中的钙含量不仅有助于提高水泥的性能,并且使水泥生料的质量得以保证。实验室模拟工业上水泥生料中钙含量的测定实验流程如下图所示:
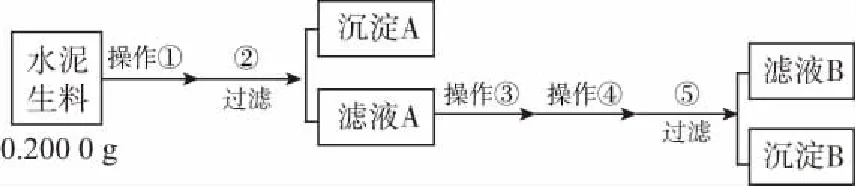
操作①为加入过量的盐酸浸取;
操作③为加入稍过量的0.25 mol/L(NH4)2C2O4溶液,加入2滴甲基橙指示剂,此时溶液显红色,无沉淀生成;
操作④为加热溶液至70~80℃,在不断搅拌下以每秒1~2滴的速度滴加6%氨水(密度0.973 g/cm3)至溶液由红色变为黄色。热水浴30 min,搅拌,冷却陈化。

(1)步骤①中酸浸前应将水泥生料进行粉碎处理,其目的是 _____________________;为达到相同目的,还可以进行的操作是__________________。
(2)步骤②滤液A中主要存在的阳离子是__________________。
(3)操作③中使用的(NH4)2C2O4灼烧可以完全分解产生四种气态产物,试写出相关的化学方程式: _____________________;(NH4)2C2O4完全分解后,恢复到室温,得到混合气体的平均摩尔质量为________。
(4)步骤⑤中过滤后为得到纯净的草酸钙,先用冷的 0.1%(NH4)2C2O4溶液洗涤沉淀几次,再用水洗涤干净,用0.1%(NH4)2C2O4溶液洗涤沉淀是为了__________________。
(5)对于草酸钙的滴定通常采用高锰酸钾法,其具体步骤如下:
(ⅰ)向沉淀中加入适量酸X,使其全部溶解,并定容到100 mL容量瓶中;
(ⅱ)用移液管移取25.00 mL溶液于250 mL锥形瓶中,用0.010 00 mol/L的KMnO4溶液滴定至终点,并记录消耗KMnO4溶液的体积;
(ⅲ)重复实验3次,取平均值,计算水泥样品中的钙含量。
加入的酸X可以选择________(填序号),不选择其他酸的原因是________。
A.硝酸 B.盐酸 C.硫酸
(6)该滴定反应的离子方程式为__________________。
(7)在滴定过程中,滴入第一滴KMnO4溶液时,褪色速度较慢,之后褪色速度明显加快,出现这种现象可能的原因是__________________。
(8)若消耗KMnO4溶液的平均体积是22.50 mL,则水泥样品中的钙含量(以氧化钙的质量分数计)为________。
三、选做题(本题包括2小题,每小题15分,任选一题作答,多答则按所答的第一题评分)
35.【物质结构与性质】(15分)
第ⅤA族和第ⅢA族元素可以形成很多具有特殊功能的材料,请根据提示回答下列相关问题:
(1)已知硼、铝、镓位于同一主族,则镓原子核外电子占据能量最高的能级符号为________;铝原子核外电子运动状态共有________种。
(2)氮、磷、砷位于同一主族,则As原子的价层电子排布图为________。
(3)在第三周期主族元素中,第一电离能在磷和铝之间的元素有________(写元素符号)。
(4)氨(NH3)和膦(PH3)是两种三角锥形气态氢化物,其键角分别为107°和93.6°,试分析PH3的键角小于NH3的原因:__________________。
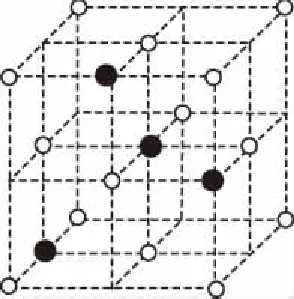
(5)磷化铝的晶体结构类型如图所示,白球代表Al原子,黑球代表P原子,若将白球和黑球看作同种原子,则该晶胞与________(填一种常见单质名称)类似;若晶胞边长为lnm,则距离最近的两个磷原子之间的距离为________nm。
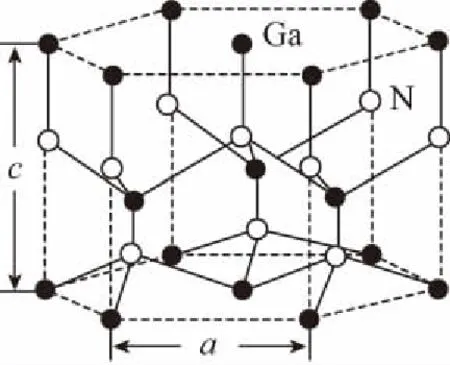
(6)氮化镓是具有重要应用价值的半导体,其部分晶体结构如图所示,每个晶胞中Ga原子个数为________个,若晶胞底边长为anm,高为cnm,则氮化镓的晶体密度为________g/cm3。(用含a、c的代数式表示,阿伏加德罗常数用NA表示)
36.【有机化学基础】(15分)
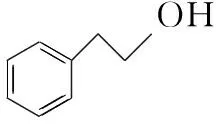
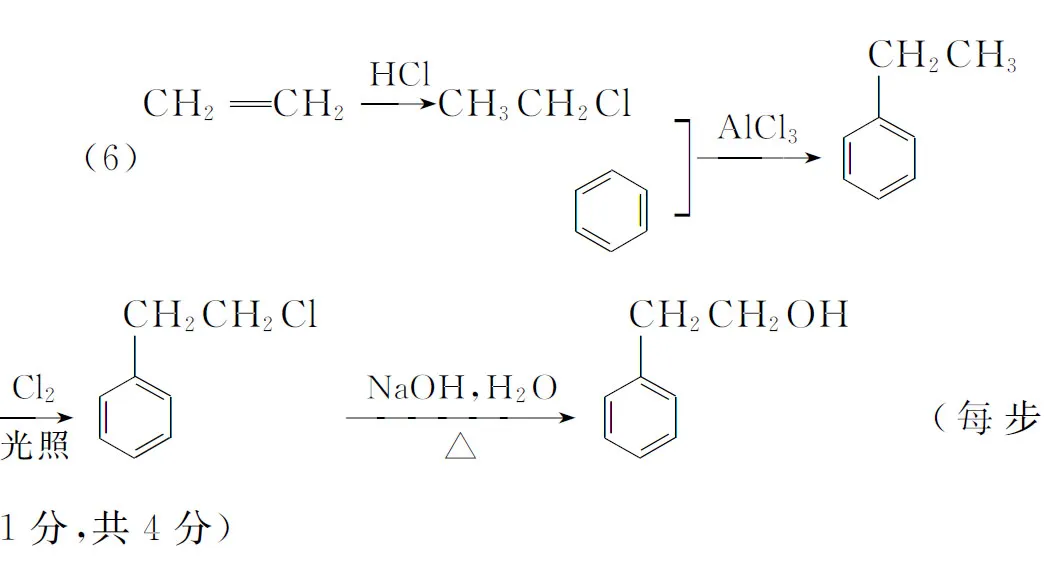
有机物A是聚合反应生产胶黏剂的单体,亦可作为合成调香剂I、聚酯材料G的原料,相关合成路线如下:
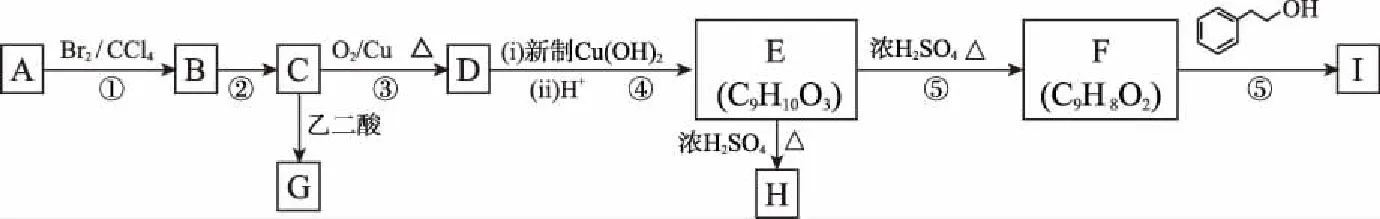
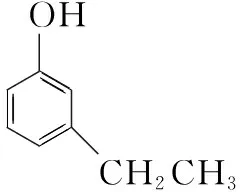
已知:烃A经质谱检测最大质荷比为118,其苯环上的一氯代物共三种,核磁共振氢谱显示峰面积比为1∶2∶2∶2∶3。
根据上述信息回答下列问题:
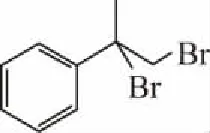
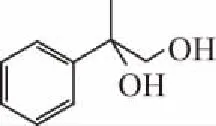
(1)A的结构简式为________,B→C的反应条件为________,E→F的反应类型为________。
(2)I中的官能团为________,若H分子中含有三个六元环状结构,则其分子式为________。
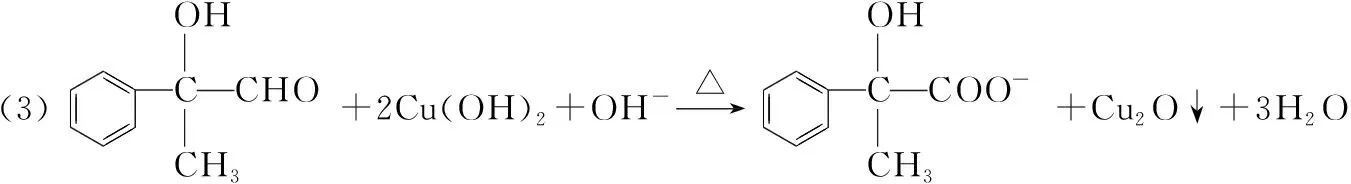
(3)D与新制氢氧化铜悬浊液反应的离子方程式为 ___________________。
(5)G是一种高分子化合物,则由C生成G的化学方程式为__________________。
参考答案和解析
7.C 【解析】青蒿素的提取利用的是萃取原理,是物理变化不是化学变化,该选项错误。故选C。
9.B 【解析】根据题意可知W、X、Y、Z对应的元素分别为C、Mg、S、Cl,元素W、Y的最简单氢化物分别为CH4、H2S,前者不溶于水,后者溶于水显酸性,A错误;元素X形成的单质Mg能与W的最高价氧化物CO2发生置换反应,B正确;元素X和Z能形成XZ2型的离子化合物,C错误;Z元素形成的单质Cl2常温下是气体,有毒,但不具有漂白性,D错误。故选B。


26.(共14分)

(2)675(mol/L)2(2分)
(3)升高温度至240℃ (1分)
(4)> (1分)
(5)1.82 (2分)
(6)n(H2O)/n(CH3OH)=1.05较为适宜,n(H2O)/n(CH3OH)越大,甲醇转化率越高,且在1.05前转化率增大速度较快 (2分)
(7)BE (1分)
(8)1∶5 (1分)


27.(共15分)
(1)-1 (1分) 4 (1分)



1.083 6×1020(或1.85NA) (1分) 0.099% (1分)
(4)第五周期第ⅤA族 (1分)


28.(共14分)
(1)增大接触面积,加快反应速率 (1分) 适当增加酸的浓度或适当提高反应温度 (1分)
(2)Ca2+、Al3+、Fe3+、H+(1分)
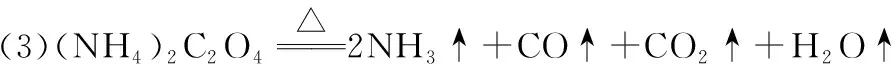
(4)降低草酸钙的溶解度,减少草酸钙的损失 (1分)
(5)C (1分) 若用盐酸酸化,KMnO4可以氧化氯离子,若用硝酸酸化,硝酸具有氧化性,可直接氧化草酸根 (2分)
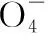
(7)反应中生成的Mn2+对该反应有催化作用,能明显加快反应的速率 (2分)
(8)63% (1分)
35.(共15分)
(1)4p (1分) 13 (1分)
(2)
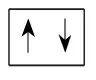
↑↓
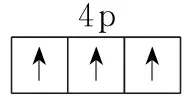
↑↑↑4p
4s(2分)
(3)Mg、Si、S (2分)
(4)N的电负性强于P,对成键电子对吸引能力更强,成键电子对离中心原子更近,成键电子对之间距离更小,排斥力更大,致使键角更大,因而PH3的键角小于NH3(2分)
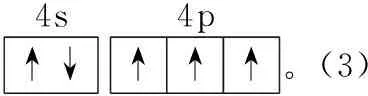
↑↓4s↑↑↑4p。(3)
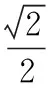
36.(共15分)
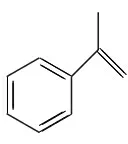
(2)酯基和碳碳双键 (1分) C18H16O4(1分)
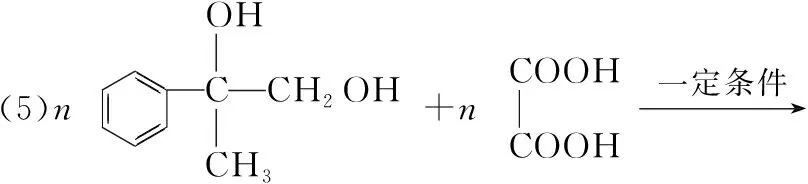

命题思路和素材来源
本套高考化学综合模拟原创试题的命题依据是 2017年版的普通高等学校招生全国统一考试大纲及其说明,其目标是为了有利于选拔具有学习潜能和创新精神的考生,以能力测试为主导,在测试考生进一步学习所必需的知识、技能和方法的基础上,全面检测考生的化学科学素养。本套原创试题的命制从以下五个维度对化学学科核心素养进行考查,分别是“宏观辨识与微观探析”“变化观念与平衡思想”“证据推理与模型认知”“科学探究与创新意识”和“科学精神与社会责任”;注重测量自主学习能力,重视理论联系实际,关注与化学有关的科学技术、社会经济和生态环境的协调发展,以促进学生在知识与技能、过程与方法、情感态度与价值观等方面的全面发展。本套原创试题,能覆盖近90%的高考考点,试题难度适中,简单题、中等题、较难题的比例接近7∶2∶1,适合高三二轮复习的模拟检测。
在选择题部分,第7题一改以往题目中考查化学与生活的方式,从中国古典文献及诗词中提取出与化学知识相关的内容作为考点,实现了《考试大纲》中提出的试题要结合中国传统知识文化的要求。第8、9、10题分别涉及阿伏加德罗常数、元素周期表和周期律、有机物分子的同分异构体等知识点,是对学生基本技能和解题能力的考查。第11题给出一个二次电池的模型,从“证据推理与模型认知”维度考查了学生的化学科学素养。第12题从“科学探究与创新意识”维度,以基本实验现象的描述和结论的分析为载体,考查用化学实验探究物质性质的相关内容。第13题通过一个图象考查学生对物质在溶液中的行为(电离、水解等)以及三大守恒原理(质量守恒、电荷守恒和质子守恒)的掌握程度,本题具有一定的难度,要求学生具有较好的抽象思维能力和图象分析能力。
在必做题部分,第26题以清洁高效的氢能源的开发为背景,着重从“变化观念与平衡思想”的维度,以化学反应与能量、化学反应速率和化学平衡为载体,实现对化学学科核心素养的考查,本题是一道中等偏难的题目,涉及较多的化学反应原理的内容,需要学生对所学知识综合运用,融会贯通,侧重考查学生分析和解决化学问题的能力。第27题以氮族元素为背景,素材取自大学《无机化学》教材,氮和磷是高中学生熟悉的元素,而砷、锑、铋则比较陌生,通过给予必要的有用信息,综合考查物质结构、元素周期表、氧化还原基本原理、元素性质等多方面的内容,是一道综合性很强的题目,侧重考查学生接受、吸收、整合化学信息的能力,体现了《考试大纲》对考试题目要来源于教材且高于教材的要求。第28题以水泥生料中钙含量的测定为背景,以流程题的形式考查与化学实验、成分分析等相关的综合知识,在高考试题“稳中求变、变中求新、新中求活”的指导思想下,本题根据2017年高考全国Ⅱ卷第26题进行大幅度改编,以求以一种全新的方式呈现给学生。

