例析多池相连电化学装置的解题方法
2018-06-12莫丽琼
莫丽琼,王 霞
(云南师范大学 云南 昆明 650500)
1 引言
电化学知识是近几年全国各省市高考题中的必考考点[1],它是基于氧化还原反应、化学反应中的能量变化等知识的深度学习,电化学分为原电池与电解池两大模块,但考题中通常不单独考察,而是多池相连综合考察,因而要求学生具有扎实的基础知识储备与强大的逻辑思维体系。因此本文举例分析常见的多池相连问题的题型特点和相应的解题方法谈谈自己的见解。
2 无外接电源型
2.1 建立认知角度
此类题型关键是确定原电池,判断方法主要有:找装置中最活泼金属,其在装置为原电池(即能自发进行氧化还原反应的电池),其余为电解池;在电极附近有可燃物通入的装置是原电池,其余为电解池。
2.2 建立角度关联
根据原电池的形成条件确定其正负极,较活泼金属或可燃物做负极,另一极为正极。与原电池负极相连的是电解池的阴极,与正极相连的是阳极,串联电池中阴阳电极交替出现。
2.3 建立思维模型
根据解题需要建立思维模型,正确书写电极反应方程式,判断电子转移方向,阴阳离子移动方向等,紧抓相同时间内电极通过电子的物质的量相等这一桥梁来解答电化学中的定量计算。
例:如图装置甲池的总电极反应式为2CH3OH+3O2+4KOH===2K2CO3+6H2O。下列叙述正确的是( )
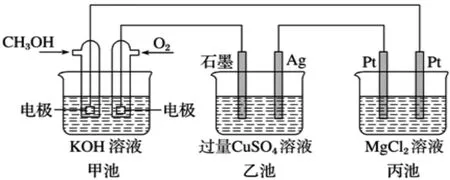
A.甲池是原电池,乙池是化学能转化为电能的装置
B.乙池中,Ag电极的电极反应式为Ag-e-=Ag+
C.反应一段时间后,若要使CuSO4溶液恢复到原浓度则向乙池中加入一定量Cu(OH)2固体
D.当甲池中消耗标准状况下280mL O2,理论上丙池中最多产生固体1.45g
解析:甲池中有CH3OH通入做原电池,乙池和丙池为电解池,能量是电能转化为化学能,A错。甲池中负极为通入CH3OH的一极,正极为通入O2的一极,乙池中Ag作阴极,电极反应为Cu2++2e-===Cu,B错。恢复原溶液的原则是电解了什么则加入什么,乙池中:2CuSO4+应加入CuO或CuCO3,C错。丙池中:当消耗标况下280mL O2,0.0125mol时,转移e-0.05 mol,生成Mg(OH)20.025mol,质量为1.45g。
3 有外接电源型
(1)建立认知角度:针对有电源的此类题型,全部为电解池、电镀池或精炼池等。(2)建立角度关联:若已知电源的正负极,则与电源负极相连的是电解池的阴极,与正极相连的是阳极,根据串联电池中电极交替出现原则顺推其他电极;若未知电源的正负极,则需要根据某极发生的现象逆推电极(隐含着电子流向、阴阳离子移动方向等解题依据)。(3)建立思维模型:与无外接电源型类似
例:如图装置电解一段时间,当某极析出0.32gCu时,Ⅰ、Ⅱ、Ⅲ中溶液pH分别为(溶液足量,体积均为100mL且电解前后溶液体积变化忽略不计)( )
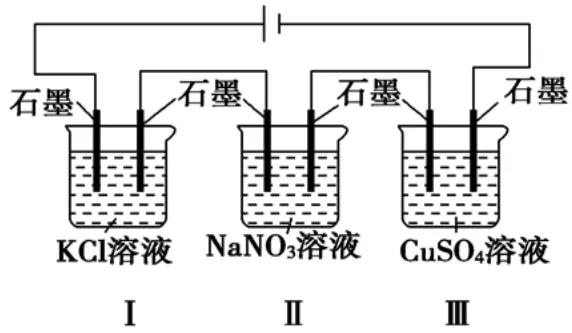
A.13、7、1 B.12、7、2
C.1、7、13 D.7、13、1
解析:Ⅰ、Ⅱ、Ⅲ均为电解池,Ⅰ中石墨(左)与电源正极相连为阳极,石墨(右)为阴极,Ⅱ、Ⅲ中依次交替。n(Cu)=0.005mol,由Ⅲ中阴极的电极反应为Cu2++2e-===Cu可知转移e-0.01mol,Ⅰ、Ⅱ、Ⅲ中电解方程式分别为当转移e-0.01mol时,则Ⅰ中生成OH-0.01mol,c(OH-)=0.1mol/L,pH=13;Ⅱ电解水,溶液仍然呈中性,溶液的pH=7;Ⅲ中生成0.01molH+,c(H+)=0.1mol/L,pH=1,故选A。
4 双控型
此类题型是前面两类的综合运用,通过电建的断开与闭合,从而改变认知角度。
例:有关下列装置的叙述中正确的是( )

A.断开K1,闭合K2后,甲、乙池能将化学能转化为电能
B.断开K1,闭合K2后,丙池中c(Cl-)减小
C.断开K2,闭合K1后,乙池右边C电极上的电极反应式为4OH--4e-===2H2O+O2↑
D.断开K2,闭合K1后,一段时间后甲、乙、丙三池中的阳极均被腐蚀了
解析:断开K1,闭合K2后,整个装置中为无外接电源型,由于锌银铜中锌为最活泼金属,故甲池是原电池,则乙、丙两池为电解池,乙池是将电能转化为化学能,A错。甲池中Zn做负极,丙池中与Zn相连的Cu(右)电极为阴极,Cu(左)电极为阳极,Cu-2e-=Cu2+,金属电极做阳极,参与电极反应,Cl-不放电,B错。断开K2,闭合K1后,三个池子均变成电解池,甲池中Zn与电源负极相连做阴极,则乙池中C(右)电极为阳极,4OH--4e-=2H2O+O2↑,C正确;石墨是惰性电极,本身不参与电极反应,D错。
解答电化学的相关题型,氧化还原反应是基础,原电池与电解池的工作原理是关键,经分析发现,无论电化学以哪种题型出现,基础知识都是考察的重点和核心,这就要求学生在强化基础知识的同时,不断减少迷思概念,形成一定的逻辑思维体系,构建解题模型,当遇到综合性较强的题型时就能迎刃而解了。
[1] 李辉,徐文华.电化学电极反应式书写“三步曲”[J].高中数理化.2015(5):56-58.
