大鼠皮下注射重组日本七鳃鳗毒素肽rLj-RGD3的血浆药代动力学研究
2018-05-16王玉平韩国柱武国宇王继红
王玉平,韩国柱,武国宇,于 萍,吕 莉*,王继红
(1.辽宁师范大学生命科学学院,辽宁 大连 116029;2.大连医科大学药理教研室,辽宁 大连 116044,大连医科大学附属第一医院药学部,辽宁 大连 116000)
rLj-RGD3是源于日本七鳃鳗口腔腺,通过基因工程技术获得的由118个氨基酸组成、分子量为1.35×105的含有3个RGD模体的重组日本七鳃鳗毒素肽[1]。研究发现,rLj-RGD3凭借其RGD模体与活化的血小板内皮细胞、肿瘤细胞及新生血管内皮细胞表面高表达的整合素(integrin)靶向结合,而具有抑制血小板聚集、肿瘤细胞转移及抗血管新生等典型的RGD毒素蛋白功能[2-6],但其药代动力学方面的研究少见报道。本研究采用双抗体夹心酶联免疫法(ELISA),研究皮下注射rLj-RGD3在大鼠体内的血浆药代动力学,为其新药研发提供实验依据。
1 材料和方法
1.1 实验材料
rLj-RGD3粉针剂,20 mg/瓶,HPLC测定纯度>97%,批号20160807,由辽宁师范大学提供;ELISA试剂盒,批号08032016,南京,金斯瑞生物科技公司产品。
MODEL550型酶标仪,美国BIORAD公司产品。3P97药代动力学计算软件,中国药理学会数学专业委员会研制。
SD大鼠,雄性,(200±20)g,由大连医科大学实验动物中心提供。实验动物质量合格证号SCXK(辽)2002-0002,实验动物使用许可证号SYXK(辽)2002-0005。喂标准饲料,自由饮水。
1.2 标准曲线的制备
取大鼠空白血浆,以样品稀释液稀释1000倍获得血浆样品稀释液。用此血浆样品稀释液稀释rLj-RGD3标准品(0.95 g/L),配制1 mg/L rLj-RGD3标准母液,再以血浆样品稀释液倍比稀释标准母液至rLj-RGD3终浓度为1600、800、400、200、100、50、0 μg/L的生物样品标准溶液,以制备生物样品标准曲线。
1.3 动物实验处理
取SD大鼠15只,按给药剂量随机分为3组(n=5),置于标准条件自由饮水进食适应3 d后,皮下注射rLj-RGD3,剂量为30、75、150 μg/kg,自由饮水。于给药前及给药后5、10、15、30、45、60、90、120、150、180、240及300 min自大鼠眼内眦静脉取血13次,每次0.2 mL,采用3.8%枸橼酸钠(体积比9∶1)抗凝,3000 r/min离心10 min获得血浆,-80 ℃保存备用。用时室温溶解并以样品稀释液10~1000倍适当稀释,采用ELISA法检测各血浆样品中rLj-RGD3血药浓度C(C=Cd×N,C为血药浓度,Cd为稀释后的药物浓度,N为稀释倍数),绘制平均血浆药物浓度-时间曲线,并采用3P97软件拟合房室模型及计算药代参数。
2 结 果
2.1 标准曲线
取标准溶液及血浆标准溶液同时进行ELISA法测定,重复5次,以OD值为纵坐标,浓度C为横坐标,进行线性回归,制备绝对标准曲线和血浆标准曲线,结果见图1A。绝对标准曲线及血浆标准曲线回归方程分别为y=0.001 4x+0.028 7,R=0.996 0及y=0.001 1x+0.032 8,R=0.999 0。
2.2 大鼠皮下注射不同剂量rLj-RGD3后血浆药-时曲线
按照1.3项下方法进行大鼠血浆药动学的研究,ELISA法测定的OD值,经随行标准曲线计算血药浓度,绘制平均血药浓度(C)-时间(T)曲线如图1B,将血药浓度用3P97软件计算出相应药代动力学参数见表1。
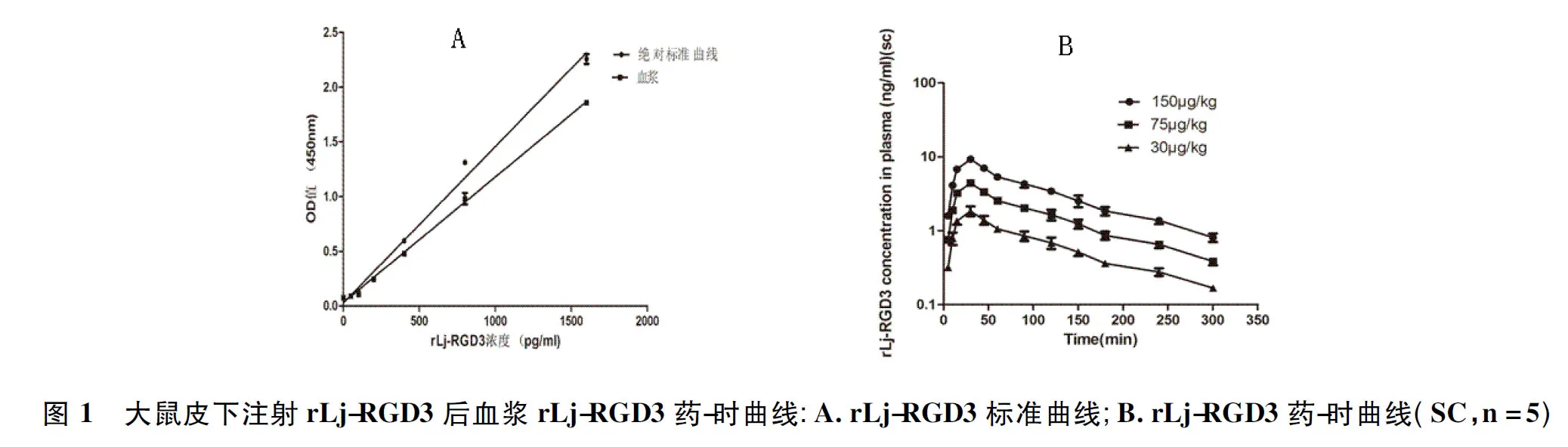
表 1 rLj-RGD3在大鼠血浆中的药动学参数
注:T1/2ka吸收半衰期,T1/2α分布半衰期,T1/2β消除半衰期,V/Fc表观分布浓度,AUC药时曲线下面积,CLs血浆总清除率,Tpeak最高血药峰时间,Cmax药峰浓度
3 讨 论
目前对蛋白多肽类药物药代动力学的研究常采用同位素标记法、免疫测定法及生物测定法等方法进行药物浓度的测定[7]。其中免疫测定法包括放射免疫测定法、免疫放射定量法、ELISA等。而ELISA法因具有检测快速、灵敏度高、特异性好、选择性强等优点,首选用于蛋白多肽类药物的检测。本研究即是采用了ELISA法研究rLj-RGD3的药代动力学。
本研究结果表明,皮下注射3种剂量rLj-RGD3后,吸收迅速,达峰时间26 min左右,不随剂量改变而发生显著变化。3P97程序拟合房室模型符合二室模型。在30、75、150 μg/kg下,Cmax分别为(1.45±0.21)、(3.68±0.25)、(7.86±0.47)μg/mL;T1/2β、CLs不随剂量的改变而发生显著改变;AUC与剂量成正比。提示,皮下注射rLj-RGD3在30~150 μg/kg剂量范围内,呈线性药代动力学。
研究结果可知,SC rLj-RGD3的T1/2ka为10 min左右,说明皮下给药吸收很快。但皮下注射后药物的半衰期时间却长达85 min左右(P>0.05),其可能的原因是皮下注射后药物进入血液需要一段时间,使得药物在体内分布达到平衡状态后血浆药物浓度降低一半所需要的时间,即半衰期较长。
综上,大鼠皮下注射rLj-RGD3吸收迅速,其血浆药代动力学参数显示为线性动力学。
参考文献:
[1] XIAO R,PANG Y,LI Q W.The buccal gland of Lampetra japonica is a source of diverse bioactive proteins[J].Biochimie,2012,94(5):1075-1079.
[2] WANG J H,HAN X X,YANG H,et al.A novel RGD-toxin protein,Lj-RGD3,from the buccal gland secretion of Lampetra japonica,impacts diverse biological activities[J].Biochimie,2010,92(10):1387-1396.
[3] 王继红,于凤,韩晓曦,等.日本七鳃鳗富含半胱氨酸RGD蛋白Lj-RGD1抑制血小板聚集及抗血管新生功能[J].中国生物化学与分子生物学报,2012,28(6):531-537.
[4] 王继红,张亚前,吕莉,等.日本七鳃鳗Arg-Gly-Asp毒素蛋白Lj-RGD3野生型与RGD全缺失突变体Lj-112的抗血管新生作用[J].生物工程学报,2011,27(10):1428-1437.
[5] 张丕桥,王继红,刘欣,等.重组七鳃鳗细胞毒素蛋白rLj-RGD3表达及对Hela细胞活性的影响[J].生物工程学报,2009,25(5):686-694.
[6] YEH C H,PENG H C,YANG R S,et al.Rhodostomin,a snake venom disintegrin,inhibits angiogenesis elicited by basic fibroblast growth factor and suppresses tumor growth by a selective αvβ3blockade of endothelial cells[J].Mol Pharmacol,2001,59(5):1333-1342.
[7] 韩国柱,何巍,任开环.蛋白多肽类药物的药动学特点及其影响因素[J].医药导报,2003,22(1):9-11.
