碳酰肼基和含有咪唑啉基团的1,3,4-噁二唑衍生物的合成及其对埃及伊蚊的构-效关系
2018-05-10付骋宇编译
付骋宇,张 波 编译
碳酰肼基和含有咪唑啉基团的1,3,4-噁二唑衍生物的合成及其对埃及伊蚊的构-效关系
付骋宇,张 波 编译
(陕西出入境检验检疫局,陕西西安 710068)
蚊媒病是持续危害人类健康的全球问题。疟疾仍是按蚊传播的危害性最大的寄生虫病,寨卡病毒是伊蚊传播的黄病毒,已经传播到南美、中美和加勒比地区。因为没有疫苗和其他特定处理措施用于防治寨卡病毒的传染,化学杀虫剂仍是控制蚊子减少病毒传播的主要方法。然而,目前大部分农药抗性的出现导致对新杀虫剂的持续需求。目前大多数杀成虫药抑制乙酰胆碱酯酶的活性或阻断电压敏感的钠通道的失活。
咪唑啉环类杂环化合物具有广谱生物活性。吡虫啉是开发的第一个新烟碱类杀虫剂,其结构中含有吡啶和咪唑啉环。新烟碱类杀虫剂作用于昆虫中枢神经系统突触后膜上的烟碱型乙酰胆碱受体。
设想化合物的结构由3部分组成:芳香环(A)、噁二唑环(B)和咪唑啉酮环(C)(图1)。此外,可用含有酰肼基团的羰基来代替噁二唑环。1,3,4-噁二唑环是药物化学中有用的杂环,取代的1,3,4-噁二唑环化合物有不同生物活性,比如:抗菌、除草、杀虫、抗病毒、抗肿瘤和消炎活性。除了广谱的生物活性外,1,3,4-噁二唑环是酰胺和酯官能团的生物电子等排体,研究表明这些环容易与不同受体以氢键相互作用。
在笔者之前的研究中,合成了一系列3-乙酰基-2,5-二取代-2,3-二氢-1,3,4-噁二唑。在试验的17个化合物中,只有3-乙酰基-5-(4-氟苯基)-2-苯基-2,3-二氢-1,3,4-噁二唑和3-乙酰基-5-(4-氟苯基)-2-(4-溴苯基)-2,3-二氢-1,3,4-噁二唑对埃及伊蚊幼虫有杀灭活性,对1龄幼虫的LC50分别为24.1、30.9 mg/L。近期爆发的寨卡病毒感染加快了新颖蚊子控制剂的研究,在综合媒介管理策略中对蚊子幼虫和成虫的控制工具都很重要。笔者持续研究的目标是发现新颖杀虫剂,本文中合成了17种含有噁二唑和咪唑啉环的新颖化合物,并评估了它们对埃及伊蚊的杀幼虫和杀成虫活性。

注:(A)芳香环,(B)噁二唑环和(C)咪唑啉环。
1 材料和方法
1.1 化学
羰基氰基-对-三氟甲氧基苯腙(FCCP)购自Abcam公司(美国马赛诸塞州剑桥市),其他所有化学试剂和溶液均购自Sigma-Aldrich公司(美国密苏里州,圣路易斯市)和Merck公司(德国达姆施塔特)。用薄层色谱(TLC)检测化合物的均匀性和纯度,商品化硅胶板(德国默克Merck薄层板TLC Silica gel 60G F254 25 Glass plates 20 x 20 cm),展开剂为甲醇:氯仿(60:40)。薄层板同时采用紫外光(波长254nm)和碘显色。用反向高效液相色谱(HPLC,Chromasil C183.6×150 mm柱,英国Hichrom公司)检测合成化合物的纯度,流动相为乙腈︰水(50︰50,体积比)。用Schmelzpunktbestimmer SMP II熔点测定仪测定熔点(德国吕伯林根,Gottfried-Keller-Weg)。红外光谱仪为FTIR-8400S(日本东京,岛津)。核磁共振氢谱(1H-NMR)以四甲基硅烷(TMS)作为内标,氘代二甲亚砜(DMSO-d6)为溶剂,Advance 400NMR型核磁共振仪(美国加州费里蒙特Bruker Biospin公司)。化学位移以相对于TMS的值表示,使用以下缩写来描述峰的形式:s,单峰;d,双峰;t,三重峰;m,多重峰。元素分析仪[碳(C),氢原子(H),氮原子(N)]型号为CNHS-Thermo Scientific Flash 2000(美国马萨诸塞州沃尔瑟姆,赛默飞世尔科技公司)。
1.2 酰肼衍生物合成步骤
3-(甲基磺酰基)-2-氧代咪唑啉-1-碳酰肼(1),CAS号:64341-28-2。
3-(甲基磺酰基)-2-氧代咪唑啉-1-碳酰氯(1.74 mmol)在磁力搅拌下溶于甲醇,加入水合肼(1 mL),室温下搅拌8 h。过滤混合物,并以甲醇洗涤。
化合物1:白色固体,收率60%,熔点(mp) 222~ 223 ℃。红外最大吸收波(cm-1):3566,3358,3020, 2997,2918,1685,1508,1477,1288。1H-NMR (300 MHz, DMSO-d6): 3.37(s,3H,SO2CH3),3.72-3.85(m,4H,-CH2-),4.85(s,2H,-NH2), 9.36(s,1H,-NH)。对于C5H10N4O4S (分子量222.22 g/mol),计算值:C:27.02 H:4.54 N:25.21,实测值:C:27.02 H:4.54 N:25.21。
1.3 碳酰肼衍生物的合成步骤(2a-h)
室温下在酰肼(1 mmol)(1)和三甲胺(2 mmol)的干二氯甲烷溶液(5 mL)中滴加预制好的苯甲酰氯(1 mmol),磁力搅拌混合反应体系3 h。以蒸馏水洗涤沉淀物,过滤。用TLC检测化合物纯度。
′-(4-氟苯甲酰)-3-(甲磺酰)-2-氧代咪唑啉-1-碳酰肼(2a):白色固体,收率70%,熔点(mp) 271~ 273 ℃。红外最大吸收波(cm-1):3371, 3321, 3010, 2928, 1695, 1473, 1280, 812。1H-NMR (300 MHz, DMSO-d6): 3.37(s,3H,-SO2CH3),3.77-4.01(m,4H,-CH2-),7.42-8.40(m,4H,Ar-H),9.01和10.47(s,2H,-NH2)。对于C12H13FN4O5S (分子量344.32 g/mol),计算值:C:41.86 H:3.81 N:16.27,实测值:C:41.66 H:3.79 N:16.20。
′-(4-氯苯甲酰)-3-(甲磺酰)-2-氧代咪唑啉-1-碳酰肼(2b):白色固体,收率70%,熔点(mp) 248~ 250 ℃。红外最大吸收波(cm-1):3367, 3282, 3026, 2993, 2933, 1689, 1479, 1280, 848。1H-NMR (300 MHz, DMSO-d6): 3.37(s,3H,-SO2CH3),3.75-3.92 (m,4H,-CH2-),7.58-7.90(m,4H,Ar-H),9.36和10.67(s,2H,-NH-)。对于C12H13ClN4O5S (分子量360.77 g/mol),计算值:C:39.95 H:3.63 N:15.53,实测值:C:40.01 H:3.60 N:15.55。
3-(甲磺酰)-′-(4-硝基苯甲酰)-2-氧代咪唑啉-1-碳酰肼(2c):浅黄色,收率60%,熔点(mp) 286~ 288 ℃。红外最大吸收波(cm-1):3302, 3020, 2993, 2937, 1687, 1479, 1251, 800。1H-NMR (300 MHz, DMSO-d6): 3.37(s,3H,-SO2CH3),3.73-3.92(m,4H,-CH2-),7.20-7.33(d,4H,Ar-H),9.02和9.24(s,2H,NH)。对于C12H13N5O7S (分子量371.33 g/mol),计算值:C:38.81 H:3.53 N:18.86,实测值:C:38.84 H:3.54 N:18.80。
′-(4-甲基苯甲酰)-3-(甲磺酰)-2-氧代咪唑啉-1-碳酰肼(2d):白色固体,收率65%,熔点(mp) 245~ 246 ℃。红外最大吸收波(cm-1):3373, 3300, 3032, 2982, 2924, 1695, 1473, 1253, 802。1H-NMR (300 MHz, DMSO-d6): 2.49-2.51(s,3H,-CH3),3.39(s,3H,-SO2CH3),3.74-3.89(m,4H,-CH2-),7.28-7.84(m,4H,Ar-H),9.41(s,2H,-NH-)。对于C13H16N4O5S (分子量340.35 g/mol),计算值:C:45.88 H:4.74 N:16.46,实测值:C:46.01 H:4.72 N:16.50。
′-苯甲酰-3-(甲磺酰)-2-氧代咪唑啉-1-碳酰肼(2e):白色固体,收率70%,熔点(mp) 240~242 ℃。红外最大吸收波(cm-1):3371, 3327, 3024, 2989, 2935, 1693, 1473, 1251, 802。1H-NMR (300 MHz, DMSO-d6): 3.39(s,3H,-SO2CH3),3.74-3.90(m,4H,-CH2-),7.51-7.89(m,5H,Ar-H),9.36和9.44(s,2H,-NH-)。对于C12H14N4O5S(分子量326.33 g/mol),计算值:C:44.17 H:4.32 N:17.17,实测值:C:44.15 H:4.30 N:17.20。
′-(4-甲氧基苯甲酰)-3-(甲磺酰)-2-氧代咪唑啉-1-碳酰肼(2f):浅黄色,收率60%,熔点(mp) 261~ 263 ℃。红外最大吸收波(cm-1):3281, 3227, 3009, 2922, 2841, 1703, 1489, 1249, 898。1H-NMR (300 MHz, DMSO-d6): 3.39(s,3H,-SO2CH3),3.74-3.90 (m,4H,-CH2-),4.33(s,3H,OCH2),7.00-7.90(m,4H,Ar-H),9.37(s,2H,NH)。对于C13H16N4O6S (分子量356.35 g/mol],计算值:C:43.82 H:4.53 N:15.72,实测值:C:43.91 H:4.50 N:15.80。
′-(4-溴苯甲酰)-3-(甲磺酰)-2-氧代咪唑啉-1-碳酰肼(2g):白色固体,收率65%,熔点(mp) 290~ 291 ℃。红外最大吸收波(cm-1):3371, 3026, 2991,2929, 1697, 1473, 1251, 898。1H-NMR (300 MHz, DMSO-d6): 3.39(s,3H,-SO2CH3),3.77-3.92(m,4H,-CH2-),7.72-7.83(m,4H,Ar-H),9.36和9.47(s,2H,-NH-)。对于C12H13BrN4O5S (分子量405.22 g/mol),计算值:C:35.57 H:3.23 N:13.83,实测值:C:35.52 H:3.26 N:13.81。
′-(2,4-二氯苯甲酰)-3-(甲磺酰)-2-氧代咪唑啉-1-碳酰肼(2h):白色固体,收率55%,熔点(mp) 287~ 288 ℃。红外最大吸收波(cm-1):3367, 3302, 3020, 2993, 2929, 1687, 1479, 1251, 891。1H-NMR (300 MHz, DMSO-d6): 3.39(s,3H,-SO2CH3),3.77-3.89 (m,4H,-CH2-),7.46-7.56(m,3H,Ar-H),9.36和9.57(s,2H,-NH-)。对于C12H12Cl2N4O6S (分子量395.22 g/mol),计算值:C:36.47 H:3.06 N:14.18,实测值:C:36.47 H:3.01 N:14.20。
1.4 噁二唑衍生物合成步骤(3a-h)
在反应瓶中加入碳酰肼(1 g)和15 mL三氯氧磷,回流6 h。待反应物冷却至室温,将其倒入冰水混合物中,过滤沉淀物,洗涤,干燥。
1-[5-(4-氟苯基)-1,3,4-噁二唑-2-基]-3-(甲磺酰基)咪唑啉-2-酮(3a):白色固体,收率50%,熔点(mp) 251~253 ℃。红外最大吸收波(cm-1):3375, 3080, 1683, 1593, 1475, 1234, 1097, 846。1H-NMR (300 MHz, DMSO-d6): 3.39(s,3H,-SO2CH3),3.75-4.11 (m,4H,-CH2-),7.44-8.02(m,4H,Ar-H)。对于C12H11FN4O4S (分子量326.30 g/mol),计算值:C:44.17 H:3.40 N:17.17,实测值:C:44.24 H:3.43 N:17.10。
1-[5-(4-氯苯基)-1,3,4-噁二唑-2-基]-3-(甲磺酰基)咪唑啉-2-酮(3b):白色固体,收率50%,熔点(mp) 276~278 ℃。红外最大吸收波(cm-1):3010, 2929, 1683, 1550, 1475, 1253, 809。1H-NMR (300 MHz, DMSO-d6): 3.39(s,3H,-SO2CH3),3.74-4.08(m,4H,-CH2-),7.68-7.69(m,4H,Ar-H)。对于C12H11ClN4O5S(分子量342.76 g/mol),计算值:C:42.05 H:3.23 N:16.35,实测值:C:42.10 H:3.26 N:16.40。
1-(甲磺酰基)-3-[5-(4-硝基苯基)-1,3,4-噁二唑-2-基]咪唑啉-2-酮(3c):淡黄色,收率40%,熔点(mp) 261~263 ℃。红外最大吸收波(cm-1):3024, 2931, 1685, 1555, 1471, 1230, 856。1H-NMR (300 MHz, DMSO-d6): 3.39(s,3H,-SO2CH3),3.75-4.12(m,4H,-CH2-),8.16-8.47(m,4H,Ar-H)。对于C12H11N5O6S(分子量353.31 g/mol),计算值:C:40.79 H:3.14 N:19.82,实测值:C:40.74 H:3.10 N:19.90。
1-[5-(4-甲基苯基)-1,3,4-噁二唑-2-基]-3-(甲磺酰基)咪唑啉-2-酮(3d):白色固体,收率40%,熔点(mp) 241~242 ℃。红外最大吸收波(cm-1):3026, 2929, 1683, 1550, 1477, 1251, 800。1H-NMR (300 MHz, DMSO-d6): 2.50(s,3H,-CH3),3.39(s,3H,-SO2CH3),3.74-4.07(m,4H,-CH2-),7.40-7.84(m,4H,Ar-H)。对于C13H14N4O4S (分子量322.34 g/mol),计算值:C:48.44 H:4.38 N:17.38,实测值:C:48.48 H:4.34 N:17.40。
1-(甲磺酰基)-3-(5-苯基-1,3,4-噁二唑-2-基)-咪唑啉-2-酮(3e):白色固体,收率50%,熔点(mp) 249~250 ℃。红外最大吸收波(cm-1):3024, 2929, 1683, 1548, 1469, 1249, 891。1H-NMR (300 MHz, DMSO-d6): 3.39(s,3H,-SO2CH3),3.76-3.90(m,4H,-CH2-),7.50-8.24(m,5H,Ar-H)。对于C12H12N4O4S (分子量308.31 g/mol),计算值:C:46.75 H:3.92 N:18.17,实测值:C:46.80 H:3.90 N:18.15。
1-[5-(4-甲氧基苯基)-1,3,4-噁二唑-2-基]-3-(甲磺酰基)咪唑啉-2-酮(3f):淡黄色,收率40%,熔点(mp) 265~266 ℃。红外最大吸收波(cm-1):3026, 2929, 1683, 1548, 1469, 1288, 831。1H-NMR (300 MHz, DMSO-d6): 3.36(s,3H,-SO2CH3),3.60(s,H, OCH3),3.74-3.90(m,4H,-CH2-),7.10-7.90(m,4H,Ar-H)。对于C13H14N4O5S (分子量338.34 g/mol),计算值:C:46.15 H:4.17 N:16.56,实测值:C:46.12 H:4.18 N:16.51。
1-[5-(4-溴苯基)-1,3,4-噁二唑2-基]-3-(甲磺酰基)咪唑啉-2-酮(3g):白色固体,收率45%,熔点(mp) 292~293 ℃。红外最大吸收波(cm-1):3020, 2928, 1683, 1550, 1473, 1280, 895。1H-NMR (300 MHz, DMSO-d6): 3.36(s,3H,-SO2CH3),3.73-4.07(m,4H,-CH2-),7.70-8.07(m,4H,Ar-H)。对于C12H11BrN4O4S (分子量387.21 g/mol),计算值:C:37.22 H:2.86 N:14.47,实测值:C:37.20 H:2.82 N:14.50。
1-[5-(2,4-二氯苯基)-1,3,4-噁二唑2-基]-3-(甲磺酰基)咪唑啉-2-酮(3h):白色固体,收率40%,熔点(mp) 277~279 ℃。红外最大吸收波(cm-1):3026, 2933, 1683, 1585, 1467, 1259, 854。1H-NMR (300 MHz, DMSO-d6): 3.37(s,3H,-SO2CH3),3.75-4.13(m,4H,-CH2-),7.57-7.80(m,3H,Ar-H)。对于C12H10Cl2N4O4S(分子量377.20 g/mol),计算值:C:38.21 H:2.67 N:14.85,实测值:C:38.20 H:2.64 N:14.90。
1.5 供试蚊子和生物测定
用于点滴法生物测定的蚊子为奥兰多品系(ORL)埃及伊蚊羽化3~7 d的雌性成虫。ORL是自1952年以来未进行过田间补充的实验室培养敏感品系。氯菊酯对该品系的半数致死量(LD50)为0.1~0.2 ng。先前已对标准饲养流程进行了描述,并用此方法培育大小为(2.3±0.3) mg的雌性成虫。
幼虫的生物测定方法以前已有描述,以1龄幼虫为试虫,在96孔微量滴定板进行,每孔容量为200 μL。向每只幼虫提供10 μL 2%食物溶液(苜蓿粉︰猪饲料1︰1)的上清液。分别吸取每种化合物储备液2、1、0.5、0.2 μL,以DMSO稀释至100 μg/μL,加入微孔中,充分接触幼虫虫体。设氯菊酯为阳性对照,DMSO为阴性对照。在不同的日期至少重复试验3次。
按照已描述的方法进行成虫点滴生物测定。取0.5 μL 10 μg/μL丙酮溶液处理低温麻醉的蚊子。将试虫置于25 ℃使其苏醒,并饲喂10%蔗糖溶液。处理24 h后检查,完全不动或濒临死亡状态(以无法飞行和站为特征)都视为死亡,计算死亡率。在不同日期重复3次试验,设氯菊酯和丙酮溶剂为对照。
对达到80%以上致死率的化合物进行进一步试验,研究其LD50和95%置信限(Cls)。在3个不同日期,分别用一系列剂量处理ORL雌性埃及伊蚊。对各个不同日期每个剂量的24 h昆虫死亡率合并、分析,用SigmaPlot v13绘制剂量-死亡率数据图形,进行非线性回归四参数逻辑模型分析,确定LD50值和95%置信限。
1.6 电生理学
为了评估活性化合物对昆虫神经系统功能的影响,以佛罗里达大学的黑腹果蝇()野生俄勒冈R品系3龄幼虫为试虫。按已有的方法试验、记录幼虫中枢神经系统电生理活动。在pH为7.2的生理盐水(含氯化钠0.157 M,氯化钾0.003 M,氯化钙0.002 M,HEPES 0.004 M)中剥离获得中枢神经系统,并去除血脑屏障,使化学物质容易渗透进入中枢神经系统。用玻璃吸管吸附电极监测外周神经干的递降放电活动。用PowerLab将电信号处理和转换为放电频率。然后将试验化合物加到盐水浴(1 mL水浴中加入1 μL DMSO溶液)中,用吸管慢慢搅匀。以3 min平均放电率,以及以其与时间作图来评估30 min内药物的作用。
1.7 细胞呼吸试验
用海马细胞能量代谢实时测定仪/生物能量代谢测定仪(安捷伦公司,美国加利佛尼亚州圣克拉拉市)来评估N2A细胞的线粒体呼吸和糖酵解活动。试验采用已报道的方法,并做了小的改动。简言之,在未涂层的XFe96仪器孔板中加入达尔伯克改良伊格尔培养基,在培养基中添加5%胎牛血清和抗生素,约24 h后把细胞接种到培养基中。试验时,用DMSO或待测化合物(30 μM)处理细胞3 h,然后进行代谢流量分析。通过测定N2A细胞耗氧率(OCR) (测定线粒体呼吸的方法)或细胞外酸化率(ECAR) (测定糖酵解作用的方法)来评定细胞的代谢流量。
在测定OCR和ECAR的前1 d,将传感器盒在XF校准物(安捷伦公司)中进行水合,37 ℃下在XF Prepstation(安捷伦公司)中保存过夜。第2 d,测定OCR前,将细胞清洗3次,在无二氧化碳的恒温箱中,37 ℃条件下,在培养基(bicarbonate-freelow-buffered assay medium)中培养1 h,然后向细胞中加入寡霉素1.0 μm,FCCP 0.6 μm和鱼藤酮/抗霉素A(1︰1,1.3 μm)(列出的最终浓度)。测定ECAR时,测定前,在含二氧化碳的恒定培养中,37 ℃条件下,用呼吸缓冲液冲洗细胞3次共1 h。使用Wave2.3软件(安捷伦公司)收集和分析所有数据。
1.8 化学信息学
用MarvinSketch软件(版本号 17.21.0;计算模块由ChemAxon研发,http://www.chemaxon.com/ products/marvin/marvinsketch/, 2017)进行农药化学信息学分析。
2 结果与讨论
2.1 合成
目标化合物的合成路线见图2。化合物(1,2a-h,3a-h)结构由红外光谱、氢核磁共振谱和元素分析确定。化合物(1, 2a-h)红外光谱显示有N-H键伸缩振动(3221-3566)。所有化合物(1, 2a-h,3a-h)的红外光谱都显示含有C-H键伸缩振动(3009~3080)、C=O键伸缩振动(1683~1697)、芳香环C=C键伸缩振动(1467~1593)和S=O键伸缩振动(1230~1288)。酰肼基团的NH质子在4.85、9.36 ppm有2个单峰共振。碳酰肼基团的NH质子在9.36~9.57 ppm有一单峰。芳香环的质子在7.28~8.84 ppm有一多重峰。化合物的元素分析结果与预测的结构一致。
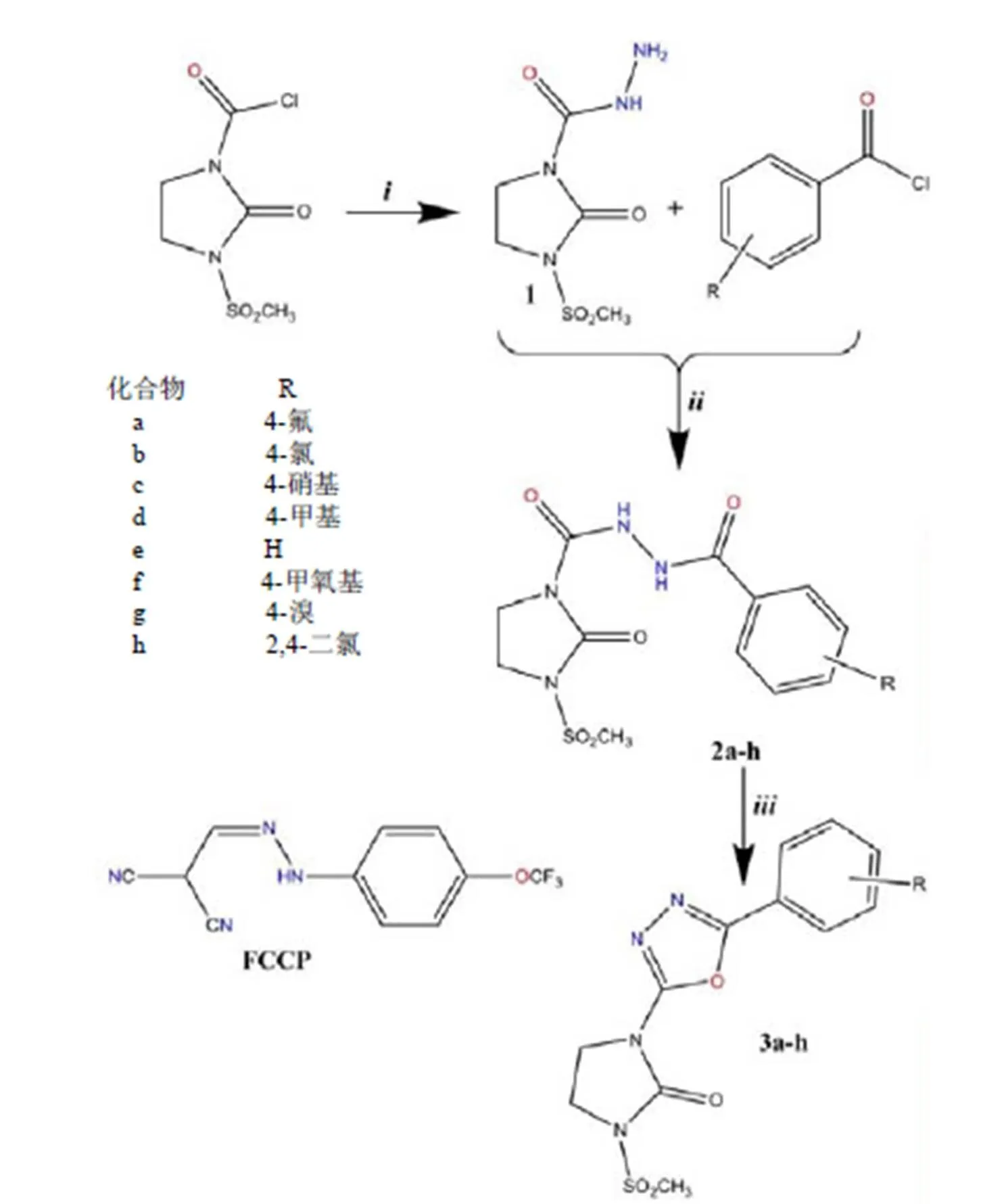
注:i:水合肼;ii:三甲胺、CH2Cl2;iii:POCl3
2.2 杀蚊活性
化合物对埃及伊蚊幼虫的初步活性筛选研究表明所有化合物在1、0.5、0.25、0.1 μg/μL浓度对1龄幼虫均无致死作用。溶剂对照对幼虫的致死率为零,而阳性对照氯菊酯在0.04 ng/μL浓度对幼虫的致死率为100%。表1列出了对埃及伊蚊ORL品系成虫的点滴试验结果,表明随化合物结构不同,其毒性有较大变化。例如:化合物2a为氟代物,3d含有甲基,3f的芳香环上有一甲氧基取代,它们的活性最弱,对幼虫的致死率约50%或更低。相比之下,其他所有化合物在剂量为5 μg/蚊时致死率高于60%。化合物2b活性最高,在3个重复中几乎致所有蚊子死亡,其次是3c、3g和3h,再其次是2g、3b、2c、2d、3e、2e、3a和2f。
对所有剂量为5 μg/蚊时致死率≥80%的化合物进行了进一步活性试验,测定了LD50。表1列出了它们的LD50、95%置信限和拟合参数。所有测试的化合物的LD50为2.3~5.0 μg/蚊,其中3h和2c活性最高。虽然没有发现log(log)与活性间有显著相关性,但化合物3h有1个氯取代基,2c有1个硝基,这2基团为化合物提供了亲脂性,其表皮/细胞的渗透性增加。芳环上有1个硝基的化合物2c和苯环2,4-位为卤原子的3h是最有发展前景的化合物。
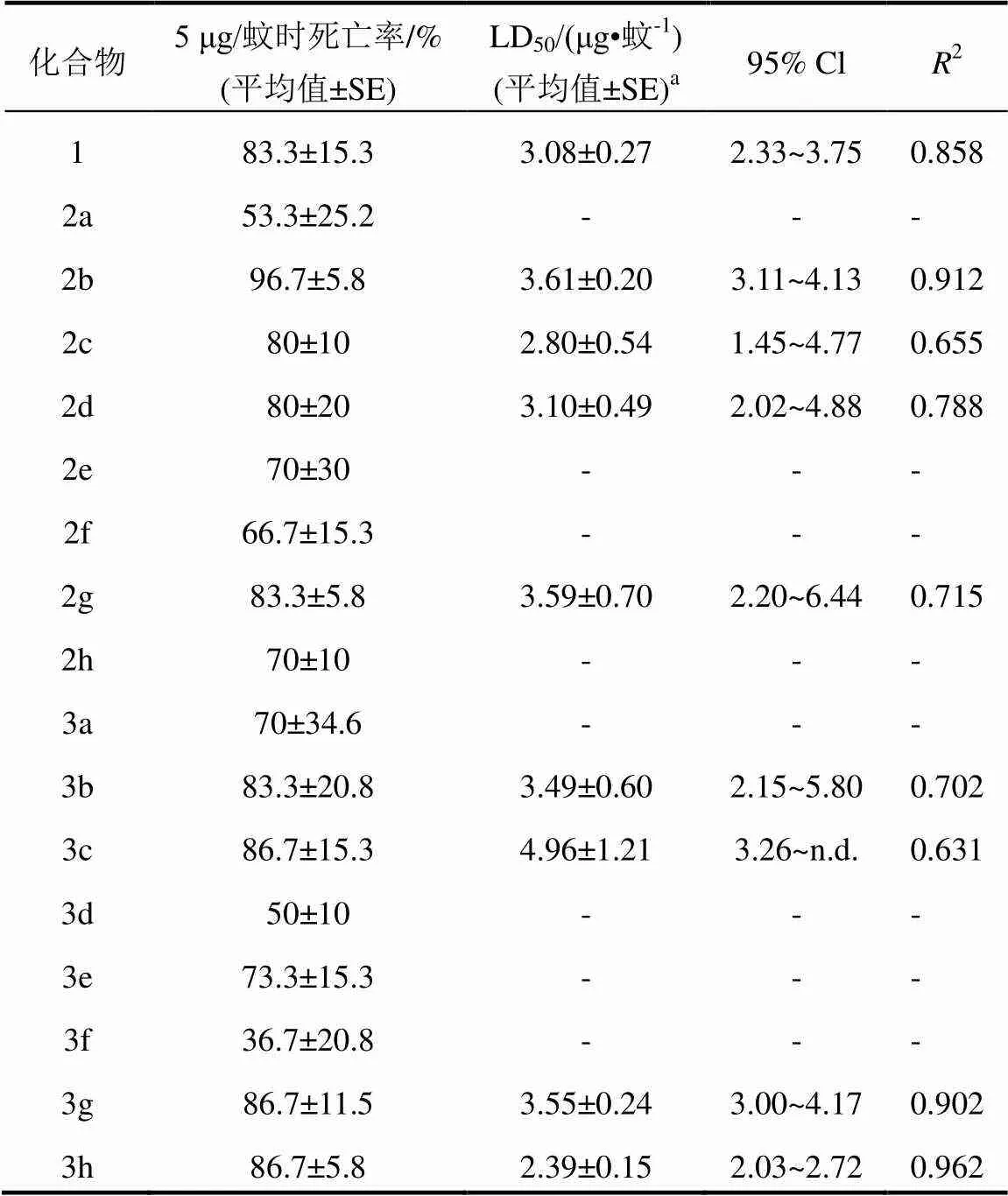
表1 对ORL品系埃及伊蚊成虫的24 h致死率(n=3)
注:a:在进行初筛后,对致死率≥80%的化合物进行进一步对成虫点滴试验测定其LD50。
-酰基化酰肼和1,3,4-噁二唑环具有相似的活性。-酰基化酰肼(2b、2c、2d、2g)和其对应噁二唑衍生物(3b、3c、3g、3h)有活性。在合成过程中在氢供体和受体基团被保护下,进行环合使化合物产生活性或增加活性。
2.3 作用机制研究
大多数重要农药与线粒体发生交叉反应。考虑到此交叉反应对化合物的选择性和可能的靶标方法的重要性,评估了系列2和3化合物对线粒体的活性,以线粒体解偶联剂FCCP作为基准物。化合物2a显示出低毒性,2c具有高毒性(表1)。这些化合物与FCCP有一些微小的结构相似性(图2和表2),它们都具有相邻的氮原子,离苯环最近的氮原子的计算值分别为6.7和6.4,与FCCP(图2)的6.4相似。由图6可知,化合物的组别与其极性表面积(PSA)相关,即极性原子表面和。除3c与同组其他化合物相比具有更高的PSA外,这2组化合物表现出明显区别。类似地,以pH 7.4时的log看,化合物自然分组,在pH 7.4时,log=log+。这2种特性都与化合物到达昆虫靶点或非靶向哺乳动物细胞的能力相关。还评估了闭环类似物3d和3h,这2个化合物具有相似的低毒性和高毒性,但均没有与氮结合的酸性质子。电生理试验表明,FCCP在10~30 nM浓度会导致苍蝇中枢神经系统幅度小的可变的神经放电,并伴随着神经放电频率降低(A),与ATP产生中断相一致。从浓度-效应数据的非线性拟合曲线得到IC50(纳摩尔)(图4B)。化合物3d和3h处理后昆虫神经放电增加,然后恢复到对照水平,化合物2a和2c则几乎没有影响。因此,对黑腹果蝇3龄幼虫神经放电的影响与对蚊子的毒性无关。
测试了化合物对哺乳动物细胞中线粒体呼吸的影响。由图5可以看出,4个化合物中的3个(2a,2c和3d)对一些线粒体呼吸参数有影响,1个化合物(3h)没有活性。活性化合物增加了基础呼吸、由FCCP刺激的最大呼吸、与ATP产生相关的呼吸和备用呼吸能力。质子漏和急性毒性没有显着变化。这些结果表明细胞应激能力的增加反映在线粒体生理学上。尽管化合物3h是对蚊子毒性最强的化合物之一,但它对细胞的线粒体活性没有任何影响。因此,在本试验中虽然观察到对线粒体的影响,但没有得到明确的结构-毒性关系。
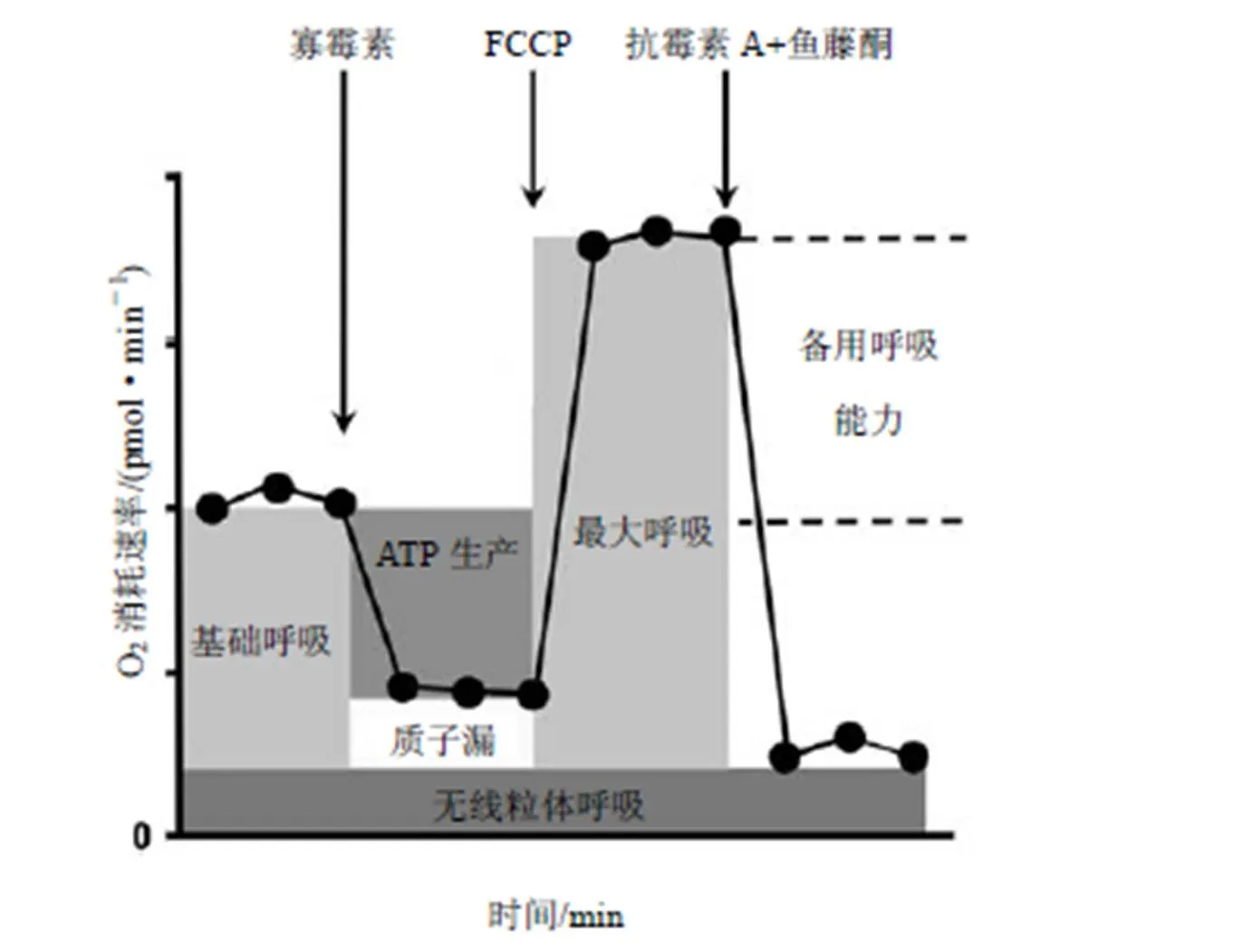
注:基础呼吸为处理前的细胞耗氧量。应用寡霉素阻断复合物IV ATP合酶,以表示细胞ATP生产的呼吸。利用FCCP解偶联作用估算最大呼吸速率,从而估算出基础率以上的备用呼吸能力。最后使用抗霉素A+鱼藤酮分别阻断复合物I和III,以及除线粒体过程外的所有呼吸。然后计算质子漏(基础呼吸与ATP生成无关)和急性毒性(对处理没有反应)(图4)。
图3 对线粒体功能参数毒理作用试验分析过程

表2 合成化合物的物理化学性质
注:PSA表示极性表面积。

注:B中拟合曲线被限定为底端0,顶端30。

注:用化合物(30 μM)处理N2A小鼠细胞3 h,然后测定线粒体的功能。每一柱形代表平均值±标准偏差,n=6~8,P<0.05表示具有统计显著性。
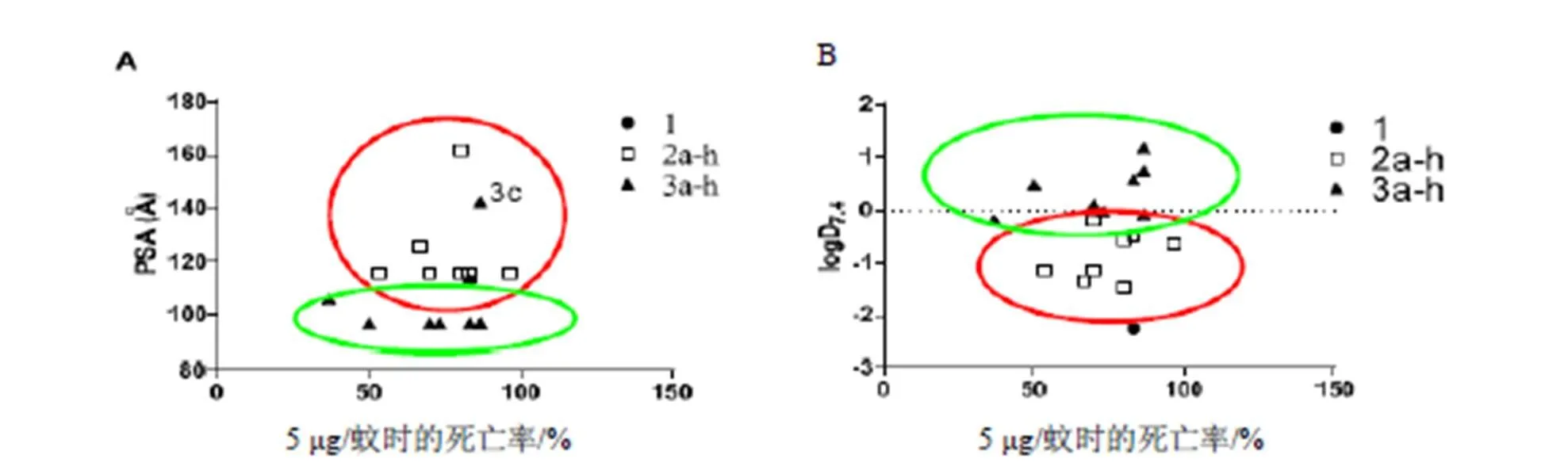
注:由图可以看出化合物的化学结构特性有2个主要交集。两者都与化合物到达昆虫靶点的能力有关。
3 结 论
本研究合成了一系列含有咪唑啉部分的1,3,4-噁二唑基团的噁二唑衍生物,并通过核磁共振、红外光谱和元素分析确定了它们的结构。这17个化合物的构-效关系表明在苯基取代试验中,对化合物2b、2c、2d、2g、3b、3c、3g和3h进行氯基、硝基、甲基和溴基取代可有效增加杀成虫活性,进一步结构变化可开发新的有效杀虫剂。合成化合物系列有限,进行的作用机制研究无法确定对蚊子的致死作用是通过神经毒性还是作用于线粒体呼吸所致。
付骋宇(1978—),女,高级工程师。研究方向:食品安全与真伪鉴别。E-mail: fu_chengyu@sina.com。
2018-03-12。
10.16201/j.cnki.cn31-1827/tq.2018.02.04
TQ450
A
1009-6485(2018)02-0023-07
