Orbitrap高分辨质谱法高通量筛查生化药品、中成药与保健品中非法添加的13种消化类化学药物
2018-04-18郭常川张迅杰贺美莲
郭常川,孙 华,石 峰*,邢 晟,张迅杰,李 可,贺美莲,姜 玮,3*
(1.山东省食品药品检验研究院,山东 济南 250101;2.山东大学 药学院,山东 济南 250012;3.山东大学 化学与化工学院,山东 济南 250100)
消化不良是一种临床症候群,主要由胃动力障碍所引起,包括胃蠕动差的胃轻瘫和食道反流病,是一种发病人群很广的常见疾病。近年来,市面上出现很多针对消化不良症状的声称“纯天然”、“无化学添加”的生化药品、中成药或保健品。然而,此类产品质量良莠不齐,一些不法分子为片面追求治疗效果、获取经济暴利,擅自在其中添加化学药品,不仅违反了《药品管理法》和《食品安全法》的规定,还严重危及广大人民群众的身体健康。中成药、生化药品或保健品若在说明书中明确注明含有某种化学成分,则符合法律法规;若未注明却被检出,则为非法添加。因此,为严厉打击非法添加行为,保证人民群众的食品和用药安全,亟需开发快速、准确、高灵敏、高选择性的用于非法添加消化类化学药物的快速筛查方法。
当前,已报道的非法添加检测手段以液质联用法(LC-MS)[1-3]为主,也有关于高效液相色谱法(HPLC)[4]、薄层色谱法(TLC)-表面增强拉曼(SERS)联用法[5-6]、胶束电动色谱法[7]的报道。Orbitrap高分辨质谱仪(Orbitrap HRMS)是最新的高分辨质谱技术,分辨率可达1 000 000以上,质量精度可达0.1~1 ppm[8],可进行高精度的目标物或非目标物的筛查。近年来,Orbitrap 高分辨质谱技术的应用日益增多,已用于食品安全[9-10]、药品安全[11]、中成药成分分析[12]、药物动力学[13]、蛋白组学[14]、代谢组学[15]研究等领域。
本文首次将超高效液相色谱-Orbitrap高分辨质谱联用(UHPLC-HRMS)技术用于消化类化学药物非法添加的快速筛查、鉴定和定量研究。通过Full MS/dd-MS2(Data-dependent MS2) 模式,在一个分析周期(10 min)内完成对样品的高精度一级、二级扫描,得到准确质量数和准确碎片离子信息,同时对潜在的阳性样品进行定量分析。本方法具有快速、准确、高灵敏度、高选择性的特点,为打击非法添加行为提供了新手段、新技术。
1 实验部分
1.1 仪器与试剂
Thermo Q Exactive PlusTM超高效液相色谱-质谱联用系统包括Ultimate 3000液相泵、自动进样器、柱温箱以及Orbitrap高分辨质谱部分(Thermofisher Scientific,德国);XCalibur 4.0软件(Thermofisher Scientific,美国)用以质谱仪控制和数据处理;Mettler XS205电子天平(Mettler Toledo,瑞士);KQ-300 GDV温控超声仪(昆山舒美,中国);Sigma 3K15高速冷冻离心机(Sigma-Aldrich,德国);IKA Vortex3旋涡混匀器(IKA,德国)。色谱柱为Thermo Hypersil Gold C18(2.1 mm×100 mm,3 μm,Thermofisher Scientific,美国)。
对照品左卡尼汀、法莫替丁、西咪替丁、盐酸雷尼替丁、消旋山莨菪碱、甲氧氯普胺、奥美拉唑、雷贝拉唑钠、泮托拉唑钠、多潘立酮、西沙比利和枸橼酸莫沙必利均购自中检院,伊托必利购自加拿大TRC公司;HPLC级甲醇、乙腈以及超纯水均购自Fisher公司(美国),HPLC级甲酸、甲酸铵、乙酸铵购自ACS恩科化学公司(美国);样品来源:156批生化药品(复方胃蛋白酶颗粒)来自2017年国家评价性抽验检品,38批中成药、43批保健品来自山东省食品药品监督管理局或山东省各市、县食品药品监督管理局抽样。将未检出以上13种成分的10批样品混合均匀,作为阴性样品基质。10批阴性样品编号分别为YC201700004,YC201700025,YC201700039,YC201700040,YC201700055,YC201700057,YC201700058,YC201700068,YC201700114,YC201700117。
1.2 溶液的制备
1.2.1对照品溶液的制备精密称取各对照品适量,置于25 mL容量瓶中,加甲醇溶解并定容至刻度,摇匀,作为对照品储备液(质量浓度为200 mg/L)。向空白基质中加标准品,配成相当于实际样品质量浓度为8、40、200、400、800 μg/L的标准溶液和QC(质量控制)溶液。
1.2.2供试品溶液的制备取供试品约0.5 g,精密称定,置于10 mL容量瓶中,加提取溶剂甲醇-水(50∶50,体积比)适量,超声提取15 min,冷却至室温,加提取溶剂定容至刻度,上清液过滤膜,取续滤液即得供试品溶液。
1.3 液相色谱-质谱联用条件
1.3.1色谱条件色谱柱为Thermo Hypersil Gold C18(2.1 mm ×100 mm,3 μm)。流动相:0.1%甲酸水溶液(A)-乙腈(B),梯度洗脱程序:0~1.0 min,5%B;1.0~5.0 min,5%~85%B;5.0~7.5 min,85%B;7.5~7.6 min,85%~5%B;7.6~10.0 min,5%B。流速:300 μL·min-1;柱温:40 ℃;自动进样器温度:20 ℃;进样量:5 μL。
1.3.2质谱条件Q ExactiveTM质谱系统配有HESI离子源,采用正离子模式,喷雾电压为3.0 kV,毛细管和喷雾温度分别为350 ℃和250 ℃。鞘气和辅助气压力分别设为40、15 arb,S-lens RF电压为50 V。喷雾气和碰撞气均为氮气。使用校正溶液(含咖啡因、四肽MRFA和Ultramark 1621的混合溶液)每3 d校正1次质量轴。扫描方式采用正离子Full MS/dd-MS2模式。Full MS一级全扫描范围为m/z100~1 000,自动增益控制AGC、最大注入时间IT分别设为1.0e6和100 ms;dd-MS2数据依赖的二级扫描AGC设为2.0e5,最大IT设为50 ms,分离窗口设为1.0m/z。各化合物的归一化碰撞能量设为20%、40%、60%。
2 结果与讨论
2.1 方法的建立
考虑到13种化合物的极性差异较大,故选择甲醇-水(体积比50∶50)作为提取溶剂,结果表明其对13种化合物均有较高的提取效率,且滤液洁净,无需进一步净化即可直接进样,简化了样品前处理。
由于13种化合物结构中均含有较多的N原子,正离子质谱扫描模式下响应高,因此选择正离子模式。分别将13种化合物标准溶液流动注入质谱仪进行参数优化,获得相应的准分子离子峰,输入至方法设置中。各化合物二级质谱扫描的碰撞能量统一设为20%、40%、60%,得到的二级质谱图是在3种碰撞能量下二级质谱图的叠加,有效避免了采用单一碰撞能量可能导致的不同仪器间重现性差的情况。在建立的LC-MS联用方法中,扫描方式选择正离子Full MS/dd-MS2模式,此模式包含一次一级全扫描和一次数据依赖的二级扫描。一级质谱全扫描采用70 000 FWHM分辨率,确保得到高分辨质谱准确质量数;二级质谱扫描采用17 500 FWHM,保证高分辨扫描的同时加快扫描速度。
对比了甲醇-水和乙腈-水混合体系作为流动相的效果,并在水相中分别添加了少量甲酸、甲酸铵、乙酸铵等。结果表明,乙腈-0.1%甲酸水体系能得到最佳的分离效果,获得最佳的色谱峰形和较高的灵敏度,因此选择乙腈-0.1%甲酸水体系作为流动相,并采用“1.3.1”所述梯度洗脱程序。
2.2 专属性
称取阴性样品适量,按“1.2.2”方法处理得到空白基质溶液,进样5 μL分析,空白基质溶液的提取离子色谱图显示,各化合物保留时间处未出现干扰峰或干扰峰很小(远低于检出限),对定量分析没有影响,专属性强。单次测定在10 min内即可完成,分析效率高,尤其适用于高通量筛查。另取200 μg/L的QC溶液进样5 μL分析,记录色谱图(图1)。
化合物的保留时间、准确质量数和碎片离子信息如表1所示。理论质量数与实际测得的质量数相对偏差越小,表明筛查结果的可信程度越高。表1中13种分析物的实测和理论质量数偏差均不超过3.08 ppm,显示了Orbitrap HRMS高度可靠的质量精度。代表性化合物雷尼替丁的二级质谱图及裂解机理如图2所示,二级质谱碎片离子辅助确证化合物的存在,裂解机理阐明了主要碎片离子的化学结构及裂解途径。
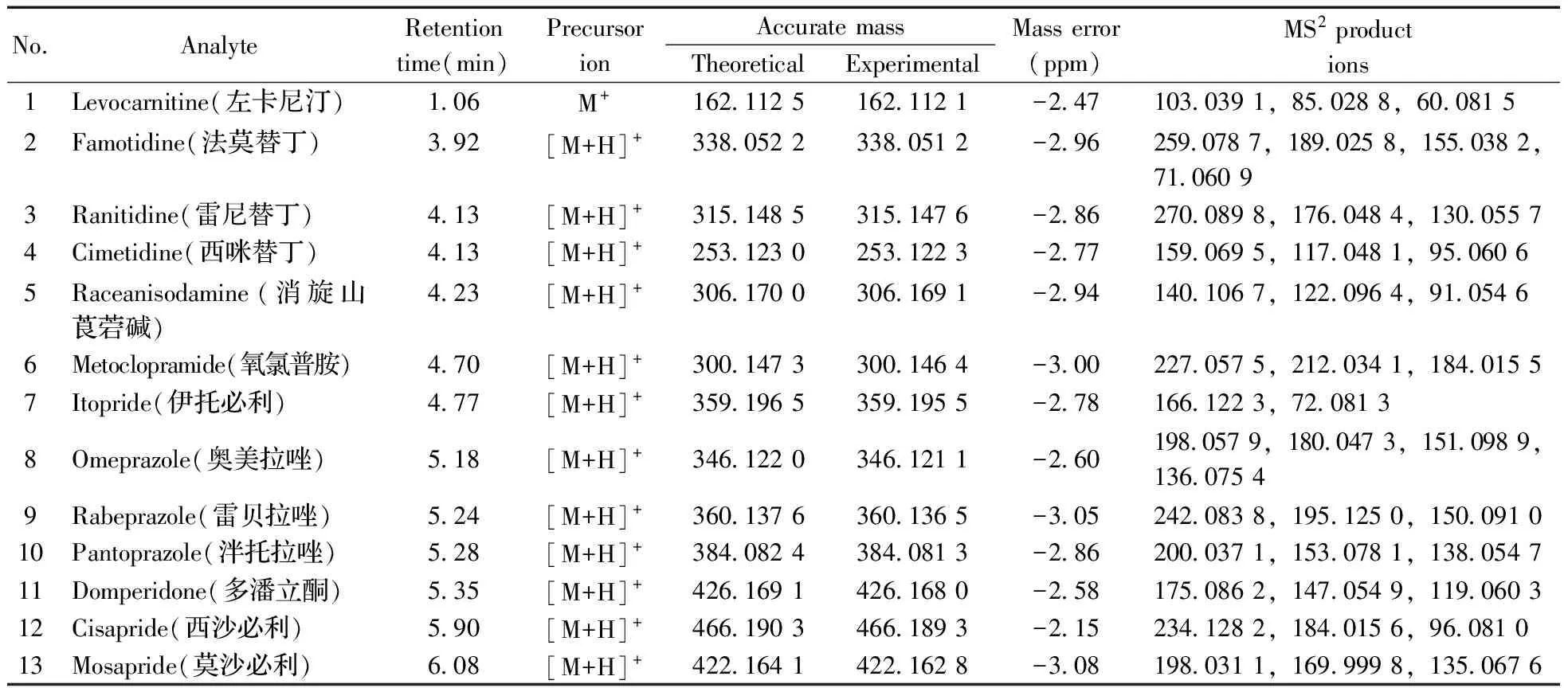
表1 消化类药物的保留时间和准确质量数测定Table 1 Retention time and accurate mass of digestive system drugs
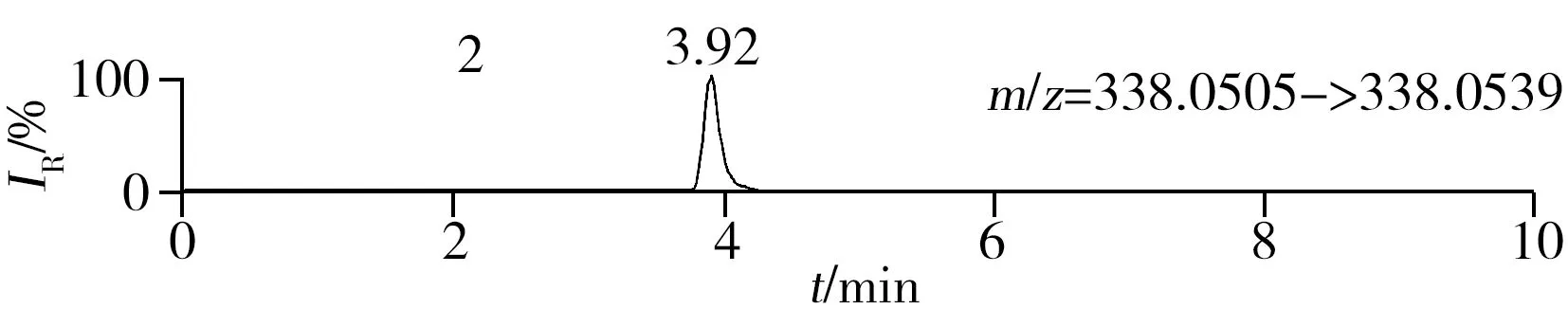
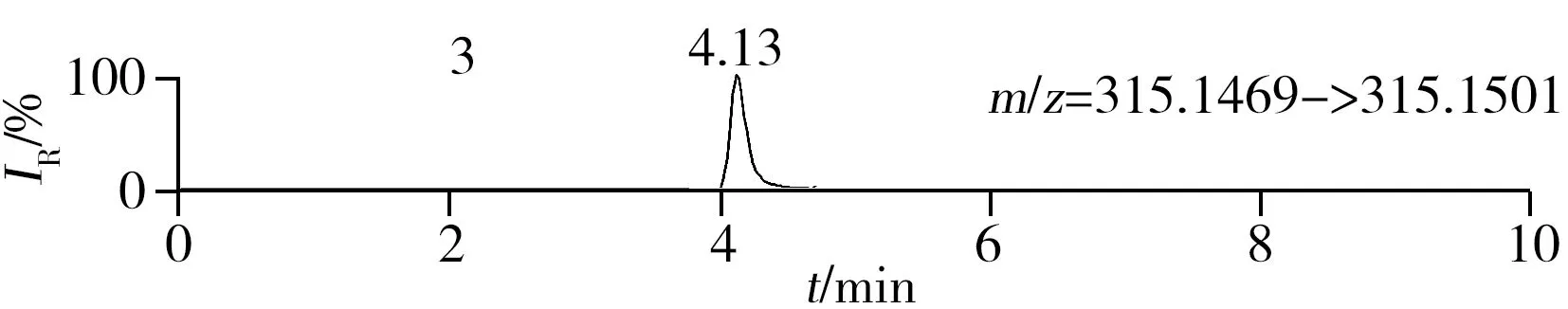
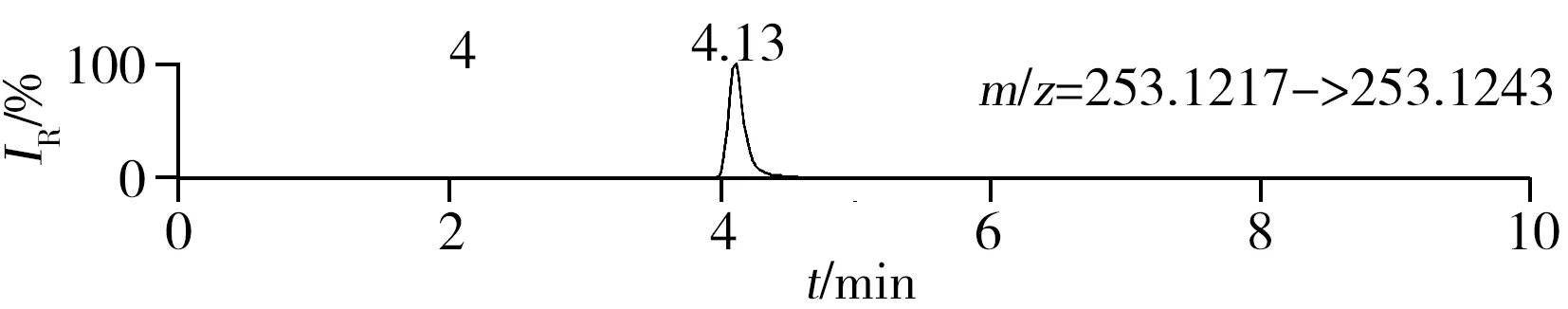
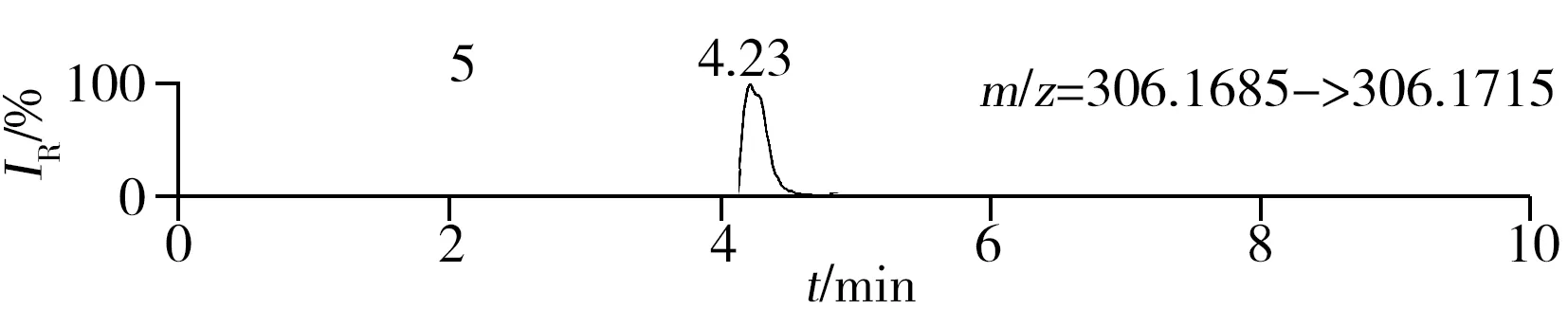
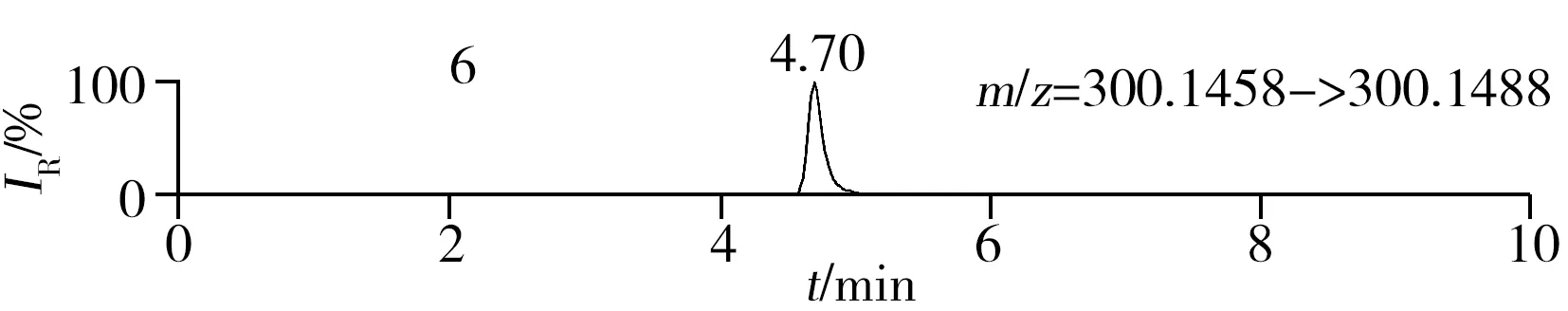
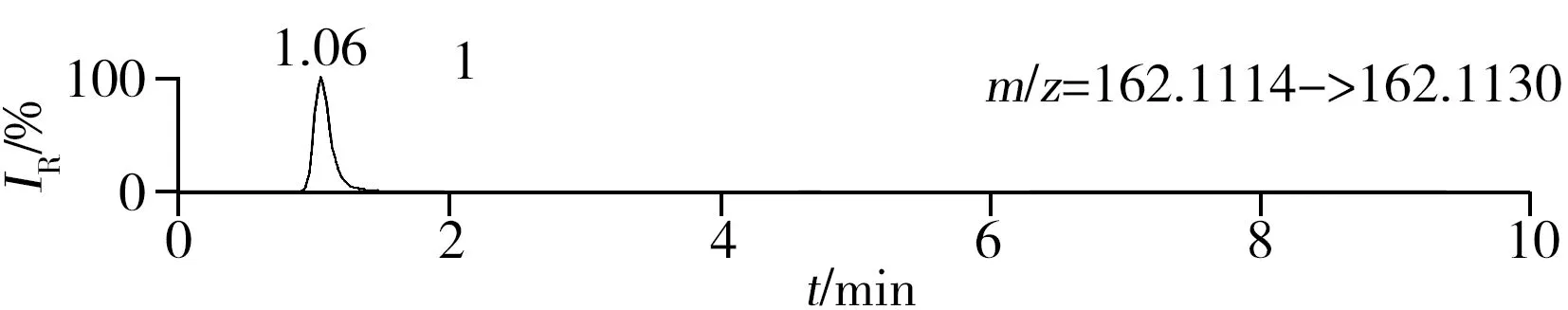
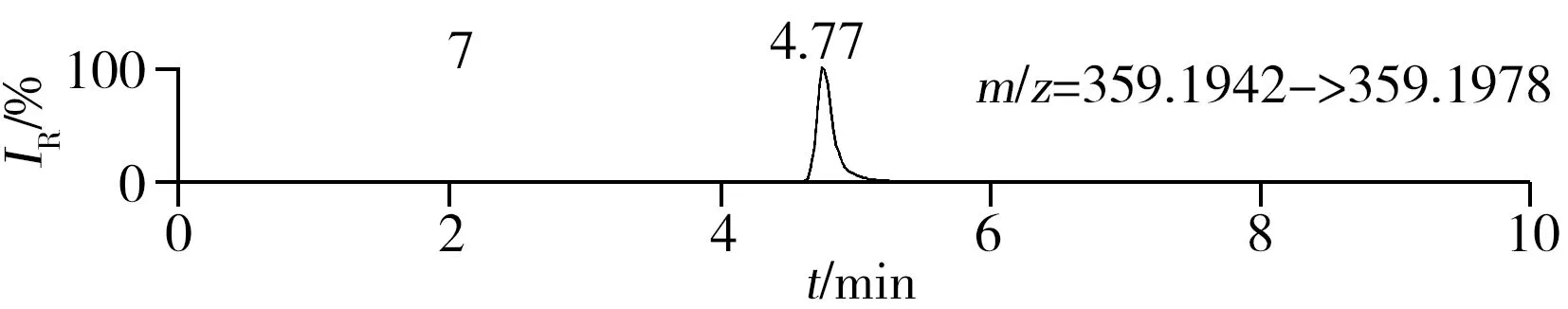
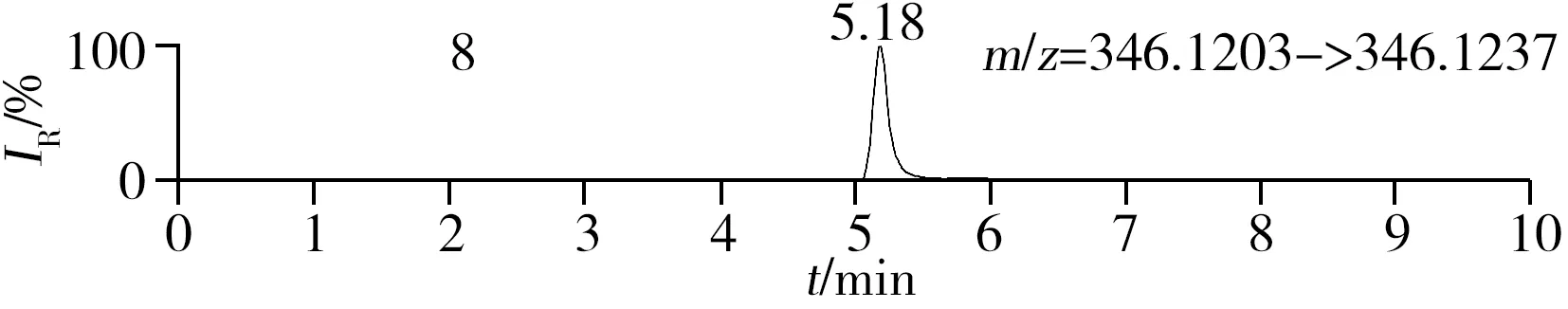
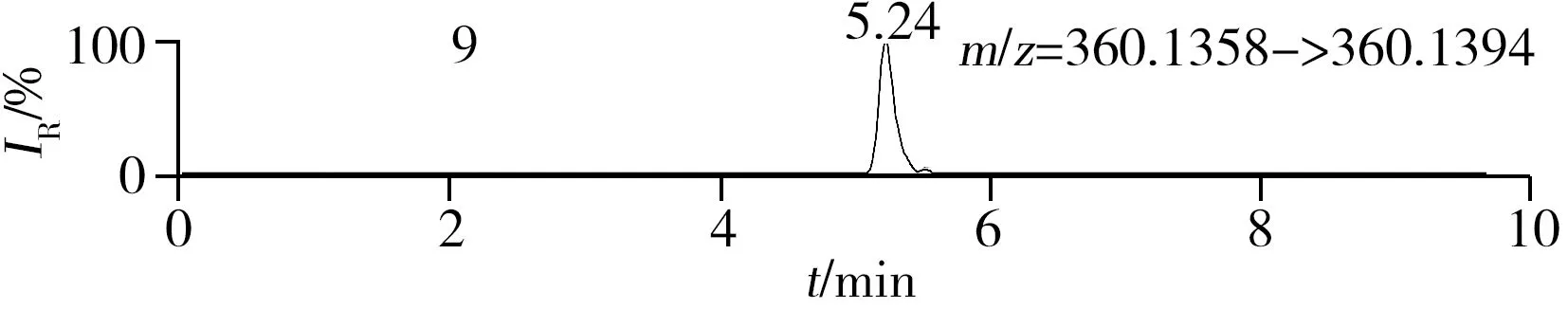
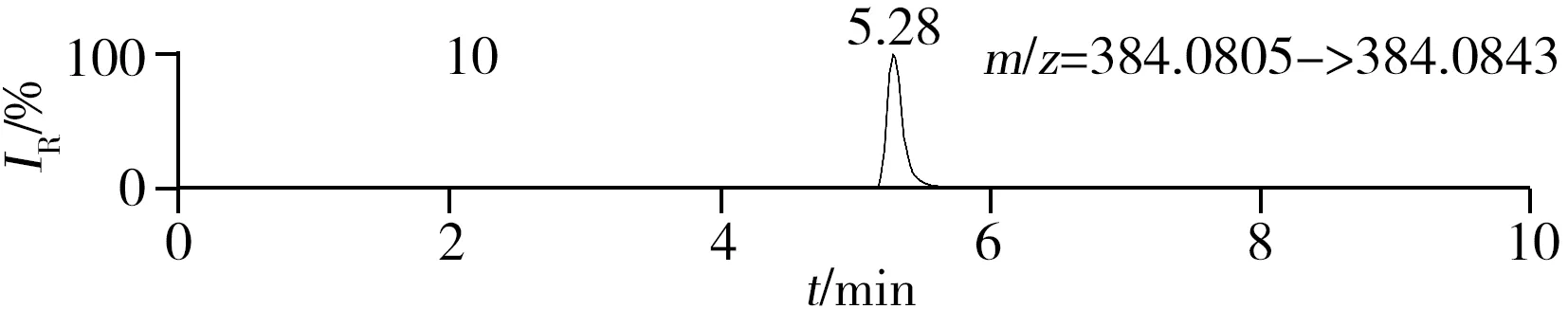
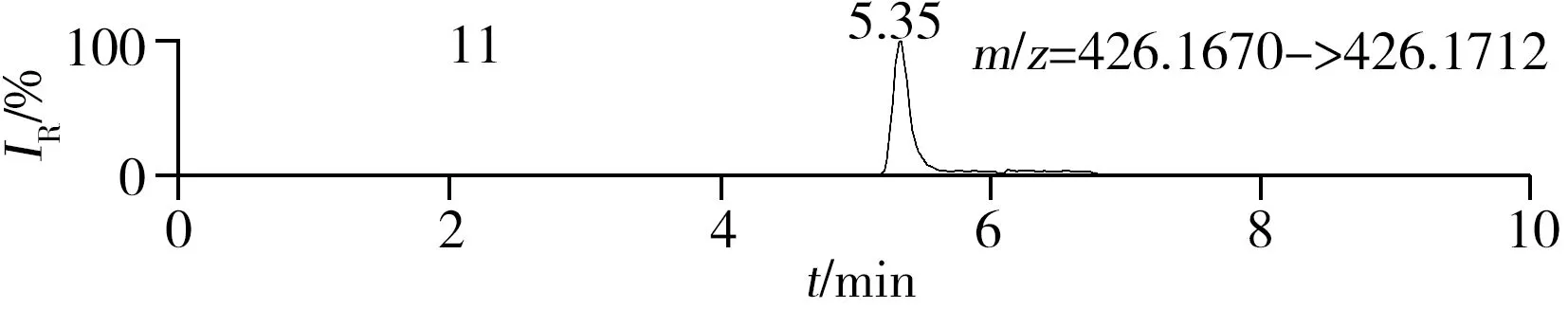
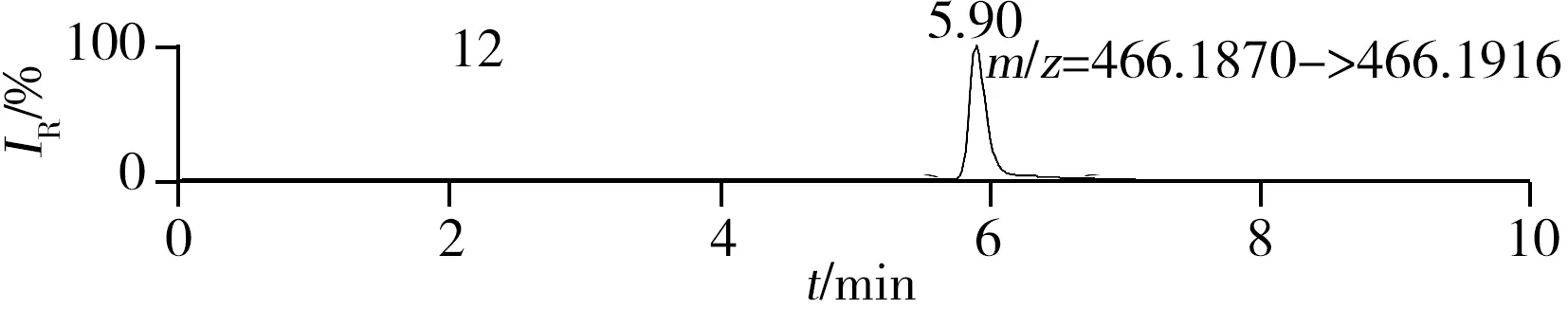
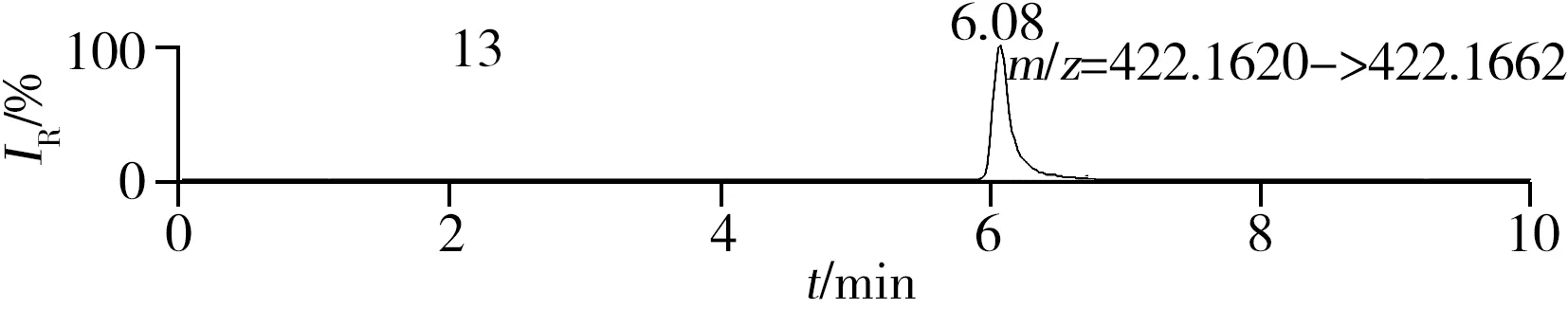
图1 QC溶液(200 μg/L)的提取离子色谱图Fig.1 Extracted ion chromatograms of digestive drugs in 200 μg/L spike solutionthe noted numbers were the same as those in Table 1
2.3 检出限
逐级稀释QC溶液并进样分析,记录色谱图,按照3倍信噪比计算检出限。结果表明各化合物的检出限均为1.0 μg/L。
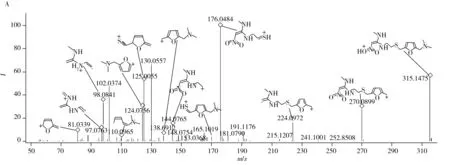
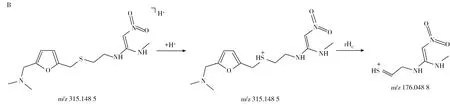
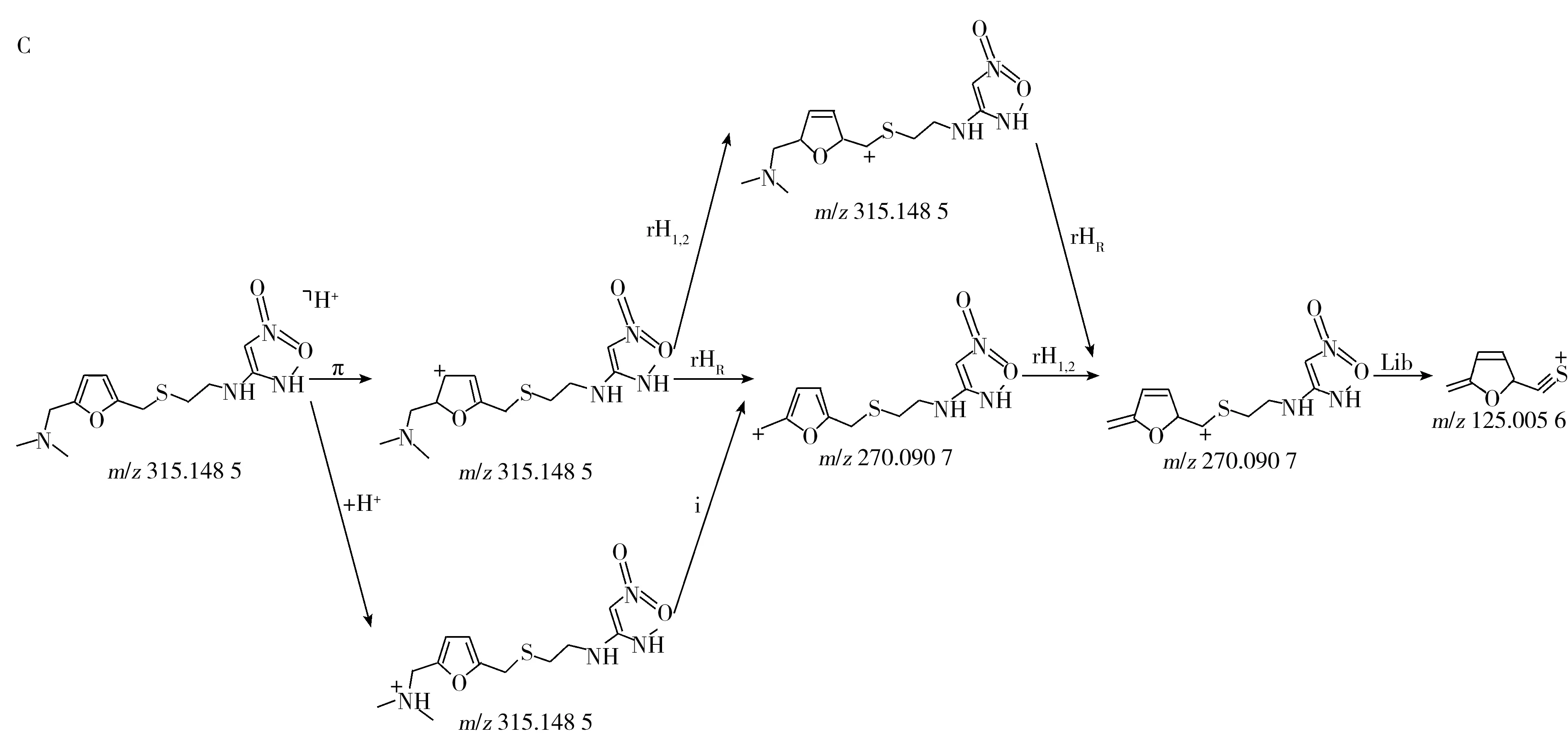
图2 雷尼替丁的二级质谱图(A)以及碎片离子m/z 176.048 8(B)与m/z 270.090 7及m/z 125.005 6(C)的裂解机理Fig.2 MS2 mass spectra(A) and fragmention mechanisms of fragment ions m/z 176.048 8(B),m/z 270.090 7 and m/z 125.005 6(C)
2.4 线性范围与定量下限
按“1.2.1”配制系列标准溶液,进样5 μL测定峰面积。以峰面积(y)对标准溶液质量浓度(x,μg/L)拟合校正曲线,建立回归方程。结果表明,13种化合物的峰面积与质量浓度线性关系良好,线性范围均为8.0~800 μg/L,相关系数(r)为0.998 5~1.000 0(表2)。以线性范围最低点作为定量下限,13种化合物的定量下限均为8.0 μg/L。
2.5 回收率、准确度与精密度
分别精密移取对照品储备液10 μL、阴性供试品0.5 g,置于10 mL容量瓶中,加提取溶剂适量,超声提取15 min,冷却至室温,加提取溶剂定容至刻度,上清液过滤膜,取续滤液即得供试品溶液(质量浓度约为200 μg/L),平行制备6份。进样,按拟定方法测定回收率,计算平均回收率及相对标准偏差(RSD)。回收率平均值用于评价准确度,RSD值用于评价精密度,实验结果见表2,13种化合物的回收率为94.6%~106.2%,RSD为1.2%~2.9%。
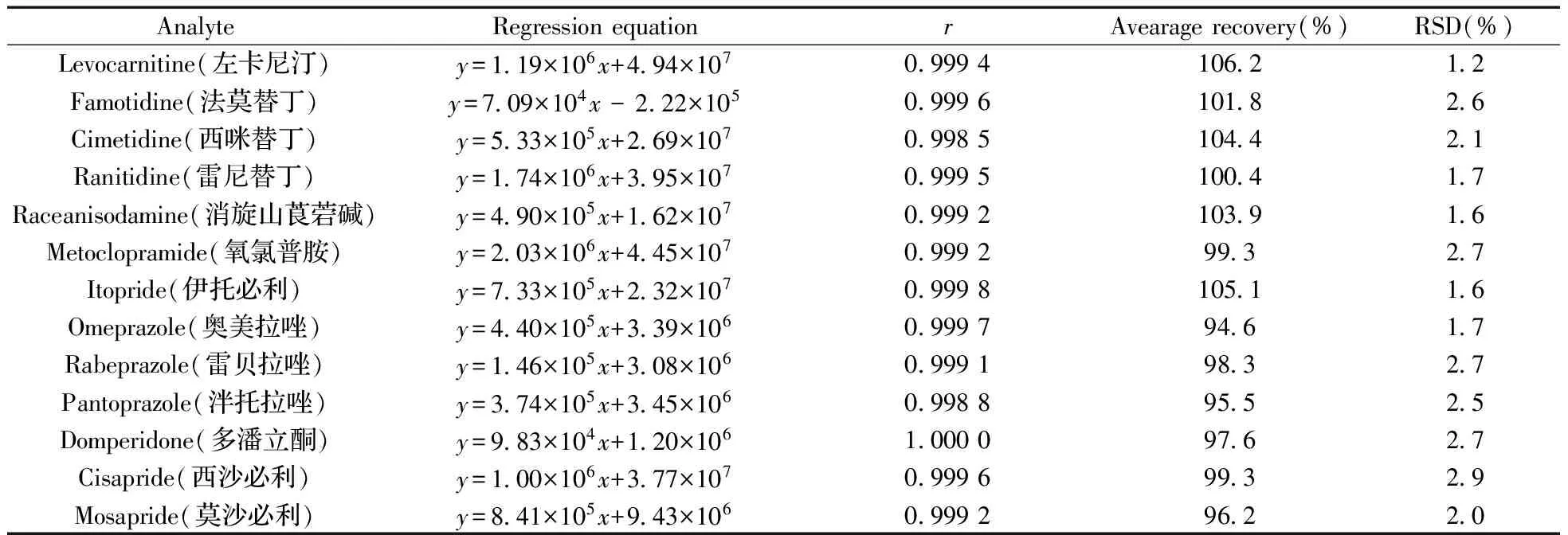
表2 13种消化类化学药物的回归方程,相关系数和回收率Table 2 Regression equation,correlation coefficient(r) and recovery of digestive system drug
2.6 基质效应与稳定性
取200 μg/L的QC溶液和200 μg/L的纯溶剂对照品溶液,分别进样,计算响应值百分比,即为基质效应。结果表明13种化合物的基质效应均在92.3%~105.6%之间,表明空白基质对化合物响应影响很小。
用空白基质配制200 μg/L的标准溶液,分别在1、2、4、6、8、12、24 h进样,以各化合物的提取离子峰面积为指标,代入标准曲线计算浓度与实际浓度的比值(稳定性)在94.5%~102.8%之间,由此可见配制的标准溶液在24 h内稳定。
2.7 实际样品分析
将建立的高分辨质谱法用于156批生化药品、38批中成药、43批保健品中非法添加消化类化学药物的筛查。比较供试品和对照品的提取离子色谱图、一级质谱和二级质谱,若供试品某成分的保留时间、一级质谱准确质量、碎片离子准确质量均与对照品一致,则判定该成分为非法添加物。
经筛查发现,156批生化药品均未检出左卡尼汀等13种化学药物,而5批中成药中检出西咪替丁(含量为1.4~17.9 mg/g),3批保健品中检出多潘立酮(含量8.61~14.3 mg/g),代表性阳性样品(检出多潘立酮)图谱见图3所示。以上结果表明消化类化学药物非法添加在中成药和保健品中较为突出。另一方面,156批生化药品均未检出非法成分,可能与其来源是正规药品企业有关。以上结果表明本文所建立的高通量HRMS法具有良好的可靠性。
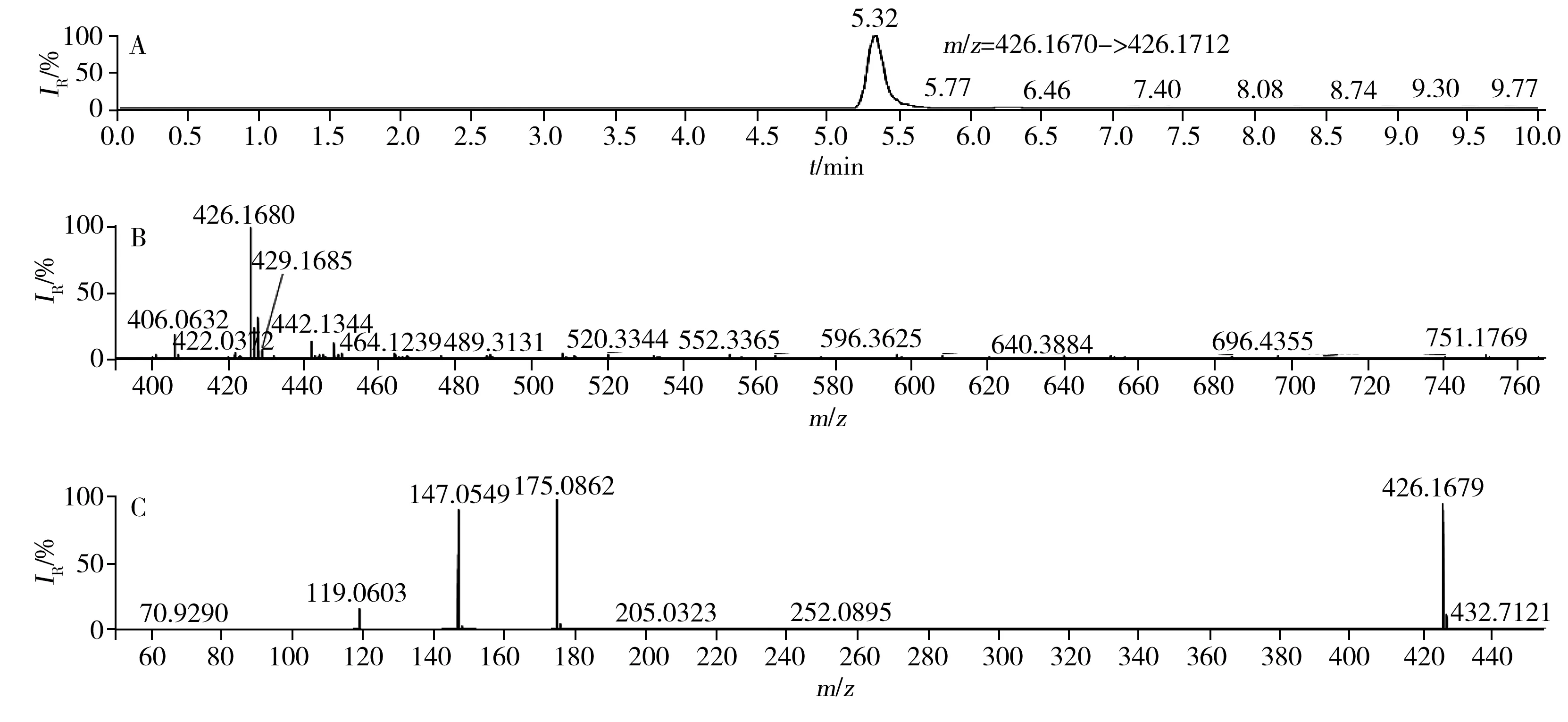
图3 代表性阳性样品YW201708461的提取离子色谱图(A)、一级质谱图(B)和二级质谱图(C)Fig.3 Extracted ion chromatogram(A),MS(B) and MS2(C) spectra of digestive drugs in representative positive sample YW201708461
3 结 论
本研究建立了一种快速筛查非法添加消化类化学药物的方法,可在10 min 内同时测定13种消化类药物。该法选择性好、灵敏度高、快速简便、可操作性强、准确可靠,极大地提高了检测效率,适用于生化药品、中成药及保健品非法添加检测,已用于日常检测工作中,为监管相关非法添加提供了有力的技术支持。
参考文献:
[1] Choi J Y,Heo S,Yoo G J,Park S K,Yoon C Y,Baek S Y.FoodAddit.Contam.:A,2015,32(7):1029-1039.
[2] Heo S,Choi J Y,Yoo G J,Park S K,Baek S Y.Biomed.Chromatogr.,2017,31(4):6.
[3] Kim E H,Seo H S,Ki N Y,Park N H,Lee W,Do J A,Park S,Baek S Y,Moon B,Oh H B,Hong J.J.Chromatogr.A,2017,1491:43-56.
[4] Huang Y C,Lee H C,Lin Y L,Li C Y,Tsai C F,Cheng H F.FoodAddit.Contam.:A,2016,33(2):179-185.
[5] Li H,Zhu Q X,Chwee T S,Wu L,Chai Y F,Lu F,Yuan Y F.Anal.Chim.Acta,2015,883:22-31.
[6] Lv D Y,Cao Y,Lou Z Y,Li S J,Chen X F,Chai Y F,Lu F.Anal.Bioanal.Chem.,2015,407(5):1313-1325.
[7] Maier V,Znaleziona J,Jirovsky D,Skopalova J,Petr J,Sevcik J.J.Chromatogr.A,2009,1216(20):4492-4498.
[8] Zubarev R A,Makarov A.Anal.Chem.,2013,85(11):5288-5296.
[9] Jia W,Shi L,Chu X.FoodChem.,2018,239:427-433.
[10] Marín-Sáez J,Romero-González R,Garrido F A.J.Chromatogr.A,2017,1518:46-58.
[11] Cheng Q,Shou L,Chen C,Shi S,Zhou M.J.Chromatogr.B,2017,1064:92-99.
[12] Wang S S,Xu H Y,Ma Y,Wang X G,Shi Y,Huang B,Tang S H,Zhang Y,Li D F,Liang R X,Yang H J.J.Pharm.Biomed.Anal.,2015,111(Suppl C):104-118.
[13] Zuo L,Zhong Q,Wang Z,Sun Z,Zhou L,Li Z,Xu T,Shi Y,Tang J,Du S,Zhang X.J.Pharm.Biomed.Anal.,2017,146:347-353.
[14] Li X,Shi F,Gong L,Hang B,Li D,Chi L.Int.J.Nanomed.,2017,12:4443-4454.
[15] Huang X H,Guo C N,Chen Z L,Liu Y H,He L M,Zeng Z L,Yan C Q,Pan G F,Li S P.J.Chromatogr.B,2015,1000:147-154.
