改性粘土预处理垃圾渗滤液中氨氮的吸附热力学和动力学研究
2018-03-05唐艳妮姜丽丽
吕 利,唐艳妮,姜丽丽
(1.四川省地质工程勘察院,成都 610072;2.成都自来水有限责任公司,成都 610051;3.西藏金海矿产资源开发有限公司,成都 610000)
垃圾渗滤液水质复杂,属于高浓度有机废水,其中包含有多种有毒有害的无机物和有机物、病原微生物以及某些致癌和促癌物质,其危害非常大,并且当前垃圾渗滤液的处理面临处理难度大、成本高、效果不稳定等特点。
粘土矿物在废水处理领域的运用,具有很大的潜力,并在环境工程方面已被重点关注。近年来,世界各地许多专家学者将粘土矿物作为有机污水的吸附混凝剂进行了大量的研究,取得了不错的成就[1]。成都粘土广泛分布较广,布展于成都断陷盆地东侧台地上,呈“地毯式”分布于不同的地貌单元上,总面积达数千平方公里[2]。
本文以成都粘土为研究对象,通过十六烷基三甲基溴化铵(HDTMA)对粘土进行改性,研究改性前后粘土的性质变化及对垃圾渗滤液中氨氮的吸附热力学和动力学性能,为垃圾渗滤液的处理方法提供一定的理论指导。
1 实 验
1.1 实验材料
实验采用的粘土为成都粘土。成都粘土的物质组成:成都粘土的矿物成分主要为伊利石(水云母),次为蒙脱石;此外,还有少量高岭石、绿泥石和石英。成都粘土的化学成分主要由SiO2,Al2O3,Fe2O3组成。其含量分别为:SiO2=63.6%~69.2%;Al2O3=13.4%~15.9%;Fe2O3=6.2%~9.2%。三者总含量达85%以上[2]。
实验所用垃圾渗滤液取自成都洛带长安垃圾填埋场,氨氮的浓度2 133.33mg/L,pH值7.4。
1.2 主要试剂和设备
主要试剂:硫酸银、硫酸汞、浓硫酸、重铬酸钾、硫酸亚铁铵、领苯二甲酸氢钾、碘化汞、碘化钾、氢氧化钠、酒石酸钾钠、硫代硫酸钠、轻质氧化镁、硼酸。
主要设备:搅拌器、分析天平、分光光度计、烘箱、离心机、pH计、恒温水浴锅。
1.3 实验方法
1.3.1 改性粘土的制备方法
改性粘土的制备[3-4]:取原土 20.000g于500 mL 的烧杯中,加入400 mL 去离子水,充分搅拌,配成 5%的悬浮液;加入一定量的十六烷基三甲基溴化铵(HDTMA),在60℃水浴作用下机械搅拌 3.0 h,静置,进行离心分离;用去离子水将粘土洗涤3~5次后,置于烘箱中,设置温度在 80℃~90℃间,烘干,然后研磨,过 200 目筛;在 105℃温度下活化2.0h,所得样品放入干燥箱,即为HDTMA改性粘土。
1.3.2 改性粘土的表征
1.3.2.1 X射线衍射分析(XRD)
将原土及改性后的粘土放入烘箱中在105℃烘 4 h 后,用研钵研磨至过 200目筛,在 XRD 粉末衍射仪上进行测试。测试控制条件:入射波 1.540 6 nm,管电流 30.0 mA,管电压 40.0 kV,扫描速度 4.0°/min,起始角 2°,终止角 20°,步宽 0.02°。
1.3.2.2 红外光谱分析(IR)
将原土及改性后的粘土分别与预先烘干的 KBr 粉末混匀,用研钵充分研磨,压片,在 400~4 000 cm-1波数范围内,采用IRPrestige 傅立叶红外光谱仪进行红外光谱分析。
1.3.2.3 热分析(DSC)
将原土及改性后的粘土用 DSC204F1 差示扫描量热仪进行热分析,检测条件:开始温度 35℃;结束温度 600℃;99.999%的氮气升温速率V=10 K/min。
1.3.3 吸附热力学和动力学实验
在1 000 mL烧杯中,取1 000 mL渗滤液和100g的粘土,在pH=7,搅拌速度200 r/min的条件下,搅拌50min,静置放置6h,吸附完成后,取上清液进行氨氮测定[5]。
液相吸附对应的吸附量主要是根据渗滤液中某被吸附物在吸附平衡前后浓度的变化来计算的[6],具体计算公式见式(1):
q=(C0-Ce)V/m
(1)
式中, C0是溶液的初始浓度(mg/L),Ce是吸附平衡后溶液浓度(mg/L),V是溶液的体积(L),m是改性粘土的质量(g)。
1.4 模型建立
1.4.1 吸附热力学模型
吸附热力学是在不同温度条件下研究吸附质对吸附量的影响过程,并得到各种热力学数据。对于吸附过程热力学参数的确定,主要通过以下公式得到:
Ke=CA/Ce
(2)
lnKe=-△Hθ/RT+C
(3)
△Gθ=-RTlnKe
(4)
△Gθ=△Hθ-T△Sθ
(5)
其中,ΔGθ为吸附过程的自由能变值(kJ/mol);ΔHθ为吸附过程的焓变值(kJ/mol);ΔSθ为吸附熵变值(kJ ·mol-1·K-1);Ke是平衡常数;CA是达到平衡时指标的被吸附浓度(mg/L);Ce是指标的平衡浓度(mg/L),C为常数,T是温度(K)[7]。
1.4.2 吸附动力学模型
吸附动力学的研究主要是研究吸附量与吸附时间关系的动力学曲线,一般采用有限液法或者独立瓶法获得动力学曲线,但是有限液法的测试对溶液量有一定的要求。本文采用的是独立瓶法来研究改性粘土吸附垃圾渗滤液中氨氮过程的动力学,在相同条件下,取等体积、等初始浓度的垃圾渗滤液进行实验,每个取样时间点取样的溶液各不干扰,各自独立[8]。
准二级吸附速率方程和粒子内扩散方程线性表达式如下:
(6)
qt=Kint1/2+C
(7)
其中:qt是某时刻吸附量(mg/g);qe是平衡吸附量(mg/g);ks是准二级动力学模型速率常数 (g.mg-1.min-1);Kin为吸附内扩散速率常数(mg.g-1.min-1/2)[9]。
2 实验结果与分析
2.1 改性粘土结果表征及分析
2.1.1 X射线衍射分析
根据测试方法步骤,分别对原土和改性土进行XRD分析,得到X射线衍射图谱,见图1。
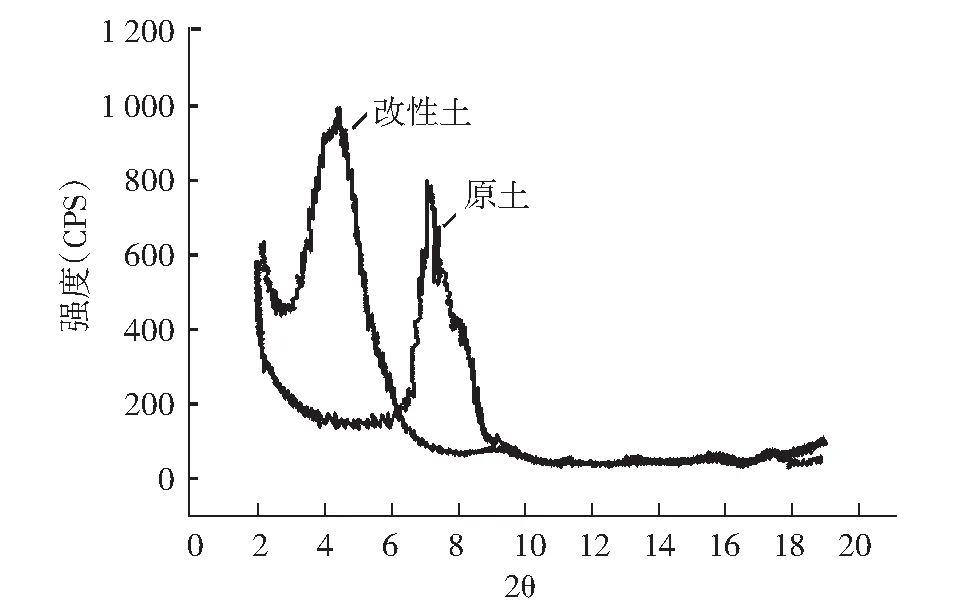
图1 原土及改性土的XRD图Fig.1 XRD diagram of original soil and modified soil
根据图1的数据,由布拉格方程:
2dsinθ=nλ
(8)
计算粘土的层间距(d值)。根据计算结果,原土的层间距为1.244nm,属于原始粘土的特征,改性粘土的层间距为1.998 nm,改性粘土与原土相比,其层间距增大了 0.754 nm。由此可见, HDTMA已通过离子交换作用进入粘土层间,使改性后粘土层间距大大增加。
2.1.2 红外光谱分析
根据测试方法步骤,分别对原土和改性土进行红外光谱分析(IR)分析,得到IR图谱,见图2。
根据图2可以看出,由于粘土层间吸水,在 3 451 cm-1附近出现粘土层间羟基的伸缩振动峰;在 1 639 cm-1和1 400 cm-1处,出现羟基的伸缩振动峰,这是粘土晶格中含有晶格水的体现。
HDTMA 改性土在 2 918 cm-1和 2 850 cm-1附近出现了明显的甲基、亚甲基和次甲基的对称和不对称伸缩振动吸收峰,1 400 cm-1附近出现了 C-H 对称弯曲吸收峰。再结合图 2 的 XRD 图谱,亦说明 HDTMA 分子已经进入粘土层间。
2.1.3 热分析
根据测试方法步骤,分别对原土和改性土进行热分析,得到DSC图谱和DTG图,见图3和图4。
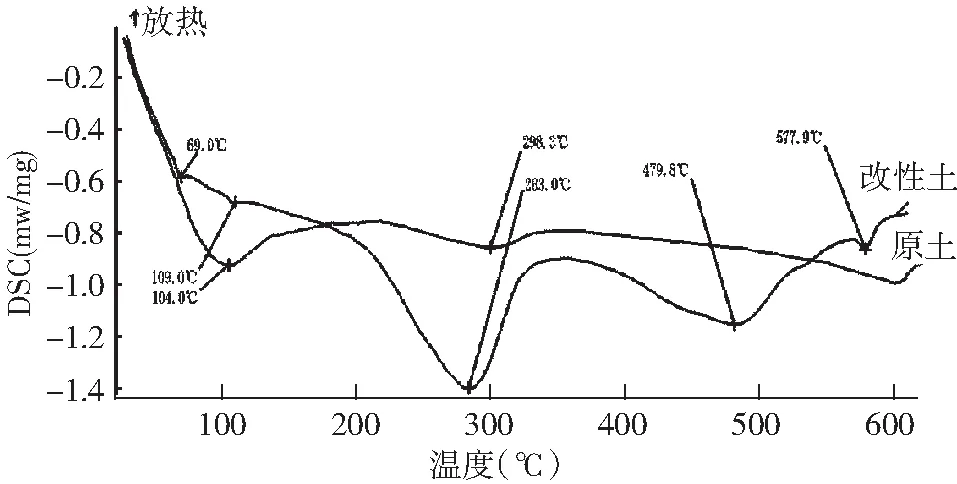
图3 原土及改性土的DSC图Fig.3 DSC diagram of original soil and modified soil

图4 原土及改性土的DTG图Fig.4 DTG diagram of original soil and modified soil
从图3可知:原土在104℃附近有一个失水吸热峰,在600℃的范围内粘土的结构比较稳定;由于进入层间的 HDTMA有机物开始熔融产生了相变,导致HDTMA改性土在283℃有一个明显吸热峰;而在479.8℃的吸收峰是HDTMA 分子链分解所致。
从图4可知:在260.0℃附近,HDTMA开始熔融,失重率变化10%左右,这与DSC图谱分析结果一致,也侧面反应改性剂进入了粘土的层间。
2.2 吸附时间、温度对吸附效果的影响
分别取7份1 000 mL的垃圾渗滤液于7个烧杯中,按1.3.3章节规定条件,分别在30℃(303.15 K)、40℃(313.15 K)、60℃(333.15 K)下进行实验,考查原土和改性粘土对氨氮的吸附量随时间的变化,所得成果见图5和图6。
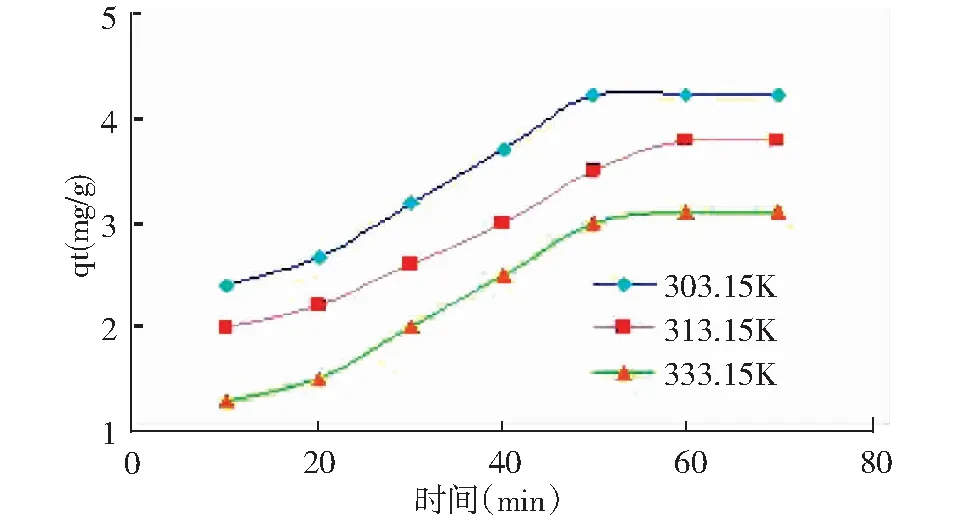
图5 不同温度下原土吸附氨氮量随时间的变化(C0=2 133.33 mg/L)Fig.5 Variation of ammonia nitrogen adsorption onto original clay with time at different temperatures

图6 不同温度下改性粘土吸附氨氮量随时间的变化(C0=2 133.33 mg/L)Fig.6 The change of ammonia nitrogen adsorption onto original clay with time at different temperatures
由图5、图6可知,在前40 min,粘土对氨氮的吸附,随时间的增加而增加,50 min后,吸附量增加逐渐缓慢,而后基本趋于稳定。可见,粘土吸附渗滤液中氨氮的平衡的时间为50 min左右。
在 303.15 K,313.15 K,333.15 K 不同温度下,原土对氨氮的平衡吸附量在2.80 ~4.00mg/g之间,而改性土对氨氮的平衡吸附量在7.60~8.62mg/g之间。由此可知,在实验控制条件下,改性后的粘土吸附效果比原土提高了大约2~3倍,同时随着温度的升高,粘土和改性土的平衡吸附量均逐渐减少,温度升高不利于氨氮吸附作用的进行。
2.3 吸附等温曲线
取垃圾渗滤液数升,通过添加去离子水改变其氨氮浓度。分别配置7份2 000 mL的垃圾渗滤液稀释液,使其氨氮浓度分别为1 600 mg/L、1 400 mg/L、1 200 mg/L、1 000 mg/L、800 mg/L、600 mg/L、400 mg/L。
按1.3.3章节规定条件,分别在30℃(303.15 K)、40℃(313.15 K)、60℃(333.15 K)下进行实验,考查氨氮不同Ce及对应的qe值,如图7所示。
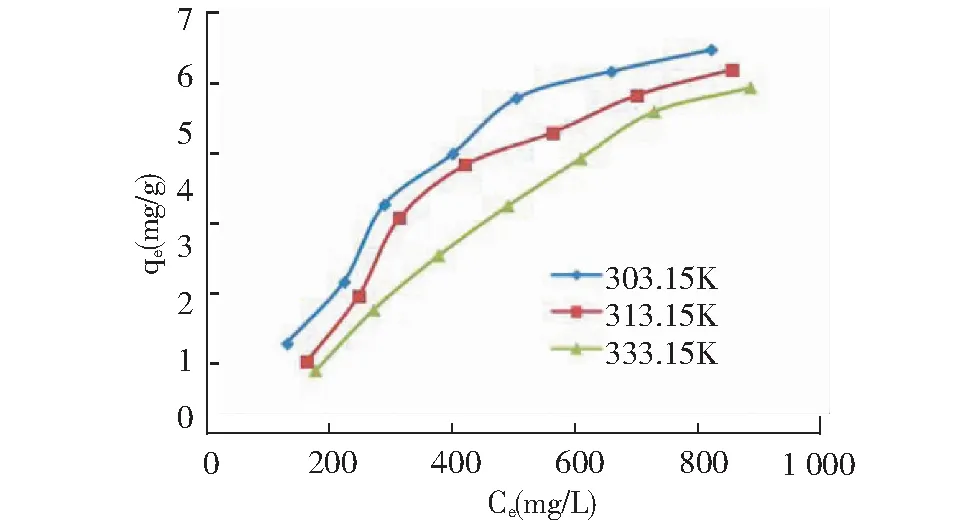
图7 不同温度下改性粘土平衡吸附量qe随氨氮平衡浓度Ce的变化Fig.7 Change of equilibrium adsorption capacity(qe) of modified clay with ammonia nitrogen balance(Ce)at different temperatures
根据实验结果,在303.15 K,313.15 K,333.15 K不同温度下,随着垃圾渗滤液初始浓度的增加,改性土的平衡浓度不断加大,平衡吸附量也随之增加。但是,随着温度的升高,改性土对氨氮平衡吸附量不断减小,不利于吸附作用。
根据Langmuir等温方程和Freundlich等温方程,见式(9)和式(10),对所得等温吸附数据拟合,以相关系数R2为拟合评价标准,对改性粘土吸附氨氮的过程分别进行判定。
Ce/qe=1/bqm+Ce/qm
(9)
qe=KFCe1/n
(10)
式中,q为吸附量(mg/g),Ce为吸附浓度(mg/L),qm为最大吸附量(mg/g), b为Langmuir吸附常数,KF、n为与吸附剂和吸附质种类及实验温度等因素有关的Freundlich型吸附常数。在固液吸附体系中,KF可反映吸附量的相对大小,n可表示吸附强度的相对大小,n越小吸附越不易进行[10]。分别以Ce/qe对Ce,lgqe对lgCe作图,见图8。
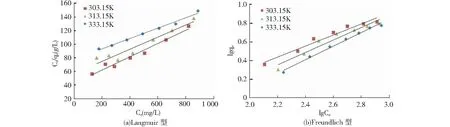
图8 改性粘土吸附氨氮的吸附等温线Fig.8 Adsorption isotherm of ammonia nitrogen onto modified clay
根据上述数据建立氨氮吸附模型,列于表1。

表1 氨氮在改性粘土上的吸附模型Tab.1 Adsorption model of ammonia nitrogen onto modified clay
由Langmuir等温方程和Freundlich等温方程计算吸附模型相关参数,见表2。
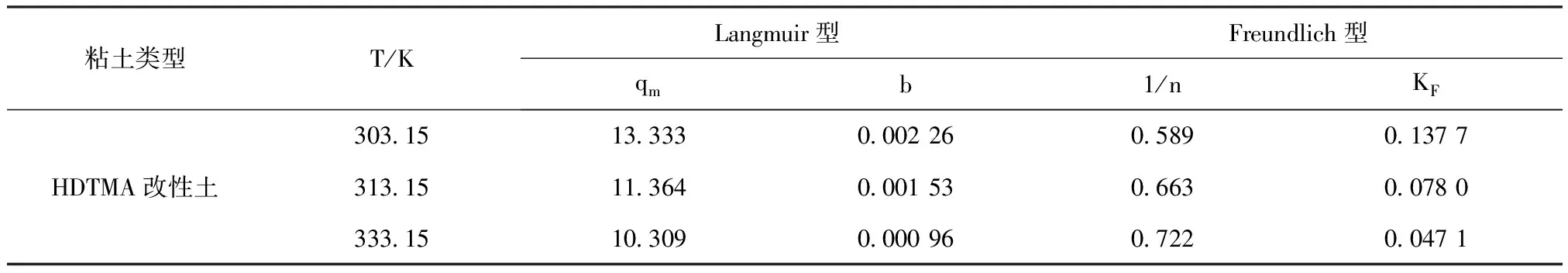
表2 氨氮在改性粘土上的吸附模型参数Tab.2 Adsorption model parameters of ammonia nitrogen onto modified clay
由图8和表1、表2可知:改性粘土吸附垃圾渗滤液中氨氮的过程,均可以较好地用Langmuir等温方程和Freundlich等温方程描述。
Langmuir等温吸附模型所得最大吸附量qm与平衡吸附量差异不大,符合Langmuir等温方程。在Langmuir等温方程中,b为吸附平衡常数,其值的变化与吸附剂、吸附质本身的特性和实验温度有关,b值越大,则表示吸附能力越强;Freundlich等温方程中,随着温度的升高,Freundlich等温方程中的n 、KF不断减小,不利于吸附的进行,吸附量减小。两种模型均证实了“温度升高,不利于改性粘土对氨氮的吸附作用的进行”。
Langmuir模型是理想的単分子层吸附理论,表面上各个吸附位置分布均匀;而Freundlich模型是多分子层吸附的经验公式,假设吸附表面存在着一定的不均匀性[11]。说明氨氮吸附过程存在单分子层的吸附,也存在多分子层的吸附。
2.4 改性粘土预处理垃圾渗滤液中氨氮的吸附热力学
用2.2章节得出的实验数据,按式(2)计算出不同温度下的 Ke。本文在研究过程中假设ΔHθ不随温度的变化而变化,对 lnKe与 1/T进行线性拟合,由式(3)可推出不同条件下平衡吸附量所对应的 ΔHθ,再由式(4)和式(5)可求得 ΔGθ、△Sθ。 具体数据见表3。

表3 改性粘土吸附氨氮的热力学参数Tab.3 Thermodynamic parameters of adsorption of ammonia nitrogen by modified clay
从表3可看出:改性粘土对氨氮的吸附过程标准摩尔吉布斯自由能变△Gθ<0,说明该吸附作用过程是自发进行的。随着温度的升高,△Gθ的绝对值减小,说明升温使得反应推动力变小,对吸附作用的进行不利;吸附过程的标准摩尔焓变△Hθ<0,说明改性粘土吸附氨氮的过程属于放热反应;标准摩尔熵变△Sθ<0,说明氨氮在改性粘土表面的吸附,混乱程度逐渐减弱,有序性逐渐增加。
在固液吸附体系中,标准摩尔吉布斯自由能变决定吸附的推动力和吸附优先性,化学吸附的自由能变大于物理吸附的自由能变,化学吸附的标准摩尔吉布斯自由能在-400 kJ/mol~-80 kJ/mol范围内,物理吸附的标准摩尔吉布斯自由能在-20 kJ/mol~0 kJ/mol范围内。根据表3中标准摩尔吉布斯自由能△Gθ的实验数据,HDTMA改性粘土吸附垃圾渗滤液氨氮的过程也属于物理吸附。物理吸附的吸附热一般小于化学吸附,化学吸附吸附热在84 kJ/mol~417 kJ/mol范围内[8];表中△Hθ的数据可看出,HDTMA改性粘土吸附渗滤液中主要指标的△Hθ的绝对值很小,亦说明该吸附主要为物理吸附过程。
2.5 改性粘土预处理垃圾渗滤液中氨氮的吸附动力学参数
根据2.2章节的实验数据用式(6)和式(7)进行拟合,见图9,并得到动力学相关参数,见表4。

图9 改性粘土吸附氨氮的动力学拟合曲线Fig.9 Kinetic fitting curve of adsorption of ammonia nitrogen onto modified clay
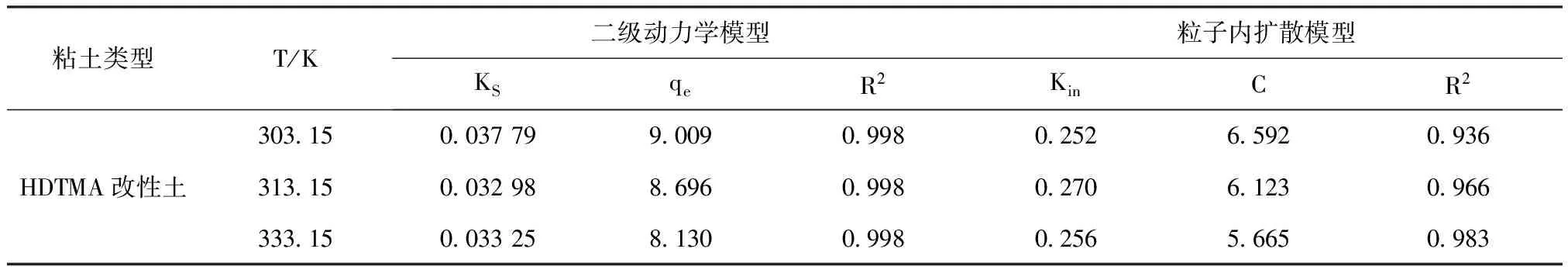
粘土类型T/K二级动力学模型粒子内扩散模型KSqeR2KinCR23031500377990090998025265920936HDTMA改性土31315003298869609980270612309663331500332581300998025656650983
根据图9及表4,将动力学数据用准二级吸附速率方程和粒子内扩散方程进行拟合,结果发现,平衡吸附量的测量值与计算值相差不大,相关系数R2都较高,说明吸附体系动力学符合准二级吸附速率方程和粒子内扩散方程。
由表4可知,在粒子内扩散的方程中,其常量值C不为零,说明在吸附的初始阶段,吸附反应进行很快,但只是改性粘土的表面的吸附,外扩散的过程很快,然后伴随着的才是氨氮的内扩散过程,所以内扩散过程是整个吸附过程的控制步骤,起主要作用。
改性粘土吸附垃圾渗滤液中氨氮时,二级动力学吸附速率方程中的吸附速率常数 KS和qe值随着温度的升高呈减小趋势。说明在实验过程中升温是不利于吸附作用的,改性粘土吸附氨氮的过程是放热过程。
3 讨 论
粘土对污染物质的吸附包括了物理吸附和化学吸附,其中以物理吸附为主。由于物理吸附对同一电性的物质没有选择性进行单层吸附后,被吸附的分子还可以以分子间引力再吸附第二层、第三层,因子可以形成多层分子吸附。同时,粘土本身独特的孔状结构也起着很重要的作用,这不仅是因为孔隙的存在增加了巨大的内表面积使比表面积达到很大的程度,同时还因为被吸附的分子大小必须与孔隙的大小相适应,这样才有利于吸附更好的进行。以十六烷基三甲基溴化铵(HDTMA)作为改性剂改性粘土,使粘土的层间距增大,从而使改性剂吸附在粘土表面及孔隙内,在固体表面形成吸附层,增大了对污染物的吸附。
在氨氮的吸附过程中通常有两种类型的力在起作用:一种作用力与焓变有关,它影响着吸附剂对吸附质的作用力与吸附质和溶剂之间作用力的大小;另一种作用力与熵变有关,它影响的是吸附体系中自由度或者混乱度的变化。与焓变相关的吸附作用力有范德华力、氢键 、配位基交换、偶极间力和化学吸附(共价键的形成)等。在水相中与熵变有关的作用力是指围绕在溶解的吸附质周围的高度规整的水化膜的消失而引起的混乱度的增加[12]。本研究中, △Hθ的绝对值很小,表明吸附过程中无化学键力和配位基交换力,同时由于改性土吸附氨氮的吸附等温线呈线性,主要表现为氨氮在有机改性土中的分配作用,因此推断其主要吸附机制为疏水键力的分配作用,同时可能存在偶极键力和范德华力的作用。
吸附过程的△Sθ为负值,表明垃圾渗滤液中氨氮更倾向于优先选择在改性土表面吸附。一般来说,气体分子在固体上的吸附往往伴随者熵值的变小,因为分子从杂乱无章的气态变成在固体吸附剂表面的整齐排列。而对于从复杂的溶液体系中向表面不均一的改性粘土表面的吸附来说情况并不如此。在固液吸附体系中,同时存在溶质的吸附和溶剂的解吸,溶质分子吸附在吸附剂上,自由度减小,是一熵减小的过程,而溶剂分子的解吸是一熵增大的过程。因为垃圾渗滤液成份复杂,各种有机污染物和无机污染物混合,氨氮分子的吸附引起的熵减小远大于其余组成物质脱附引起的熵增加,从而使熵变为负值,由此也可以判定,改性粘土作为预处理垃圾渗滤液中氨氮的价廉矿物材料,具有较大的开发空间。
4 结 论
4.1 经X射线衍射、红外光谱、热分析手段,对原土和改性后粘土特征进行分析:改性粘土层间间距增大了0.754 nm,HDTMA改性剂分子很好的进入了粘土层间。
4.2 在 303.15 K,313.15 K,333.15 K 不同温度下,粘土吸附渗滤液中氨氮的平衡的时间为50 min左右;原土对氨氮的平衡吸附量在2.80 ~4.00mg/g之间,而改性土对氨氮的平衡吸附量在7.60~8.62mg/g之间。在实验控制条件下,改性后的粘土吸附效果比原土提高了大约2~3倍。
4.3 改性粘土对氨氮的吸附既符合Langmuir等温吸附模型,也符合Freundlich等温吸附模型。吸附过程存在单分子层的吸附,也存在多分子层的吸附。
4.4 改性粘土预处理垃圾渗滤液中氨氮的吸附过程标准摩尔吉布斯自由能△Gθ在-0.127 kJ/mol~-0.080 kJ/mol范围内,说明吸附作用过程是自发进行的,属物理吸附过程;标准摩尔焓变△Hθ<0,属放热反应,温度升高,不利于改性粘土对氨氮的吸附作用的进行。
4.5 改性粘土预处理垃圾渗滤液中氨氮的吸附体系动力学符合准二级动力学方程和粒子内扩散方程,内扩散过程是整个吸附过程的控制步骤,起主要作用。
[1] 邱 瑾.印染废水的脱色治理方法的比较研究[J].环境污染与防治,1994,16 (5):14-16.
[2] 罗筱青.成都粘土的工程地质特性及其评价[J].地质灾害与环境保护,1999,2(10)60-62.
[3] Ramos Vianna1.M.M.G,Dweck.J,Kozievitch V.F.J,etal.Characterization and Study of sorptive Properties of differently Prepared Organoclays from a Brazilian natural Bentonite [J].Journal of Thermal Analysis and Calorimetry,2005,82:595-602.
[4] Qing-ru Zeng,Bo-han Liao,Bo Yang,etal.Sorption of Methyl-parathion and Carbaryl by an Organobentonite [J].Biol Fertil Soils,2006,42:457-463.
[5] 吕 利,吴 勇,张 路,等.改性成都粘土预处理垃圾渗滤液的研究[J].环境科学与技术,2013,36(4):146-151.
[6] 张永民.膨润土改性及其在印染废水处理中的应用研究[D].重庆:重庆工商大学,2009.
[7] 郭照冰,等.磷在蛋壳粉中的吸附热力学和动力学[J].环境化学,2011,30(5):1006-1010.
[8] 赵振国.吸附作用应用原理[M].北京:化学工业出版社,2005:71-76.
[9] 何文光.不均匀表面的吸附平衡与吸附动力学[J].新乡师范学院学报,1962,(2):64-69.
[10] 天津大学物理化学教研室.物理化学(下)[M].天津:高等教育出版社,2001.12.
[11] 赵振国.吸附作用应用原理[M].北京:化学工业出版社,2005:87-97.
[12] 舒月红,贾晓珊.CTMAB-膨润土从水中吸附氯苯类化合物的机理—吸附动力学与热力学[J].环境科学学报,2005,25(11):1530-1536.
