心率变异及皮肤交感反应对帕金森病的鉴别诊断价值
2018-01-10张娟利党亮君邓永宁曹红梅屈秋民西安交通大学第一附属医院神经内科陕西西安710061
张 萌,张娟利,党亮君,邓永宁,曹红梅,屈秋民(西安交通大学第一附属医院神经内科,陕西西安 710061)
心率变异及皮肤交感反应对帕金森病的鉴别诊断价值
张 萌,张娟利,党亮君,邓永宁,曹红梅,屈秋民
(西安交通大学第一附属医院神经内科,陕西西安 710061)
目的探讨心率变异(heart rate variability, HRV)和皮肤交感反应(sympathetic skin response, SSR)对于帕金森病(Parkinson’s disease, PD)鉴别诊断的价值。方法选取西安交通大学第一附属医院神经内科门诊及住院临床确诊的36例PD、17例特发性震颤(essential tremor, ET)及59例非典型帕金森症(Parkinsonism-Plus, PD-plus)患者,测定平静呼吸、深呼吸、Vasaval动作时HRV指数及四肢的SSR潜伏期。结果①平静呼吸时PD组较ET组HRV指数降低,HRV异常率高,差异具有统计学意义(P<0.05),PD组与PD-plus组间HRV差异无统计学意义,深呼吸及Vasaval动作时三组间差异无统计学意义;②上肢、下肢SSR潜伏期均值及异常率在PD组、PD-plus 组及ET组间差异无统计学意义;③HRV指数区别PD和PD-plus的灵敏度为82.6%、特异度为22.8%;区别PD和ET的灵敏度为82.6%、特异度为66.9%。测定SSR潜伏期区别PD和PD-plus的灵敏度为52.6%、特异度为39.0%;区别PD和ET的灵敏度为52.6%、特异度为29.4%。结论PD患者较ET患者HRV降低,HRV异常率高;测定HRV指数有助于鉴别PD和ET,但是对于鉴别PD和PD-plus价值不大;测定SSR潜伏期对于鉴别PD、PD-plus及ET价值不大。
帕金森病;鉴别诊断;自主神经障碍;心率变异;皮肤交感反应
帕金森病(Parkinson’s disease, PD)是常见的神经系统变性疾病,目前诊断主要依据临床表现。研究发现,70%~80% PD患者存在自主神经功能障碍(autonomic nervous system dysfunction, ANSD),且ANSD可能发生于运动症状之前[1-3]。在2015年国际运动障碍协会(International Movement Disorders Association, MDS)PD诊断标准中,MIBG(间碘苄胍,metaiodoenzylguanidine)显像心脏去交感神经支配作为PD支持标准之一,早期严重ANSD(直立性低血压和排尿障碍)作为PD的警示特征,提示ANSD对于PD的诊断和鉴别诊断具有重要价值。既往PD的ANSD研究多采用多汗、便秘、流涎等临床表现的观察记录,受被检查者主观因素影响较多,缺乏客观的检查指标。随着神经电生理技术的发展,心率变异(heart rate variability, HRV)、皮肤交感反应(sympathetic skin response, SSR)可以客观、量化地评价ANSD,但是HRV和SSR在PD鉴别诊断中的价值尚不明确。为此,本研究比较了PD、非典型帕金森症(Parkinsonism-plus, PD-plus)、特发性震颤(essential tremor, ET)患者HRV指数及SSR潜伏期的差异,探讨HRV、SSR对于PD鉴别诊断的价值。
1 资料与方法
1.1病例来源收集2013年1月至2016年2月在西安交通大学第一附属医院神经内科门诊或住院的临床确诊的PD、ET、PD-plus患者作为研究对象,全部研究对象由神经内科两名教授独立作出相应诊断。PD诊断符合英国PD协会(UKPDS)诊断标准[4],且抗PD治疗效果明显;ET和PD-plus的诊断分别参考BAIN[5]和GILMAN等[6]提出的诊断标准。排除继发性帕金森综合征、心律失常及糖尿病患者,所有研究对象均未服用抗心律失常药物及影响自主神经功能的药物,自愿参加本研究,并签署知情同意书。
1.2HRV及SSR检测HRV和SSR检测采用美国Medtronic公司生产的Keypoint台式肌电-诱发电位仪。HRV检测分别记录受试者平静呼吸、深呼吸、Vasaval动作时的HRV指数。异常结果判断:正常呼吸HRV指数<10%,深呼吸HRV指数<20%,Vasaval动作时HRV指数<1.00。SSR检测,受试者仰卧放松,室温25 ℃,上肢记录点击置于手心,参考电极置于手背;下肢记录电极置于足心,参考电极置于足背,每名受试者记录4次,每次刺激间隔时间在1 min以上,观察出波情况并测量其潜伏期。异常结果判断:上肢潜伏期>1 600 ms、下肢潜伏期>2 200 ms或波形未引出。

2 结 果
2.1PD、PD-plus、ET组间患者一般资料的比较共纳入PD患者36例,其中男性18例(50.0%),年龄30~76岁(60.0±2.3岁)。PD-plus患者59例,其中男性28例(47.5%),年龄29~80岁[(52.1±1.3)岁]。ET患者17例,男性8例(47.1%),年龄33~76岁[(55.9±2.9)岁]。3组性别、年龄比较,差异均无统计学意义(均P>0.05,表1)。
表1PD、PD-plus、ET组间患者一般资料的比较
Tab.1 Comparison of general data among PD, PD-plus and ET groups
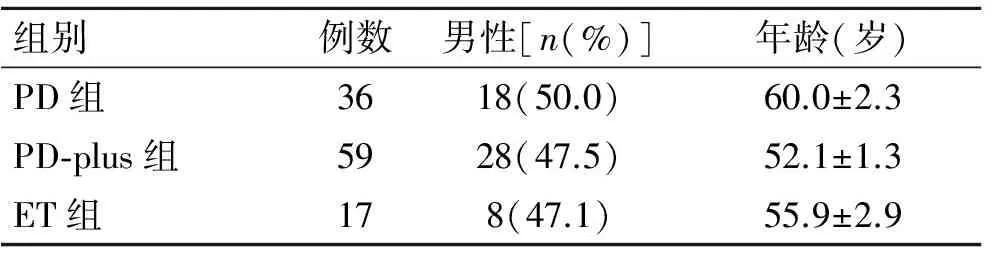
组别例数男性[n(%)]年龄(岁)PD组3618(50.0)60.0±2.3PD⁃plus组5928(47.5)52.1±1.3ET组178(47.1)55.9±2.9
2.2PD、PD-plus、ET组间HRV指数的比较平静呼吸时ET组HRV指数显著高于PD组(P=0.017),PD组和PD-plus组相比HRV指数差异无统计学意义;深呼吸及Vasaval动作时3组间HRV指数差异无统计学意义。HRV异常率ET组较PD组显著降低(P=0.001),PD组及PD-plus组间HRV异常率差异无统计学意义(表2)。
表2PD、PD-plus、ET组间HRV指数的比较
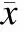

与PD组比较,*P<0.05。
2.3PD、PD-plus、ET组间SSR的比较SSR潜伏期在PD组、PD-plus组及ET组间差异无统计学意义。SSR潜伏期异常率在3组间差异无统计学意义(表3)。
表3PD、PD-plus、ET组间SSR潜伏期的比较
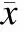
2.4HRV、SSR对PD、PD-plus及ET鉴别诊断的敏感性、特异性分析HRV指数区别PD和PD-plus的灵敏度为82.6%、特异度为22.8%、约登指数为0.05;区别PD和ET的灵敏度为82.6%、特异度为66.9%、约登指数为0.5。测定SSR潜伏期区别PD和PD-plus的灵敏度为52.6%、特异度为39.0%;区别PD和ET的灵敏度为52.6%、特异度为29.4%(表4、表5)。
表4HRV、SSR对PD、PD-plus鉴别诊断的价值
Tab.4 Value of HRV and SSR in differential diagnosis of PD and PD-plus
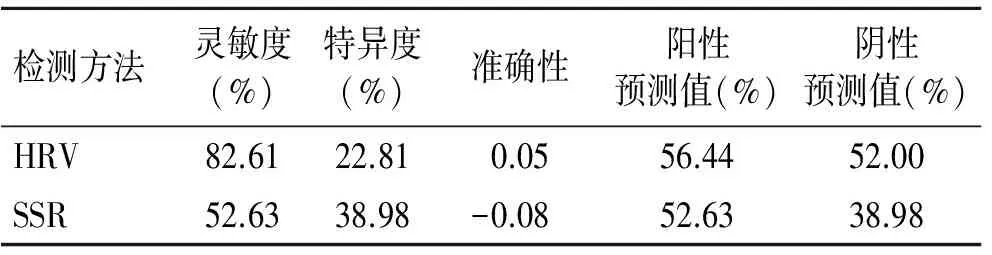
检测方法灵敏度(%)特异度(%)准确性阳性预测值(%)阴性预测值(%)HRV82.6122.810.0556.4452.00SSR52.6338.98-0.0852.6338.98
表5HRV、SSR对PD、ET鉴别诊断的价值
Tab.5 Value of HRV and SSR in differential diagnosis of PD and ET
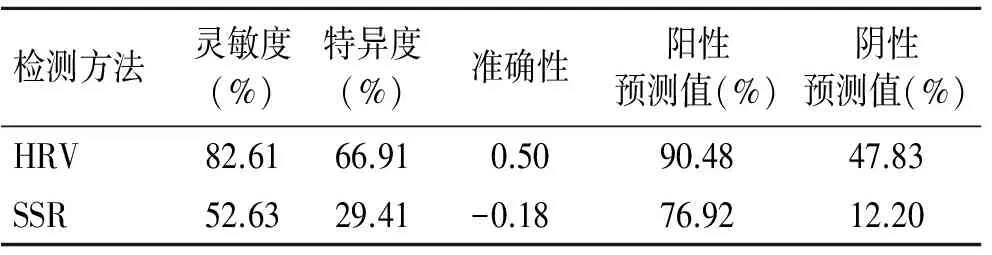
检测方法灵敏度(%)特异度(%)准确性阳性预测值(%)阴性预测值(%)HRV82.6166.910.5090.4847.83SSR52.6329.41-0.1876.9212.20
3 讨 论
PD是一种常见于中老年的神经变性疾病,临床症状主要包括静止性震颤、运动迟缓、肢体僵硬、姿势平衡障碍等运动症状及嗅觉减退、便秘、睡眠行为异常、抑郁等非运动症状。非运动症状在PD患者中十分常见,其发生率、发生类型与性别、年龄相关[7]。研究者发现PD患者的运动症状越重,其自主神经症状就越明显。许多疾病临床表现出现运动障碍,需要与PD鉴别诊断。如ET表现为手、头部及身体其他部位的姿位性和运动性震颤,PD-plus表现为静止性震颤,这些疾病与原发性PD的临床特点相似,尤其在疾病早期,造成原发性PD确诊具有一定困难[8]。
HRV作为近年来比较受关注的非侵入性检查方法,很多临床研究结果显示其对研究自主神经功能及其调节具有重要意义,如冠心病、高血压、心肌梗死、糖尿病等疾病研究[9]。HRV是反映窦性心搏逐次之间的变异程度,可反映心脏自主神经的调节功能。HRV的变化可作为健康受损的早期监控指标:HRV升高是健康人自主神经调节功能强的表现,HRV降低常常提示自主神经调节功能受损[9]。研究者发现,PD患者HRV各指标显著低于健康对照组[10-11]。本研究结果显示,在平静呼吸情况下,PD组较ET组间HRV指数明显降低,HRV异常率升高,提示PD患者存在自主神经功能损害。结合灵敏度、特异度分析结果,HRV指数对于鉴别PD和ET具有一定价值,但是对于鉴别PD和PD-plus价值不大。
SSR是中枢神经系统参与下的催汗反应,涉及中枢神经系统,主要反映泌汗体表电压的变化情况,是一种无创、易操作的检查自主神经的电生理方式,因其较少受情绪、药物等因素的影响,被认为结果能较为客观反应周围神经或中枢神经系统损伤而引起的自主神经功能障碍。既往研究者发现,PD患者与正常对照组相比,SSR潜伏期延长、波幅降低,且PD患者SSR变化与患者年龄、病情严重程度、病程相关[12],均提示PD患者存在一定的自主神经功能损害,SSR可作为判断患者自主神经调节功能的参考指标。本研究结果发现,SSR潜伏期在PD组、PD-plus组及ET组间差异不具有统计学意义。且SSR潜伏期对于区别PD、PD-plus及ET患者的灵敏度、特异度不高,提示SSR潜伏期对于鉴别PD、PD-plus及ET价值不大。
PD的病理基础是中脑黑质致密部多巴胺能神经元减少50%以上,导致产生的多巴胺减少,与其拮抗的递质-乙酰胆碱相对增多,功能亢进。自主神经功能损害是PD的非运动症状重要表现之一。其原因可能是:PD病变除位于黑质、蓝斑外,还可累及到丘脑背部、迷走神经背核、交感神经节、肾上腺髓质等,出现Lewy小体、神经细胞脱失及胶质细胞增生等病理变化,神经元的广泛损伤则会导致自主神经功能的障碍,导致相应的自主神经功能障碍[13]。
ET表现为手、头部及身体其他部位的姿位性和运动性震颤,是缓慢进展的,在注意力集中、精神紧张、疲劳、饥饿时加重,多数病例在饮酒后暂时消失,次日加重;可能是与家族遗传相关的复杂性疾病。目前确切病因仍不清楚,病理解剖没有特异性改变[14]。PD-plus又称非典型性帕金森样病,是一种慢性进行性神经变性疾病,常见的类型包括进行性核上性麻痹(progressive supranuclear palsy, PSP)、多系统萎缩(multiple system atrophy, MSA)以及皮质基底节变性(corticobasal degeneration, CBD)。PSP表现为核上性眼球运动障碍、假性球麻痹、构音障碍、颈部肌张力障碍、痴呆等;脑部形态变化是中脑、小脑上脚萎缩和顶叶皮质萎缩。MSA散发、进展快速,病理上主要以黑质、纹状体、脑干、小脑核、脊髓中间外侧束的胶质细胞和神经元内嗜银α-突触核蛋白阳性包涵体为特征。CBD罕见,表现为不对称性肢体运动症状,伴有不同程度的认知功能障碍或痴呆;常规头颅MRI表现为不对称额叶或额顶叶萎缩[15-16]。总之,PD、PD-plus及ET患者的病因、发病机制、临床表现均不同,导致其自主神经损害不同。
综上所述,HRV及SSR作为PD的自主神经功能检测的有价值的、可被量化的、客观的检查手段,其中HRV可被用于PD、ET的鉴别诊断,对于早期诊断PD,指导早期的治疗,有重要的意义。HRV对于鉴别PD和PD-plus价值不大,SSR潜伏期对于鉴别PD、PD-plus及ET价值不大,故尚需研究发现其他手段作为PD早期鉴别诊断的有力工具。
[1] GOLDSTEIN DS. Dysautonomia in Parkinson disease[J]. Compr Physiol, 2014, 4(2):805-826.
[2] ASAHINA M, VICHAYANRAT E, LOW DA, et al. Autonomic dysfunction in parkinsonian disorders: Assessment and pathophysiology[J]. J Neurol Neurosurg Psychiatry, 2013, 84(6):674-680.
[3] 张克忠,张廉,袁永胜,等. 帕金森病患者非运动症状的临床特征分析[J]. 川北医学院学报, 2012, 27(4):327-330
[4] BERARDELLI A, WENNING GK, ANTONINI A, et al. EFNS/MDS-ES/ENS [corrected] recommendations for the diagnosis of Parkinson’s disease[J]. Eur J Neurol, 2013, 20(1):16-34.
[5] BAIN P, BRIN M, DEUSCHL G, et al. Criteria for the diagnosis of essential tremor[J]. Neurology, 2000, 54(11 Suppl 4):S7.
[6] GILMAN S, WENNING GK, LOW PA, et al. Second consensus statement on the diagnosis of multiple system atrophy[J]. Neurology, 2008, 71(9):670-676.
[7] 张树山,朱陶,李程旭,等. 帕金森病非运动症状临床特点研究[J]. 川北医学院学报, 2016, 31(4):520-524.
[8] 胡智伟,邹小冬. 具有帕金森样症状患者相关疾病探讨[J]. 脑与神经疾病杂志, 2012, 20(1):31-34.
[9] VANDERLEI LC, PASTRE CM, HOSHI RA, et al. Basic notions of heart rate variability and its clinical applicability [J]. Rev Bras Cir Cardiovasc, 2009, 24(2):205-217.
[10] DELGADO G, ESTANOL B, RODRIGUEZ-VIOLANTE M, et al. Cardiovascular variability in Mexican patients with Parkinson’s disease[J]. Arq Neuro-psiquiatr, 2014, 72(10):762-767.
[11] 陈琳,黄卫. 帕金森病患者心血管自主神经功能障碍的临床研究[J]. 临床神经病学杂志, 2016, 29(3):190-193
[12] KOSZEWICZ M, MENDAK M, KONOPKA T, et al. The characteristics of autonomic nervous system disorders in burning mouth syndrome and Parkinson disease[J]. J Orofac Pain, 2012, 26(4):315-320.
[13] RAJPUT AH, ROZDILSKY B. Dysautonomia in Parkinsonism: A clinicopathological study[J]. J Neurol Neurosurg Psychiatry, 1976, 39(11):1092-1100.
[14] 潘觉宜. 帕金森震颤和特发性震颤的肌电图震颤分析[D]. 长春:吉林大学, 2016.
[15] 冯结映,黄飚,钟小玲,等. 帕金森病和帕金森叠加综合征的影像诊断[J]. 放射学实践, 2013, 28(11):1105-1108.
[16] 王冰,张芳. 帕金森叠加综合征患者生存质量影响因素[J]. 郑州大学学报(医学版), 2010, 45(2):252-255.
ValueofheartratevariabilityandsympatheticskinresponseindifferentialdiagnosisofParkinson’sdisease
ZHANG Meng, ZHANG Juan-li, DANG Liang-jun, DENG Yong-ning,CAO Hong-mei, QU Qiu-min
(Department of Neurology, the First Affiliated Hospital of Xi’an Jiaotong University, Xi’an 710061, China)
ObjectiveTo evaluate the value of heart rate variability (HRV) and sympathetic skin response (SSR) in differential diagnosis of Parkinson’s disease (PD).MethodsWe selected 36 PD, 17 essential tremor (ET) and 59 Parkinsonism-Plus (PD-plus) patients diagnosed in our department. We recorded HRV during the period of quiet breath, deep breath and Vasaval as well as SSR incubation period of the upper limbs and lower limbs.Results① During the period of quiet breath, HRV decreased significantly in PD group compared with that in ET group (P<0.05), and abnormality rate of HRV in PD group was higher than that in ET group. HRV did not significantly differ between PD and PD-plus. HRV did not significantly differ among the three groups during the period of deep breath and Vasaval. ② SSR incubation period showed no significant difference among PD, PD-plus and ET groups. ③ The specificity and sensibility of HRV in PD and PD-plus differential diagnosis were 22.8% and 82.6%, while for PD and ET differential diagnosis the values were 66.9% and 82.6%. The specificity and sensibility of SSR in PD and PD-plus differential diagnosis were 39.0% and 52.6%, 29.4% and 52.6%, respectively, for PD and ET differential diagnosis.ConclusionCompared with those in ET patients, HRV in PD patients decreases and HRV abnormality rate increases. HRV is of great value in differential diagnosis of PD and ET but not in differential diagnosis of PD and PD-plus. Determining SSR incubation period does not have much value in differential diagnosis of PD, PD-plus and ET.
Parkinson’s disease; differential diagnosis; autonomic nervous system dysfunction; heart rate variability; sympathetic skin response
2017-07-09
2017-09-27
国家自然科学基金资助项目(No.81301097)
Supported by the National Natural Science Foundation of China (No.81301097)
屈秋民,主任医师. E-mail: quqiumin@medmail.com.cn;张娟利为共同第一作者.
优先出版:http://kns.cnki.net/kcms/detail/61.1399.R.20171205.1533.012.html(2017-12-05)
R742.5
A
10.7652/jdyxb201801020
(编辑 韩维栋)
