透彻剖析典型考题
2018-01-02朱怀义
朱怀义
(江苏省睢宁高级中学北校 221200)
透彻剖析典型考题
朱怀义
(江苏省睢宁高级中学北校 221200)
以“酸碱中和滴定”内容的考题为例,介绍了搞好习题教学的方法.
高考题;剖析;化学
典型考题【2010年上海高考11】将0.40gNaOH和1.06gNa2CO3混合并配成溶液,向溶液中滴加0.10mol·L-1稀盐酸.下列图像能正确表示加入盐酸的体积和生成CO2的物质的量的关系的是( )
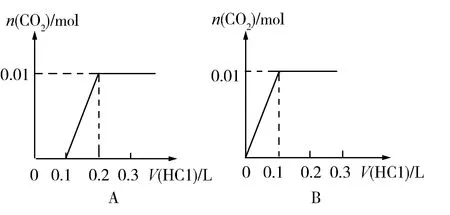
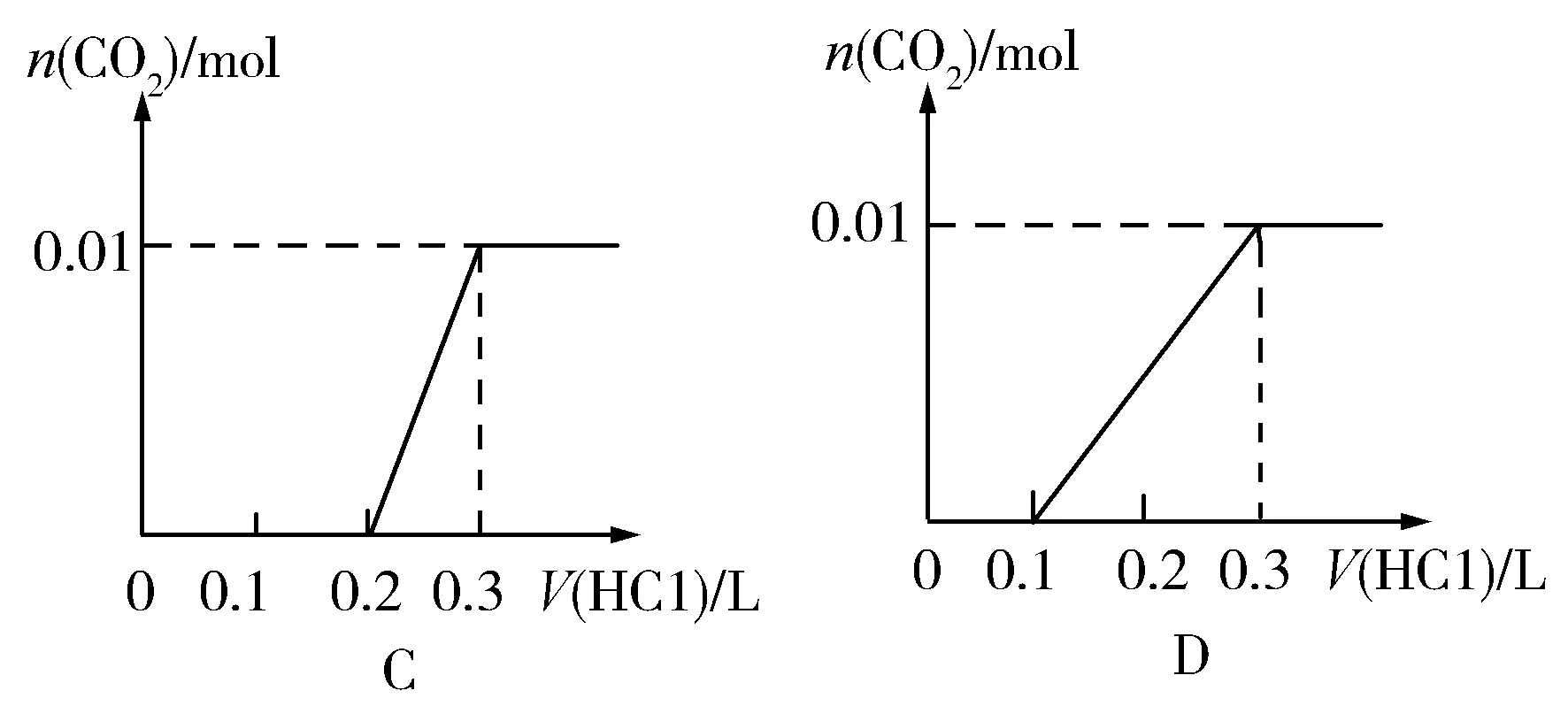
简析学生认为,向混合溶液中滴加稀盐酸,发生的离子反应为:

①
②
所以有不少学生错选了D.“错误亦美丽”,学生毕竟认识到反应有先后,不足之处是没有真正认识“向碳酸钠溶液中滴加稀盐酸”的微观过程.
剖析1 强化量变意识,细化“滴定”反应历程.
酸碱中和滴定临近终点时,少一滴、多一滴都会导致混合液pH发生突变,但滴定是有方向性的,方向性决定了反应物相对物质的量多少,将导致反应历程变化,这点可能被弱化了.
矫正练习【《化学1》第62页7(2)】(苏教2014年版)少量碳酸钠与盐酸反应,有二氧化碳气体放出;而少量盐酸与过量碳酸钠溶液反应,则生成碳酸氢钠和氯化钠,无气体放出.请写出上述过程中发生反应的离子方程式.
少量碳酸钠与盐酸反应,相当于将碳酸钠溶液滴向盐酸,发生反应②;而将盐酸滴向碳酸钠溶液,相当于少量盐酸与过量碳酸钠溶液反应,开始无气体,发生反应
③
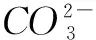
④
所以,上述考题答案为C.
剖析2 密切知识关联,逐渐丰厚知识链节.
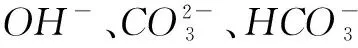
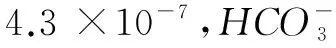
矫正练习【据《化学1》第62页7(1)改编】(苏教2014年版)碳酸氢钠是一种酸式盐,既可以与酸反应,又可以与碱反应.请写出碳酸氢钠溶液分别与盐酸和氢氧化钠溶液反应的离子方程式.
结合以上分析可知,向NaOH和Na2CO3混合溶液中逐滴滴加盐酸,发生多步反应的顺序为①③④,而不是③①④、也不是③④①.请你说明其中原因.
碳酸氢钠溶液与盐酸反应离子方程式为④, 碳酸氢钠溶液与氢氧化钠溶液反应离子方程式为
⑤

⑥
⑦
这提醒学生在恪守知识学习的循序渐进性时,要适时沟通知识的前后联系,以达融会贯通之效.
剖析3 展开变式训练,当堂检测学生的理解程度.
并不忌讳“听不懂课、听懂但不会解题”现象的普遍存在;剖析例题,实际是教师在做示范,效果如何是不能以教师的良好感觉为准的.根据题意,当堂展开变式训练,可检测出学生的理解和运用的真实情况.
变式练习某化学兴趣小组,向某浓度的NaOH溶液中缓慢、持续通入一段时间CO2气体,分析所得溶液溶质组成的可能情况;若取一定体积的反应后所得溶液,并向溶液中逐滴滴加稀盐酸,请绘制表示加入盐酸的体积和生成CO2的物质的量的关系的图像.
简析向NaOH溶液中缓慢持续通入CO2气体,先发生反应⑥,实现NaOH向Na2CO3的转化,再发生反应⑦,实现Na2CO3向NaHCO3的转化.所得溶液溶质的组成情况可能有四种:NaOH和Na2CO3、Na2CO3、Na2CO3和NaHCO3、NaHCO3;表示加入盐酸的体积和生成CO2的物质的量的关系的图像依次与例题C、A、D、B相似.
剖析4 展开拓展训练,实现解题能力质的提升.
拓展练习【2014年上海高考20,B选项有变化】向等物质的量的NaOH和Na2CO3溶液的混合溶液中加入盐酸,下列离子方程式与事实不符合的是( ).


不同省、市的多年高考,为突破教学重点、高考热点提供了十分难得的训练题源.在平时教学时,要不厌其烦地向学生传递“出错不可怕,通过纠错,将迈上新台阶,获得更大提升”的“错误观”.例题讲解的关键在于引导,学生若能因此走出认识误区、丰富知识体系,优化思维品质、提升解题素养,则更显教师的能力非凡!以上感悟,如有不当之处,敬请指正.
[1]人民教育出版社,课程教材研究所,化学课程研究开发中心. 化学选修5-有机化学基础[M](第2版).北京:人民教育出版社,2007(2).
G632
A
1008-0333(2017)31-0074-02
2017-07-01
朱怀义,睢宁高级中学北校化学教研组长,县高中化学学科带头人.
季春阳]
