刺五加配方颗粒质量标准研究
2017-12-20郑晓英黄俊忠
谭 沛 ,郑晓英 ,黄俊忠 ,张 辉
(1.华润三九医药股份有限公司,广东 深圳 518110; 2.广东省食品药品检验所,广东 广州 510180)
刺五加配方颗粒质量标准研究
谭 沛1,郑晓英1,黄俊忠2,张 辉1
(1.华润三九医药股份有限公司,广东 深圳 518110; 2.广东省食品药品检验所,广东 广州 510180)
目的建立刺五加配方颗粒的质量标准。方法采用薄层色谱(TLC)法,以刺五加对照药材和异嗪皮啶对照品作为阳性对照,对刺五加配方颗粒进行定性鉴别;采用高效液相色谱(HPLC)法测定刺五加配方颗粒中紫丁香苷成分含量,并进行方法学验证。结果定性鉴别中,刺五加配方颗粒斑点分离清晰;含量测定中,紫丁香苷进样量在0~5.668 g范围内与峰面积线性关系良好(r=0.9995),平均回收率为98.62%,RSD=1.16%(n=6)。结论所建立的定性及定量方法简单可行,精密度及重复性良好,可用于刺五加配方颗粒的质量控制。
刺五加;配方颗粒;紫丁香苷;薄层色谱法;高效液相色谱法;质量控制
刺五加收载于2015年版《中国药典(一部)》,为五加科植物刺五加 Acanthopanax senticosus(Rupr.et Maxim.)Harms的干燥根和根茎或茎,有益气健脾、补肾安神功效,主要用于治疗脾肺气虚、体虚乏力、食欲不振、肺肾两虚、久咳虚喘、肾虚腰膝酸痛、心脾不足、失眠多梦[1]。其药用部位主要有根、根茎及茎,主要成分有刺五加苷、甾体苷、酚苷、香豆精苷、木脂素苷等,含量也不尽相同,其中刺五加苷以紫丁香苷含量最高[2-4],且紫丁香苷为主要的活性指标成分,同时也是现行2015年版《中国药典(一部)》刺五加药材项下的含量测定指标成分。刺五加配方颗粒是由刺五加饮片经现代水提取、浓缩、干燥、制粒技术制成的模拟传统水煎液的颗粒,相对于传统水煎液具有携带、保持方便,质量稳定等优势。目前关于刺五加药材及相关复方制剂的研究报道较多,其质量控制方法也较多,但刺五加配方颗粒研究基础较薄弱,有关研究报道仅1篇,尚无关于其质量标准的研究。为此,本研究中参考现行版《中国药典(一部)》刺五加项下有关内容的规定,采用薄层色谱(TLC)法对刺五加配方颗粒中异嗪皮啶及刺五加对照药材进行专属性鉴别,并参考相关文献[5-15]建立了测定刺五加配方颗粒中紫丁香苷含量的高效液相色谱(HPLC)法,旨在为刺五加配方颗粒的质量控制提供科学依据,以期探讨刺五加饮片经现代技术生产制成刺五加配方颗粒的质量成分变化,以达到从整体上控制刺五加配方颗粒质量的目的。现报道如下。
1 仪器与试药
1.1 仪器
Agilent1100型高效液相色谱仪,包括Agilent化学工作站,G1314A型紫外检测器,G1313A型自动进样器(安捷伦科技<中国>有限公司);色谱柱:InertSustain C18柱 (250mm ×4.6mm,5 μm);CPA224S 型万分之一电子分析天平,CP225D型十万分之一电子分析天平(德国 Sartorius公司);KQ-300DE型超声提取器(昆山市超声仪器有限公司)。
1.2 试药
刺五加配方颗粒(共15批,批号代号分别为 A1,A2,A3,…,A15,由 6 家配方颗粒生产企业提供);刺五加对照药材(批号为 120991-200807)、异嗪皮啶对照品(批号为 110837-200304,规格 20mg,纯度 99.5% ,供含量测定用)、紫丁香苷对照品(批号111754-200603,规格20mg,纯度100%,供含量测定用,经五氧化二磷减压干燥12 h以上后使用),均购自中国食品药品检定研究院。甲醇(Merck公司,批号为3CH0025)为色谱纯,水为超纯水;其他试剂均为分析纯。
2 方法与结果
2.1 TLC 鉴别
2.1.1溶液制备
取本品粉末 1 g,加75%乙醇 50m L,超声 30 min,滤过,滤液蒸干,残渣加水10m L使溶解,用三氯甲烷振摇提取2次,每次5mL,合并三氯甲烷液,蒸干,残渣加甲醇1mL使溶解,作为供试品溶液。取刺五加对照药材5 g,加75%乙醇 50 mL,同法制成对照药材溶液。取异嗪皮啶对照品,加甲醇制成每1 mL含1mg的溶液,作为对照品溶液。
2.1.2薄层色谱试验
照薄层色谱法(2015年版《中国药典(四部)》通则0502)试验,吸取供试品溶液和对照药材溶液各10μL,对照品溶液1μL,分别点于同一硅胶G薄层板上,以三氯甲烷-甲醇(19∶1)为展开剂,展开,取出,晾干后置紫外光灯(365 nm)下检视。结果供试品溶液色谱中,在与对照药材溶液色谱及对照品溶液色谱相应位置上显相同颜色荧光斑点(见图1)。本试验中还考察了不同试验温度、湿度以及不同厂家的硅胶G板对结果的影响,结果表明,该方法所建立的定性方法具有较好的耐用性及专属性。

图1 刺五加配方颗粒薄层鉴别色谱图
2.2 紫丁香苷含量测定
2.2.1色谱条件与系统适用性试验
色谱柱:InertSustain C18柱 (250mm ×4.6mm,5μm);以十八烷基硅烷键合硅胶为填充剂;流动相:甲醇-水(20 ∶80);检测波长:265 nm;流速:1 mL /min;进样量:10μL。理论板数按紫丁香苷峰计算应不低于3000。系统适用性HPLC色谱图见图2。
2.2.2溶液制备
对照品溶液:称取紫丁香苷对照品0.02834 g,精密称定,置25mL容量瓶中,加水溶解,定容至刻度,摇匀,即得对照品溶液Ⅰ。精密吸取对照品溶液Ⅰ2 mL,置25 mL容量瓶中,加水溶解,定容至刻度,摇匀,即得每1mL含紫丁香苷0.090688mg的溶液,作为对照品溶液Ⅱ。
供试品溶液:取本品适量,研细,取约1.5 g,精密称定,置具塞锥形瓶中,精密加水25mL,密塞,称定质量,超声处理(功率 300W,频率 40 kHz)30min,放冷,再称定质量,用水补足减失的质量,摇匀,离心5min(转速为3000 r/min),取上清液,滤过,取续滤液,即得。
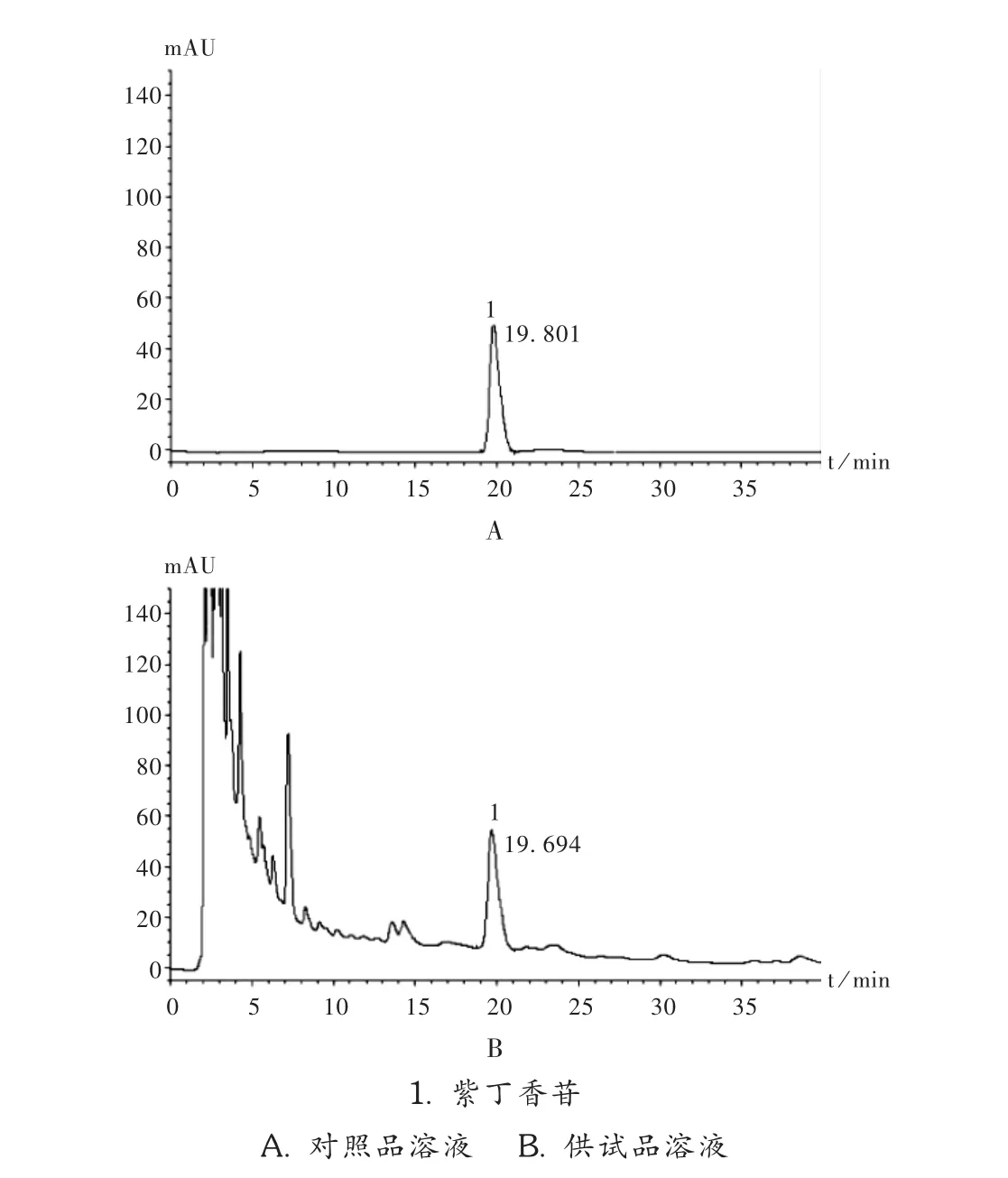
图2 系统适用性高效液相色谱图
2.2.3方法学考察
线性关系考察:精密吸取对照品溶液Ⅱ1,3,10μL,对照品溶液Ⅰ1,3,5μL,按拟订色谱条件进样测定,以进样量为横坐标、峰面积为纵坐标(Y)进行线性回归,得回归方程 Y=2290.7X+149.12,r=0.9995(n=6)。结果表明,紫丁香苷进样量在0~5.668μg范围内与峰面积线性关系良好。
精密度试验:精密吸取对照品溶液10μL,按拟订色谱条件重复进样6次,测定紫丁香苷峰面积。结果的RSD为0.1%(n=6),表明仪器精密度良好。
重复性试验:取同一批样品(批号代号为A3)6份,精密称定,依法制备供试品溶液,分别按拟订色谱条件进样,测定紫丁香苷的含量。结果平均含量为 1.44 mg/g,RSD为1.0%(n=6),表明方法重复性良好。
稳定性试验:取同一批刺五加配方颗粒(批号代号为A3),依法制备供试品溶液,按拟订色谱条件,分别于0,6,12,24,36,48 h 时进样 10 μL,测定紫丁香苷峰面积。结果的 RSD为 1.2%(n=6),表明供试品溶液在48 h内稳定。
加样回收试验:取已知含量的同一批样品(批号代号为 A3,含量为 1.4382 mg /g)6 份,每份取约 0.75 g,精密称定,分别置预先加入用甲醇配制、质量浓度为1.132 g/L的紫丁香苷对照溶液1m L并已挥干的锥形瓶中,依法制备供试品溶液,按拟订色谱条件进样,测定含量,计算回收率。结果见表1。
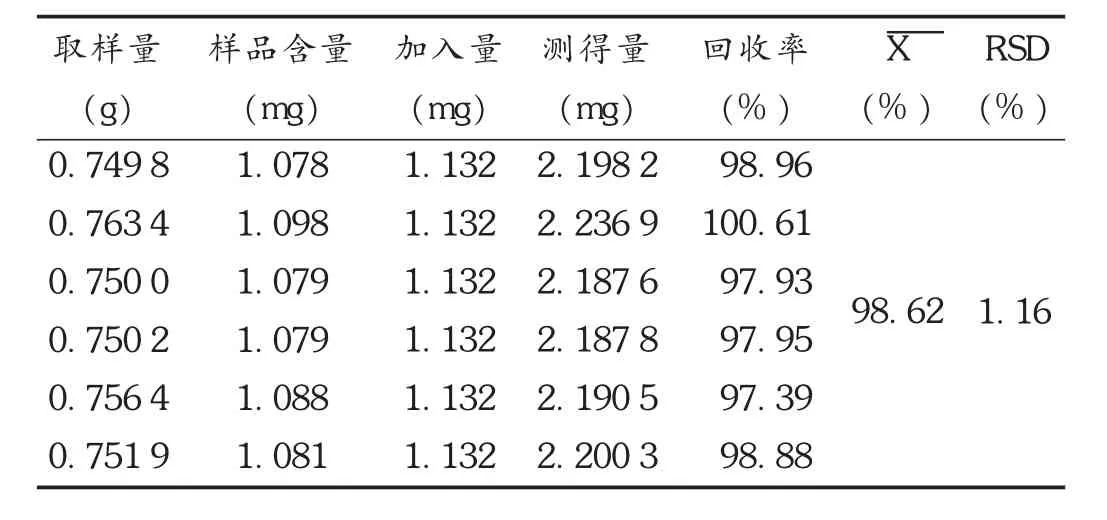
表1 紫丁香苷加样回收试验结果(n=6)
2.2.4样品含量测定
分别精密称取15批刺五加配方颗粒,依法制备供试品溶液,按拟订色谱条件进样,测定紫丁香苷含量。结果见表2。

表2 15批刺五加配方颗粒样品紫丁香苷含量测定结果(n=2)
3 讨论
3.1 TLC 法
刺五加配方颗粒为单方颗粒制剂,制备过程中只加入了少量麦芽糊精作为赋形剂,研究表明,其对TLC鉴别和含量测定无干扰。本试验中还考察了高温、低温、高湿、低湿及不同厂家薄层板对方法耐用性的影响,并对15批样品进行定性鉴别,结果薄层色谱斑点分离清晰,方法重复性较好。
3.2 HPLC 法
本试验中建立的紫丁香苷含量测定方法,主要参考2015年版《中国药典(一部)》刺五加【含量测定】项下方法制订。考虑到刺五加配方颗粒经水提取工艺制成,水溶性较好,与刺五加药材存在一定的差异。因此,本试验中考察了渗透性和水溶性较好的两种不同提取溶剂(甲醇、水),结果两者的提取效率一致,溶解效果较好。考虑到甲醇的有机毒性比水大,本试验中选择了较环保的水作为提取溶剂。本试验中还考察了提取时间及比较了不同取样量的提取效果,确定最佳供试品溶液提取条件。经方法学验证,本研究中建立的方法稳定性、精密度较好,线性及重复性良好,准确度高,耐用性良好。
3.3 含量差异原因分析
刺五加配方颗粒为刺五加饮片在临床的补充剂型,相对而言更有质量可控、稳定、均一的优势,但实测15批刺五加配方颗粒中紫丁香苷的含量结果差异较大,低于或接近刺五加饮片含量的均有2批,与实际当量不符。分析原因可能有以下几个方面。
原料刺五加饮片的自身差异:不同年生植物中,以4年生和5年生含量最高;不同产地植物中,道地东北地区因其适宜的生产环境,紫丁香苷的含量稍高于其他产地,而在通化地区和临江地区其苷含量会随着季节变化而变化,表现为春秋季较高,夏季较低,其主要原因可能也与紫丁香苷的化学性质及其次生代谢有关[12];不同种群结构,因其种植样地的种群密度、生物量及种群中紫丁香苷的产量均不一致以及不同药用部位中的紫丁香苷含量均不同[7,16]。
缺乏统一的生产标准:由于目前配方颗粒尚无统一的生产工艺和质量控制标准,紫丁香苷的含量也会因生产工艺参数及其规模的差异而不同。
厂家包装差异:每个生产厂家的实际包装当量不一致及大、小包装的当量差异引起紫丁香苷的含量差异。
样品稳定性:刺五加配方颗粒样品的稳定性也会对其含量产生影响。
综上所述,本研究中建立的刺五加配方颗粒定性及定量方法简单可行,精密度及重复性良好,可为刺五加配方颗粒的质量控制提供借鉴。同时,在对刺五加配方颗粒含量分析时,需注意其样品代表性以及取样的影响,全面考虑其含量差异,并进一步对原料进行系统性研究,以分析不同刺五加配方颗粒中紫丁香苷含量存在差异的原因。
[1]国家药典委员会.中华人民共和国药典(一部)[M].北京:中国医药科技出版社,2015:206-207.
[2]侯团章.中草药提取物(第一卷)[M].北京:中国医药科技出版社,2004:119-128.
[3]张 晶,刘芳芳,薛 起,等.HPLC法测定刺五加不同部位刺五加苷 B、E 含量[J].药物分析杂志,2008,28(12):2018-2020.
[4] 曹先兰,李珠莲 .刺五加国外实验研究[J].中草药,1980,11(6):277-283.
[5]阮金霞,贾冬梅,李丽红.刺五加颗粒的薄层鉴别研究[J].黑龙江中医药,2007,36(4):55.
[6]隆 颖,栗建明,莫结丽,等.HPLC法测定刺五加注射液中紫丁香苷和异嗪皮啶的含量[J].中国药品标准,2011,12(6):410-412.
[7]袁 霞,刘唯芬,张艳君.RP-HPLC法测定刺五加中紫丁香苷和异秦皮啶的含量[J].沈阳药科大学学报,2012,29(1):36-38.
[8]姜文红,刘 静,仲昭庆,等.HPLC法同时测定刺五加浸膏中3 种有效成分的含量 [J].药物分析杂志,2010,30(6):1145-1147.
[9]史 磊,张 涛,李 峰,等 .RP-HPLC法测定刺五加滴丸中紫丁香苷含量研究 [J].山东中医杂志,2014,33(11):926-928.
[10]杜 波,王金杰,荆维荣.高效液相色谱法测定复方刺五加 片中紫丁香苷的含量[J].黑龙江医药,2011,24(1):6-7.
[11]杨 红.刺五加胶囊中紫丁香苷含量的HPLC测定[J].时珍国医国药,2013,24(2):404-405.
[12]张崇禧,张莹莹,田 芯,等.HPLC测定不同产地刺五加中紫丁香苷的含量[J].中成药,2008,30(11):1648-1651.
[13]樊如强,金学英,胡 荣,等.大孔树脂分离纯化刺五加中紫丁香苷、刺五加苷E和异嗪皮啶的工艺研究[J].中国现代应用药学,2014,31(3):302-307.
[14]张崇禧,周燕霞,鞠会艳,等.用HPLC法测定刺五加根叶中紫丁香苷的质量分数[J].北华大学学报(自然科学版),2010,11(4):370-372.
[15]韩 梅,王丽娟,郭双双,等.不同种群结构刺五加根和茎中紫丁香苷的含量[J].吉林农业大学学报,2016,38(4):434-438.
[16]杨棕贺.不同生境刺五加种群结构与紫丁香苷含量研究[D].长春:吉林农业大学,2015.
Quality Standard of Dispensing Granules of Acanthopanax Senticosus
Tan Pei1, Zheng Xiaoying1, Huang Junzhong2, Zhang Hui1
(1.China Resources Sanjiu Medical & Pharmaceutical Co., Ltd., Shenzhen, Guangdong, China 518110; 2.Guangdong Institute for Food and Drug Control, Guangzhou, Guangdong, China 510180)
Objective To establish the quality standard of dispensing granules of Acanthopanax senticosus.Methods The TLC method was used for the qualitative identification of dispensing granules of Acanthopanax senticosus with the contrast medicinal materials of Acanthopanax senticosus and isopropyridine reference substance as the positive control.The content of syringin in the dispensing granules of Acanthopanax senticosus was determined by HPLC,and the method was verified by methodological.Results In qualitative identification,the TLC spots of dispensing granules of Acanthopanax senticosus was clear with good separation degree.The syringin had a good linear relationship in the range of 0-5.668 μg(r=0.9995),and the average recovery rate was 98.62% , RSD =1.16% (n=6).Conclusion The qualitative and quantitative method is simple and feasible,it has good precision and repeatability,which can be used for the quality control of dispensing granules of Acanthopanax senticosus.
Acanthopanax senticosus;dispensing granules;syringin;TLC;HPLC;quality control
R284.1;R282.71
A
1006-4931(2017)24-0011-04
10.3969 /j.issn.1006-4931.2017.24.004
谭沛(1965-),男,汉族,硕士研究生,高级工程师,主要从事中药及天然药物的研发,(电话)0755-8336099(电子信箱)Tanpei@ 999.com.cn。
张辉(1973-),男,满族,大学本科,高级工程师,主要从事中药及天然药物的研发,(电子信箱)ycahui@999.com.cn。
2017-05-09;
2017-06-13)
