阿伏加德罗常数变式分类突破
2017-11-27曾澄福
曾澄福
(广东省深圳市南山外国语学校(集团)滨海学校,广东 深圳 518000)
阿伏加德罗常数变式分类突破
曾澄福
(广东省深圳市南山外国语学校(集团)滨海学校,广东 深圳 518000)
在考纲要求及阿伏加德罗常数定义的基础上,从物质的量的基本公式出发,围绕与之相关的宏观物理量(物质质量、气体体积、溶液浓度)、微观结构及特殊反应等五个方面,结合适当的变式训练,系统阐释了高考对阿伏加德罗常数的考查.
阿伏加德罗常数;宏观物理量;微观结构;特殊反应;变式训练
2017年高考大纲对于阿伏加德罗常数的要求是:了解物质的量及其单位、摩尔质量、气体摩尔体积、物质的量浓度、阿伏加德罗常数的含义;能根据微粒(原子、分子、离子等)物质的量、数目、气体体积(标准状况下)之间的相互关系进行有关计算.
一、阿伏加德罗常数的定义及考查内容
在国际上规定:1 mol粒子集体所含有的粒子数与0.012 Kg的12C所含有的碳原子数相同,约为6.02×1023.把1 mol任何粒子的粒子数叫做阿伏加德罗常数,符号为NA,通常用6.02×1023mol-1表示.
有关NA的正误判断是高考经典考题,该题型主要以物质的量为中心,通过物质的量、阿伏加德罗常数、物质的质量、气体的体积、物质的量浓度等之间的换算关系(即N=n·NA、N=(m/M)·NA、N=(V/Vm)·NA、N=c·V·NA),主要考查气体摩尔体积的适用条件、物质微粒的构成、化学键数目、混合物中(含溶液)原子含量、反应中的微粒变化和能量变化、氧化还原反应中电子转移数目与元素价态的变化、溶液pH和浓度等.解决此类问题的关键是留心关键字词,做题时谨慎细致,避免急于求成而忽略问题的本质.
二、阿伏加德罗常数高考题分类突破
高考中关于阿伏加德罗常数基本上都是以选择题形式出现,为了让学生在一轮复习中对阿伏加德罗常数进行系统准确把握,现把历年高考中的NA试题进行分类阐释,并改编成判断题形式进行变式训练.
1.由宏观物理量决定的微粒计算
(1)物质质量或摩尔质量
以N=(m/M)·NA为计算依据,主要变化量是m或M.此类题型注意把握特殊物质的摩尔质量以及某些物质间摩尔质量呈相等或倍数关系.例如D2O、T2O的摩尔质量、混合单烯烃和环烷烃中碳原子数或氢原子数的判断等.
变式1:判断正误,正确的划“√”,错误的划“×”(后面的例题省略题目说明)
(1)标准状况下,14g由N2与CO组成的混合气体含有的原子数目为NA( ).
(2)2.0g H218O与D2O的混合物中所含中子数为NA( ).
答案:(1)√ (2)√
2.气体体积
以N=(V/Vm)·NA为计算依据,主要变化量是V或Vm,此类题型要关注物质的聚集状态.在标准状况下,单质溴、H2O、HF、苯、CCl4、CH2Cl2、CHCl3、CH3OH、CH3CH2OH,碳原子数大于4的烃,均为液体;SO3为固体.以上物质在标准状况下不能使用22.4 L·mol-1(标准状况下气体的摩尔体积)进行计算.
变式2:(1)常温下,22.4 L四氯化碳中含有的电子数为10NA( ).
(2)惰性电极电解食盐水,若电路中通过NA个电子,则阳极产生气体11.2 L ( ).
答案:(1)× (2)×
(3)溶液浓度
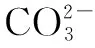
变式3:(1)在1 L 0.1 mol·L-1碳酸钠溶液中,阴离子总数大于0.1NA( ).
答案:(1)√ (2)×
2.由物质微观结构决定的微粒计算
此类题型要求学生对物质的微观构成要非常熟悉,弄清楚微粒中相关粒子数(质子数、中子数、电子数)及离子数、电荷数、化学键之间的关系.常涉及稀有气体He、Ne等单原子分子,Cl2、N2、O2、H2等双原子分子,及O3、P4、18O2、D2O、Na2O2、CH4、CO2等特殊物质.关注一些物质在晶体和溶液两种状态时离子的种类、数目不同.
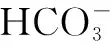
变式4:(1)30g甲醛中含共用电子对总数为4NA( ).
(2)1 mol Na2O2固体中含离子总数为4NA( ).
答案:(1)√ (2)×
3.与特殊化学反应相关的微粒计算
一是由于护理专任教师参加临床实践的时间有限,医院缺乏相应的管理机制,对于实践内容、培养目标和指导老师等没有具体的要求,多以“客人”相待,难以深入临床实践[6]。二是学校缺乏适当旳激励机制和考核评价体系,包括职称评定方式、聘任制度和评优考核等均以关注教学和科研为主,而未对临床实践作出明确的要求,这也导致教师参加临床实践的积极性不高。
(1)一些特殊的氧化还原反应
氧化还原反应中转移电子数目的判断是关于NA一类典型的“陷阱”.高考常涉及的特殊氧化还原化学反应有: Na2O2与水(或CO2); Cl2与水(或碱);变价金属铁(或铜)与Cl2、S或硝酸; MnO2与浓盐酸,Cu与浓H2SO4、硝酸;向FeI2溶液中,通入Cl2……
变式5:(1)5.6 g铁粉与硝酸反应失去的电子数一定为0.3NA( ).
(3)过氧化钠与水反应时,生成0.1mol氧气转移的电子数为0.2NA( ).
答案:(1)× (2)√
(2)常见的可逆反应或隐含反应
此类题目的关键是注意一些“隐含反应”及其可逆性,任何可逆反应都不能进行到底,如隐含反应:


变式6:
(1)标准状况下,44.8 L NO与22.4 L O2混合后气体中分子总数为3NA( ).
(2)100g17%的氨水,溶液中含有的NH3分子数为NA( ).
答案:(1)× (2)×
[1] 康晓丹,衷明华.高考中阿伏加德罗常数的应用[J]. 江西化工,2015(02).
[2] 王海华.高考热点阿伏加德罗常数[J].中国校外教育,2012(17).
[责任编辑:季春阳]
G632
A
1008-0333(2017)25-0089-02
2017-07-01
曾澄福(1973.9-),男,江西吉安,中学高级,硕士,从事中学化学教育.
