基于碳量子点修饰纳米硅胶荧光猝灭-恢复测定粮食样品中还原型谷胱甘肽
2017-11-10王玉乐樊欢欢向国强宁可可段俊跃杨登辉
王玉乐,樊欢欢,向国强*,张 衡,宁可可,段俊跃,杨登辉
(1.河南工业大学 粮油食品学院,河南 郑州 450001; 2.河南工业大学 化学化工学院,河南 郑州 450001)
基于碳量子点修饰纳米硅胶荧光猝灭-恢复测定粮食样品中还原型谷胱甘肽
王玉乐1,樊欢欢2,向国强2*,张 衡2,宁可可2,段俊跃2,杨登辉2
(1.河南工业大学 粮油食品学院,河南 郑州 450001; 2.河南工业大学 化学化工学院,河南 郑州 450001)
制备了碳量子点修饰硅胶 (SiO2@CDs),经过Cu2+处理后,根据SiO2@CDs荧光强度恢复程度与还原型谷胱甘肽(GSH)成正比的现象,建立了基于SiO2@CDs荧光猝灭-恢复测定GSH的新方法. 考察了溶液pH值和反应时间对检测体系的影响. 在最佳的实验条件下,GSH浓度在0.2×10-6~8.0×10-6mol/L范围内与SiO2@CDs的荧光恢复程度呈良好线性,检出限(3σ)为0.03×10-6mol/L. 用于粮食样品中GSH的检测,回收率在90.0%~115.2%之间.
碳量子点;荧光法;谷胱甘肽;粮食样品
谷胱甘肽(GSH)乃生物机体内重要的活性物质,且半胱氨酸的侧链集团上有一个非常活泼的巯基,这种结构是谷胱甘肽的许多重要生理功能的基础[1],例如清除自由基、解毒、维持DNA的生物合成、细胞的正常生长及细胞的免疫等. 谷胱甘肽分为还原型(GSH)和氧化型(GSSG)两种形态. 还原型谷胱甘肽(GSH)是一种特殊的氨基酸衍生物[2],占谷胱甘肽总含量99.5%. 目前,针对谷胱甘肽等小分子的传统检测方法有比色法[3]、分光光度法[4]、电化学测量[5]、酶催化法[6]以及高效液相色谱法[7]等. 这些分析方法各有优点,但是操作相对复杂,仪器设备昂贵等不足. 荧光传感器因其灵敏度高,检测简便,快速,在诸多分析方法中具有明显优势.
最近,基于QDs荧光猝灭-恢复现象建立的分析方法多见报道[8-11]. 但是大多数工作所用的QDs 都含有有毒重金属元素Cd、Hg、Pb等[12-13],生物相容性是这种纳米材料临床应用的瓶颈. 碳量子点(Carbon dots, CDs)由于优良的荧光性质和良好生物相容性,在荧光传感分析中受到了广泛关注[14-16]. 相比于传统的荧光有机染料,量子点(QDs)具有宽激发光谱、窄发射光谱、高荧光量子产率和寿命长等优点,是一种理想的分析探针[17-19].
将碳量子点修饰到纳米硅胶表面(SiO2@CDs),研究表明. Cu2+与CDs表面基团结合,降低SiO2@CDs荧光强度;当体系中加入GSH后,SiO2@CDs荧光强度得到恢复,且恢复程度与GSH浓度相关,从而实现了对GSH的测定. 本方法操作简单,灵敏度高,成本低,可用于粮食样品中GSH的测定.
1 实验部分
1.1 试剂和仪器
Cary Eclipse荧光光谱仪(Agilent,美国);透射电镜仪(JEM-2011,日本);电子天平(BS224S,上海赛多利斯天平公司);激光散射粒度分析仪(Nano zs-90,英国Malvern公司);pH计(PHS-3C,上海精密科学仪器公司).
无水柠檬酸(AR 96%,Aladdin);N-(β-氨乙基-γ-氨丙基)甲基二甲氧基硅烷(AEAPMS)(AR 96%,Aladdin);正硅酸四乙酯(TEOS)(AR 96%,国药集团化学试剂有限公司);还原型谷胱甘肽(GSH)(BR 99%,国药集团化学试剂有限公司);三氯乙酸(AR 99%,国药集团化学试剂有限公司);各种金属盐均购于Aladdin公司,均为分析纯(AR)或更高纯度实验用水为二次蒸馏水.
GSH提取剂配制:称取5 g三氯乙酸,186 mg EDTA-Na2·H2O溶解于适量二次蒸馏水中,定容至100 mL备用.
1.2 碳量子点修饰纳米硅胶(SiO2@CDs)的制备
[20]的方法制备碳量子点(CDs),将无水柠檬酸(0.1 g)加入到有机硅AEAPMS(2 mL)中,加热至230 ℃,反应3 min. 所得反应液用石油醚洗涤三次后溶于适量无水乙醇中. CDs修饰纳米硅胶SiO2@CDs的制备:向25 mL无水乙醇中加入氨水(500 μL)、TEOS(700 μL)室温下搅拌10 min后,加入CDs(70 μL)无水乙醇溶液继续搅拌24 h,产物经离心(4 000 rpm、5 min)后,用无水乙醇洗和蒸馏水洗涤. 所得SiO2@CDs经干燥后,以无水乙醇为溶剂配制成10 g/L悬浮液备用.

图1 碳量子点修饰纳米硅胶的制备Fig.1 Preparation of Carbon Quantum Dot doped Silica gel nanoparticles
1.3 实验方法
1.3.1 SiO2@CDs的荧光猝灭
在10 mL的具塞试管里加入2 mL SiO2@CDs 10 g/L悬浮液和2 mL Cu2+(2 mg/L)溶液,用pH为8的PB缓冲溶液定容,然后在40 ℃水浴锅内加热10 min,流水冷却后备用.
1.3.2 基于荧光猝灭-恢复的GSH测定方法
在10 mL的具塞试管中依次加入1.0 mL用上述Cu2+处理过的SiO2@CDs(SiO2@CDs-Cu2+)悬浮液,一定量的GSH工作液(或样品溶液),用pH为7.0的PB缓冲溶液定容后,振荡20 s;同时做试剂空白实验;以360 nm作为激发波长,测定实验溶液在荧光发射峰460 nm处的荧光强度F和试剂空白溶液荧光强度F0,计算ΔF=F-F0.
1.4 样品处理
本实验所用粮食谷物样品,均购于超市(郑州,中原区)分别取适量样品置于研钵内研碎,称取出1.0 g粉碎后的样品,加入7 mL GSH提取剂,振荡,离心(12 000 rpm、10 min、4 ℃),收集上清液待测.
2 结果与讨论
2.1 碳量子点修饰纳米硅胶(SiO2@CDs)的表征
以柠檬酸为碳源制备的荧光碳点(表面含-OH和-COOH)与有机硅试剂(AEAPMS)(含有-NH2)通过形成酰胺键(-COOH与-NH2之间的反应)实现碳点与有机硅的连接. 从FT-IR光谱图可以看出,CDs和CDs修饰纳米硅胶在1 654 cm-1(C=O) 处都有C=ONR伸缩振动和3 456 cm-1处N-H振动,而纳米硅胶没有这一特征峰. 每一步的反应产物在800 cm-1和1 100 cm-1处都有Si-O伸缩振动和Si-CH2-伸缩振动峰. 上述特征峰表明成功的合成了CDs修饰纳米硅胶. TEM测试表明SiO2@CDs的平均粒径为200 nm.激光散射粒度分析实验结果显示SiO2@CDs的平均粒径为201 nm,与TEM结果相吻合. (图2)
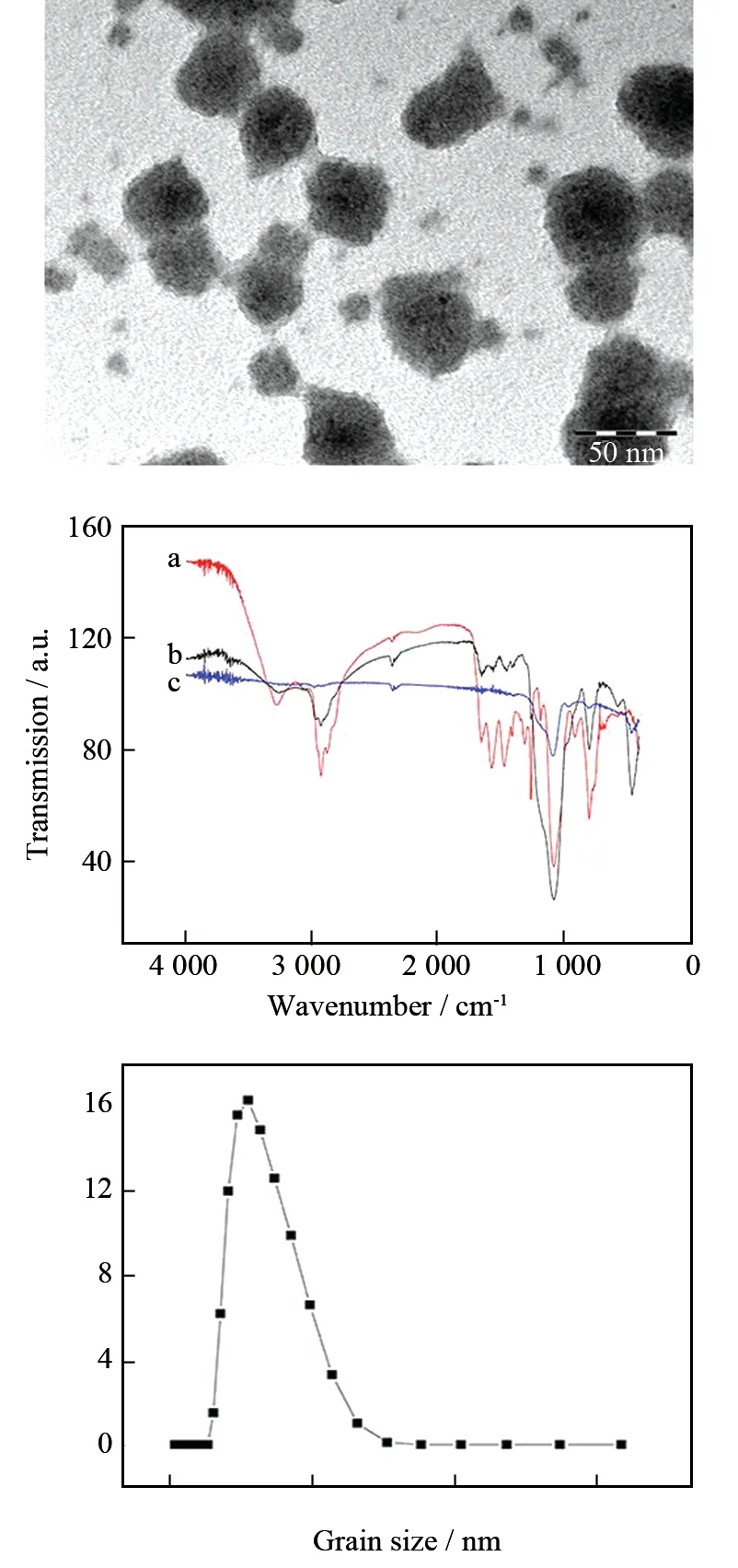
图2 CDs修饰纳米硅胶的表征(TEM(上),FT-IR(中,其中a表示CDs;b表示CDs 修饰硅胶纳米粒子;c表示硅胶纳米粒子),激光粒度散射分布(下))Fig.2 Characterization of CDs doped silica gel nanoparticles(TEM (top), FT-IR spectrum (middle): (a) CDs; (b) CDs doped silica gel nanoparticles; (c) silica gel nanoparticles; laser scat-tering particle size chart (down))
2.2 Cu2+对SiO2@CDs的荧光猝灭
根据文献[21]报道,AEAPMS修饰CDs由于AEAPMS中乙二胺分子结构与Cu2+具有较强的结合能力而使得Cu2+是CDs的良好猝灭剂,且具有较好的选择性. 由图3明显看出,随着Cu2+浓度增大,SiO2@CDs的荧光强度逐渐降低(彩色线). 因此,本实验方法选取Cu2+作为SiO2@CDs的荧光猝灭剂.
2.3 GSH对猝灭的SiO2@CDs荧光的恢复
考察了GSH对SiO2@CDs-Cu2+体系的荧光恢复情况,如图4所示. 随着GSH浓度的增大,SiO2@CDs-Cu2+体系的荧光逐渐增大,表明SiO2@CDs的荧光逐渐恢复. 由于Cu2+对SiO2@CDs的荧光猝灭作用是Cu2+与CDs表面基团结合引起,而GSH中的-SH集团具有更强的与Cu2+结合能力,GSH的加入使得CDs表面结合的Cu2+部分被解析下来与GSH结合,这使得SiO2@CDs荧光得以恢复.
2.4 测定条件优化
2.4.1 pH的影响
图5是pH对GSH测定的影响,可以看出,SiO2@CDs-Cu2+与SiO2@CDs-Cu2+-GSH体系的荧光信号随着pH值变化表现出相似规律,都是随着pH增大(5~7),荧光信号逐渐增强;而当pH进一步增大时(7~9)时,荧光信号开始明显降低. 而ΔF值在PH 7时达到最大值. 因此,选定pH 7作为体系pH条件.
2.4.2 反应时间的影响
根据传感机理,加入GSH将置换与AEAPMS结合的Cu2+,因此反应时间也是影响荧光恢复的重要因素. 考察了反应时间对荧光恢复量(ΔF)的影响,结果表明,加入GSH后反应20 s,反应体系的荧光恢复量(ΔF)达到最大,并在一定时间保持不变. 因此,选取20 s作为最佳反应时间.
2.5 共存物质的干扰
在优化的实验条件下,共存物质对GSH测定的影响. 当相对误差±10%时,体系中GSH浓度为2.5×10-6mol/L时,共存物质的干扰允许浓度如表1 所示. 由表1可知,多数氨基酸有较大的干扰允许量,而半胱氨酸因为也含有-SH基团,其干扰允许浓度为2.0×10-6mol/L. 大多数金属离子对GSH测定没有干扰.

SiO2@ CDs 1.0 g/L, Cu2+ 0~500 μg/L, pH 8.0.图3 Cu2+对CDs修饰硅胶纳米粒子的荧光猝灭作用Fig.3 Fluorescence quenching effect of Cu2+ on the CDs doped silica gel nanoparticles

SiO2@CDs (1.0 g/L), GSH (0.2×10-6~8.0×10-6 mol/L), PB buffer solution at pH 7, vibration 20 s.图4 GSH对SiO2@CDs-Cu2+体系的荧光恢复作用Fig.4 Fluorescence recovery of GSH to SiO2@CDs-Cu2+ system
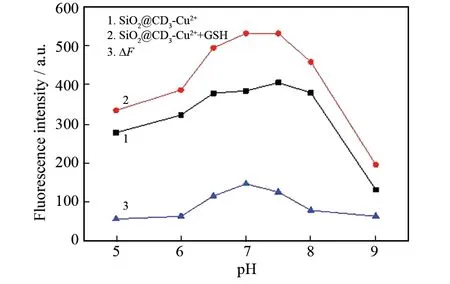
SiO2@CDs (1.0 g/L), GSH (2.5 ×10-6 mol/L), PB buffer solution at different pH, vibration 20 s.图5 pH对荧光猝灭-恢复体系的影响Fig.5 Effects of pH on the fluorescence quenching-recovery system

表1 常见干扰物质的最大允许浓度Table 1 Tolerance amounts of foreign substances
2.6 分析性能
在优化条件下,分析方法对GSH的检出线(3σ)为0.03×10-6mol/L,线性范围位0.2×10-6mol/L~8.0 ×10-6mol/L(ΔF=51C+19.6),相对标准偏差(RSD)为4.9%(C=2.5×10-6mol/L)

表2 样品中GSH含量的测定(n=3, mean ±SD, μg/g)Table 2 Analytical results of GSH in grain samples (μg/g, n=3)
3 实际样品分析
将本方法应用于稻米,绿豆和小麦样品中GSH的测定. 采用标准曲线法对提取液中GSH含量进行了测定,并做了加入回收实验,回收率在90%~115.2%之间.
参考文献:
[1] POMPELLA A, BANHEGYI G, WELLMAN-ROUSSEAU M. Thiol metabolism and redox regulation of cellular functions [J]. Free Radical Research, 2003, 37(4): 469-470.
[2] ZHANG L, YIN H B, LUO J J, et al. Construction of electrochemical impedance sensor based on poly dopamine-hyaluronic acid composite membrane for detection of hydrogen peroxide [J]. Chinese Journal of Analytical Chemistry, 2013, 41(4): 534-539.
[3] ZENG X D, ZHANG X L, ZHU B C, et al. A colorimetric and ratiometric fluorescent probe for quantitative detection of GSH at physiologically relevant levels [J]. Sensors & Actuators B Chemical, 2011, 159(1): 142-147.
[4] LIU J F, BAO C Y, ZHONG X H, et al. Highly selective detection of glutathione using a quantum-dot-based OFF-ON fluorescent probe [J]. Chemical Communications, 2010, 46(17): 2971-2973.
[5] LIU L J, XI F H, ZHANG Y M, et al. Selective analysis of reduced thiols with a novel bionanomultilayer biosensor based on the inhibition principle [J]. Sensors and Actuators B: Chemical, 2009, 135(2): 642-649.
[6] MA Y H, ZHANG Z Y, REN C L, et al. A novel colorimetric determination of reduced glutathione in A549 cells based on Fe3O4magnetic nanoparticles as peroxidase mimetics [J]. Analyst, 2012, 137(2): 485-489.
[8] XIA Y S L, SONG L, ZHU C Q. Turn-on and near-infrared fluorescent sensing for 2, 4, 6-trinitrotoluene based on hybrid (gold nanorod)-(quantum dots) assembly [J]. Analytical Chemistry, 2011, 83(4): 1401-1407.
[9] WU P, YAN X P. Ni2+-modulated homocysteine-capped CdTe quantum dots as a turn-on photoluminescent sensor for detecting histidine in biological fluids[J]. Biosensors & Bioelectronics, 2010, 26(2): 485-490.
[10] 颜梅, 葛慎光, 卢娟娟, 等. 基于双分子识别荧光猝灭法高选择性测定多巴胺[J]. 分析化学, 2011, 39(11): 1711-1715.
YAN M, GE S G, LU J J, et al. Fluorescence quenching method for determination of dopamine based on double molecular recognition [J]. Chinese Journal of Analytical Chemistry, 2011, 39(11): 1711-1715.
[11] 徐琴, 魏焕平, 胡效亚. 基于ZnS量子点荧光淬灭-恢复方法测定还原型谷胱甘肽[J]. 分析化学, 2013, 41(7): 1102-1106.
XU Q, WEI H P, HU X Y. Glutathione detection based on ZnS quantum-dot-based off-on fluorescent probe [J]. Chinese Journal of Analytical Chemistry, 2013, 41(7): 1102-1106.
[12] 陈志兵, 陆佩佩, 查珺, 等. 牛血清白蛋白与VB2间的荧光共振能量转移[J]. 光谱实验室, 2013, 30(3): 1025-1028.
CHEN Z B, LU P P, ZHA J. Fluorescence resonance energy transfer between bovine serum Al bumin and Ribof l avin [J]. Chinese Journal of Spectroscopy Laboratory, 2013, 30(3): 1025-1028.
[13] WANG H J, LIU T, JI X, et al. Cadimium sulfate quantum dots synthesized and coupled with listeria monocytogenes antibody IgG [J]. Chinese Journal of Analytical Chemistry, 2010, 38(5): 632-637.
[14] 张川洲, 谭辉, 毛燕, 等. 发光碳量子点的合成、性质和应用[J]. 应用化学, 2013, 30(4): 367-372.
ZHANG C Z, TAN H, MAO Y, et al. Synthesis and properties of luminescent carbon dots and its applications[J]. Chinese Journal of Applied Chemistry, 2013, 30(4): 367-372.
[15] SUN Y P, ZHOU B, LIN Y, et al. Quantum-sized carbon dots for bright and colorful photoluminescence [J]. Journal of the American Chemical Society, 2006, 128(24): 7756-7757.
[16] LI H T, KANG Z H, LIU Y, et al. Carbon nanodots: synthesis, properties and applications [J]. Journal of Materials Chemistry, 2012, 22(46): 24230-24253.
[17] 谢海燕. 基于量子点的生物医学功能纳米材料的制备与应用[D]. 武汉: 武汉大学, 2004: 11-15.
XIE H Y. The preparation and application of quantum dots-based biomedical fuctional nanomaterials [D]. Wuhan: Wuhan University, 2004: 11-15.
[18] KUANG K, ZHAO Y, MA W, et al. Recent developments in analytical applications of quantum dots [J]. TRAC Trends in Analytical Chemistry, 2011, 30(10): 1620-1636.
[19] 杨冬芝, 徐淑坤, 陈启凡. 量子点的荧光特性在生物探针方面的应用[J]. 光谱学与光谱分析, 2007, 27(9): 1807-1810.
YANG D Z, XU S K, CHEN Q F. Applications of quantum dots to biological probes [J]. Spectroscopy and Spectral Analysis, 2007, 27(9): 1807-1810.
[20] ZHAI X Y, ZHANG P, LIU C J, et al. Highly luminescent carbon nanodots by microwave-assisted pyrolysis [J]. Chemical Communications, 2012, 48(64): 7955-7957.
[21] 王杰, 毛小娇, 郑鹄志, 等. Cu2+对碳点的荧光猝灭机理研究[J]. 西南大学学报(自然科学版), 2015, 37(5): 123-127.
WANG J, MAO X J, ZHENG H Z, et al. Study of the mechanism of quenching effect of Cu2+on fluorescent carbon dots [J]. Journal of Southwest University (Natural Science Edition), 2015, 37(5): 123-127.
Determinationofreducedglutathioneingrainsamplesbasedonfluorescencequenching-recoveryofcarbondotsdopedsilicagelnanoparticles
WANG Yule1, FAN Huanhuan2, XIANG Guoqiang, ZHANG Heng2, NING Keke2, DUAN Junyue2, YANG Denghui2
(1.SchoolofFoodScienceandTechnology,HenanUniversityofTechnology.Zhengzhou450001,Henan,China;2.SchoolofChemistryandChemicalEngineering,HenanUniversityofTechnology,Zhengzhou450001,Henan,China)
Carbon dots doped silica gel nanoparticles (SiO2@CDs) were prepared. The fluorescence intensity of the SiO2@CDs was significantly quenched in the presence of Cu2+with adding reduced glutathione(GSH), and the fluorescence of SiO2@CDs was recovered after Cu2+reacted with GSH. The degree of recovery of the SiO2@CDs fluorescence intensity was proportional to the GSH concentration. Based on the results, a new analytical method for GSH was developed. Under the optimized experiment conditions, the detection limit (3σ) of the method was 0.03×10-6mol/L with a linear rang of 0.2×10-6-8.0×10-6mol/L. The method has been successfully applied for the detection of GSH in grain samples with the recoveries of 90.0%-115.2%.
carbon dots; fluorescence method; glutathione (GSH); grain samples
O657.3
A
1008-1011(2017)05-0633-06
2017-05-21.
河南省教育厅高校科技创新人才项目(13HASTIT016).
王玉乐(1992-),女,研究方向:食品分析技术.*
, E-mail:xianggq@126.com.
[责任编辑:张普玉]
