树枝状聚合物纳米药物的制备及性能表征
2017-10-19单玉萍周思源汪世阳
单玉萍, 陈 阳, 周思源, 汪世阳
(长春工业大学 化学与生命科学学院, 吉林 长春 130012)
树枝状聚合物纳米药物的制备及性能表征
单玉萍, 陈 阳*, 周思源, 汪世阳
(长春工业大学 化学与生命科学学院, 吉林 长春 130012)
以甲氨蝶呤作为药物负载,采用紫外可见分光光度计研究了不同代数(G2.0、G4.0、G4.5、G8.0)polyamidoamine树枝状大分子(PAMAM)对甲氨蝶呤的包覆效果,结果表明,相同末端-NH2基团不同代数的PAMAM树枝状大分子载药量依次为G8.0>G4.0>G2.0,而具有-COOH基团的G4.5PAMAM树枝状大分子的包覆效果相对最差。
PAMAM树枝状大分子; 甲氨蝶呤; 纳米药物; 药物负载
0 引 言
MTX是一种二氢叶酸还原酶抑制剂,其与二氢叶酸还原酶有高度亲和力,比二氢叶酸结合二氢叶酸还原酶的能力高出10倍,使二氢叶酸不能转变为四氢叶酸,造成DNA合成障碍,干扰RNA,从而抑制细胞的生长,是广谱抗肿瘤药物。与此同时,对体内尤其是增殖迅速的组织,如粘膜、骨髓等同样也可以造成损害,导致一系列的临床症状,表现出对人体较大的毒性作用[1-2]。人们一直努力开发能够减少副作用的新型药物转运体系,以降低MTX的毒副作用。聚酰胺-胺型树枝状大分子(PAMAM)具有稳定、无免疫原性,对生物活性剂转运效率等特点[3-4],是近年来国外开发的一类新型功能高分子,引起相关领域普遍关注[5]。PAMAM分子在结构上具有高度的集合对称性、精确的分子结构、大量的官能团、分子内存在空腔及分子链增长具有可控性等许多独特的性质,使其有可能成为MTX最理性的包覆药物。
PAMAM分子通过Michael加成和酰胺化反应的重复次数控制,每重复一次得到的树枝状大分子称为一代[6-7]。聚酰胺-胺树枝状大分子由初始引发核、与初始引发核径向连接的重复支化单元和与最外层重复支化单元连接的末端基组成,通过这种方法合成的树枝状大分子具有确定分子量、结构精确、分子形状及尺寸可控,呈分散性[8],还具有稳定、在使用剂量下无毒性、适时降解且降解产物无毒性等特点[9]。
聚酰胺-胺树枝状大分子表面官能团的数目随代数的增加而呈指数增长,最终导致表面空间拥挤而产生几何变化[10],当代数较低时一般为开放性的分子构型,随着代数的增加和支化的继续,从第四代树枝状大分子开始就形成了较为封闭的、多孔的球状结构,第八代则是表面几乎无空隙的球状结构[11]。
PAMAM独特的多孔球状结构,内部空腔不仅可物理包裹小分子药物,通过静电引力和氢键相互作用将药物分子捕获在树枝状大分子内或树枝状大分子间[12],而且其端基官能团比同类聚合物具有更高的化学反应性,可以连接各种药物、抗体等。该载药系统可通过简单搅拌包埋药物,避免化学合成对药物的破坏和释放。当进入人体后,PAMAM载药一方面通过扩散从大分子内部释放出来,另一方面,在树枝状大分子表面以共价结合药物分子可通过化学键的水解或者酶解进行释放。
树枝状大分子作为药物载体可延长药物在血液中的滞留时间,控制药物在体内的释放效率,保护药物以免受到环境的破坏,且可以通过改变酸碱度释放药物,实现靶向和控制释放,具有很好的缓控释作用和靶向性[13-14]。
目前,国外期刊多见于PAMAM分子作为药物载体的缓控释及靶向性等研究。此外,PAMAM分子体进入细胞的动态过程也有报导。叶玲[15]等研究了G5.0 PAMAM分子与药物MTX的包合与释放,结果表明,G5.0 PAMAM分子对药物有很好的缓控释作用。Yang B[16]等利用AFM力示踪技术追踪PAMAM单分子进入细胞的动态过程。首次明确了PAMAM单分子进入细胞所需的力和速率。但是对比不同代数PAMAM分子的载药能力国内外罕有报导。
由于不同代数PAMAM结构的不同,将显著影响对药物的载药量。文中将采用不同代数的PAMAM树枝状大分子作为载体,通过物理包覆方法,研究PAMAM包覆MTX负载率的影响,为树枝状聚合物纳米药物的制备提供实验参考。
1 实验部分
1.1试剂与仪器
PAMAM树枝状大分子G2.0、G4.0、G8.0、G4.5,均来自威海晨源高分子;
甲氨蝶呤MTX(Aladdin);
超滤管(3K);
移液枪(Eppendorf);
离心机(Eppendorf);
磁力搅拌器;
分析天平;
Cary 50型紫外可见分光光度计,上海魁元科学仪器有限公司;
G2.0:Mw=3 256 g/mol,末端氨基数16,溶剂为甲醇溶液,质量分数40%;
G4.0:Mw=14 215 g/mol,末端氨基数64,溶剂为甲醇溶液,质量分数40%;
G8.0:Mw=233 383 g/mol,末端氨基数1 024,溶剂为甲醇溶液,质量分数40%;
G4.5:Mw=23 438 g/mol,末端羧基数128,固体粉末。
1.2物理包覆
称取MTX 1 mg投入反应瓶中,加入1 mL去离子水,形成饱和溶液。按照摩尔比(MTX)/(PAMAM树枝状大分子)=1/50进行包覆。通过公式 [m/M(MTX)/50]*Mw(PAMAM树枝状大分子)/40%,计算得到需要的不同代数PAMAM树枝状大分子甲醇溶液的质量。反应体系用氮气保护,密封,避光,控制温度35 ℃,磁力搅拌器搅拌,转速500 r/min,搅拌反应12 h。
由于G4.5PAMAM树枝状大分子为固体,故计算公式为[m/M(MTX)/50]*M(G4.5PAMAM树枝状大分子)。其余实验步骤均同上。
1.3实验处理
反应12 h后,取下反应瓶,将PAMAM树枝状大分子与MTX包覆物转移至3 K的超滤管离心10 min,转速10 000 r/min。由于PAMAM树枝状大分子与MTX的包覆物分子尺寸较大,留在超滤管上层,所以加入1 mL无水乙醇于超滤管中,离心清洗上层产品除去残留杂质后,再用去离子水离心清洗,得到干净的产物。G2.0、G4.0、G4.5、G8.0 PAMAM树枝状大分子与MTX包覆物的处理方法均与上述相同。得到的不同代数的PAMAM树枝状大分子与MTX包覆物产品均用UV-Vis进行表征。
2 结果与讨论
不同代数PAMAM树状大分子示意图如图1所示。
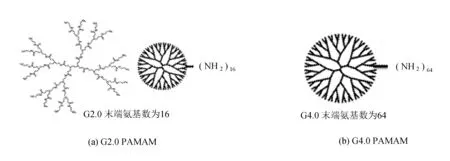
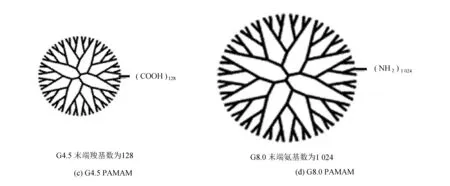
图1 G2.0、G4.0、G4.5、G8.0 PAMAM结构示意图
所有代数PAMAM树状大分子都是对称枝状的球形结构。整数代PAMAM树状大分子有着共同的重复单元。
图1(a)为G2.0 PAMAM树状大分子的结构式及示意图,G2.0PAMAM树状大分子的末端有16个-NH2基团;
图1(b)为G4.0PAMAM树状大分子示意图,末端为64个-NH2基团;
图1(c)为G4.5PAMAM树状大分子示意图,末端为128个-COOH基团;
图1(d)为G8.0PAMAM树状大分子结构示意图,末端为1 024个-NH2基团。随着PAMAM树状大分子代数增加,分子尺寸也随之增大,分子球体表面化学基团数量呈指数增加。
通过实验,将MTX药物分子包覆进入不同代数的PAMAM树枝状大分子中。树枝状大分子负载药物甲氨蝶呤的示意图如图2所示。
树枝状结构表示PAMAM树枝状化合物,球形结构表示MTX药物分子。药物分子经过包覆后可以进入PAMAM树枝状大分子内部间隙。实验得到的产物用于后续表征测试分析。
不同代数 PAMAM树枝状大分子和MTX的UV-Vis图谱如图3所示。

(a) G2.0 PAMAM的UV-Vis图谱
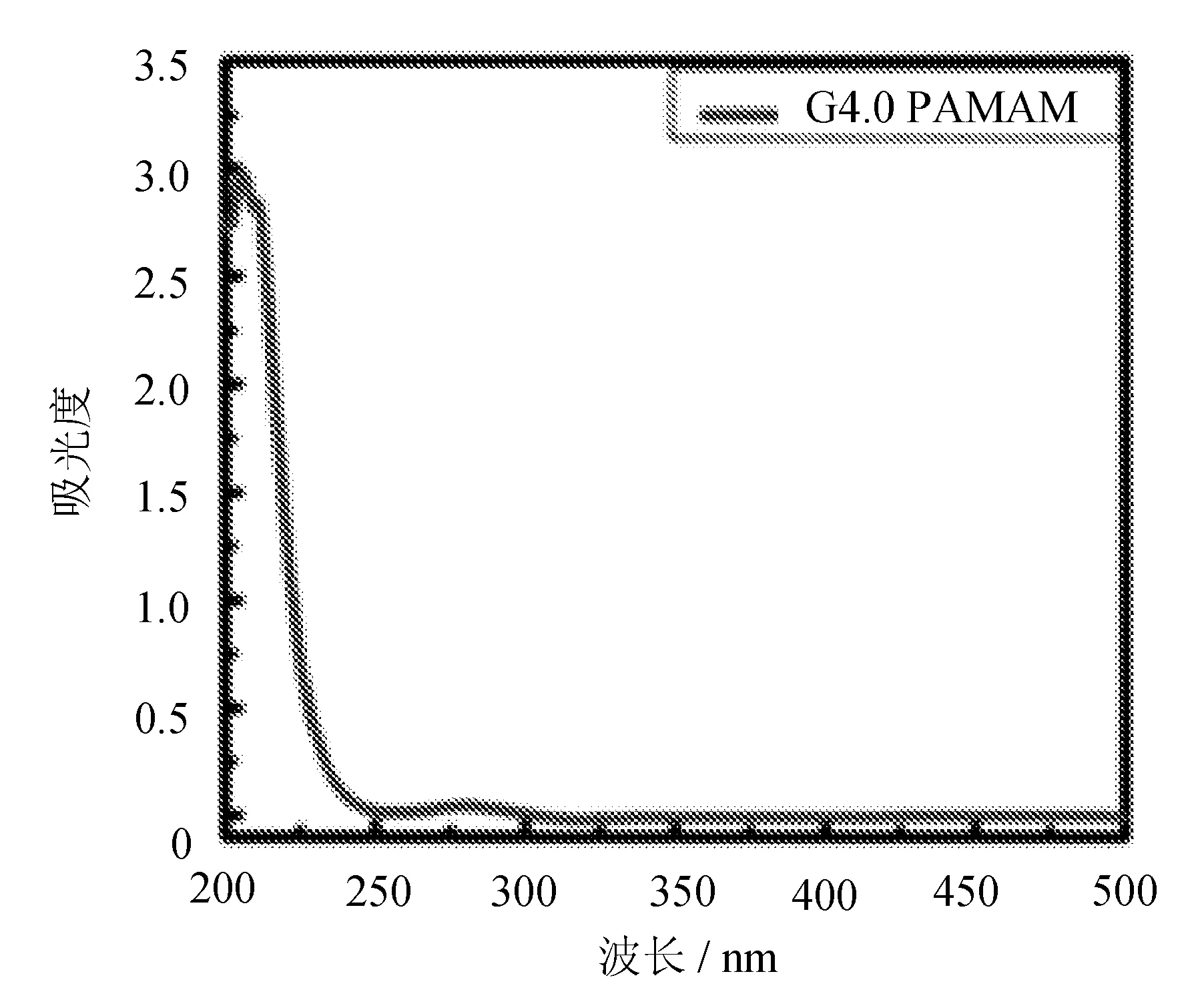
(b) G4.0 PAMAM的UV-Vis图谱

(c) G4.5 PAMAM的UV-Vis图谱
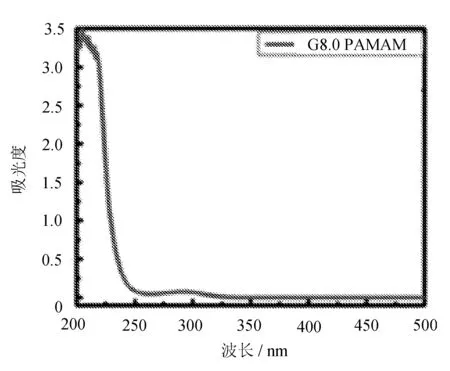
(d) G8.0 PAMAM的UV-Vis图谱
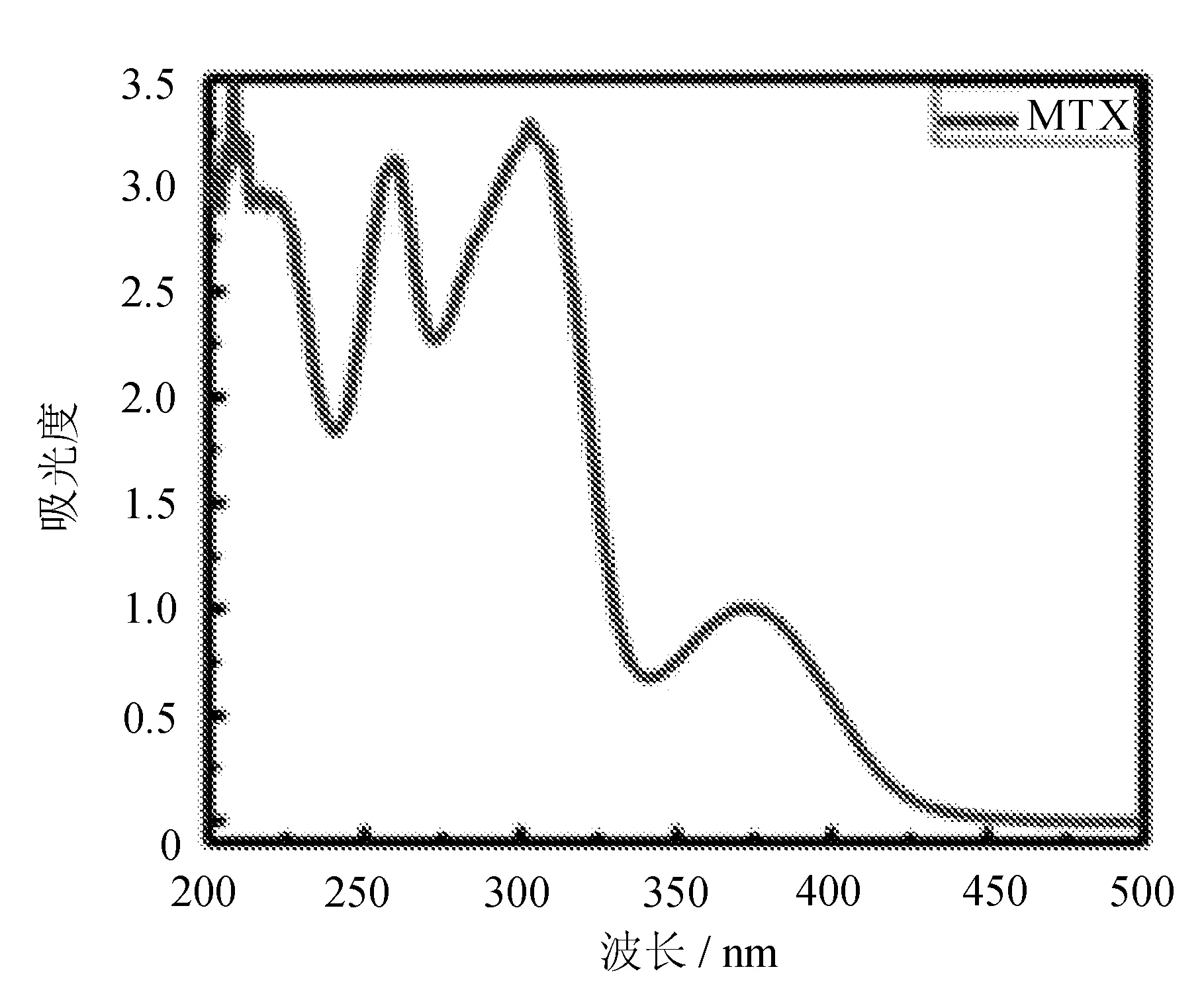
(e) MTX的UV-Vis图谱图3 不同代数PAMAM树枝状大 分子和MTX的UV-Vis图谱
由图3可见,不同代数PAMAM树枝状大分子的紫外吸收峰形相似,在λ=279 nm附近均有紫外吸收特征峰,λ=210 nm附近具有较高的紫外吸收峰。其紫外吸收曲线的相似性可能是因为PAMAM树枝状大分子都具有相同的结构重复单元和对称的枝化结构(见图1)。而MTX在λ=370、302、265、205 nm处有紫外吸收峰,其中λ=370 nm处紫外吸收峰的峰值较低,而波长在302、265、205 nm处对应的紫外吸收峰高度相近。
通过实验得到不同代数PAMAM树枝状大分子负载药物MTX后形成的包覆产物的UV-Vis图谱如图4所示。
图中(a)、(b)、(c)、(d)分别是G2.0、G4.0、G4.5、G8.0 PAMAM树枝状大分子与MTX形成纳米药物的UV-Vis图谱。
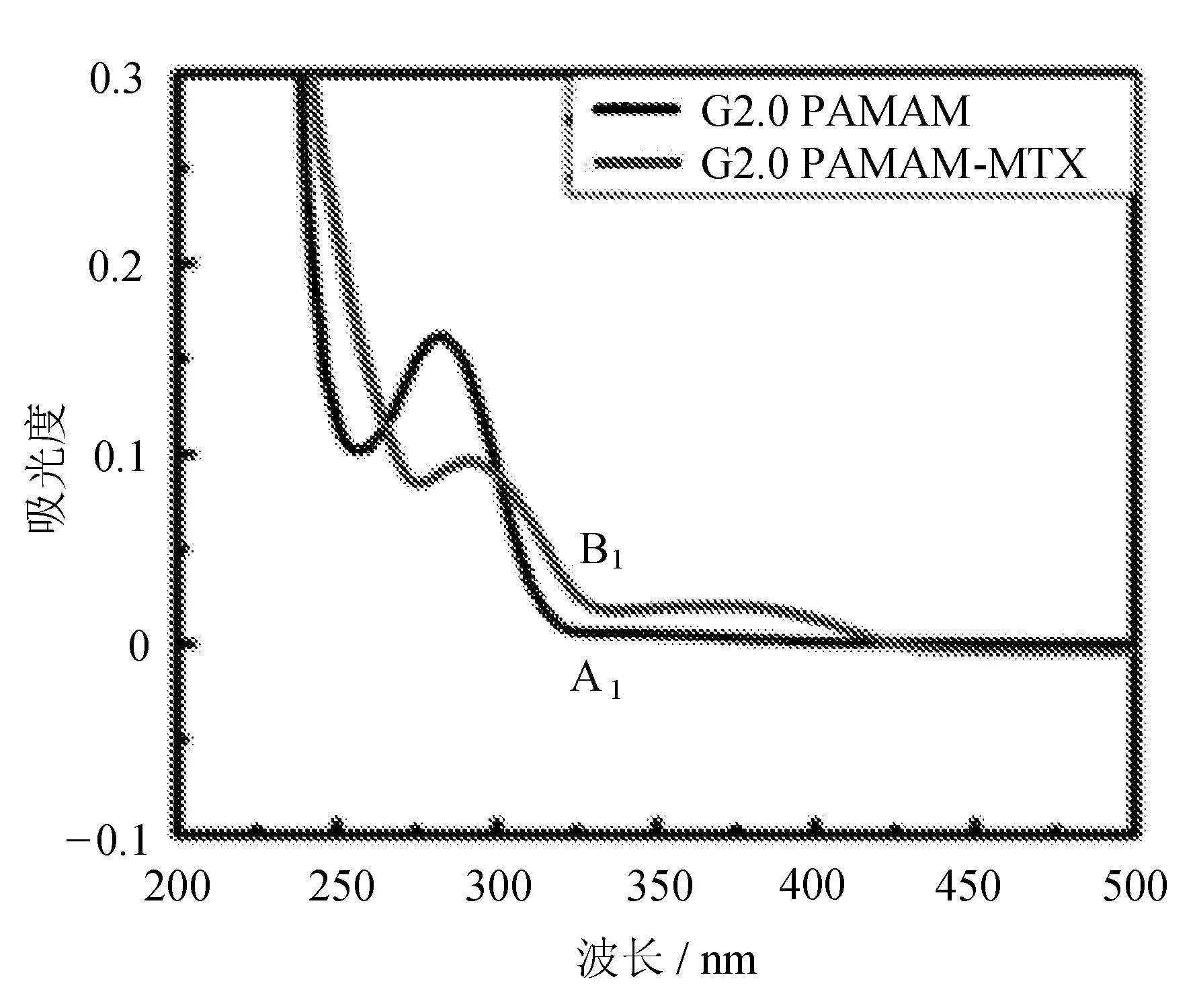
(a) G2.0 PAMAM-MTX纳米药物的UV-Vis图谱

(b) G4.0 PAMAM-MTX纳米药物的UV-Vis图谱
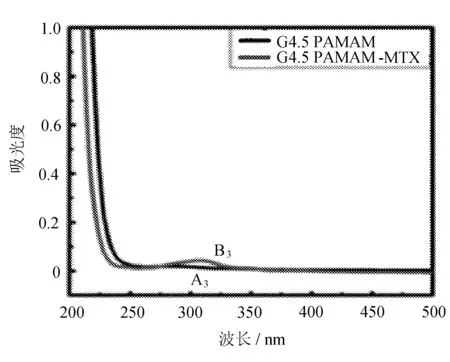
(c) G4.5 PAMAM-MTX纳米药物的UV-Vis图谱
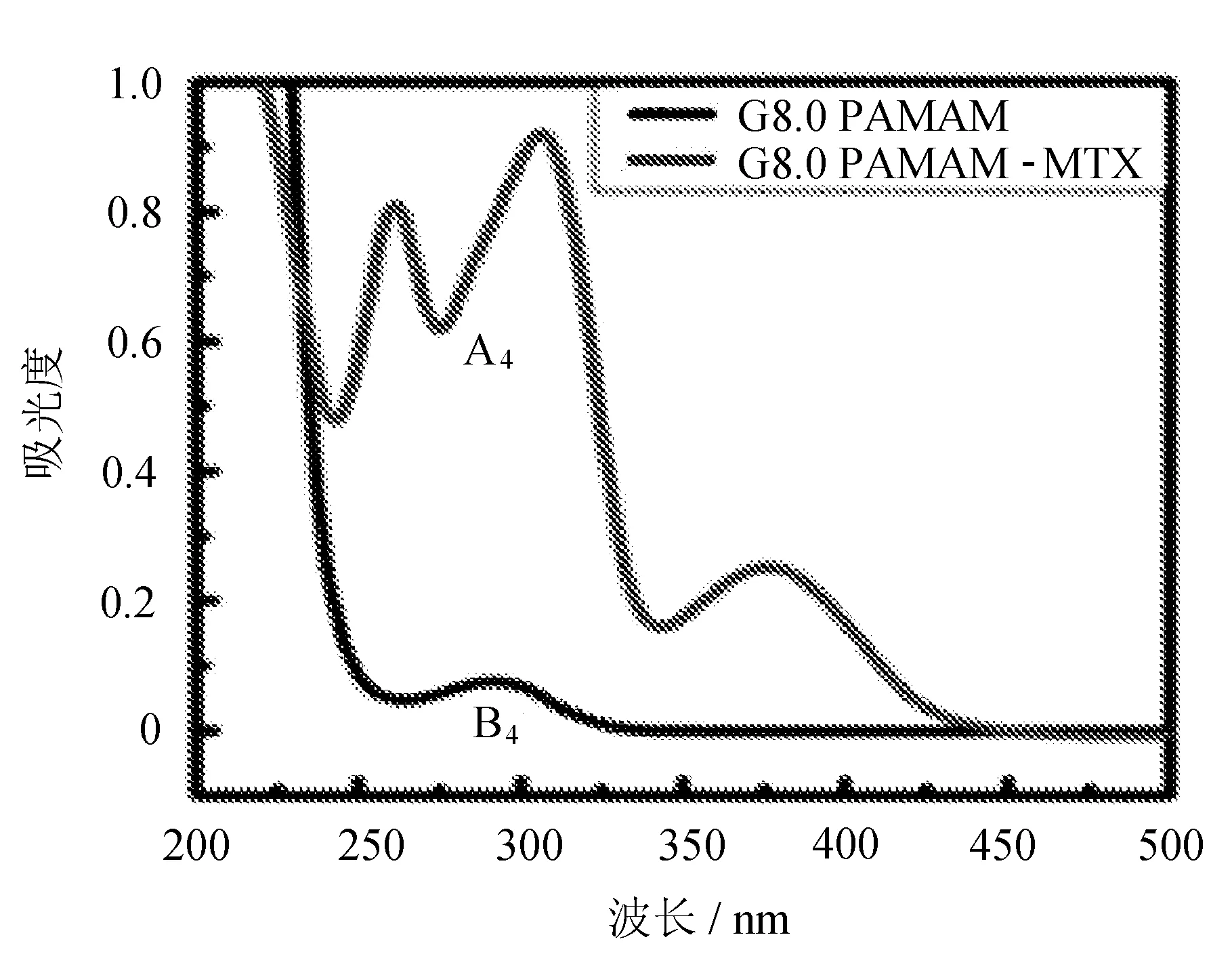
(d) G8.0 PAMAM-MTX纳米药物的UV-Vis图谱图4 不同代数PAMAM-MTX纳米药物的UV-Vis图谱
图中,B1、B2、B3、B4是不同代数PAMAM-MTX纳米药物的UV-Vis图谱。对照A1、A2、A3、A4不同代数PAMAM树枝状大分子紫外吸收曲线可以看出,包覆产物的紫外吸收曲线发生很大变化。其中波长在370、302、260 nm处的峰为产物的UV-Vis特征峰,所有产物的UV-Vis图谱中,紫外吸收峰对应的波长位置相同。其中,λ=370 nm处是MTX的UV-Vis特征峰。PAMAM树枝状大分子包覆MTX后,MTX在λ=302 nm或260 nm处较强的UV-Vis特征峰掩盖了PAMAM树枝状大分子在λ=275 nm附近较弱的UV-Vis特征峰,但在波长200~260 nm区间内PAMAM的UV-Vis特征峰未受影响,由此可知,MTX包覆进入了PAMAM内部空腔。
整数代的PAMAM树枝状大分子的末端都是相同的氨基,不同整数代PAMAM的末端树枝状结构的数量随着代数的增加而呈指数增加,空间尺寸和内部空腔数量也随之增大(见图1)。由于载体大小不同,不同整数代PAMAM树枝状大分子包裹MTX药物分子的量也不同。不同整数代的末端为氨基的PAMAM包覆MTX产物的UV-Vis图谱如图5所示。
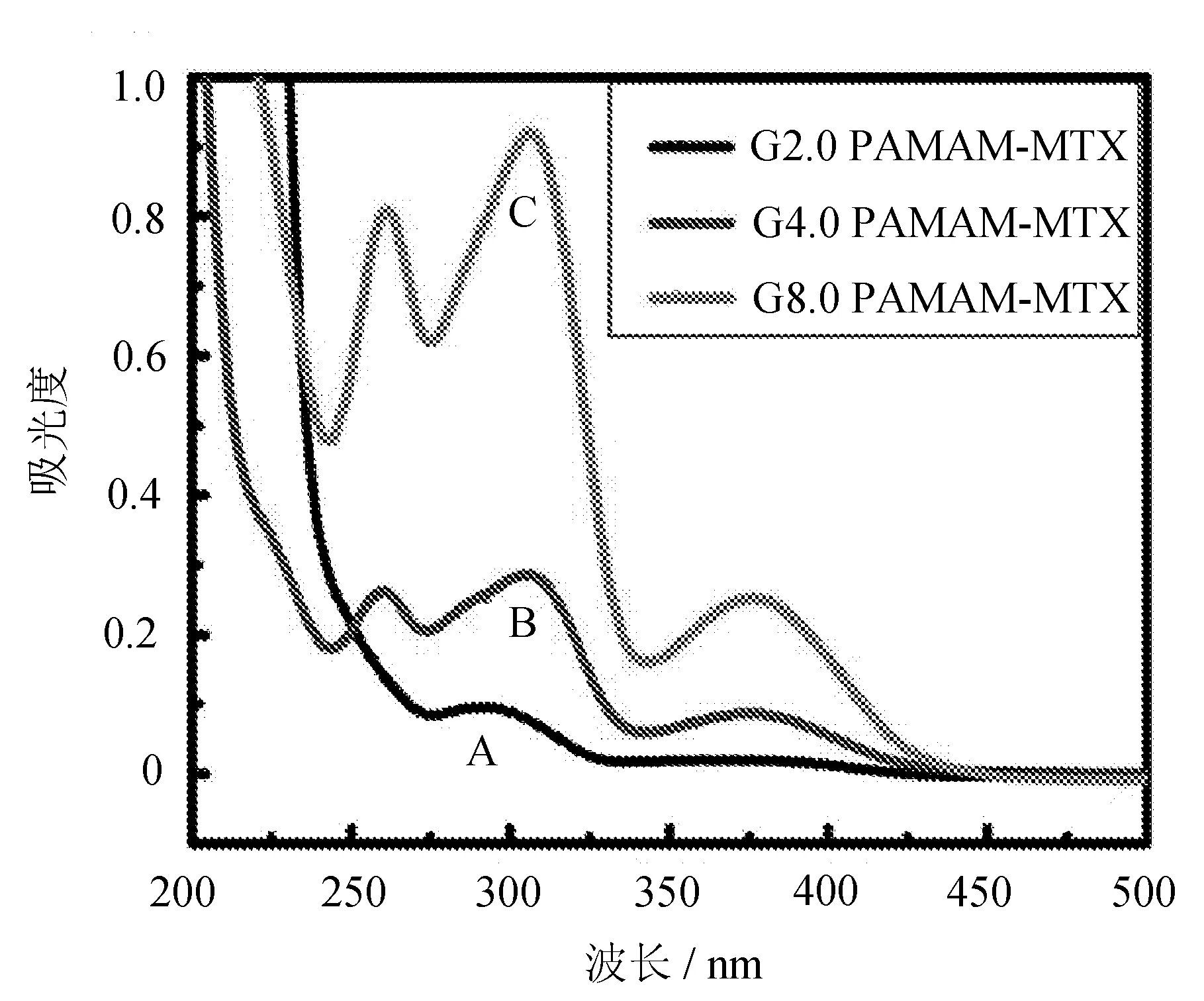
图5 不同整数代的末端为氨基的PAMAM 包覆MTX产物的UV-Vis图谱
图中:A、B、C三条曲线分别对应不同代数的PAMAM-MTX产物。不同代数的PAMAM-MTX纳米药物的UV-Vis峰对应波长位置基本相同。由于不同代数PAMAM包覆MTX的量不同,所以在λ=250 nm到λ=370 nm之间,PAMAM-MTX纳米药物中MTX的UV-Vis特征峰对应纵坐标的吸光度值大小也不同。在包覆反应实验中,投入不同代数PAMAM树枝状大分子的物质的量相同,MTX投药量均为1 mg,由此可知,PAMAM-MTX中MTX的量体现了不同整数代PAMAM包覆药物的性能。由郎伯比尔定律A=lg(1/T)=Kbc可知,K为摩尔吸收系数,b为吸收层厚度,c为吸光物质的浓度,对于MTX在K、b、c为定值情况下,由于吸光度A值可确定不同整代数的PAMAM包覆MTX的实际效果。图5中所示G2.0、G4.0、G8.0 PAMAM-MTX包覆量呈上升趋势。G2.0包覆量最低,G8.0包覆量最高。这清晰表明,PAMAM树枝状大分子随着代数增加,空间结构增大,内部空腔增多,其包覆药物的能力也显著提高。
G4.5PAMAM-MTX和G4.0PAMAM-MTX的UV-Vis对比图如图6所示。
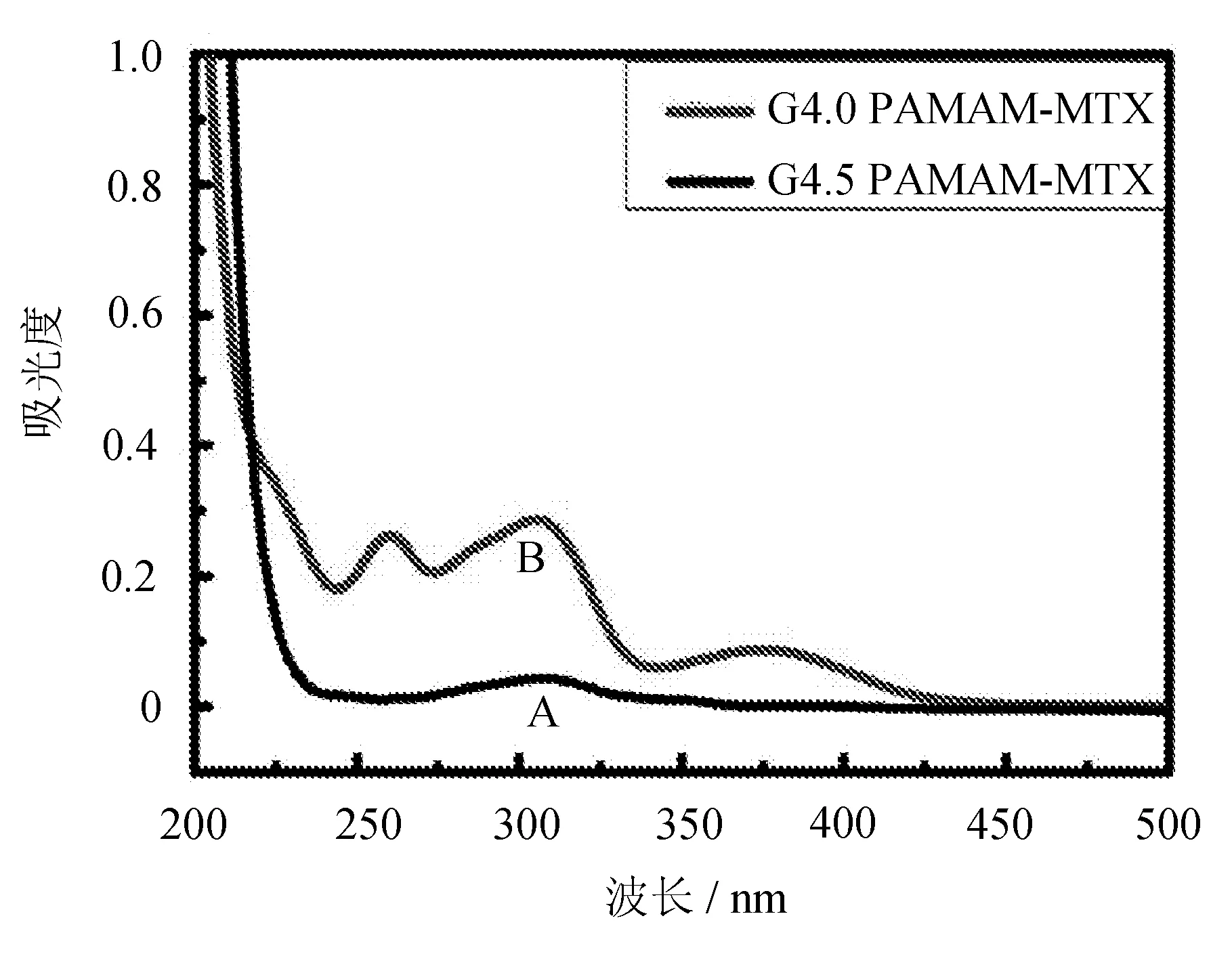
图6 G4.5PAMAM-MTX和G4.0PAMAM-MTX 的UV-Vis对比图
图6中,G4.0PAMAM-MTX和G4.5PAMAM-MTX纳米药物中MTX的量相差很大,G4.0 PAMAM包覆MTX的量明显高于G4.5 PAMAM。G4.0和G4.5代PAMAM树枝状大分子相差半代,二者都是树枝状展开的球形空间结构。G4.5 PAMAM分子尺寸较G4.0 PAMAM略大,但二者末端基团不同,G4.0末端是-NH2,G4.5末端是-COOH。分子尺寸稍大的G4.5 PAMAM包覆药物的性能比分子尺寸略小的G4.0 PAMAM差,这与二者末端不同官能团的性质有直接关系。G4.5 PAMAM末端的大量羧基在溶液中电离形成带负电的球体,与同是带羧基的MTX相互排斥,尽管G4.5 PAMAM分子尺寸较大,但分子球体表面大量的负电荷屏蔽了内部树枝结构形成的空腔[17],导致G4.5PAMAM树枝状大分子包覆药物能力明显下降。另外,PAMAM对pH有很强敏感性,由于G4.5PAMAM和MTX带有大量羧基使得反应体系呈酸性而导致PAMAM树枝状结构僵化[18],这也导致包覆药物的能力会下降。所以,相对于PAMAM的分子大小来说,PAMAM树枝状大分子表面官能团的性质对载体包覆药物能力影响更大。
3 结 语
采用物理包覆的方法制备的不同代收PAMAM-MTX纳米药物,整数代末端带-NH2的PAMAM包覆药物MTX的性能从高代数到低代数依次减弱。这是因为树枝状结构呈指数减小后,内部空腔减小导致的。另外,G4.5代PAMAM树枝状大分子和MTX末端大量羧基在溶液中电离而使溶液为酸性,由于PAMAM树枝状大分子对pH敏感,在酸性溶液中分子变得僵硬,这也对包覆效果有很大影响。而类似G4.5这样的半代PAMAM树枝状大分子末端是-COOH形成表面带负电的球面,带有负电的球面会与溶液中因MTX电离产生的-COOH末端产生排斥作用,从而大大降低PAMAM树枝状大分子包覆药物的性能。
[1] Watala C. How do the full-generation poly(amido)amine (PAMAM) dendrimers activate blood platelets-Platelet membrane zeta potential and other membrane-associated phenomena[J]. International Journal of Pharmaceutics,2016,500(16):379-389.
[2] Katchamart W. Efficacy and toxicity of methotrexate (MTX) monotherapy versus MTX combination therapy with non-biological disease-modifying antirheumatic drugs in rheumatoid arthritis: a systematic review and meta-analysis[J]. Annals of the Rheumatic Diseases,2009,68(12):1105-1112.
[3] Patri A K. Dendritic polymer macromolecular carriers for drug delivery[J]. Current Opinion in Chemical Biology,2002,6(4):466-471.
[4] Cooper S L, Chen C Z. Dendrimer biocide-silver nanocomposites their preparation and applications as potent antimicrobials[J]. University of Delaware,2003:514-646.
[5] 叶玲.聚酰胺-胺(PAMAM)树枝状大分子对甲氨蝶呤的包覆及缓释研究[J].高等学校化学学报,2005,26(2):353-355.
[6] Natali S, Mijovic J. Dendrimers as drug darriers: dynamics of PEG ylated and methotrexate-loaded dendrimers in aqueous solution[J]. Macromolecules,2010,43(6):3011-3017.
[7] Pan G. Studies on PEG ylated and drug-loaded PAMAM dendrimers[J]. Journal of Bioactive & Compatible Polymers,2005,20(1):113-128.
[8] López-Andarias J. Development of microwav-eassisted reactions for PAMAM dendrimer synthesis[J]. European Journal of Organic Chemistry,2012:2331-2337.
[9] 武旭业.物理交联聚乙烯醇/羟基末端聚酰胺-胺树型高分子水凝胶的制备与性质研究[J].高等学校化学学报,2004,25(2):382-387.
[10] 唐杨.树枝状大分子作为药物载体的研究新进展[J].材料导报,2008,22(4):100-103.
[11] 崔玉花.聚酰胺-胺(PAMAM)树枝状大分子的研究进展[J].济南大学学报:自然科学版,2007,21(4):77-81.
[12] Milhem O. Polyamidoamine starburst(R) dendrimers as solubility enhancers[J]. International Journal of Pharmaceutics,2000,197(1/2):239-241.
[13] Ling Y E. Complex and in vitro release of methotrexate-PAMAM dendrimer[J]. Chemical Research in Chinese Universities,2005(2):353-355.
[14] Ling Y E. Investigation of PAMAM dendrimer-MTX complex: Formation and in vitro release[J]. Acta Polymerica Sinica,2006,6(1):32-36.
[15] Spyridopoulou K P. Methylene tetrahydrofolatereductase gene polymorphisms and their association with methotrexate toxicity: a meta-analysis[J]. Pharmacogenetics & Genomics,2012,22(2):117-133.
[16] Yang B, Xu H, Wang S, et al. Studying the dynamic mechanism of transporting a single drug carrier-polyamidoamine dendrimer through cell membranes by tracing[J]. Nanoscale,2016,42(8):18027-18031.
[17] Maiti P K, Messina R. Counterion distribution and zeta-potential in PAMAM dendrimer[J]. Macromolecules,2015,31(13):5002-5006.
[18] Imae D W T. Fluorescence emission from dendrimers and its pH dependence[J]. Journal of the American Chemical Society,2004,126(41):13204-13205.
Preparationandcharacterizationofpolyamidoaminedendrimersnano-drugs
SHAN Yuping, CHEN Yang*, ZHOU Siyuan, WANG Shiyang
(School of Chemistry & Life Science, Changchun University of Technology, Changchun 130012, China)
Taking Methotrexate (MTX) as drug encapsulation, the encapsulation effect of different algebra (G2.0、G4.0、G4.5、G8.0)polyamidoamine dendrimers (PAMAM)to MTX is investigated with UV-visible spectrophotometer. The results indicate that encapsulation rate of the PAMAM with -NH2base is as following: G8.0>G4.0>G2.0; while the encapsulation effect of G4.5PAMAM with -COOH is the worst.
PAMAM dendrimers; Methotrexate (MTX); nano-drugs; drug encapsulation.
O 652.1
A
1674-1374(2017)04-0386-07
2017-04-16
吉林省自然科学基金资助项目(20160520133JH)
单玉萍(1982-),女,汉族,黑龙江尚志人,长春工业大学教授,博士,主要从事细胞膜上跨膜转运动态过程研究,E-mail:shanyp@ccut.edu.cn. *通讯作者:陈 阳(1994-),男,汉族,吉林德惠人,主要从事树枝状聚合物包覆纳米药物的制备及性能表征方向研究,E-mail:chenyang5186@126.com.
10.15923/j.cnki.cn22-1382/t.2017.4.12
