c-MET通路和抑制剂在非小细胞肺癌中的研究进展
2017-09-05俞晓晴综述徐艳珺范云审校
俞晓晴 综述 徐艳珺 范云 审校
自2007年MET扩增被发现可能是一代表皮生长因子受体酪氨酸激酶抑制剂(epidermal growth factor receptortyrosine kinase inhibitor, EGFR-TKI)的耐药机制之一以来,c-Met通路在非小细胞肺癌(non-small cell lung cancer,NSCLC)中的研究逐渐成为一个热点[1,2]。肝细胞生长因子(hepatocyte growth factor, HGF)/c-Met是一个复杂又独特的信号通路,在正常组织发育和肿瘤发生发展中都起着举足轻重的作用。c-Met参与调控多个生物学功能,包括增殖和侵袭,当失调的c-Met异常激活,可以导致肿瘤的生长和转移。c-Met已逐渐成为新的抗肿瘤治疗靶点。多项临床试验将MET抑制剂用于治疗各种实体瘤,特别是在NSCLC中,MET抑制剂表现出了一定的疗效。本文将针对c-MET通路在NSCLC中的研究进展及MET抑制剂在NSCLC中的临床研究结果作一综述。
1 c-MET通路及其异常激活的类型
MET基因位于人类7号染色体长臂(7q21-31),长度约125 kb,同时含有21个外显子[3,4]。c-MET是MET基因编码产生的具有自主磷酸化活性的跨膜受体,属于酪氨酸激酶受体(receptor tyrosine kinases, RTKs)超家族,由膜外Sema域、PSI域、IPT域和膜内JM域、催化TK域、C末端组成,主要表达于上皮细胞(图1)。HGF是目前发现的c-MET的唯一配体,属于纤维蛋白溶酶原家族,由N末端、Kringle域、C末端组成,主要表达于间质细胞,亦可表达于肿瘤细胞而通过自分泌机制发挥作用。HGF与c-MET的Sema域结合使c-MET发生二聚、酪氨酸磷酸化,激活众多下游信号通路,如PI3K-Akt、Ras-MAPK、STAT和Wnt/β-catenin等,从而发挥其促细胞增殖、细胞生长、细胞迁移、侵袭血管及血管生成等效应,在组织正常发育和肿瘤进展中发挥关键作用。c-MET通路正常表达时促进组织的分化与修复,当调节异常时则促进肿瘤细胞的增殖与转移。c-MET通路异常激活主要包括MET 14外显子跳跃突变、MET扩增和MET蛋白过表达3种类型。
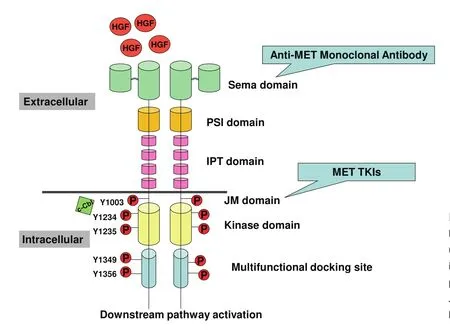
图 1 MET通路Fig 1 MET signialing pathway. Semaphorin(Sema) domain; Plexin-semaphorinintegrin (PSI) domain; Immunoglobulinplexin-transcription (IPT) domain;Juxtamembrane (JM) domain; TKI: tyrosine kinase inhibitor.
1.1 MET 14外显子跳跃突变 MET 14外显子编码部分的JM域,包含Y1003和c-Cbl E3泛素连接酶结合位点。当发生MET 14外显子跳跃突变时,Y1003和c-Cbl的结合位点缺失,从而导致受体泛素化降低[5],MET蛋白质降解,使MET持续激活[6],并作为原发致癌驱动基因。
研究[7]报道显示MET 14外显子跳跃突变在肺腺癌中发生率约为3%。然而,国内研究[8]显示中国肺腺癌中的发生率仅为0.9%,远低于既往研究报道的3%。
MET 14外显子跳跃突变形式多样,目前,以DNA为基础的NGS是最常用检测技术[9,10]。另外,MET 14外显子跳跃突变常伴有免疫组化(immunohistochemistry, IHC)下的MET过表达。因此,可以先用IHC对患者进行筛选,缩小目标人群[6]。
MET 14外显子跳跃突变不与EGFR、KRAS、ALK等肺癌其他突变共存,提示MET 14外显子跳跃突变是原发致癌驱动基因[11]。但MET 14外显子跳跃突变可与MET扩增和MDM2扩增重叠,在NSCLC中与MET高扩增并存机率约为3.3%,同时与MET蛋白高表达相关[12]。当下针对MET 14外显子跳跃突变的治疗药物主要是克唑替尼和卡博替尼。
1.2 MET扩增 MET扩增即MET拷贝数扩增,包括整体染色体重复和局部区域基因的重复[13]。整体染色体重复即多倍体,肿瘤细胞中出现多条7号染色体。有研究[14]表明,多倍体扩增通常伴有其他基因突变,如EGFR、KRAS,这提示多倍体扩增不是驱动基因。MET扩增与EGFR、KRAS或其他驱动基因的激活有明确的联系,是获得性耐药的机制之一[15]。
通常使用荧光原位杂交技术(fluorescence in situ hybridization, FISH)检测MET拷贝数扩增。对于FISH诊断MET扩增还没有统一的标准,常用的有Cappuzzo评价系统和PathVysion两种方法[6](表1)。MET高扩增在肺腺癌中发生率为1.0%,在高加索人群和亚裔人群中没有明显差异,提示发生率与人种无关[12]。尽管MET扩增的发生率不高,但常伴有较强的MET蛋白表达,同时也是预后不良的因素之一。MET抑制剂对于MET高扩增的患者有明显获益[16]。约15%-20%的EGFR获得性耐药患者可检测到MET扩增,MET扩增可同时伴有T790M突变或小细胞肺癌(small cell lung cancer, SCLC)转化。MET扩增也是三代EGFR-TKIs的重要耐药机制之一[6]。
1.3 MET蛋白过表达 许多因素都会引起MET激活,如其他致癌驱动基因,缺氧的环境,炎症因子,促血管生成因子和HGF[4]。MET激活状态中最常见的表现就是转录上调引起的蛋白过表达。但将MET蛋白过表达作为激活形式之一目前尚有争议。尽管MET蛋白过表达在肺腺癌中的发生率可高达65%[17],但并非作为原发致癌驱动因素,更多的时候是作为其他驱动基因激活后产生的二次事件,从而促进肿瘤的生长[6]。

表 1 MET扩增的评价标准Tab 1 Quantification criteria for MET amplification
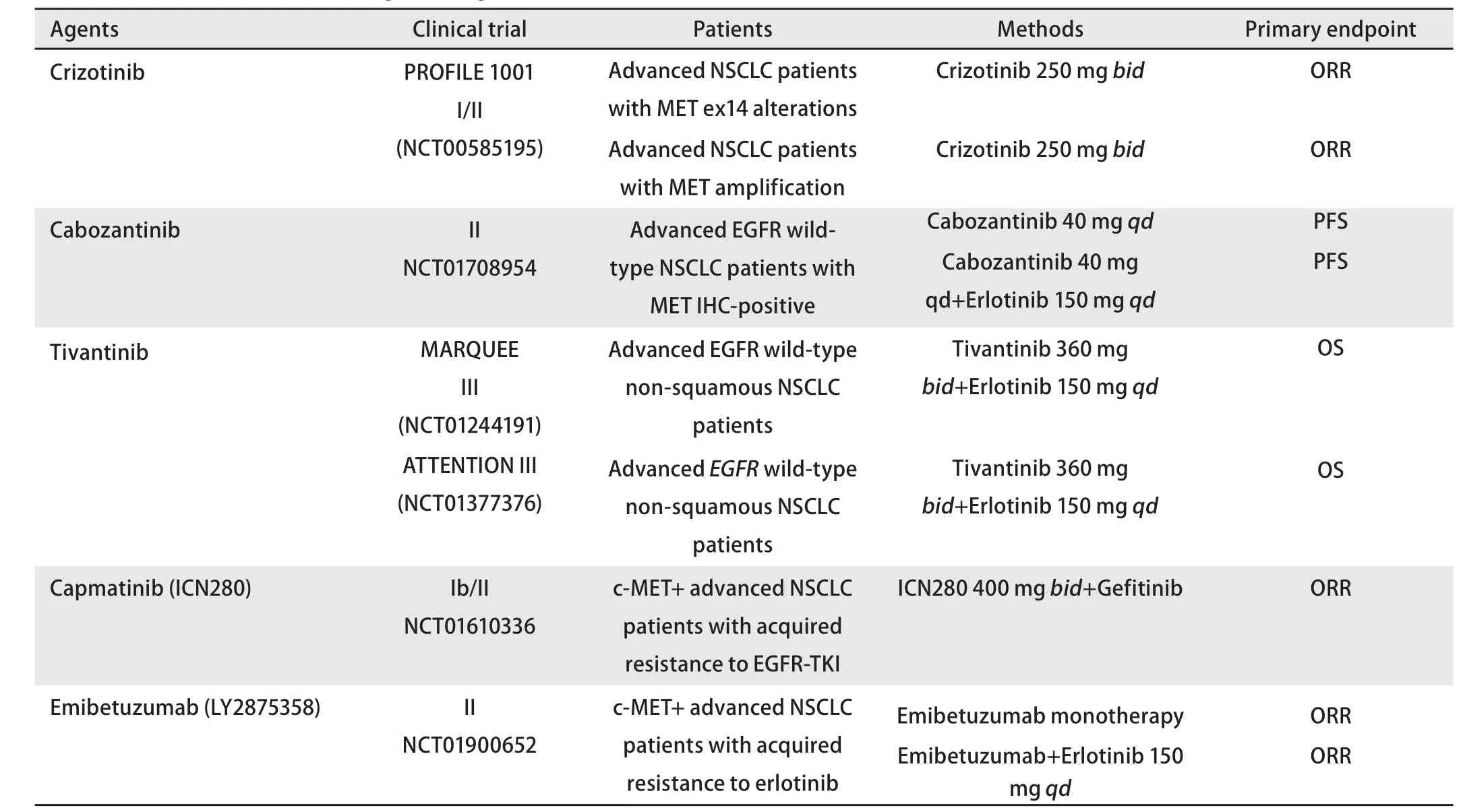
表 2 目前治疗c-MET通路异常药物的临床试验Tab 2 Latest clinical trials with drugs treating c-MET activation
2 针对c-MET通路异常激活的治疗策略
针对MET或其配体HGF的靶向药物很多,主要分为两大类:单克隆抗体和靶向MET基因的小分子TKIs。MET抑制剂又分为多激酶或选择性的MET抑制剂。克唑替尼、卡博替尼属于多激酶MET抑制剂。选择性MET抑制剂包括竞争性ATP抑制剂Capmatinib(ICN280)、tepotinib和非竞争ATP抑制剂tivantinib。单克隆抗体分为MET抗体(onartuzumab, emibetuzumab)和抗GF抗体(ficlatuzumab, rilotumumab)[6](表2)。
2.1 MET 14外显子跳跃突变治疗 在2016年美国临床肿瘤学会(American Society of Clinical Oncology, ASCO)年会上报告了一项关于克唑替尼治疗MET 14外显子跳跃突变晚期NSCLC患者的I期/II期临床研究[18]。入组18例MET 14外显子跳跃突变患者,71%为腺癌,18%为肉瘤样癌,6%为腺鳞癌,6%为鳞癌。在15例可评估疗效的患者中,10例患者疗效评价部分缓解(partial response, PR)(67%),其中5例确定PR,另5例未确定PR。中位PFS未达到。不良反应主要有腹泻、恶心、呕吐、周围性水肿和视觉障碍。大部分不良反应为1级-2级,有1例患者因3级水肿停止治疗。该研究显示克唑替尼对于MET 14外显子跳跃突变的患者治疗有效,不良反应能耐受。综上,克唑替尼治疗MET 14外显子跳跃突变的前景可观。
2.2 原发MET扩增治疗
2.2.1 克唑替尼 2014年ASCO年会上报告了一项研究克唑替尼治疗MET基因扩增的晚期NSCLC的I期临床试验[19]。该研究共入组13例原发MET扩增患者,其中低扩增1例,中扩增6例,高扩增6例,接受克唑替尼250 mg bid治疗。结果显示,在可评估的12例患者中,4例患者疗效评价为PR(33%),其中扩增1例(20%),高扩增3例(50%)。中位缓解持续时间为35周,中位治疗持续时间为15.7周。常见不良反应基本与上述一致。综上,克唑替尼用于MET扩增前景尚可,并且发现扩增程度与疗效成正相关。
2.2.2 卡博替尼联合厄洛替尼 一项比较卡博替尼,厄洛替尼或双药联合作为二线/三线治疗EGFR野生型晚期NSCLC患者疗效的II期临床试验[20]入组125例患者,随机分组,最后可评估的为111例。其中使用厄洛替尼单药治疗38例(34%),使用卡博替尼单药治疗38例(34%),卡博替尼联合厄洛替尼治疗35例(32%)。结果显示,与厄洛替尼单药组(PFS 1.8个月)相比,卡博替尼单药(4.3个月)和卡博替尼联合厄洛替尼(4.7个月)均有显著的PFS获益。同时,卡博替尼单药(HR=0.39, P=0.000,3)或双药联合(HR=0.37, P=0.000,3)对总生存期(overall survival, OS)也均有获益。常见3级、4级不良反应主要是腹泻、高血压、乏力、口气黏膜炎、血栓。卡博替尼组1例患者因呼吸衰竭死亡,考虑与药物治疗相关。双药联合组1例患者因肺部感染死亡,考虑与药物治疗相关。综上研究结果,卡博替尼治疗MET扩增前景可观。但双药联合毒副作用较重,且PFS与卡博替尼单药相差不大。资料中推荐卡博替尼单药治疗NSCLC中的MET扩增。
2.2.3 Tivantinib联合厄洛替尼 MARQUEE[21]和ATTENTION[22]两项III期研究针对晚期EGFR野生型非鳞NSCLC患者,结果都没有达到预期终点,OS均没有获益,提示tivantinib联合厄洛替尼对于MET原发扩增无效。尽管两组试验中tivantinib联合厄洛替尼组较厄洛替尼单药组均提示有PFS获益,但没有统计学差异。
2.2.4 MEK抑制剂 日本的一项基础研究提示MEK抑制剂(曲美替尼和PD0325901)对于MET扩增的NSCLC细胞系治疗有效。并且当联合MET抑制剂(克唑替尼)时,治疗MET扩增的NSCLC细胞系疗效特别显著。这项实验结果鼓励我们进一步探讨MET抑制剂联合MEK抑制剂治疗NSCLC中的MET扩增的可行性研究[23]。
2.3 EGFR-TKI耐药后MET扩增的治疗 由于MET扩增是EGFR-TKI治疗出现获得性耐药的原因之一,而且MET活化导致的EGFR-TKI耐药,患者的EGFR通路仍然活跃。对于这类患者,若要克服耐药,需要采用EGFR-TKI联合MET TKI的治疗策略,相关临床试验应运而生[如Capmatinib(ICN280)联合吉非替尼(NCT01610336)[24]、Emibetuzumab(LY2875358)联合厄洛替尼(NCT01900652)[25]]。
2.3.1 Capmatinib(ICN280)联合吉非替尼 吴一龙教授牵头的一项Ib期/II期临床研究,目前报道了对于EGFR-TKI耐药的cMET+ NSCLC患者,ICN280 400 mg(bid)联合吉非替尼治疗具有较好的耐受性,并表现出一定的临床疗效,cMET高扩增的患者可能临床获益更大。在2016年ASCO年会上报道了其在MET基因异常NSCLC中的疗效[24]。该研究II期结果显示在83例入组肺癌患者中,66例(80%)曾接受EGFR-TKI单药或联合治疗,42例(51%)中断了治疗,多数(34%)是因为疾病进展。在65例可评价疗效的患者中,12例PR[客观缓解率(objective response rate, ORR)=18%],40例稳定(SD=62%),疾病总体控制率为80%。在53例IHC 3+或IHC 2+且GCN≥5的肺癌患者中,10例出现部分缓解(ORR=19%);在23例GCN≥6的肺癌患者中,7例出现部分缓解(ORR=30%)。最常见的不良反应依次为低蛋白血症(29%)、周围性水肿(27%)、食欲减退(23%)。最常见的3级-4级不良反应为淀粉酶升高(7%)。该研究结果提示INC280治疗EGFR TKI 耐药后cMET+ NSCLC患者安全有效,值得进一步探索。
2.3.2 Emibetuzumab(LY2875358)联合厄洛替尼 2016年ASCO年会上报道了一项比较emibetuzumab单药或联合厄洛替尼治疗厄洛替尼耐药伴MET表达阳性的晚期NSCLC的II期临床试验[25]中,在IHC测定MET表达≥60%的患者中,联合用药组的ORR为3.8%,emibetuzumab单药组的ORR为4.8%。在MET表达≥10%的患者中,联合用药组的ORR为3.0%,单药组ORR为4.3%。DCR和PFS都是联合用药组(50%/3.3个月)比emibetuzumab单药组(26%/1.6个月)要好。综上,emibetuzumab治疗厄洛替尼耐药的MET+ NSCLC有临床获益,且联合用药的疗效要好于单药,毒副作用可控。
3 未来的发展方向
3.1 克唑替尼治疗MET 14外显子跳跃突变的耐药机制及其治疗策略
3.1.1 耐药机制 有3个病例报道研究克唑替尼治疗MET 14外显子跳跃突变的耐药机制[26-28]。3例患者均为MET 14外显子跳跃突变,一线或二线接受化疗和局部放疗,疾病进展后接受克唑替尼治疗直到疾病再次进展,疗效评价PR。重新进行基因检测,1例患者提示在原有MET 14外显子跳跃突变D1010H的基础上,新出现MET 19外显子D1228N突变,还有1例患者发现原有的MET 14外显子跳跃突变(D1010H)水平降低至10.9%,而MET Y1230C突变升至3.5%。另1例患者发现在原有MET 14外显子跳跃突变基础上,新发MET 19外显子D1228N/H和Y1230H,同时出现3个突变。上述病例提示D1228和Y1230突变可能是MET 14外显子跳跃突变患者对克唑替尼产生获得性耐药的主要原因。
3.1.2 耐药后的治疗策略 Klempner等[29]报道了1例65岁高加索男性NSCLC患者,Ia期手术,17个月后复发,多发肝转移和2个脑转移病灶。对手术病理组织进行基因检测,发现MET 14外显子跳跃突变,MET扩增阴性,没有其它驱动基因突变。对脑转移病灶进行SRS放疗后,开始服用克唑替尼,4周后发生肝转氨酶升高至4级,影像检查发现肺部肿瘤缓解,但多发脑转移。肝转氨酶降至1级后,开始服用卡博替尼60 mg每天,4周后复查发现脑转移病灶完全消失,肺部肿瘤持续缩小,肝转氨酶保持正常值。该病例提示,在MET原发突变克唑替尼耐药之后,卡博替尼是进一步治疗的选择之一。
3.2 MET抑制剂联合免疫治疗 免疫治疗已经成为继化疗、放疗、手术、靶向治疗之后的又一种肺癌标准治疗方式。肿瘤突变负荷与pembrolizumab疗效密切相关。有报道显示,可以将肿瘤突变负荷作为抗原的替代标志,当抗原高表达时提示肿瘤负荷较高。在MET 14外显子跳跃突变患者中,肿瘤突变负荷平均为6.9个突变/Mb,低于肺癌平均突变负荷10.7个突变/Mb,但高于EGFR-突变(平均4.5)和ALK+ NSCLC(平均2.8)。在EGFR突变和ALK+ NSCLC患者中,很少会同时伴有PD-L1表达。尽管在MET 14外显子跳跃突变的患者中PD-L1表达水平目前还未知,但这些患者的平均肿瘤突变负荷高于EGFR+或ALK+ NSCLC患者,特别是在MET扩增亚组中。这提示MET抑制剂联合免疫治疗治疗可能会有一定的疗效[30]。
4 小结
MET不仅是EGFR-TKI耐药后的新靶点,亦是原发致癌驱动基因。针对MET通路异常激活的几种形式,如何筛选出可能从MET抑制剂中获益的患者群体,是目前面临的主要挑战。MET抑制剂在MET通路异常激活的患者中初显成效,现在最被认可的药物是克唑替尼。但在克唑替尼耐药之后,我们的治疗手段就极其有限。如何应对不可避免要产生的耐药现象,需要更多的药物临床试验和转化研究给我们提供启发。耐药之后,需要再次行基因检测,因此我们可以看到,在实现精准医学的过程中,分子检测非常重要,贯穿了整个疾病的诊治过程。未来,MET通路异常激活的NSCLC患者必将会获得更好的疗效和更长的生存期。
