丹参花挥发油提取工艺优化及抗氧化活性研究
2017-09-03陈燕文李玉娟胡晶红席晓志刘谦李佳郝志
陈燕文,李玉娟, 胡晶红, 席晓志, 刘谦, 李佳, 郝志
(山东中医药大学药学院,山东 济南 250355)
丹参花挥发油提取工艺优化及抗氧化活性研究
陈燕文,李玉娟, 胡晶红, 席晓志, 刘谦, 李佳, 郝志*
(山东中医药大学药学院,山东 济南 250355)
采用单因素法和L9(34)正交试验法,优化水蒸气蒸馏法提取丹参花挥发油的提取工艺,考察不同提取溶液、浸渍时间、蒸馏时间和料液比对丹参花挥发油收率的影响;应用DPPH法研究丹参花挥发油的抗氧化能力,并比较不同提取溶液所得挥发油的自由基清除能力。结果表明,影响丹参花挥发油收率的主要因素为蒸馏时间,其次为料液比、浸渍时间;最佳工艺条件为饱和氯化钠溶液、浸渍6 h、蒸馏8 h、料液比为1∶18,此条件下丹参花挥发油的收率为0.0935%。DPPH实验表明丹参花挥发油具有显著的抗氧化能力;在一定浓度范围内其抗氧化能力与挥发油浓度呈正相关性,蒸馏水、饱和氯化钠溶液、pH=1的硫酸水和pH=1的饱和氯化钠硫酸水4种提取液所得挥发油对DPPH的IC50值分别为1.07、1.03、1.45、1.40 mg/mL。通过验证实验表明,优化所得丹参花挥发油提取工艺稳定、易行。
丹参花;挥发油;提取工艺;DPPH;抗氧化活性
丹参,又名赤参、红根,为唇形科鼠尾草属植物丹参(SalviamiltiorrhizaBge.)的根及根茎,是我国临床应用最早的中药材之一,始载于我国现存最早的药物学著作《神农本草经》,该书将其列为上品,并详细记载了其药用功效“主心腹邪气,肠鸣幽幽如走水,寒热积聚;破症除瘕,止烦满,益气”。2015版《中国药典》列出丹参具有活血祛瘀、通经止痛、清心除烦、凉血消痈的功效,主要用于月经不调、胸痹心痛和心烦不眠等症[1]。丹参的主要药效成分包括脂溶成分丹参酮ⅡA、隐丹参酮、丹参酮Ⅰ和水溶性成分丹参素、丹酚酸B等。随着对中药材丹参需求量的不断增加,丹参地上部分的开发利用也逐渐引起了人们的重视。最新研究发现,丹参地上部分具有含量较高的挥发油,其中丹参花挥发油主要包括β-石竹烯、β-榄香烯、大根香叶烯D、β-石竹烯氧化物、棕榈酸、波旁烯、α-石竹烯等[2-3]。
挥发油是由几十至几百种化合物组成的复杂混合物,萜类及脂肪酸类是其主要组成成分,在植物体内分布非常广泛[4]。挥发油提取的常用方法有水蒸气蒸馏法、超声辅助蒸馏法、有机溶剂萃取法、压榨发、超临界流体萃取法等,其中水蒸气蒸馏法是挥发油提取最常用的方法[5-7]。张丽勇等[8]比较了不同提取方法对青蒿挥发油成分的影响,以及不同提取方法下挥发油抗菌活性能力的差异,结果显示不同提取方法所得挥发油成分不同,其中水蒸气蒸馏的挥发油抗菌活性最强。研究发现挥发油的药理活性与其化学成分密切相关,挥发油中的倍半萜类化合物β-石竹烯、β-榄香烯、α-蛇床烯等具有明显的抗炎、抗氧化、抗菌、抗肿瘤及改善老年痴呆症状的药理作用[9-12]。Li等[13]采用水蒸气蒸馏法对丹参地上部分挥发性成分进行提取,并分析了此部分挥发油的成分及抗菌、抗氧化能力,发现丹参地上部分挥发油具有较强的抗菌、抗氧化作用。本实验在已有研究的基础上,采用单因素和正交试验优化水蒸汽蒸馏法提取丹参花挥发油的工艺流程,应用DPPH法研究了丹参花挥发油的抗氧化活性,并比较不同提取溶液所得丹参花挥发油的抗氧化能力,以期为丹参资源的进一步开发利用提供理论基础。
1 材料与仪器
1.1 材料
丹参花采自山东中医药大学药圃,经山东中医药大学张永清教授鉴定为唇形科植物丹参的花;1,1-二苯基-2-苦基肼(DPPH)(批号:2016027,南京奥多福尼生物科技有限公司)、无水乙醇、浓硫酸、氯化钠、无水硫酸钠、石油醚均为分析纯。
1.2 仪器
UV5100B型紫外分光光度计(上海元析仪器有限公司);挥发油提取器(南京金正玻璃仪器厂);GFL-230型恒温干燥箱(天津市莱玻特瑞仪器设备有限公司);LD-Y500A高速万能粉碎机(上海丁帅电热有限公司);KDM型调温电热套(山东省鄄城新华电热仪器厂);CP225D型十万分之一电子分析天平(上海越平科学仪器有限公司)。
2 实验方法与结果
2.1 丹参花挥发油提取工艺
将新鲜丹参花于50 ℃的恒温干燥箱内烘干,粉碎过20目筛。准确称取100 g丹参花粉末,置于2 000 mL的圆底烧瓶内,加适量水冷浸数小时;加一定量水和2 mL石油醚于挥发油提取器内,置电热套上蒸馏数小时。将水层缓缓放出,收集石油醚层,加入1.5 g无水硫酸钠干燥过夜,除去硫酸钠,自然挥去石油醚得淡黄色的挥发油,称重,-20 ℃条件下保存。按下式计算挥发油收率:
挥发油收率(%)=挥发油重量(g)/丹参花重量(g)×100% 。
2.2 单因素法优化丹参花挥发油提取工艺
根据预实验结果,本文考察了提取溶液、浸渍时间、蒸馏时间和料液比对丹参花挥发油收率的影响。
2.2.1 不同提取溶液对丹参花挥发油收率影响
按照2.1 项下工艺,分别加入14倍量的蒸馏水、饱和氯化钠溶液、pH=1的硫酸水溶液和pH=1的饱和氯化钠硫酸水溶液,冷浸2 h,蒸馏6 h进行提取,每组实验重复3次,取均值,实验结果见图1。比较不同条件下挥发油的收率,结果表明饱和氯化钠和酸性条件下都可以提高挥发油收率。从表1结果可知,在加酸条件下所得挥发油颜色为淡蓝色,而用蒸馏水和饱和氯化钠溶液提取所得挥发油为淡黄色;但是加酸条件下挥发油的气味比较淡,所以加酸提取挥发油的可行性有待于进一步考察。综合考虑各因素,选定饱和氯化钠溶液为提取丹参花挥发油的最佳提取溶液。
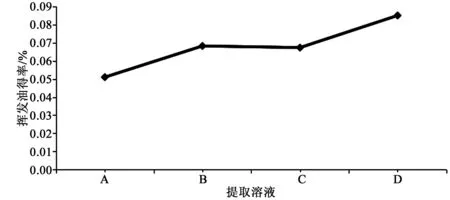
A蒸馏水; B饱和氯化钠溶液; C pH=1的硫酸水; D pH=1的饱和氯化钠硫酸溶液。图1 提取溶液对挥发油收率的影响Fig.1 Effect ofextraction solution on yield of essential oil
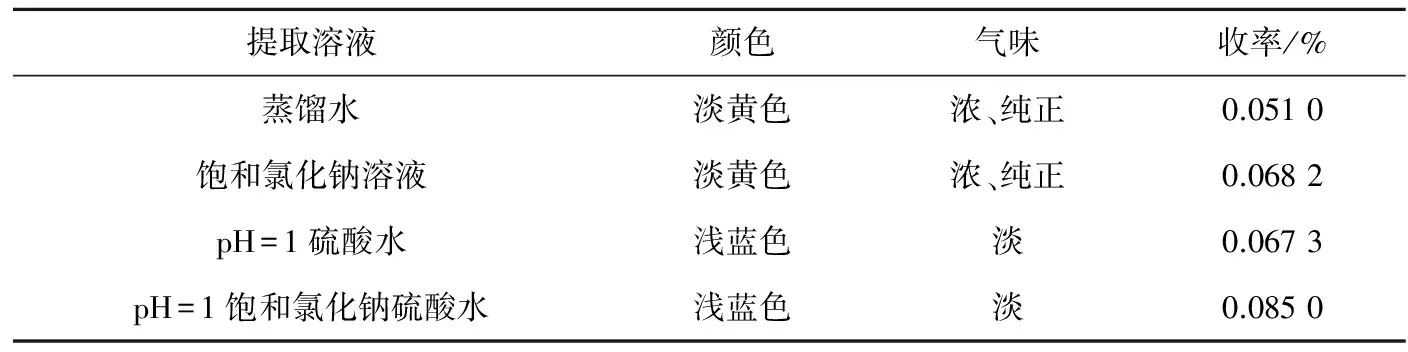
表1 不同提取溶液对挥发油收率及颜色的影响
2.2.2 浸渍时间对丹参花挥发油收率影响
按照2.1 项下工艺,设定了浸渍时间分别为2、3、4、5、6、7、8 h,提取溶液为蒸馏水,料液比(g/mL)为1∶14,蒸馏时间为6 h条件下进行水蒸气蒸馏,收集挥发油,干燥称重计算收率。实验结果见图2。
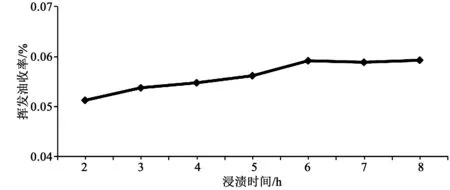
图2 浸渍时间对挥发油收率的影响Fig.2 Effect of soaking time on yield of volatile oil
由图2可知,随着浸渍时间的不断增加,丹参花挥发油的收率稳步上升,其中在6 h时收率达到最大。随后浸渍时间再延长挥发油收率不再明显增加,本着节能省时的原则,采用6 h为最佳浸渍时间。
2.2.3 蒸馏时间对丹参花挥发油收率影响
按照2.1 项下工艺,设定蒸馏时间分别为2、4、6、7、8、9、10 h,提取溶液为蒸馏水,料液比为1∶14,浸渍时间为2 h,水蒸气蒸馏收集挥发油,干燥,称重计算收率。实验结果见图3。
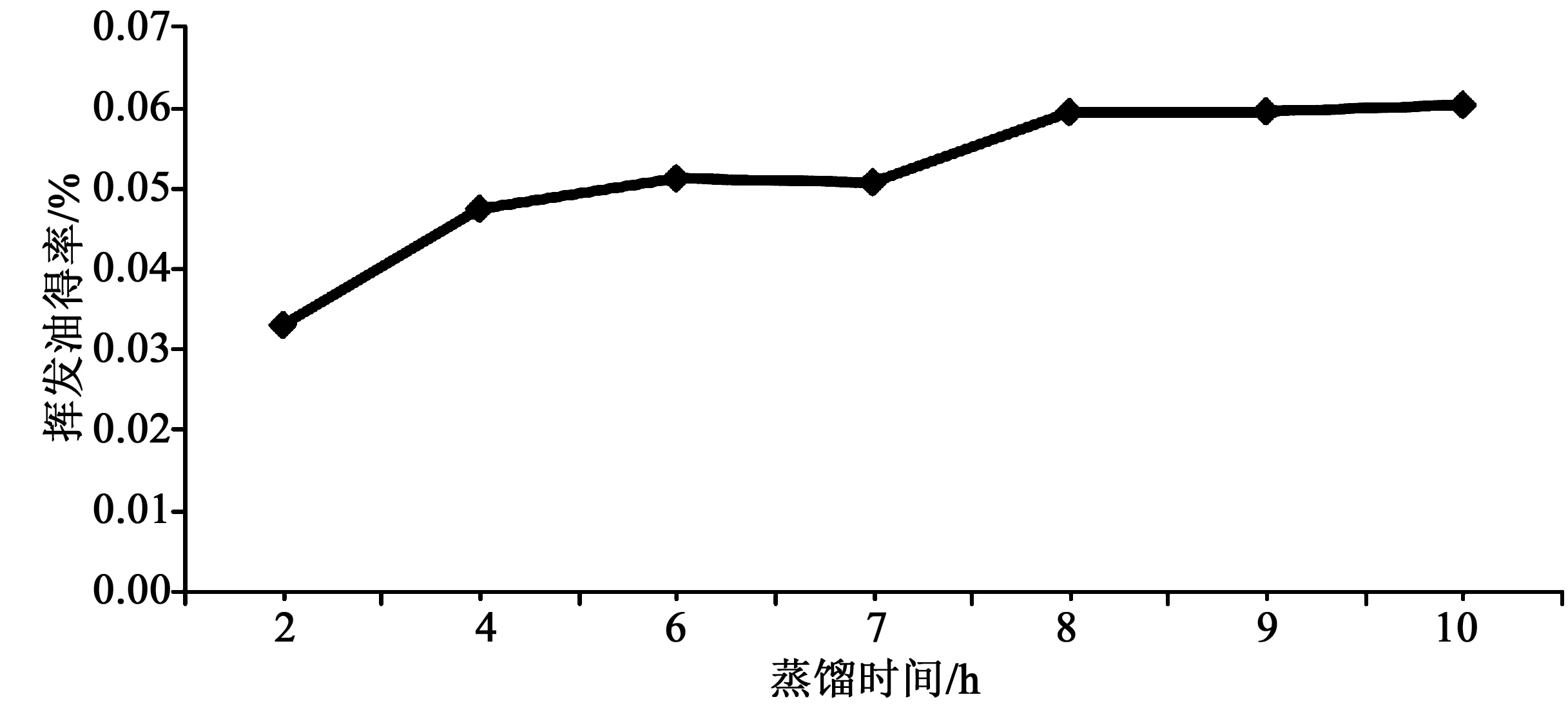
图3 蒸馏时间对挥发油收率的影响Fig.3 Effect of distillation time on yield of volatile oil
由图3可知,在一定时间范围内随着蒸馏时间的延长,丹参花挥发油的收率不断增加,当蒸馏时间为8 h时挥发油收率达到最大值。
2.2.4 料液比对挥发油收率影响
按照2.1项下工艺,设定料液比分别为1∶8、1∶10、1∶12、1∶14、1∶16、1∶18、1∶20,在提取溶液为蒸馏水,浸渍时间为2 h ,提取时间为6 h条件下,水蒸气蒸馏收集挥发油,干燥,称重计算收率。实验结果见图4。
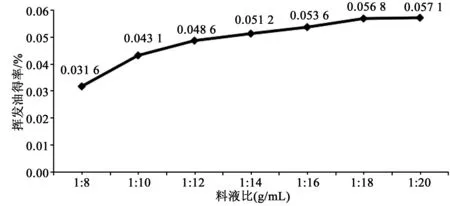
图4 料液比对挥发油收率的影响Fig.4 Effect of material / solution ratio on yield of volatile oil
由图4可知,在其他实验条件不变的情况下,随着料液比例的不断减小,挥发油收率呈现一定的上升趋势,但料液比达到1∶18以后,挥发油收率随料液比变化不再明显,本着节水和尽可能得到较高挥发油收率的原则,本实验选定1∶18为丹参花挥发油提取的最佳料液比。
由各单因素实验结果,综合考虑挥发油收率和挥发油外观形状,本实验选定应用饱和氯化钠溶液、料液比1∶18、浸渍时间6 h、蒸馏时间8 h为丹参花挥发油的最优提取工艺。
2.3 正交试验优化丹参花挥发油提取工艺参数
2.3.1 正交试验设计
参照单因素实验结果,综合考虑丹参挥发油的外观性状和收率,本正交试验选择饱和氯化钠溶液为蒸馏溶剂,然后选择浸渍时间(A),蒸馏时间(B)和料液比(C)3个因素,每个因素分3个水平,设计L9(34)正交试验,因素水平表见表2。

表2 正交试验因素水平表
2.3.2 正交试验结果
按照表2的实验设计和2.1 项下工艺进行实验,计算挥发油收率,实验结果见表3、4。
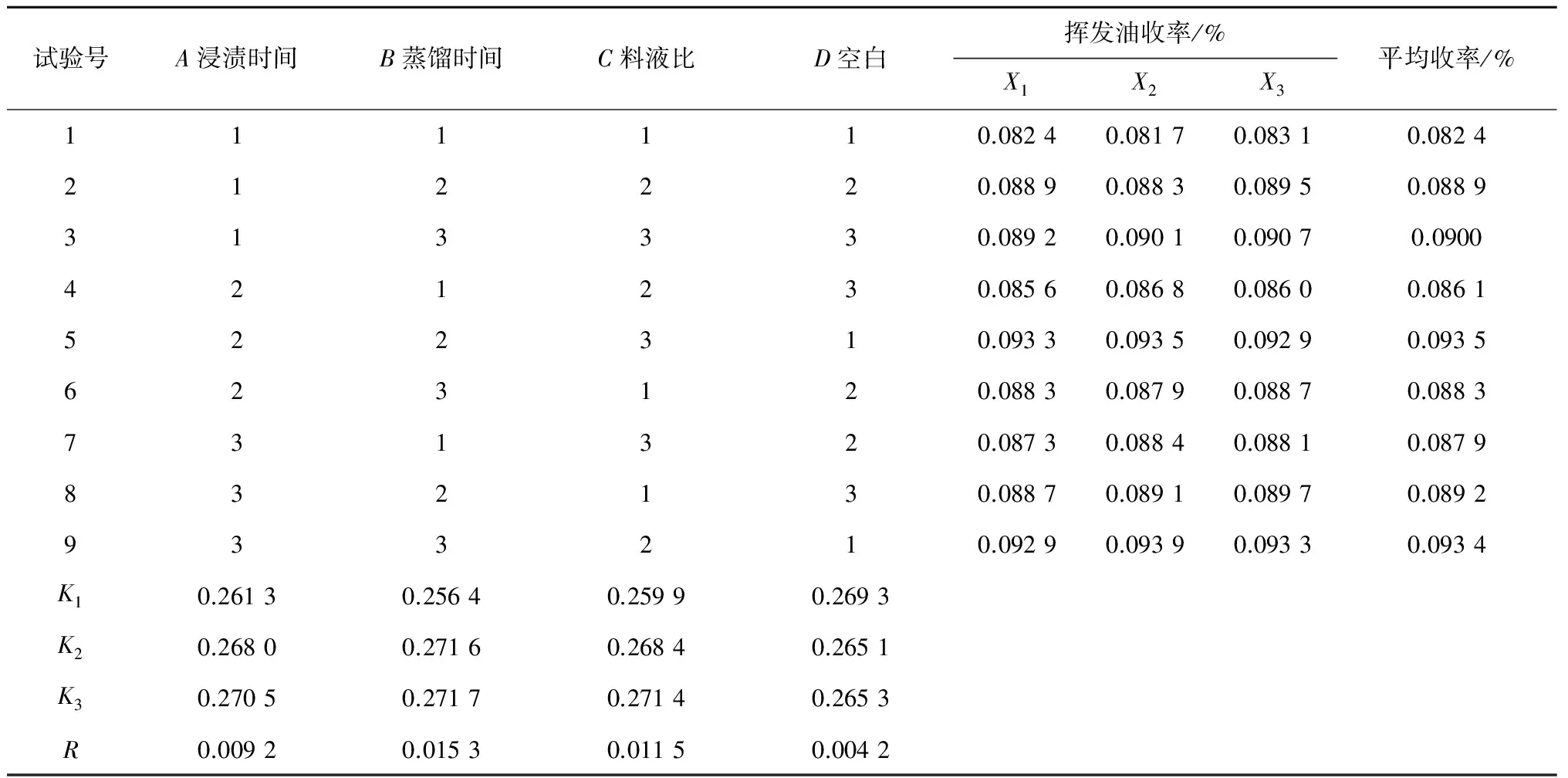
表3 挥发油提取L9(34)正交试验表
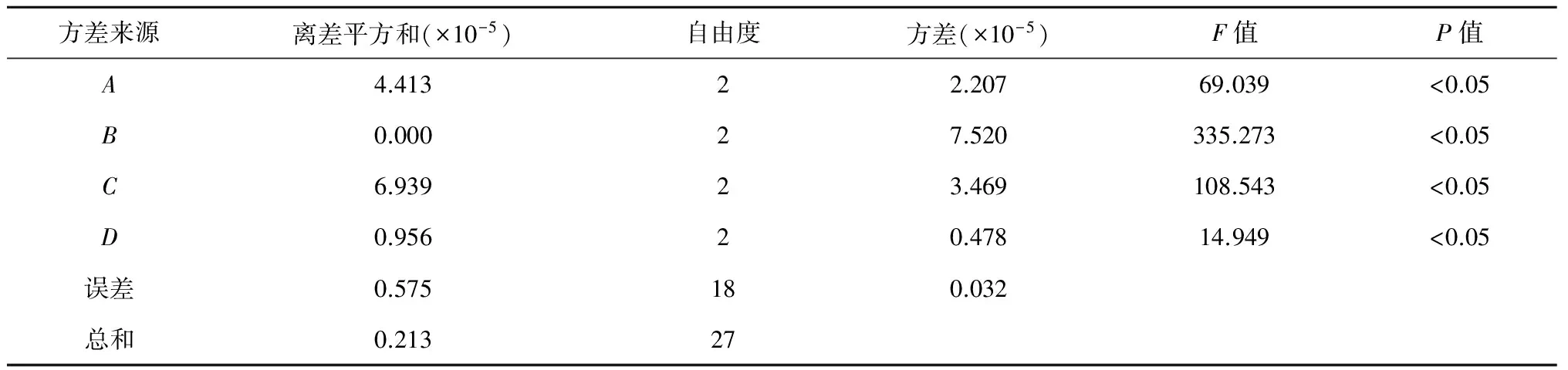
表4 挥发油提取方差分析表
综合表3的极差分析和表4的方差分析结果可知,3种因素对丹参花挥发油提取率的影响都有显著性的统计学意义(P<0.05)。其中蒸馏时间(B)对挥发油提取率的影响最大,其次为料液比(C),浸渍时间(A)影响最小。所以丹参花挥发油的最佳提取工艺为A2B2C3,即浸渍6 h、蒸馏8 h、料液比1∶18 (g/mL)。正交试验结果与单因素实验结果一致。
2.3.3 验证实验
为进一步验证正交试验结果的重现性与可靠性,分别称取3组100 g丹参干燥花细粉,按照正交试验结果的最优条件,根据2.1 项下工艺进行蒸馏实验,3组实验挥发油的收率分别为0.094 3%、0.092 7%、0.092 9%,3组的平均收率为0.093 3%,相对标准偏差为0.94%。说明正交试验所得丹参花挥发油的最佳提取工艺稳定、可靠。
2.4 丹参花挥发油抗氧化活性研究
2.4.1 样品溶液及DPPH溶液的配制
准确称取各提取溶剂所得挥发油适量,用无水乙醇定容至50 mL的容量瓶中,低温保存。准确称取35 mg DPPH用无水乙醇溶解,稀释定容至100 mL的容量瓶中,得0.35 mg/mL DPPH溶液,低温储存。临用稀释至35 μg/mL。
2.4.2 丹参花挥发油清除DPPH能力的测定计算
各量取1 mL样品溶液和2 mL DPPH溶液,充分混匀,室温,静置避光条件反应数小时。517 nm波长下测定各组吸光度,每组重复3次。
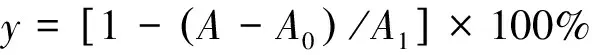
其中,y为样品对DPPH的清除率;A为3 mL样品溶液+3 mL DPPH的吸光度;A0为3 mL样品溶液+3 mL无水乙醇的吸光度;A1为3 mL DPPH+3 mL无水乙醇的吸光度。
2.4.3 反应时间对丹参花挥发油清除DPPH能力的影响
取2.4.1 项下配置的浓度为1 mg/mL的样品溶液,按2.4.2 项下方法与一定体积的DPPH溶液充分混匀,室温,静置避光条件下分别反应0.5、1、1.5、2、3、4、6、8、10、12、14 h,517 nm波长下测定吸光度,按上述公式计算各反应时间点样品对DPPH的清除率,实验结果见图5。
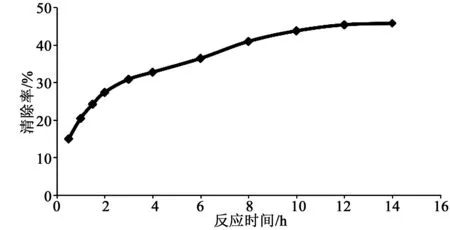
图5 反应时间对挥发油DPPH自由基清除率的影响Fig.5 Effect ofreaction time on DPPH free radical scavenging rate of essential oil
由图5可知,在一定时间内丹参花挥发油对DPPH的清除率不断增加,12 h以后清除率变化不再明显,表明该时间点以后挥发油基本反应完全。所以本着省时的原则,可以认为12 h为丹参花挥发油清除DPPH的时间节点。
2.4.4 丹参花挥发油抗氧化活性的比较研究
取2.4.1 项下配置的系列样品溶液,按2.4.2 项下方法测定各提取液所得挥发油对DPPH的清除率。从得到的实验数据中可以发现,当丹参花挥发油浓度过高或过低时,挥发油对DPPH的清除率y对挥发油浓度x不成线性正相关变化;在清除率为20%~80%范围内,y随x的变化具有良好的线性关系。所以选择此范围内样品对DPPH的清除率y对样品浓度x建立线性回归方程,并计算蒸馏水、饱和氯化钠溶液、pH=1的硫酸水、pH=1的饱和氯化钠硫酸水提取所得挥发油对DPPH清除的IC50值,其结果见表5。
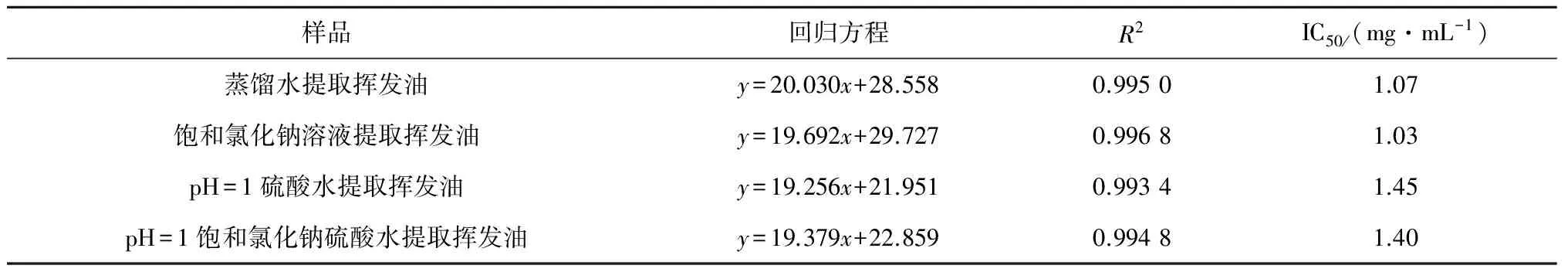
表5 提取溶液对挥发油抗氧化IC50值的影响
由表5实验结果可知,在清除率为20%~80%范围内,清除率y与挥发油浓度x线性关系良好。蒸馏水、饱和氯化钠溶液、pH=1硫酸水和pH=1的饱和氯化钠硫酸水提取所得挥发油对DPPH清除率的IC50值分别为1.07、1.03、1.45、1.40 mg/mL,IC50值越低说明该样品抗氧化能力越强,所以在酸性条件下蒸馏提取的丹参花挥发油抗氧化性普遍降低,而加盐对挥发油的抗氧化能力没有显著影响。故作者认为利用水蒸气蒸馏法提取丹参花挥发油不宜加硫酸提取,此结论与2.2.4 项下结论一致。
3 结论
本研究首次应用正交试验对水蒸气蒸馏法提取丹参花挥发油工艺进行优化,并通过清除DPPH自由基的实验对丹参花挥发油的抗氧化活性进行探究。在考察提取溶液对实验结果影响的过程中发现,饱和氯化钠溶液和加酸提取液能明显增加挥发油的收率,可能因为饱和氯化钠可以减少挥发油在水中的溶解性;而在酸性条件下硫酸可以破坏细胞的黏膜层,水解苷类化合物生成某些挥发性萜类,促进了挥发油的提取。但在考察丹参花挥发油抗氧化能力的实验中发现,加硫酸提取的挥发油对DPPH自由基的半数清除率IC50值明显大于不加硫酸所得挥发油。说明硫酸虽然能提高水蒸气蒸馏法提取丹参挥发油的收率,但却明显降低了丹参花挥发油的抗氧化能力,可能因为丹参花挥发油的主要成分为萜类化合物,而萜类化合物多为不饱和结构,在强酸条件下其结构易被硫酸氧化破坏失去原有的还原能力。所以饱和氯化钠水溶液为丹参花挥发油的最佳提取溶液,丹参花挥发油的最佳提取工艺为:饱和氯化钠为溶液、浸泡6 h、蒸馏8 h、料液比1∶18,在此条件下挥发油收率最高,为0.093 3%。
综合本研究实验数据可知,丹参花挥发油抗氧化活性显著,利用价值较高,可为丹参资源的进一步综合开发利用提供可靠的参考依据。但丹参花挥发油的抗炎、抗菌、抗肿瘤及改善老年痴呆症状的药理作用有待于进一步地研究,这是本课题组今后的工作方向。
[1]国家药典委员会.中华人民共和国药典2015年版一部[M].北京:中国医药科技出版社,2015:76-77.
[2]周晓希.中国丹参挥发性成分评价与活性分析[D].西安:陕西师范大学,2014.
[3] 梁倩,王俊儒,梁宗锁.丹参花挥发油GC指纹图谱的建立[J].西北林学院学报,2008,23(4):152-155.
[4] 吴立军. 实用天然有机产物化学[M].北京:人民卫生出版社, 2007:1011-1013.
[5]李秀琴,孙秀燕,何仲贵,等.柴胡挥发油提取方法的研究[J].中国药学杂志,2004,39(2):103-105.
[6]段宾宾,刘鹏飞,王文基,等.不同提取方法对怀菊花挥发油成分的影响及挥发油在卷烟加香中的应用[J].烟草化学,2011(5):48-52.
[7]罗凯,朱琳,阚建全.水蒸汽蒸馏、溶剂萃取、同时蒸馏萃取法提取花椒挥发油的效果比较[J].食品科技,2012,37(10):234-236.
[8]张丽勇,林秀梅,战月,等.不同方法提取青蒿挥发油成分分析及抗菌活性比较[J]中国实验方剂学杂志,2011,17(22):60-63.
[9] DAHHAM S S, TABANA Y M, IQBAL M A, et al. The anticancer, antioxidant and antimicrobial properties of the sesquiterpene β-Caryophyllene from the essential oil ofAquilariacrassna[J]. Molecules, 2015, 20:11808-11829.
[10] HOU J, SUN T, HU J, et al. Chemical composition, cytotoxic and antioxidant activity of the leaf essential oil ofPhotiniaserrulata[J]. Food Chemistry, 2007, 103(2): 355-358.
[11] JUNG J I, KIM E J, KWON G T , et al. β-Caryophyllene potently inhibits solid tumor growth and lymph node metastasis of B16F10 melanoma cells in high-fat diet-induced obese G57BL/6N mice[J].Carcinogenesis,2015,36(9):1028-1039.
[12] CHENG Y, DONG Z, LIU S. β-caryophyllene ameliorates the alzheimer-like phenotype in APP/PS1 mice through CB2 receptor activation and the PPARγ pathway[J]. Pharmacology, 2014, 94(1/2):1-12.
[13] LI X, WANG Z Z.Chemical composition, antimicrobial and antioxidant activities of the essential oil in leaves ofSalviamiltiorrhizaBunge[J].Journal of Essential Oil Research, 2014, 21(5): 476-480.
Study on extraction technology of volatile oil from flower ofSalviamiltiorrhizaBge. and its antioxidant activity
CHEN Yan-wen, LI Yu-juan, HU Jing-hong, XI Xiao-zhi, LIU Qian, LI Jia, HAO Zhi*
(Shandong University of Traditional Chinese Medicine, Jinan 250355, China)
∶Through single factor experiment and L9(34) orthogonal test, the extraction process of volatile oil from flower ofS.miltiorrhiza. by steam distillation was optimized and the effects of different extraction solutions, soaking time, extracting time, and solid-to-liquid ratio on the yield of the volatile oil from the flower ofS.miltiorrhiza. were investigated. The antioxidant capacity of volatile oil fromS.miltiorrhizaflower was evaluated by DPPH method, and the free radical scavenging capacities of volatile oils from different extraction solutions were compared. The results showed that the primary factors affecting the yield of volatile oil fromS.miltiorrhizaflower were distillation time, followed by solid-liquid ratio and soaking time. The optimum extraction conditions were as follows: saturated sodium chloride solution, soaking 6 hours, extracting 8 hours, solid-to-solvent ratio 1∶18(g/mL). Under this condition, the extraction rate of volatile oil from flower ofS.miltiorrhizawas 0.0935%. The DPPH assays showed that volatile oil from flower ofS.miltiorrhizahas significant antioxidant capacity. In a certain concentration range, antioxidant capacity was positively correlated with the concentration of volatile oil from flower ofS.miltiorrhiza. In the DPPH assays, the IC50values of volatile oil extracted by four kinds of extraction solution (distilled water, saturated sodium chloride solution, aqueous sulfuric acid of pH=1, saturated sodium chloride and aqueous sulfuric acid of pH=1) were 1.07, 1.03, 1.45 and 1.40 mg/mL, respectively. The results showed that the optimized extraction process of volatile oil from flower ofS.miltiorrhizawas stable and practicable.
∶ flower ofS.miltiorrhiza; volatile oil; extraction process; DPPH; antioxidant activity
10.3976/j.issn.1002-4026.2017.04.004
2017-03-06
山东省科技发展计划(2008GG2NS02022);山东省现代农业产业技术体系中草药产业创新团队建设项目(2015);山东省高等学校科技计划(J15LM55)
陈燕文(1990—),男,硕士研究生,研究方向为中药资源及其质量控制。
*通信作者,郝志(1968—),男,博士,副教授,研究方向为中医心理学。E-mail:haozhizy@163.com
R284.2
A
1002-4026(2017)04-0019-07
