土壤矿物对有机质的吸附与固定机制研究进展*
2017-08-31磊应蓉蓉石佳奇龙林玉锁
王 磊应蓉蓉石佳奇龙 涛†林玉锁
(1 环境保护部南京环境科学研究所,南京 210042)
(2 国家环境保护土壤环境管理与污染控制重点实验室,南京 210042)
土壤矿物对有机质的吸附与固定机制研究进展*
王 磊1,2应蓉蓉1,2石佳奇1,2龙 涛1,2†林玉锁1,2
(1 环境保护部南京环境科学研究所,南京 210042)
(2 国家环境保护土壤环境管理与污染控制重点实验室,南京 210042)
鉴于土壤有机质在生态系统及碳储存方面的重要性,关于土壤矿物对土壤有机质的吸附与固定机理方面的研究越来越受到了学术界的广泛关注。本文综述了近年来报道较多的土壤矿物对土壤有机质的吸附机制,以及主要影响因素。在众多矿物类型中,水合铁、铝氧化物及黏土矿物对有机质的吸附性较强,配体交换、络合、氢键、阳离子桥接、缩合及范德华力作用是土壤矿物与有机质之间的主要作用机制。土壤pH是影响矿物表面电荷及吸附位点的关键因素,进而影响矿物对有机质的吸附。土壤矿物表面的有机质含量对其继续吸附有机质具有一定的影响。吸附态有机质大多呈层状结构,越接近矿物表面的有机质与土壤矿物的结合越紧密。土壤有机质的稳定性受有机质与矿物间的作用力影响,一般而言,以化学键合吸附在矿物表面的有机质最稳定,其次为直接与矿物表面作用的电子“供体-受体”机制,范德华力和静电作用稳定性较差。近年来,随着分析设备和技术的进步,一些新的表征与探测方法(如热重分析、差示扫描量热法、傅里叶转换红外光谱、扫描电子显微镜、原子力显微镜、扫描透射X射线显微镜、中子散射技术等)被用于“矿物-有机质”结合机制的研究中,这些新手段毫无疑问会帮助更好地认识矿物与有机质间的作用机理。关于微生物在矿物吸附有机质、“矿物-有机质”复合体形成和演化过程中所起的作用,研究相对较少,但很明显这是至关重要的。
土壤有机质;土壤矿物;吸附及固定;作用机制;“矿物-有机质”复合体
土壤有机质是陆地碳元素的主要存在形式,是陆地有机碳最大的汇,土壤有机质中的碳含量较全部空气和植物中碳元素含量的总和还要多,据报道,土壤中约储存了1.46×1016kg的有机碳[1]。土壤有机质在生态系统、环境保护及全球碳储存与循环中重要性不言而喻。近年来,关于土壤矿物对土壤有机质的吸附与固定机理方面的研究受到了学术界的广泛关注[2-10]。矿物类型及矿物的物理化学性质均被证明会对矿物与有机质之间的作用机理造成不同程度影响[11-15]。
土壤有机质与土壤矿物是土壤的重要组成成分,也是土壤中化学性质最活跃的两种组分,二者密不可分。土壤矿物按成因可以分为原生矿物和次生矿物,但化学性质活泼且对土壤性质影响较大的主要为次生矿物[12,14]。相较于土壤矿物,土壤有机质来源更广,成分更加复杂。腐殖质是土壤有机质存在的主要形态类型,占土壤有机质总量的85%~90%,因此土壤有机质大多指土壤腐殖质。从溶解性上可以将腐殖质分为腐殖酸、富里酸及胡敏素,其中,腐殖酸及富里酸溶解性较好,是可溶性有机质(Dissolved organic matter,DOM)的主要成分,而胡敏素不可溶。由于腐殖酸和富里酸具有一定的溶解性,因此两者是土壤有机质在土壤及地下水中迁移的主要形式。
表层与深层土壤有机质的组成区别主要在于其来源。表层土壤有机质受季节、土地利用方式、植物演替和外来有机质输入影响较大,因此,这部分有机质的差异较大,化学结构较为无序,性质不稳定。虽然表层土壤(通常指有机残落物层和淋溶层土壤上部)的有机质含量明显高于下层,但是表层土壤中的有机质有相当一部分以其生物残体及初级降解产物的形式存在,缺少一定的保护,矿化速率一般高于下部淋溶层和风化层的有机质[10-11]。吸附在矿物表面或存在于土壤团聚体内部的土壤有机质结构和形态较为稳定[3]。因此,从有机质的储存角度而言,表层土壤有机质的稳定性不如深层土壤(淋溶层和风化层)有机质。土壤有机质自土壤表层向深层次迁移的主要方式是通过上层有机质的淋溶转移。下层土壤有机质含量通常较低,因此,下层土壤对有机质的固定通常是指土壤矿物对DOM的吸附[4]。
近年来,关于土壤矿物与有机质作用机制的研究主要集中于以下四个方面:(1)土壤矿物对有机质的吸附与解吸;(2)矿物性质(pH、有机质含量)对吸附有机质的影响;(3)吸附态有机质的结构与稳定性;(4)矿物-有机质作用机制的研究方法。本文主要从以上角度对近期的研究进展进行概括与总结。
1 土壤矿物对有机质的吸附与解吸
土壤矿物对有机质的固定主要是由于土壤矿物的吸附作用,土壤矿物对土壤有机质的吸附造成了矿物表面性质的改变[16-18]。有研究表明,土壤有机质在土壤矿物表面的吸附与解吸作用是控制土壤有机质流动及生物降解的主要因素[12]。一般而言,吸附于土壤矿物表面的有机质与吸附前的有机质在性质上有较显著的差异,例如:提高了有机质的热稳定性和化学稳定性,导致有机质微结构发生重排[19-20]等。与此同时,土壤矿物表面性质的改变也会造成土壤团聚体结构发生变化。土壤矿物对有机质吸附的环境意义在于:一方面,提高了有机质的稳定性,延长了有机碳在生态系统中的循环周期;另一方面,土壤矿物对有机质的吸附,增强了土壤的吸附能力,提高了土壤固持了养分的能力,降低土壤养分的流失[21]。矿物对土壤有机质吸附有机物污染物的影响在文献[22]中曾有阐述,概括而言,由土壤矿物表面性质主导的有机质的选择性吸附,使原本结构较“无序”的有机质分馏(Fractionation)为极性与非极性组分,从而为有机污染物的赋存提供了更好的场所[22]。
吸附态土壤有机质与土壤矿物结合一般较稳定,难以解吸或去除。相较于吸附前的有机质,吸附态有机质的生物降解速率显著降低,可降解的比例较低[23]。有机质在土壤矿物上的吸附机制主要有配体交换[24]、阳离子桥接与阴离子交换[25-26],以及“熵驱动”疏水分配作用[27]。有机质在土壤矿物表面的吸附与多种因素有关,如土壤矿物类型与含量、土壤pH、土壤团聚体结构及土壤孔隙的水文传质系数等[12-15]。一般而言,富含铁、铝等金属氧化物及黏土矿物的土壤对有机质的吸附作用较强[13,15]。
1.1 土壤矿物对有机质的吸附
土壤矿物中对有机质的吸附起到主要作用的成分主要为次生的黏土矿物和铁铝氧化物。已有研究表明,土壤中黏土矿物和铁氧化物的含量越高,土壤对有机质的饱和吸附量越高[4,15,24,27]。铁铝氧化物与黏土矿物对有机质的吸附机制已有较多报道[2-4,8,24-27]。
配体交换作用及静电作用是铁铝氧化性吸附有机质的主要机制。有研究表明,配体交换形成的络合作用是铁氧化物吸附有机质的主要方式之一[24,28-29]。例如:铁氧化物表面的羟基与有机质中的羧基可以发生配体交换作用,从而吸附在氧化物表面[24]。Chassé和Ohno[8]发现羧基较多的芳香族有机质和含氮的脂肪族有机质对铁氧化物的亲和力较强。此外,由于铁铝氧化物具有两性的特点,在低pH时其表面主要呈现为净的正电荷,高pH时表面主要为净的负电荷。由于土壤有机质大多具有负电性,因而矿物表面带正电的点位是理想的吸附点位[27]。Kothawala等[30]比较了不同深度的5种土纲的52个土壤样品,发现土壤中非晶态(也称可提取态)水合铁铝氧化物含量与其对有机质的饱和吸附量之间具有很好的正相关性。不难理解,定形的晶态金属氧化物有效表面积要明显低于无定形态的金属氧化物。Kaiser和Zech[31]发现,土壤中总铁氧化物含量与对有机质的吸附性也具有很好的正相关性,但该研究没有深入分析成因。因此,无定型态的铁铝氧化物可能是对有机质吸附起主导作用的成分。
与铁氧化物比较,黏土矿物对有机质的吸附作用则较弱,黏土矿物对有机质的吸附主要与本身的比表面积有关。Tombacz等[32]发现两种铁氧化物(赤铁矿砂与四氧化三铁)对腐殖酸的吸附能力要高于高岭石和蒙脱石。Meier等[33]发现在相同条件下针铁矿对有机质的吸附量约为高岭石的3倍。从矿物类型上,蒙脱石和高岭石均为次生铝硅酸盐类矿物,差异在于比表面积。一般而言,黏土矿物比表面积越大,其对有机质的吸附越强[3,13,34-35]。Wang和Xing[36]发现,单位质量的2∶1型蒙脱石对腐殖酸的饱和吸附量约为同等条件下1∶1型的高岭石的两倍。Dontsova和Bigham[37]的研究发现一种微生物多糖在高岭石上的吸附量明显低于蒙脱石。有机质与黏土矿物表面的作用主要是有机质中疏水组分与黏土矿物表面的范德华力。然而,黏土矿物表面通常存在多价阳离子,如钙、镁等,可作为离子桥连接黏土矿物及有机质中的负电基团,促进黏土矿物对有机质的吸附[28,38]。这种情况下,2∶1型的黏土矿物(如蒙脱石)由于层间距有限,表面难以被大分子有机质利用,而尽管高岭石的比表面积较低,但是可以吸附较大分子的有机质,表面利用率较高。
黏土矿物与水合铁铝氧化物的相互作用也会影响彼此对有机质的吸附。有报道发现,水合金属氧化物可以同时与黏土矿物及有机化合物结合,形成“黏土-金属氧化物-有机质”复合体[39-40]。以往研究多集中于黏土矿物和铁铝氧化物单独对有机质的吸附[28,41],事实上,黏土矿物表面的永久性负电荷可以与带正电荷的水合金属氧化物形成静电吸附作用。Saidy等[3,42]最新研究发现,体系中水合铁铝氧化物(水铁矿)的存在会促进有机质在高岭石上的吸附,而同等情况下,对伊利石和蒙脱石吸附有机质的影响较小,研究认为水铁矿所带正电荷可以在中和伊利石表面的负电荷后依然具有一定浓度的正点性,因而对有机质的吸附性依然较好。这些水合铁氧化物通过阳离子离子交换取代部分层间阳离子,从而吸附在黏土矿物的负电中心,类似于改性黏土的取代机理[43-44]。由于2∶1型黏土矿物层间距有限,铁铝氧化物较难以利用此类矿物的内表面,因此,铁铝氧化物的存在对蒙脱石吸附有机质的影响较小。
1.2 吸附态有机质的解吸
吸附在土壤矿物上的有机质一般较难解吸。Saidy等[3]发现,在单步解吸实验中,吸附在黏土矿物或“黏土矿物-金属氧化物”复合物上的有机质,可解吸部分仅占吸附量的6%~14%,即便加入金属氧化物也未使吸附在黏土矿物上的有机质解吸,说明几乎未发生选择吸附。而Kahle等[45]的研究发现有约17%~50%的吸附态有机质可在单步解吸中释放回溶液,解吸比例明显高于Saidy等的实验。比较二者实验方法可以发现,Kahle等的解吸液中添加了硫酸盐。因此,可能是离子的竞争作用加速了部分吸附态有机质的解吸。
吸附机制的不同可能是导致有机质在不同矿物表面解吸差异的主要原因。Kaiser和Guggenberger[29]认为,吸附在水合铁铝氧化物及一些深层土壤矿物上的有机质解吸量极低,在于有机质与土壤矿物间存在化学吸附。Mikutta等[41]认为配体交换作用吸附在矿物表面的有机质难以解吸,而通过阳离子桥接作用或范德华力吸附的有机质较易发生解吸。范德华力存在于黏土矿物的疏水表面与有机质的非极性基团之间,“阳离子桥”是多价离子连接的矿物表面负电中心与带负电的有机质官能团。Saidy等[3]研究发现,“黏土矿物-金属氧化物-有机质”复合物的稳定性对吸附有机质的解吸影响显著。例如吸附在“高岭石-针铁矿”上的有机质解吸率明显低于吸附在单独高岭石、“伊利石-针铁矿”复合矿物和“蒙脱石-针铁矿”复合矿物上的有机质;吸附在“伊利石-水铁矿”复合矿物上的有机质解吸率也明显低于吸附在“伊利石-针铁矿”复合矿物和“伊利石-赤铁矿”复合矿物上的有机质[3]。很多情况下,“黏土矿物-金属氧化物-有机质”复合物的稳定性很可能取决于矿物复合体对有机质的吸附亲和力上。而亲和力的大小具体可反映在矿物复合体对有机质拟合的Langmuir吸附模型(q=qmkc/(1+kc))的参数k中,k值越大,一般认为吸附亲和力越强。因此,矿物对有机质吸附亲和力的大小往往决定了吸附态有机质的稳定性。
2 矿物性质对其吸附有机质的影响
矿物对有机质的吸附受多种因素的影响,除2.1中所述的矿物类型外,pH(或等电点)及有机质含量对其吸附有机质的影响较显著,是近年来相关研究关注的热点。
2.1 pH对矿物吸附有机质的影响
pH对土壤矿物吸附有机质具有较大的影响,这种作用由矿物表面的等电点(Point of zero charge,PZC)决定。Mayes等[4]比较了取自美国中部和东部的213种深层土壤对DOM的吸附情况发现,在所研究的全部土壤中,土壤pH越低,其对DOM的吸附作用越强,吸附等温线的非线性越强。Mayes等的研究选用的土壤数据库相对较为全面,因此,有理由认为pH是土壤矿物吸附有机质的一个很重要的影响因素。Mayes等[4]同时发现,随着土壤pH的增加土壤对有机质的最大吸附量逐渐降低。由于有机质多带有可电离的酸性基团,电离后使有机质显负电。pH较低的土壤一般带有较多的正电荷,从而利于对带负电的有机质的吸附。而pH较高的土壤,可吸附有机质的矿物表面位点较少,因此可能对有机质吸附具有一定的选择性。有研究表明,决定铁氧化物对有机质吸附性的主要因素在于其等电点[17]。相同pH条件下,PZC较高的水合铁氧化物拥有更多的表面正电荷,因此更易于吸附带负电的有机质。此时,配体(阴离子)交换作用是有机质在土壤上的主要吸附机制。当溶液pH上升,矿物表面及溶液中负电荷的增加均不利于这种机制作用[24,27-28]。因此,土壤pH对土壤矿物吸附有机质的影响主要在于土壤pH决定了矿物表面的电荷。
2.2 有机质含量对矿物吸附有机质的影响
关于土壤有机质对土壤矿物吸附有机质的影响,目前的研究尚未有统一的结论。一些研究发现,土壤有机质可能阻挡或占据了部分矿物表面的吸附点位,因此,土壤有机质含量与有机质的饱和吸附量之间具有一定的负相关[12,17,29]。也确实有研究发现,去除部分土壤有机质,会使土壤对有机质的吸附量较处理前明显增加[27]。然而也有一些不同的研究结果,例如,Moore和Turunen[46]发现土壤总有机碳含量与土壤对DOM的饱和吸附量具有较好的正相关性,土壤对DOM的吸附作用强度也随着总有机碳含量的增加而增加。Kothawala等[12]发现在有机质含量丰富的淋溶层中,DOM在该层上吸附浓度能达到1 800 mg kg-1(有机质吸附增量),但同时也指出,此层土壤中较高含量的非晶态铁铝氧化物及较低的pH可能是导致其高吸附量的重要原因。Kleber等[19]提出了“矿物表面有机层”的概念,作者认为矿物表面起初并没有吸附有机质的特殊位点,而是在矿物表面形成的有机分子层为吸附有机质创造了潜在的吸附点位,这种观点也得到了其他研究者的认同[19,47-48]。Mayes等[4]认为,有机质含量越高,表面可供有机质选择的吸附点位越多,有机质“进入”矿物表面较规则的层状“矿物-有机质”复合体中更容易,因此表现在吸附量上也就越大;而对于低有机质含量的土壤矿物,并没有这样的条件。Kaiser和Zech[31]认为DOM的疏水性基团更容易吸附在有机质含量高的土壤上。Qualls[49]发现,DOM可以通过和有机质含量较高的泥煤发生组分上的交换吸附在泥煤上。这里所指的有机质组分交换也可以理解为DOM与土壤有机质之间的竞争吸附。因此,从发生吸附作用的吸附剂而言,一定有机质含量能够促进外源有机质的继续吸附,但这种作用主要体现在吸附态有机质与外源有机质之间的作用,而非矿物直接对有机质的吸附。
3 吸附态有机质的结构及稳定性
3.1 吸附态有机质的结构
吸附态有机质可以分为与土壤矿物直接作用的有机质和间接作用的有机质。与土壤矿物直接作用的有机质是指吸附在矿物表面的第一层有机质,而间接作用的有机质是指不与矿物表面直接接触,发生在有机质分子间的作用,但同时也受到矿物表面吸附能的影响。一般用于研究土壤矿物与有机质的结合形态的主要方法就是通过选择有代表性的土壤矿物与模版有机质分子作用。目前,一般用来模拟有机质吸附的代表物主要有两种:一种是低分子量的合成脂肪酸或芳香酸[50-52],一种是通过化学方法从土壤中提取的腐殖酸和富里酸[53]。直接与矿物表面作用的有机质是通过2.1中所述机制(如络合、静电吸附及范德华力等)作用的。此外,近年来有报道,短程有序(Short-ranged ordered,SRO)的矿物晶体对有机质的吸附主要通过晶体表面的羟基(SRO-OH)与有机质中的特定官能团直接作用[54]。Sollins等[55]提出了一种有机质稳态的概念模型——有机质“叠层”模型,有机质在矿物表面形成了类似洋葱的层状结构。在这个模型中,矿物表面直接与第一层有机质分子作用,优先作用的有机质分子通常含有孤对电子,如胺、酰胺及吡咯等基团。例如,胺基与铁氢氧化物作用,发生亲核取代反应(Fe-OH + R-NH2= Fe-NHR)脱去一分子水形成共价键的Fe-NHR[56]。直接与矿物表面作用的有机质通常具有较强的亲水性,一般带有一个或多个羧酸基团,与矿物表面羟基发生配体交换进而与矿物表面形成络合作用[8,19,57]。吸附了两亲分子的矿物表面疏水性增强(两亲性分子的疏水部分因重排而背向矿物)。此时,更多种类的有机质可以继续吸附在上述有机质分子的表面,并且逐层叠加,形成层状的有机质分子层,如图1所示。Petridis等[57]采用中子反射技术观察葡萄糖、脂肪酸在氧化铝表面的吸附态微观结构,发现亲水性的葡萄糖分子优先吸附在氧化铝的表面,脂肪酸分子继而吸附在葡萄糖分子的外层。
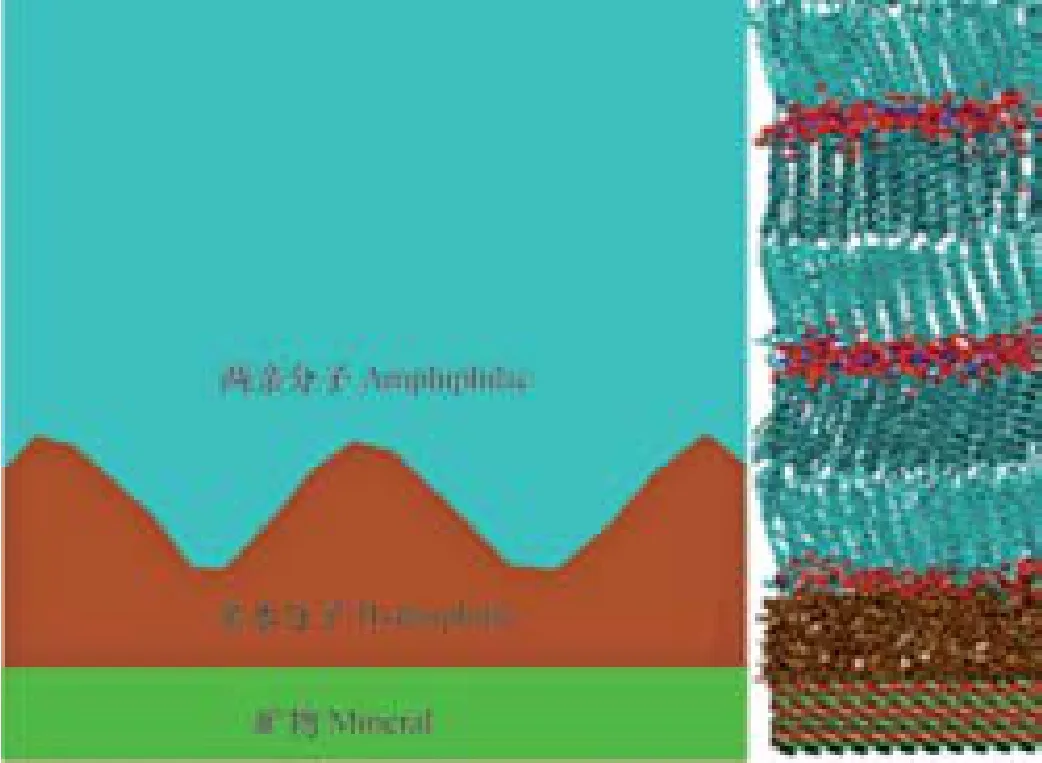
图1 矿物表面层状有机质分子结构示意图[57]Fig. 1 Molecular structure of the organic matter layers adsorbed on the surface of minerals[57]
改性黏土是通过将端部带有阳离子的有机分子与矿物层间交换态的阳离子发生阳离子置换而形成的[58]。当这种两亲性有机分子在黏土矿物上的负载量低于矿物本身的阳离子交换量(Cation exchange capacity,CEC)时,吸附态的两亲有机分子以表面吸附作用为主,呈晶态结构,区别于疏松态有机质本体对有机化合物的分配作用。当两亲性有机质分子的负载量超过其阳离子交换的量的1.5倍(>1.5×CEC)以上时,吸附态有机分子的疏水端之间逐渐融合形成较均质的有机相,也更加接近吸附前的原有形态[43,58-59]。因此可以认为,随着有机质在矿物表面吸附量的增加,有机质受矿物表面吸附力的影响逐步减小,此时,有机质分子相互之间的作用力决定了有机质形态。综上所述,吸附态有机质的形态可以总结为以下两种:(1)吸附在矿物表面的第一层有机质分子以规则的构型存在,与矿物表面的作用最紧密;(2)吸附在矿物表面第二层分子及以上有机质分子,其主要受其相邻两层有机质分子的影响,形态上与未吸附态的有机质类似,但密度一般较吸附态有机质大。
3.2 吸附态有机质与矿物间的作用力
吸附态有机质与矿物间的作用力是决定有机质吸附、解吸及稳定性的重要指标。土壤有机质是一种非均质的有机大分子结构,包含了多种化学基团,这些基团的物理性质、空间排布及反应性各异。因此,在有机质吸附过程中会存在选择性优先吸附以及竞争吸附,从而导致了有机质分子的分级或分馏[60]。据已有的报道可以总结出以下特点:疏水性大分子及部分芳香性有机质易于吸附在黏土矿物的疏水性表面[61-63];含有羧基与酚羟基的有机质更易于吸附在金属氧化物的表面[3,9,19,24,54-57]。前已述及,通过其羧基和酚羟基等基团与金属氧化物表面发生配体交换作用吸附在矿物表面的有机质较难解吸[41]。Oren和Chefetz[2]的研究发现,配体交换作用形成的内圈(Inner-sphere)“有机质-氧化物”络合体较外圈(Outer-sphere)的络合体更稳定,因此认为内圈的络合作用是造成有机质难以从矿物表面解吸的主要原因。Zhu等[64]发现“阳离子-π键”作用也是有机质中富电子芳香结构与矿物表面阳离子间的一种主要作用力。此外,“n-π电子”作用[65-66]及“偶极-偶极”作用[67-68]也曾被报道是矿物-有机质分子之间的常见作用力。而有机质中的脂肪族碳类组分一般仅能通过范德华力与矿物表面作用,这种作用力较弱[2]。总体而言,土壤矿物与有机质分子间的作用力可以分为两类:化学吸附、分子间直接的电子供体-受体(Electron donoraccepter,EDA)作用,这两类作用力较强;静电作用和范德华力作用,这类作用力较弱(表1)。
为进一步比较各代理优化算法的寻优稳健性,对算例1、算例2和算例3分别取仿真预算为T=30、T=20和T=60,在30组随机初始试验设计下求得的优化结果的统计数据如表1所示。从表1中的“最差结果”和“平均结果”可以看出,对全部3个算例,EI-PoF算法都有最高的优化精度,特别是EI-PoF算法求得的“最差结果”也与真实最优响值应非常接近,说明EI-PoF算法具有很强的寻优能力和很高的优化精度。从表1中“标准差”和“寻优成功率”可以看出,EI-PoF算法受初始试验设计随机性的影响最小、获得满意精度最优响应的成功率最高,说明EI-PoF算法稳健性好、寻优可靠度高。
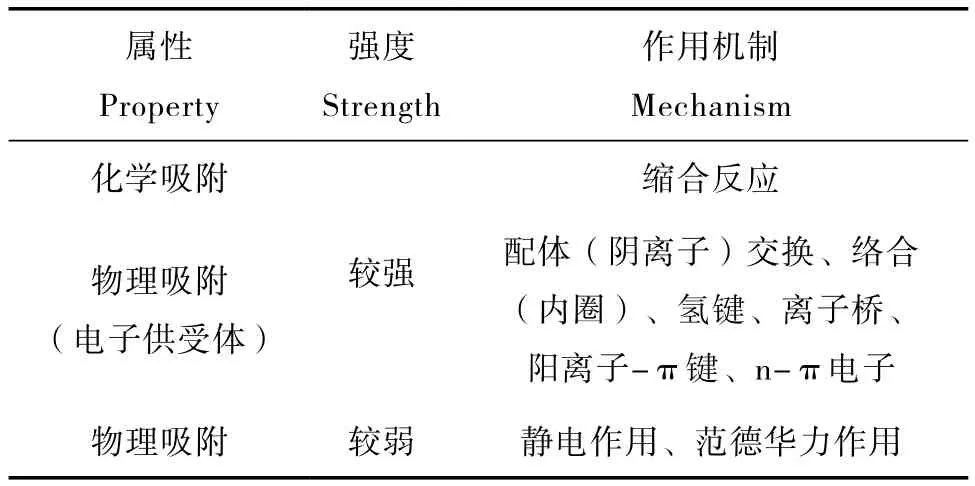
表1 矿物与有机质分子的作用机制Table 1 Classification of mechanisms of the actions between minerals and organic matter molecules
3.3 吸附态有机质的化学稳定性
吸附态有机质的化学稳定性决定了有机质可降解性进而影响其在环境中存在的时间。表层土壤中的有机质含量丰富,仅有小部分为是矿物吸附态有机质。相比较而言,深层土壤(淋溶层以下)有机质大多呈吸附态。因此,吸附态有机质稳定性的研究主要集中于表层土壤中与矿物结合的有机质及大部分深层土壤有机质。一般而言,老化时间较长或者腐殖化程度高的有机质具有较强的稳定性,较难被氧化或者还原。这种说法的依据在于腐殖化程度高的有机质存在较久,所以有理由认为腐殖化过程增加了土壤有机质的稳定性。然而,近年来的一些研究表明,这种观点似乎依据不足。例如,Paul等[69]发现,新老有机质之间并不存在组成以及性质上的差别,老化过程未对有机质最初形成时的状态造成显著的改变。一些研究表明,尚没有充分的证据可以证明腐殖化过程产生了“顽固”的有机质[70-72]。因此,腐殖化过程并非是一个有机质趋于稳定化的过程,腐殖化也并非是指稳定性差的有机质分解,而稳定性强的有机质得以保留。此外,一些研究通过测定有机质中的放射性碳龄发现,覆存于土壤中铝硅酸盐矿物表面、性质并不稳定、可被生物降解的有机质却能够较长时间在土壤环境中存在[55,73-74]。因此,这些研究表明,土壤有机质的稳定性主要是源于土壤矿物对有机质的保护作用。
吸附态有机质的稳定性还在于其抗氧化性。用于比较有机质稳定性的氧化剂主要为自由基型氧化剂,例如活化后的双氧水和过硫酸盐,利用其在催化剂存在下释放的羟基自由基和硫酸根自由基攻击有机质中的富电子基团(不饱和键、胺基、羟基及烷氧基等)[75-76]。同时,化学氧化也是污染土壤修复中较常用的修复手段之一[55,77-78]。如Cuypers等[79]的发现,活化后的过硫酸盐与土壤中无定型态有机质反应性较强,而对浓缩态有机质的影响则较小。土壤中的浓缩态有机质往往与土壤矿物的吸附与持留有关[80]。丁浩然等[81]最近的研究发现氧化剂对表层土壤和深层土壤有机质的氧化效果差异明显——表层土壤有机质的氧化去除率约为深层土壤的2倍以上,说明深层土壤中赋存的有机质较难被氧化。不难推断,易解吸及暴露至溶液中的有机质分子的富电子基团易被氧化。在表层土壤中,大部分有机质为外源动植物残体及其初级降解产物,由于其数量较大,大部分有机质以其本体存在,仅有少部分有机质能被土壤矿物吸附。由于外源有机质本体中极性基团数量较多,因此更容易被氧化。深层土壤有机质主要来源于对上层土壤淋溶DOM的吸附,含量低于表层土壤。DOM中多带有羧基与羟基等易于与土壤矿物直接作用。由于这部分基团与矿物表面的活性位点的作用使其较少的暴露于土壤表面,深层土壤表面因此多呈现出疏水性[55],从而导致有机质与氧化剂的反应程度大大降低。总体而言,氧化剂与土壤有机质间相互作用机理方面的研究还相对较少。据现有的研究结果,与深层土壤有机质相比,表层土壤有机质较容易被氧化[80]。
4 矿物-有机质作用机制的研究方法
近些年来,随着分析手段的进步,一些新的方法也被用来研究“矿物-有机质”复合体之间的作用机制。现有的分析手段主要包括宏观表征法、成像法、同步辐射法等。实际操作中,通常会结合多种分析方法的优点,共同实现对具体作用机制的分析。
4.1 宏观表征方法
简单的“矿物-有机质”作用方法包括pH测定、离子强度、等电点、Zeta电位、表面点位浓度以及比表面积等,这些方法均较为成熟、快捷,也较可靠,可以用来辅助分析“矿物-有机质”的形成及宏观变化[41,82-83]。
傅里叶转换红外光谱(Fourier transform infrared spectroscopy,FTIR)是一种用来获取有机官能团成键信息的方法。FTIR可以单独或者配合显微镜使用,用以获取有机质的空间结构解析,以及“矿物-有机质”之间具体的成键机制。Yoon等[86]运用衰减全反射FTIR光谱技术观察到了草酸分子在勃姆石表面的构象,证实了“矿物-有机质”之间形成的“内圈”键合作用。Parikh和Chorover[87]通过FTIR光谱手段证实了细菌表面的磷酸基在细菌(有机质)与铁氧化物结合体中的重要作用。Person和Axe[88]运用衰减全反射FTIR光谱观察到了不同pH下草酸分子和丙二酸分子分别与针铁矿表面的“内圈”和“外圈”键合作用。
稳定同位素技术也被用来衡量个体有机化合物的转化分析。稳定同位素技术应用的假设前提是含同位素分子的化合物与其他化合物经历同样的化学或生物过程。稳定同位素技术的独特优势还在于能够在不需要确定有机质大分子结构的情况下,确定某个特定官能团与矿物间的作用机制[89]。Kaiser等[90]运用稳定碳同位素比值法成功的量化了可溶性有机质中更易于吸附在矿物表面的疏水性组分比例。Feng等[91]也用类似的方法证明了,相比于其他化学过程,特定组分的有机质更易于吸附在相应类型矿物表面。
4.2 成像方法
与其他方法相比,成像技术可以确定“矿物-有机质”复合体的空间关系,建立复合体构造的视觉概念模型。需要说明的是,这种成像只对某类特定的现象表现出敏感性,并不能提供“矿物-有机质”复合体的综合成像,成像技术也无法获得矿物与有机质间成键的化学性质信息[89]。基于电子技术的成像主要有扫描电子显微镜(Scanning electron microscope,SEM)和透射电子显微镜(Transmission electron microscope,TEM),均可有效地获取“矿物-有机质”复合体的物理结构及有机质在矿物表面的排列图像。
原子力显微镜(Atomic force microscope,AFM)技术可以用来研究物质表面的形貌探测,从而可以用于探查“矿物-有机质”间的成键强度(即键长)及机械性质。Aubry等[92]应用AFM方法研究了疏水性不同的有机质与云母表面官能团间的作用力随离子强度的变化。研究发现,当离子强度增加时,由于双电子层结构的瓦解,有机质中的疏水性组分与云母表面的结合作用更加紧密;而离子强度增大时影响并削弱了“矿物-有机质”间的氢键作用,有机质中的亲水性组分与矿物的键合作用变弱。Rennert等[93]采用AFM的方法测量出德国某地泥煤土(高有机质含量)中“蒙脱石-有机质”复合体的有机质层厚度(约0.9 nm)。Leite等[94]通过AFM手段观察到吸附于云母及石墨表面的有机质分子呈现为“环形”的结构。
4.3 同步辐射加速和中子源技术
同步辐射加速技术也被应用于“矿物-有机质”复合体结构的研究中,该技术利用同步加速辐射源产生的高密度辐射获取“矿物-有机质”复合体的“异质性”或“多相性”信息。Lehmann等[72]使用扫描透射X射线显微镜(Scanning transmission X-ray microscopy,STXM)配合近边缘X射线吸收精细结构谱技术(Near edge X-ray absorption fine structure,NEXAFS)研究了土壤团聚体中有机质微尺度的异质性信息,发现空间解析的土壤有机质形态与提取态有机质并不相同。Henneberry等[95]通过STXM/NEXAFS的方法获得了“铁-有机质”复合体的空间解析信息,研究发现“铁-有机质”复合体的形成是通过溶液中铁与有机质的共沉淀作用形成的独特“化学组分”,这种组分受有机质的化学性质及铁元素的电子结构影响。
基于同步加速的FTIR光谱显微方法也可以被用来揭示“矿物-有机质”复合体的信息。这种方法的优势在于可以同时探测到有机相及矿物相成分,但这同时也增大了特定的结构特征与一个特定的共振图谱间的解析难度。Lehmann等[96]运用这种方法描绘了几种森林土壤样品中土壤团聚内有机大分子和矿物的分布特点。
中子散射(Neutron scattering)技术是一项相对新型的用于有机质结构分析的技术,该技术在探索矿物表面外层有机质分子层状结构上具有较大的优势。Petridis[57]和Mayes[97]均利用中子散射技术观察到天然有机质沉淀在模板矿物表面的层状结构。
研究人员结合质谱技术及显微光谱技术用于对“矿物-有机质”复合体的分析。Remusat等[98]利用扫描射线显微镜(STXM)观察到同位素聚集的微观位点,同时利用高分辨二次离子质谱成像(NanoSIMS)观察到小规模“矿物-有机质”复合体中有机质的异质性。Keiluweit等[99]利用纳米二次离子质谱成像(NanoSIMS)技术,扫描投射X射线显微镜(STXM)以及近边缘X射线吸收精细结构谱(NEXAFS)技术,在3周的时间里,跟踪“矿物-有机质”复合体在富铁矿物表面形成过程,发现铁氧化物在森林有机碳和氮元素循环过程中起到的重要作用。Liu等[100]利用扫描射线显微镜(STXM)确定目标有机质(胞外聚合物)在针铁矿表面分布区域的大小(约100~200 nm),同时利用高分辨二次离子质谱成像技术(NanoSIMS)观察到了矿物表面独特的400 nm大小的富硫区。
5 研究展望
本文所综述的近年来矿物与有机质作用关系的研究进展,能够较充分说明,矿物对有机质的吸附与持留作用是土壤有机质得以稳定存在的重要原因。土壤有机质关系到土壤的诸多性质和功能:农学上,土壤有机质与土壤肥力释放和保持的关系是农业研究重点关注的领域;环境学上,土壤有机质对污染物的吸附、老化及其降解之间的关系是环境研究关注的问题;气候学上,气候学家更多的关注土壤矿物对有机质的吸收、固定以及有机质降解(关系温室气体排放)间的内在调控机制。
随着分析技术的日趋成熟,土壤矿物与有机质间的作用机理会逐步明了。目前亟须阐明的问题可能有以下几个方面:
(1)土壤微生物在矿物对有机质的吸附与固定作用中所起到的作用尚不清楚。微生物的代谢产物本身就是土壤有机质的主要来源。微生物本身与土壤矿物的直接作用也有较多的报道[89,101,102]。微生物表面的胞外聚合物、细胞膜外层蛋白质均可以与矿物表面形成直接作用,其中的羧基、磷酰基可分别与矿物中的金属(如铁和锰等)通过配体交换直接键合[103,104]。此外,微生物需要借助与矿物间的电子传递发生氧化-还原反应获取能量。因此,“土壤矿物-微生物-有机质”之间的关系十分密切。
(2)土壤“矿物-有机质-有机污染物”之间的关系尚不清楚。关于“矿物-有机质-有机污染物”间的关系,需要回答以下四个方面的问题:①有机质与有机污染物竞争矿物表面的吸附位点的作用关系;②有机质可能会造成矿物的溶解,矿物表面形成新的活性点位,这对体系会有怎样的影响;③有机质庞大且众多的活性官能团可以促成矿物和有机污染物之间的电子传递,三者间发生化学反应的机理尚不明确(有报道为还原反应[105])。④有机质作为有机污染物的重要载体(吸附剂),矿物对有机质的吸附如何影响有机污染物的环境行为。
(3)污染土壤化学氧化修复对“矿物-有机质-污染物”环境行为的影响。化学氧化修复通过向土壤和地下水中注入氧化药剂,使之与有机污染物反应生成低毒、无毒的产物。“矿物-有机质”复合体与氧化剂的反应机理和降解产物尚不明确[79-80,106-107],因此具体有以下三个问题尚无法回答:①氧化作用后“矿物-有机质”复合体对污染物的吸附能力的变化尚未有统一的说法[78,81];②氧化剂分别与土壤有机质、有机污染物的作用关系;③有机质氧化的中间产物对有机污染物及其降解产物的吸附行为的影响。
[1] Scharlemann J P W,Tanner E V J,Hiederer R,et al. Global soil carbon:Understanding and managing the largest terrestrial carbon pool. Carbon Management,2014,5(1):81—91
[2] Oren A,Chefetz B. Sorptive and desorptive fractionation of dissolved organic matter by mineral soil matrices. Journal of Environmental Quality,2012,41(2):526—533
[3] Saidy A R,Smernik R J,Baldock J A,et al. The sorption of organic carbon onto differing clay minerals in the presence and absence of hydrous iron oxide. Geoderma,2013,209:15—21
[4] Mayes M A,Heal K R,Brandt C C,et al. Relation between soil order and sorption of dissolved organic carbon in temperate subsoils. Soil Science Society of America Journal,2012,76(3):1027—1037
[5] Kaiser K,Zech W. Dissolved organic matter sorption by mineral constituents of subsoil clay fractions. Journal of Plant Nutrition & Soil Science,2000,163(5):531—535
[6] Gentsch N,Mikutta R,Shibistova O,et al. Properties and bioavailability of particulate and mineral-associated organic matter in Arctic permafrost soils,Lower Kolyma Region,Russia. European Journal of Soil Science,2015,66(4):722—734
[7] Feng W,Plante A F,Aufdenkampe A K,et al. Soil organic matter stability in organo-mineral complexes as a function of increasing C loading. Soil Biology & Biochemistry,2014,69:398—405
[8] Chassé A W,Ohno T. Higher molecular mass organic matter molecules compete with orthophosphate for adsorption to iron(oxy)hydroxide. Environmental Science & Technology,2016,50(14):7641—7649
[9] Lalonde K,Mucci A,Ouellet A,et al. Preservation of organic matter in sediments promoted by iron. Nature,2012,483(7388):198—200
[10] Rumpel C,Kögel-Knabner I. Deep soil organic matter—A key but poorly understood component of terrestrial C cycle. Plant and Soil,2011,338(1/2):143—158
[11] Lumsdon D G,Stutter M I,Cooper R J,et al. Model assessment of biogeochemical controls on dissolved organic carbon partitioning in an acid organic soil. Environmental Science & Technology,2005,39(20):8057—8063
[12] Kothawala D N,Moore T R,Hendershot W H. Soil properties controlling the adsorption of dissolved organic carbon to mineral soils. Soil Science Society of America Journal,2009,73(6):1831—1842
[13] Jardine P M,Mayes M A,Mulholland P J,et al. Vadose zone flow and transport of dissolved organic carbon at multiple scales in humid regimes. Vadose Zone Journal,2006,5(1):140—152
[14] Kalbitz K,Schwesig D,Rethemeyer J,et al. Stabilization of dissolved organic matter by sorption to the mineral soil. Soil Biology & Biochemistry,2005,37(7):1319—1331
[15] Gjettermann B,Styczen M,Hansen H C B,et al. Challenges in modelling dissolved organic matter dynamics in agricultural soil using DAISY. Soil Biology & Biochemistry,2008,40(6):1506—1518
[16] Smernik R J,Kookana R S. The effects of organic matter-mineral interactions and organic matter chemistry on diuron sorption across a diverse range of soils. Chemosphere,2015,119:99—104
[17] Kaiser K,Guggenberger G. Mineral surfaces and soil organic matter. European Journal of Soil Science,2003,54(2):219—236
[18] Lützow M,Kögel-Knabner I,Ekschmitt K,et al. Stabilization of organic matter in temperate soils:mechanisms and their relevance under different soil conditions–A review. European Journal of Soil Science,2006,57(4):426—445
[19] Kleber M,Sollins P,Sutton R. A conceptual model of organo-mineral interactions in soils:Self-assembly of organic molecular fragments into zonal structures on mineral surfaces. Biogeochemistry,2007,85(1):9—24
[20] Chassé A W,Ohno T,Higgins S R,et al. Chemical force spectroscopy evidence supporting the layer-bylayer model of organic matter binding to iron(oxy)hydroxide mineral surfaces. Environmental Science & Technology,2015,49(16):9733—9741
[21] Xu L H,Zhu L Z. Structures of OTMA-and DODMA-bentonite and their sorption characteristics towards organic compounds. Journal of Colloid and Interface Science,2009,331(1):8—14
[22] 王磊,孙成,郭会琴. 土壤有机质对疏水性有机污染物的非线性吸附及其影响因素. 土壤,2012,44(3):366—373
Wang L,Sun C,Guo H Q. Nonlinear sorption of hydrophobic organic contaminants on soil organic matter(In Chinese). Soils,2012,44(3):366—373
[23] Schneider M P W,Scheel T,Mikutta R,et al. Sorptive stabilization of organic matter by amorphous Al hydroxide. Geochimica et Cosmochimica Acta,2010,74(5):1606—1619
[24] Gu B,Schmitt J,Chen Z,et al. Adsorption and desorption of natural organic matter on iron oxide:Mechanisms and models. Environmental Science & Technology,1994,28(1):38—46
[25] Tipping E. The adsorption of aquatic humic substances by iron oxides. Geochimica et Cosmochimica Acta,1981,45(2):191—199
[26] Sposito G. The surface chemistry of natural particles. New York:Oxford University Press,2004
[27] Jardine P M,McCarthy J F,Weber N L. Mechanisms of dissolved organic carbon adsorption on soil. Soil Science Society of America Journal,1989,53(5):1378—1385
[28] Feng X,Simpson A J,Simpson M J. Chemical and mineralogical controls on humic acid sorption to clay mineral surfaces. Organic Geochemistry,2005,36(11):1553—1566
[29] Kaiser K,Guggenberger G. The role of DOM sorption to mineral surfaces in the preservation of organic matter in soils. Organic Geochemistry,2000,31(7):711—725
[30] Kothawala D N,Moore T R,Hendershot W H. Adsorption of dissolved organic carbon to mineral soils:A comparison of four isotherm approaches. Geoderma,2008,148(1):43—50
[31] Kaiser K,Zech W. Nitrate,sulfate,and biphosphate retention in acid forest soils affected by natural dissolved organic carbon. Journal of Environmental Quality,1996,25(6):1325—1331
[32] Tombacz E,Libor Z,Illes E,et al. The role of reactive surface sites and complexation by humic acids in the interaction of clay mineral and iron oxide particles. Organic Geochemistry,2004,35(3):257—267
[33] Meier M,Namjesnik-Dejanovic K,Maurice P A,et al. Fractionation of aquatic natural organic matter upon sorption to goethite and kaolinite. Chemical geology,1999,157(3):275—284
[34] Neff J C,Asner G P. Dissolved organic carbon in terrestrial ecosystems:Synthesis and a model. Ecosystems,2001,4(1):29—48
[35] Sutton R,Sposito G. Molecular simulation of humic substance-Ca-montmorillonite complexes. Geochimica et Cosmochimica Acta,2006,70(14):3566—3581
[36] Wang K,Xing B. Structural and sorption characteristics of adsorbed humic acid on clay minerals. Journal of Environmental Quality,2005,34(1):342—349
[37] Dontsova K M,Bigham J M. Anionic polysaccharide sorption by clay minerals. Soil Science Society of America Journal,2005,69(4):1026—1035
[38] Schlautman M A,Morgan J J. Adsorption of aquatic humic substances on colloidal-size aluminum oxide particles:influence of solution chemistry. Geochimica et Cosmochimica Acta,1994,58(20):4293—4303
[39] Ohtsubo M. Interaction of iron oxides with clays. Clay Science,2011,7(4):227—242
[40] Marco-Brown J L,Barbosa-Lema C M,Sánchez R M T,et al. Adsorption of picloram herbicide on iron oxide pillared montmorillonite. Applied Clay Science,2012,58(1):25—33
[41] Mikutta R,Mikutta C,Kalbitz K,et al. Biodegradation of forest floor organic matter bound to minerals via different binding mechanisms. Geochimica et Cosmochimica Acta,2007,71(10):2569—2590
[42] Saidy A R,Smernik R J,Baldock J A,et al. Effects of clay mineralogy and hydrous iron oxides on labile organic carbon stabilisation. Geoderma,2012,173:104—110
[43] Chen B L,Zhu L Z,Zhu J X,et al. Configurations of the bentonite-sorbed myristylpyridinium cation and their influences on the uptake of organic compounds. Environmental Science & Technology,2005,39(16):6093—6100
[44] Qu X,Liu P,Zhu D Q. Enhanced sorption of polycyclic aromatic hydrocarbons to tetra-alkyl ammonium modified smectites via cation-π interactions. Environmental Science & Technology,2008,42(4):1109—1116
[45] Kahle M,Kleber M,Jahn R. Retention of dissolved organic matter by phyllosilicate and soil clay fractions in relation to mineral properties. Organic Geochemistry,2004,35(3):269—276
[46] Moore T R,Turunen J. Carbon accumulation and storage in mineral subsoil beneath peat. Soil Science Society of America Journal,2004,68(2):690—696
[47] Sollins P,Swanston C,Kramer M. Stabilization and destabilization of soil organic matter—A new focus. Biogeochemistry,2007,85(1):1—7
[48] Sollins P,Kramer M G,Swanston C,et al. Sequential density fractionation across soils of contrasting mineralogy:Evidence for both microbial-and mineral- controlled soil organic matter stabilization. Biogeochemistry,2009,96(1/3):209—231
[49] Qualls R G. Comparison of the behavior of soluble organic and inorganic nutrients in forest soils. Forest Ecology and Management,2000,138(1):29—50
[50] Hanna K,Quilès F. Surface complexation of 2,5-Dihydroxybenzoic acid(Gentisic Acid)at the nanosized hematite-water interface:An ATR-FTIRstudy and modeling approach. Langmuir,2011,27(6):2492—2500
[51] Mudunkotuwa I A,Grassian V H. Citric acid adsorption on TiO2nanoparticles in aqueous suspensions at acidic and circumneutral pH:Surface coverage,surface speciation,and its impact on nanoparticle-nanoparticle interactions. Journal of the American Chemical Society,2010,132(42):14986—14994
[52] Kang S,Xing B. Adsorption of dicarboxylic acids by clay minerals as examined by in situ ATR-FTIR and ex situ DRIFT. Langmuir,2007,23(13):7024—7031
[53] Tinnacher R M,Begg J D,Mason H,et al. Effect of fulvic acid surface coatings on plutonium sorption and desorption kinetics on goethite. Environmental Science & Technology,2015,49(5):2776—2785
[54] Kramer M G,Sanderman J,Chadwick O A,et al. Long-term carbon storage through retention of dissolved aromatic acids by reactive particles in soil. Global Change Biology,2012,18(8):2594—2605
[55] Sollins P,Swanston C,Kleber M,et al. Organic C and N stabilization in a forest soil:Evidence from sequential density fractionation. Soil Biology & Biochemistry,2006,38(11):3313—3324
[56] Gallardo I,Pinson J,Vila N. Spontaneous attachment of amines to carbon and metallic surfaces. The Journal of Physical Chemistry B,2006,110(39):19521—19529
[57] Petridis L,Ambaye H,Jagadamma S,et al. Spatial arrangement of organic compounds on a model mineral surface:Implications for soil organic matter stabilization. Environmental Science & Technology,2014,48(1):79—84
[58] Sheng G,Xu S,Boyd S A. Mechanisms controlling sorption of neutral organic contaminants by surfactantderived and natural organic matter. Environmental Science & Technology,1996,30(5):1553—1557
[59] Bonczek J L,Harris W G,Nkedi-Kizza P. Monolayer to bilayer transitional arrangements of hexadecyltrimethylammonium cations on Na-montmorillonite. Clays and Clay Minerals,2002,50(1):11—17
[60] Navon R,Hernandez-Ruiz S,Chorover J,et al. Interactions of carbamazepine in soil:Effects of dissolved organic matter. Journal of Environmental Quality,2011,40(3):942—948
[61] Kaiser K,Guggenberger G,Haumaier L,et al. Dissolved organic matter sorption on sub soils and minerals studied by13C-NMR and DRIFT spectroscopy. European Journal of Soil Science,1997,48(2):301—310
[62] Guo M,Chorover J. Transport and fractionation of dissolved organic matter in soil columns. Soil Science,2003,168(2):108—118
[63] Polubesova T,Chen Y,Navon R,et al. Interactions of hydrophobic fractions of dissolved organic matter with Fe3+- and Cu2+-montmorillonite. Environmental Science & Technology,2008,42(13):4797—4803
[64] Zhu D,Herbert B E,Schlautman M A,et al. Cationpi bonding:A new perspective on the sorption of polycyclic aromatic hydrocarbons to mineral surfaces. Journal of Environmental Quality,2004,33(4):1322—1330
[65] Haderlein S B,Schwarzenbach R P. Adsorption of substituted nitrobenzenes and nitrophenols to mineral surfaces. Environmental Science & Technology,1993,27(2):316—326
[66] Qu X,Zhang Y,Li H,et al. Probing the specific sorption sites on montmorillonite using nitroaromatic compounds and hexafluorobenzene. Environmental Science & Technology,2011,45(6):2209—2216
[67] Boyd S A,Sheng G,Teppen B J,et al. Mechanisms for the adsorption of substituted nitrobenzenes by smectite clays. Environmental Science & Technology,2001,35(21):4227—4234
[68] Sheng G,Johnston C T,Teppen B J,et al. Potential contributions of smectite clays and organic matter to pesticide retention in soils. Journal of Agricultural and Food Chemistry,2001,49(6):2899—2907
[69] Paul E A,Morris S J,Conant R T,et al. Does the acid hydrolysis-incubation method measure meaningful soil organic carbon pools? Soil Science Society of America Journal,2006,70(3):1023—1035
[70] Burdon J. Are the traditional concepts of the structures of humic substances realistic? Soil Science,2001,166(11):752—769
[71] Kelleher B P,Simpson A J. Humic substances in soils:Are they really chemically distinct? Environmental Science & Technology,2006,40(15):4605—4611
[72] Lehmann J,Solomon D,Kinyangi J,et al. Spatial complexity of soil organic matter forms at nanometre scales. Nature Geoscience,2008,1(4):238—242
[73] Grasset L,Martinod J,Plante A F,et al. Nature and origin of lipids in clay size fraction of a cultivated soil as revealed using preparative thermochemolysis. Organic Geochemistry,2009,40(1):70—78
[74] Rasmussen C,Torn M S,Southard R J. Mineral assemblage and aggregates control carbon dynamics in a California conifer forest. Soil Science Society of America Journal,2005,69(6):1711—1721
[75] Liao X Y,Zhao D,Yan X L,et al. Identification ofpersulfate oxidation products of polycyclic aromatic hydrocarbon during remediation of contaminated soil. Journal of Hazardous Materials,2014,276:26—34
[76] Sato K,Aoki M,Noyori R. A“green”route to adipic acid:Direct oxidation of cyclohexenes with 30 percent hydrogen peroxide. Science,1998,281(5383):1646—1647
[77] 龙安华,雷洋,张晖. 活化过硫酸盐原位化学氧化修复有机污染土壤和地下水,化学进展,2014,26(5):898—908
Long A H,Lei Y,Zhang H. In situ chemical oxidation of organic contaminated soil and groundwater using activated persulfate process(In Chinese). Progress in Chemistry,2014,26(5):898—908
[78] Sun Y,Pignatello J J. Chemical treatment of pesticide wastes. Evaluation of iron(III)chelates for catalytic hydrogen peroxide oxidation of 2,4-D at circumneutral pH. Journal of Agricultural and Food Chemistry,1992,40(2):322—327
[79] Cuypers C,Grotenhuis T,Nierop K G J,et al. Amorphous and condensed organic matter domains:The effect of persulfate oxidation on the composition of soil/sediment organic matter. Chemosphere,2002,48(9):919—931
[80] Han L F,Sun K,Jin J,et al. Some concepts of soil organic carbon characteristics and mineral interaction from a review of literature. Soil Biology & Biochemistry,2016,94:107—121
[81] 丁浩然,龙涛,林玉锁,等. 活化过硫酸钠氧化土壤对挥发性有机污染物吸附特性的影响. 土壤学报,2015,52(2):336—344
Ding H R,Long T,Lin Y S,et al. Effect of oxidation of soil with reactivated sodium persulfate on soil sorption of volatile organic contaminants(In Chinese). Acta Pedologic Sinica,2015,52(2):336—344
[82] Guggenberger G,Kaiser K. Dissolved organic matter in soil:Challenging the paradigm of sorptive preservation. Geoderma,2003,113(3/4):293—310
[83] Keil R G,Mayer L M. Mineral matrices and organic matter. Treatise on Geochemistry,2014,76(2):337—359
[84] Peltre C,Fernández J M,Craine J M,et al. Relationships between biological and thermal indices of soil organic matter stability differ with soil organic carbon level. Soil Science Society of America Journal,2013,77(6):2020—2028
[85] Mikutta R,Schaumann G E,Gildemeister D,et al. Biogeochemistry of mineral-organic associations across a long-term mineralogical soil gradient(0.3-4100 kyr),Hawaiian Islands. Geochimica et Cosmochimica Acta,2009,73(7):2034—2060
[86] Yoon T H,Johnson S B,Musgrave C B,et al. Adsorption of organic matter at mineral/water interfaces:I. ATR-FTIR spectroscopic and quantum chemical study of oxalate adsorbed at boehmite/ water and corundum/water interfaces. Geochimica et Cosmochimica Acta,2004,68(22):4505—4518
[87] Parikh S J,Chorover J. ATR-FTIR spectroscopy reveals bond formation during bacterial adhesion to iron oxide. Langmuir,2006,22(20):8492—8500
[88] Persson P,Axe K. Adsorption of oxalate and malonate at the water-goethite interface:Molecular surface speciation from IR spectroscopy. Geochimica et Cosmochimica Acta,2005,69(3):541—552
[89] Kleber M,Eusterhues K,Keiluweit M,et al. Chapter One—Mineral-organic associations:formation,properties,and relevance in soil environments. Advances in Agronomy,2015,130(2):1—140
[90] Kaiser K,Guggenberger G,Zech W. Isotopic fractionation of dissolved organic carbon in shallow forest soils as affected by sorption. European Journal of Soil Science,2001,52(4):585—597
[91] Feng W,Plante A F,Aufdenkampe A K,et al. Soil organic matter stability in organo-mineral complexes as a function of increasing C loading. Soil Biology & Biochemistry,2014,69(1):398—405
[92] Aubry C,Gutierrez L,Croue J P. Coating of AFM probes with aquatic humic and non-humic NOM to study their adhesion properties. Water Research,2013,47(9):3109—3119
[93] Rennert T,Kai U T,Heister K,et al. Advanced spectroscopic,microscopic,and tomographic characterization techniques to study biogeochemical interfaces in soil. Journal of Soils and Sediments,2012,12(1):3—23
[94] Leite F L,Bueno C C,Da Róz A L,et al. Theoretical models for surface forces and adhesion and their measurement using atomic force microscopy. International Journal of Molecular Sciences,2012,13(10):12773—12856
[95] Henneberry Y K,Kraus T E C,Nico P S,et al. Structural stability of coprecipitated natural organic matter and ferric iron under reducing conditions. Organic Geochemistry,2012,48(7):81—89
[96] Lehmann J,Kinyangi J,Solomon D. Organic matter stabilization in soil microaggregates:Implications from spatial heterogeneity of organic carbon contents and carbon forms. Biogeochemistry,2007,85(1):45—57
[97] Mayes M,Jagadamma S,Ambaye H,et al. Neutron reflectometry reveals the internal structure of organic compounds deposited on aluminum oxide . Geoderma,2013,192(1):182—188
[98] Remusat L,Hatton P J,Nico P S,et al. NanoSIMS study of organic matter associated with soil aggregates:advantages,limitations,and combination with STXM. Environmental Science & Technology,2012,46(7):3943—3949
[99] Keiluweit M,Bougoure J J,Zeglin L H,et al. Nanoscale investigation of the association of microbial nitrogen residues with iron(hydr)oxides in a forest soil O-horizon. Geochimica et Cosmochimica Acta,2012,95(11):213—226
[100] Liu X D,Lu X C,Sprik M,et al. Acidity of edge surface sites of montmorillonite and kaolinite. Geochimica et Cosmochimica Acta,2013,117(5):180—190
[101] Learman D R,Voelker B M,Vazquez-Rodriguez A I,et al. Formation of manganese oxides by bacterially generated superoxide. Nature Geoscience,2011,4(2):95—98
[102] Lemire J A,Harrison J J,Turner R J. Antimicrobial activity of metals:Mechanisms,molecular targets and applications. Nature Reviews Microbiology,2013,11(6):371—384
[103] Huang P M,Li Y,Sumner M E. Handbook of soil sciences:Resource management and environmental impacts. Boca Raton,Florida:CRC Press,2011
[104] Cagnasso M,Boero V,Franchini M A,et al. ATRFTIR studies of phospholipid vesicle interactions with α-FeOOH and α-Fe2O3surfaces. Colloids & Surfaces B:Biointerfaces,2012,76(2):456—467
[105] Chefetz B. DOM-affected transformation of contaminants on mineral surfaces:A review. Critical Reviews in Environmental Science and Technology,2014,44(3):223—254
[106] Martin F,Gonzalez-Vila F J. Persulfate oxidation of humic acids extracted from three different soils. Soil Biology & Biochemistry,1984,16(3):207—210
[107] Sun H W,Yan Q S. Influence of Fenton oxidation on soil organic matter and its sorption and desorption of pyrene. Journal of Hazardous Materials,2007,144(1/2):164—170
Advancement in Study on Adsorption of Organic Matter on Soil Minerals and Its Mechanism
WANG Lei1,2YING Rongrong1,2SHI Jiaqi1,2LONG Tao1,2†LIN Yusuo1,2
(1 Nanjing Institute of Environmental Sciences,Ministry of Environmental Protection of the People’s Republic of China,Nanjing 210042,China)
(2 State Environmental Protection Key Laboratory of Soil Environmental Management and Pollution Control,Nanjing 210042,China)
Soil is the largest terrestrial organic carbon sink,and soil organic matter is the main form of the carbon stored in the sink. In view of the fact that soil organic matter plays an important role in the ecological system and carbon storage,the topic of soil minerals adsorbing organic matter and its mechanism is getting more and more attention from scientists the world over. This paper presents a review of the papers published in the past years about the mechanisms of soil minerals adsorbing organic matter and its major affecting factors. It is reported that among a huge number of soil minerals,hydrated iron,aluminum oxides and clay minerals are quite high in organic matter adsorbing capacity,ligand exchange,complexation,hydrogen bond,cationic bridge,condensation and Van der Waals force,the main mechanisms,and soil pH,the key factor that influences surface charge and adsorption sites of the mineral and hence adsorption of organic matter. Amount of the soil organic matter already adsorbed on the surface of the minerals also affects somewhat capacity of the minerals keeping on adsorbing organic matter,because the already adsorbed organic matter forms a layer covering part of the surface of the minerals and adsorbing sites thereon,and the closerthe layer to the surface of the minerals,the tighter it adsorbed onto the minerals. Stability of the soil organic matter is affected significantly by the interaction between the organic matter and the minerals. Generally speaking,the adsorption of organic matter via chemical bond is the most stable and followed by that via Electronic“Donor-Acceptor”mechanism(which shows inner-sphere complex between functional groups on the surface of the minerals and the organic matter),and that via Van der Waals force and electrostatic force,in the end. In recent years,with the development of analytic equipment and technologies,some new characterizing and probing methods,such as TG,DSC,FTIR,SEM,TEM,AFM,STXM/NEXAFS,Neutron Scattering,have been invented and used in the studies on mechanisms of mineral-organic matter associations(MOAs). These instrument developments will undoubtedly bring important new insights into mechanisms of MOAs. However,relatively little has been reported about effects of microorganisms on mineral adsorption of organic matter,formation and evolution of MOA,though it is quite obvious that their effects are crucial.
Soil organic matter;Soil minerals;Sorption and immobilization;Mechanisms and affecting factors;Mineral-organic matter associations
X53;X131.3
A
(责任编辑:卢 萍)
10.11766/trxb201611040406
* 国家自然科学基金项目(21607049)、科技部863计划项目(SS2013AA06A608)和江苏省自然科学基金项目(BK20160101)资助 Supported by the National Natural Science Foundation of China(No. 21607049),the National High Technology Research and Development Program of China(No. SS2013AA06A608)and the Natural Science Foundation of Jiangsu Province(No. BK20160101)
† 通讯作者 Corresponding author,E-mail:longtao@nies.org
王 磊(1986—),男,助理研究员,研究方向为土壤与地下水污染控制。E-mail:leiwang@ nies.org
2016-11-04;
2017-03-29;优先数字出版日期(www.cnki.net):2017-04-14
