叉头框蛋白O3a表达下调对人肾小管上皮细胞EMT的影响
2017-06-15姚怡张建林赵虹
姚怡+张建林+赵虹

【摘要】 目的:研究叉头框蛋白O3a(forkhead box protein O3a,FoxO3a)下调对人肾小管上皮细胞(HK-2)上皮-间质转化(EMT)的影响和机制。方法:体外培养HK-2细胞,10 ng/mL TGF-β1诱导HK-2细胞建立EMT细胞模型,Western blot检测E-cadherin、α-SMA表达,证明细胞EMT模型建立成功。Western blot检测在EMT细胞和正常细胞中转录因子FoxO3a的表达变化。敲低正常HK-2细胞中的FoxO3a后,Western blot检测细胞的EMT程度。Western blot检测EMT细胞与低表达FoxO3a细胞中β-Catenin的表达变化。结果:TGF-β1处理HK-2细胞作用后E-cadherin表达量显著减少(P<0.01),α-SMA蛋白表达量明显增加(P<0.05),证明EMT细胞模型建立成功。与正常HK-2细胞相比,EMT细胞中转录因子FoxO3a显著减少(P<0.01)。敲低HK-2细胞中的FoxO3a后,E-cadherin表达量显著减少(P<0.01),α-SMA蛋白表达量明显增加(P<0.05),出现EMT现象。相比于正常细胞,EMT细胞的β-Catenin表达增加(P<0.05);FoxO3a敲低的细胞中β-Catenin表达也显著增加(P<0.01)。结论:HK-2细胞通过降低转录因子FoxO3a的表达,从而上调β-Catenin,促进细胞上皮-间质转分化。
【关键词】 肾小管上皮细胞; FoxO3a; β-Catenin; 上皮-间质转化
【Abstract】 Objective:To explore the effect and mechanism of forkhead box proteinO3a knocking down on the epithelial-to-mesenchymal transition of HK-2 human renal proximal tubular cells.Method:HK-2 cells cultured in vitro,10 ng/mL TGF-β1 induced EMT of HK-2 cells,The expression levels of E-cadherin,α-SMA were determined by Western blot and immunofluorescence assay.The expression of FoxO3a in EMT of HK-2 cells and HK-2 cells were determined by Western blot.Knocking down FoxO3a in the HK-2 cells,the levels of EMT marker proteins were determined by Western blot.The expression level of β-catenin in the EMT of HK-2 cells and low expression FoxO3a of the cells were determined by Western blot.Result:Compared with HK-2 cells incubated with free TGF-β1,the protein expression of E-cadherin significantly decreased(P<0.01),and the expression levels ofα-SMA markedly increased in HK-2 cells(P<0.05).The expression levels of FoxO3a markedly diminished(P<0.01)in HK-2 cells by the inducement of TGF-β1.In knocking down FoxO3a of HK-2 cells,the protein expression of E-cadherin significantly decreased(P<0.01),and α-SMA markedly increased.The expression level of β-catenin in the EMT of HK-2 cells and low expression FoxO3a of the cells significantly increased by Western blot.Conclusion:Down-regulation of FoxO3a could promote EMT of human renal proximal tubular epithelial cells by increasing the expression levels of β-catenin.
【Key words】 Renal proximal tubular cells; FoxO3a; β-Catenin; Epithelial to mesenchymal transition
First-authors address:School of Basic Medical Sciences,Shanxi Medical University,Taiyuan 030000,China
doi:10.3969/j.issn.1674-4985.2017.13.010
慢性腎脏疾病(chronic kidney disease,CKD)由于其发病率高以及增加发生晚期肾脏疾病和心血管疾病的风险,极大地威胁到人类健康[1]。纤维化是所有慢性肾脏疾病的典型性特征,其是因多种病理性因素造成肾脏损伤后,持续的炎症反应使得多种促纤维化细胞因子及血管活性物质表达增加,导致细胞外基质在肾脏间质性腔隙的过度沉积而形成瘢痕[2]。肾实质主要由肾小管上皮细胞组成,肾脏损伤后极易受到影响,所以肾小管上皮细胞受损被认为是进行性肾脏疾病的主要过程。受损的肾小管细胞通过失去上皮标记物和获得间质标记物的过程,完成上皮-间质转化过程(Epithelial-Mesenchymal Transition,EMT)增加了肾脏肌成纤维细胞的数量[3]。肾脏肌成纤维细胞的一种活性形式是α-平滑肌肌动蛋白阳性肌成纤维细胞,这种细胞被广泛认为是在肾纤维化中产生基质的主要细胞类型。叉头框蛋白(forkhead box protein,FOX)家族是调控纤维化的重要转录因子,其重要成员叉头框蛋白O3a(forkhead box proteinO3a, FoxO3a)可以通过抑制β-Catenin的表达,从而达到抑制上皮-间质转分化[4-7]。诱导上皮细胞EMT过程中,转化生长因子(TGF-β1)是其中重要的诱导因子[8]。于是本文章通过TGF-β1诱导HK-2细胞建立EMT模型,观察FoxO3a转录因子是否与人肾小管细胞EMT过程有关,并且检测正常细胞低表达FoxO3a后,细胞EMT的程度。研究细胞EMT后,β-Catenin的表达变化是否与细胞低表达FoxO3a后一致,从而探讨在肾脏细胞中FoxO3a是否通过β-Catenin调节对细胞EMT产生的影响,现报道如下。
1 材料与方法
1.1 主要材料和试剂 人肾小管上皮细胞(HK-2)(中国科学院上海生命科学研究院);Recombinant Human TGF-β1(PEPROTECH);DMEM/F12(HyClone);胎牛血清(Scien Cell);FoxO3a-siRNA、Control-siRNA、FoxO3a抗体、E-cadherin抗体、β-Catenin抗体(Cell Signaling);α-SMA抗体(Abcam)鼠抗GAPDH抗体、辣根酶标记山羊抗兔IgG、辣根酶标记山羊抗鼠IgG、FITC标记山羊抗兔IgG(北京中杉金桥);CY3-羊抗兔IgG(博士德生物)。Lipofectamine RNAiMAX (invitrogen)。
1.2 HK-2细胞培养 配制含有10%胎牛血清及1%青链霉素的DMEM/F12完全培养基,将细胞置于5% CO2、37 ℃的环境下培养。使用0.05%的胰酶含EDTA进行传代,每3~4天传代一次。待细胞的融合率达到20%~30%,无血清培养12 h,将细胞分为对照组(Control)和给药组(Treated)。对照组(-)继续无血清培养,给药组(+)加入浓度为10 ng/mL TGF-β1的无血清培养基,培养72~96 h后收集细胞进行实验。
1.3 细胞总蛋白的提取和Western blot检测 每孔加入RIPA裂解液(碧云天)70 μL,将细胞置于冰上裂解30 min后,收集细胞裂解液到EP管中,4 ℃ 12 000 r/min离心5 min。将上清液转移至新的EP管作为细胞蛋白样品,用BCA法测总蛋白浓度,蛋白样品100 ℃变性10 min进行电泳,每次上样量为60 μg。使用10%的十二烷基硫酸钠–聚丙烯酰胺(SDS-PAGE)凝胶电泳,电转移蛋白至PVDF膜上。5%的脱脂奶粉在室温下封闭2 h。一抗孵育4 ℃摇床过夜,一抗浓度为E-Cadherin(1∶1000)、α-SMA(1∶1000)、FoxO3a(1∶1000)、β-Catenin(1∶1000)、GAPDH(1∶1000)。洗膜。用辣根过氧化物酶标记的山羊抗小鼠或山羊抗兔二抗(1∶5000)稀释液室温孵育1.5 h,洗膜,化学发光法ECL法显色。使用Image J软件对Western条带灰度进行定量分析,以GAPDH为内参。
1.4 转染实验 待正常HK-2细胞融合率达40%~50%,弃去细胞培养基,PBS冲洗2次。六孔板每孔加2 mL无血清培养基,把稀释的Lipofectamine RNAiMAX和稀释的FoxO3a-siRNA及Control-siRNA混匀静置20 min。将Control-siRNA-Lipofectamine RNAiMAX 混合液加入细胞为NC组,FoxO3a-siRNA-Lipofectamine RNAiMAX混合液加入孔中为siRNA组。培养6 h后,加药诱导72 h,收集细胞进行检测。
1.5 统计学处理 采用GraphPad Prism 5软件对所得数据进行统计分析,计量资料用(x±s)表示,比较采用t检验,以P<0.05为差异有统计学意义。
2 结果
2.1 TGF-β1诱导HK-2细胞产生EMT后FoxO3a表达量情况 HK-2细胞中,10 ng/mL TGF-β1作用72 h后,Western blot检测上皮标记物E-Cadherin表达降低(P<0.01),间质细胞标记物α-SMA表达增加(P<0.05),证明EMT模型建立成功。TGF-β1给药组的FoxO3a蛋白含量与对照组相比呈现降低趋势,比较差异有统计学意义(P<0.01),提示FoxO3a与HK-2细胞EMT过程有关,见表1与图1。
2.2 敲低FoxO3a后对细胞EMT程度的影响 将FoxO3a-siRNA转入HK-2细胞中,转染72 h后Western blot检测细胞内的FoxO3a蛋白水平的表达情况。转染FoxO3a-siRNA后细胞内的FoxO3a蛋白含量显著降低(P<0.01),HK-2细胞中的E-Cadherin蛋白含量降低(P<0.01),α-SMA表达量增加(P<0.05),证明敲低转录因子FoxO3a后,可促进HK-2细胞的EMT,进一步证实FoxO3a与HK-2细胞EMT过程有关,见图2。
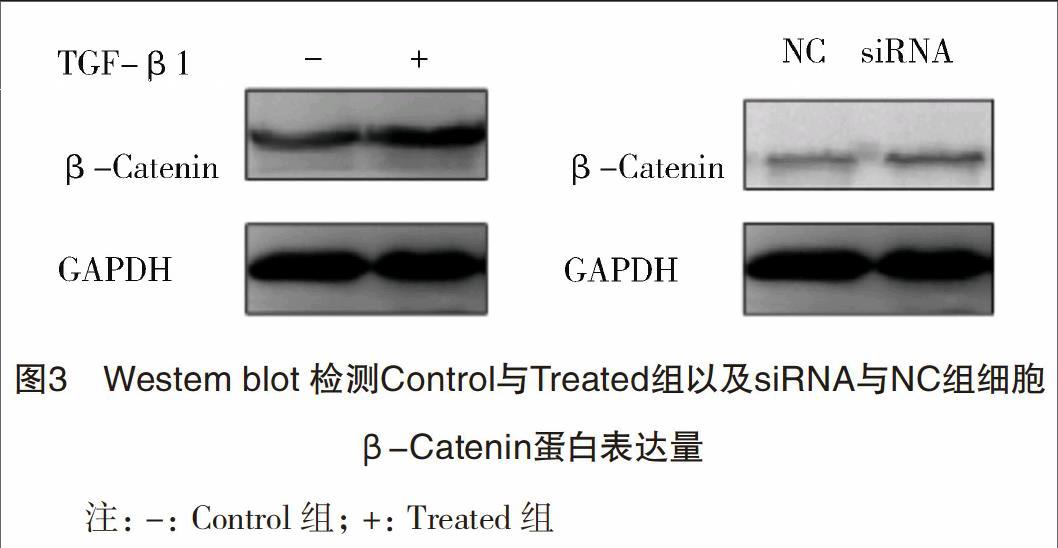
2.3 FoxO3a调控HK-2细胞EMT的可能机制 Western blot结果显示:EMT细胞中AKT通路关键分子β-Catenin表达量增高(P<0.05);而在敲低FoxO3a的 HK-2细胞中β-Catenin蛋白表达增高(P<0.01),在EMT细胞和低表达FoxO3a细胞中β-Catenin表达变化一致,说明当细胞中FoxO3a减少时,可能通过增加β-Catenin表达,促进HK-2细胞EMT。Control组TGF-β1诱导及敲低FOXO3a对HK-2细胞表达β-Catenin为(0.66±0.03),Treated组为(0.83±0.02),NC组为(0.24±0.07)siRNA组为(0.58±0.01),见图3。
3 讨论
纤维化是所有慢性肾脏疾病的主要特征,而肾小管上皮细胞发生EMT是肾脏发生纤维化的重要原因[9]。EMT过程对于肾脏损伤后的肾小管功能障碍和促进纤维化的发展都是重要且必需的。通过敲除Snail和Twist这两个转录因子等手段抑制EMT过程,能够保护肾小管细胞的完整性和功能,恢复肾小管的修復和再生能力,并减少肌成纤维细胞的堆积,减轻多种慢性肾脏疾病模型的间质性纤维化[10]。FOXO转录因子包括FoxO1,FoxO3a,FoxO4和FoxO6。其中FoxO3a又名横纹肌肉瘤样1叉头框(forkhead rhabdomyosar-coma-like 1,FKHRL1),在人类基因中位于6号染色体(6q21)。FoxO3a不仅在细胞的增殖、凋亡、氧化应激反应、衰老等过程中发挥着重要的作用,而且通过与其它转录因子的相互影响,整合不同信号,参与内环境稳定的调控[11]。最近有研究表明用药物增加FoxO3a的活性,可以抑制肺纤维化小鼠的上皮-间质转分化[5]。本研究发现,敲低FoxO3a后,HK-2细胞上皮-间质转化的关键指标E-Cadherin蛋白含量明显减少,而α-SMA蛋白含量与NC组相比显著增加。说明FoxO3a对人肾小管上皮细胞的EMT过程有调控作用。
β-连环蛋白(β-catenin)是细胞膜上钙黏蛋白复合物的主要组成成分,参与Wnt/β-catenin、TGF-β通路、NF-κB通路等多条信号通路。研究报道:TGF-β1可以诱导小管上皮细胞在细胞核中积累β-Catenin,β-Catenin作用于Wnt通路下游基因可导致细胞发生EMT过程,当敲低β-Catenin,能够抑制TGF-β1诱导EMT过程[12]。近来发现在转录因子FoxO3a可以调控β-Catenin的表达,参与癌细胞EMT的细胞通路,但具体机制仍未弄清[7]。本文发现HK-2细胞下调FoxO3a后,不仅EMT程度加深,且β-Catenin含量也增加。FoxO3a调节HK-2细胞EMT的机制可能与β-Catenin有关。综上所述,在HK-2细胞中,FoxO3a可能通过调控β-Catenin蛋白含量,促进肾小管上皮细胞EMT。
但是FoxO3a抑制肾脏纤维化的研究还不充分。过表达FoxO3a,是否能减轻细胞的EMT程度还有待于研究,且FoxO3a通过怎样的机制抑制细胞EMT过程还不清楚。希望通过研究转录因子FoxO3a,今后能够找到于临床治疗慢性肾脏疾病的新手段。
参考文献
[1] Tonelli M,Wiebe N,Culleton B,et al.Chronic kidney diseaseand mortality risk:A systematic review[J].J Am SocNephrol,2006,17(7):2034-2047.
[2] Duffield J S.Cellular and molecular mechanisms in kidney fibrosis[J].J Clin Invest,2014,124(6):2299-2306.
[3] Cannito S,Novo E,Bonzo L V,et al.Epithelial-mesenchymal transition:from molecular mechanisms,redox regulation to implications in human health and disease[J].Antioxid Redox Signal,2010,12(12):1383-1430.
[4] Tikhanovich I,Cox J,Weinman S J.FOXO Transcription Factors in Liver Function and Disease[J].J Gastroenterol Hepatol,2013,28(1):125-131.
[5]彭婷,杜海坚,李理,等.吉非替尼通过增加FoxO3a活性抑制肺纤维化小鼠上皮-间质转分化[J].中国病理生理杂志,2014,30(3):444-448.
[6] Nho R S,Peterson M,Hergert P,et al.FoxO3a (Forkhead Box O3a) deficiency protects Idiopathic Pulmonary Fibrosis(IPF) fibroblasts from type I polymerized collagen matrix-induced apoptosis via caveolin-1(cav-1) and Fas[J].PLoS One,2013,8(4):e61 017.
[7] Liu H,Yin J,Wang H,et al.FoxO3a modulates WNT/β-catenin signaling and suppresses epithelial-to-mesenchymaltransition in prostate cancer cells[J].Cell Signal,2015,27(3):510-8.
[8] Lan A, Qi Y, Du J.Akt2 mediates TGF-β1-induced epithelial to mesenchymal transition by deactivating GSK3β/snail signaling pathway in renal tubular epithelial cells[J].Cell Physiol Biochem,2014,34(2):368-382.
[9] Xiao Z,Chen C,Meng T,et al.Resveratrol attenuates renal injury and fibrosis by inhibiting transforming growth factor-β pathway on matrix metalloproteinase 7[J].Exp Biol Med (Maywood),2016,241(2):140-146.
[10] Zhou D,Liu Y.Renal fibrosis in 2015:Understanding the mechanisms of kidney fibrosis[J].Nat Rev Nephrol,2016,12(2):68-70.
[11]楊小利,欧周罗,邵志敏.多功能的转录因子FoxO3a[J].生命的化学,2012,32(5):447-451.
[12] Tian X,Zhang J,Tan T K,et al.Association of β-catenin with P-Smad3 but not LEF-1 dissociates in vitro profibrotic fromanti-inflammatory effects of TGF-β1[J].J Cell Sci,2013,126(1):67-76.
(收稿日期:2017-03-10) (本文编辑:周亚杰)
