新型丙烯海松酸基双酰胺-噻二唑化合物的合成及生物活性研究
2017-04-24林桂汕阮战辉段文贵刘陆智杨章旗
林桂汕,阮战辉,段文贵*,刘陆智,杨章旗
(1.广西大学化学化工学院,南宁530004;2.广西林业科学研究院,南宁530002)
新型丙烯海松酸基双酰胺-噻二唑化合物的合成及生物活性研究
林桂汕1,阮战辉1,段文贵1*,刘陆智1,杨章旗2
(1.广西大学化学化工学院,南宁530004;2.广西林业科学研究院,南宁530002)
松香是来自松树的非木质林产品,是我国的再生性天然优势生物质资源,主要成分为树脂酸。为拓展松香在生物活性方面的应用途径,以松香为原料,与丙烯酸Diels-Alder加成反应制备丙烯海松酸(1),再与氨基硫脲反应获得丙烯海松酸基双噻二唑(2),最后与系列取代苯甲酰氯进行N-酰化反应,合成得到7个新型丙烯海松酸基双酰胺-噻二唑化合物(3a~3g)。采用FTIR、1H NMR、13C NMR、ESI-MS等技术手段对目标化合物进行结构表征;分别采用稗草小杯法和油菜平皿法测试目标化合物对稗草(Echinochloacrusgalli)株高生长和油菜(Brassicacampestris)胚根生长的抑制活性。结果表明,在100 μg/mL质量浓度下,目标化合物对油菜胚根生长的抑制活性较强,化合物3e(R=p-Br)的抑制率高达92.4%(活性级别为A级),化合物3b (R=p-CH3)和3d (R=p-Cl)的抑制率分别为77.4%和73.2%(活性级别均为B级)。采用离体法(即琼脂稀释法)测试目标化合物对苹果轮纹病菌(Physalosporapiricola)、黄瓜枯萎病菌(Fusariumoxysporumf. sp.cucumerinum)、番茄早疫病菌(Alternariasolani)、小麦赤霉病菌(Gibberellazeae)和花生褐斑病菌(Cercosporaarachidicola)的抑菌活性。结果表明,目标化合物在50 μg/mL质量浓度下对所测5种植物病原菌表现出一定抑制效果。目标化合物3e对油菜胚根生长具有较好的抑制活性,值得进一步研究。
松香;丙烯海松酸;双酰胺-噻二唑;除草活性;抑菌活性
松香是来自松树的非木质林产品,是我国的再生性天然优势生物质资源,其主要成分是三环二萜类树脂酸。通过松香中的左旋海松酸与丙烯酸进行Diels-Alder加成反应可获得松香基二元酸丙烯海松酸(acrylpimaric acid)。利用其具有的稠合多脂环的刚性及二元酸的结构特性,丙烯海松酸已广泛应用于表面活性剂[1]、涂料[2]和胶黏剂[3]等领域。另外,由于丙烯海松酸具有氢化的菲环骨架、手性碳以及多种官能团,其衍生物显示多种生物活性,如丙烯海松酸噻二唑衍生物、丙烯海松双酰基硫脲衍生物、丙烯海松酰胺衍生物对大肠杆菌(Escherichiacoli)显示出较好的抑制活性[4-6]。本课题组曾设计合成丙烯海松酸基双酰胺类化合物和丙烯酸海松酸基双磺酰胺-噻二唑类化合物,研究发现它们分别具有一定的抗真菌和除草活性[7-8]。以上研究结果表明,通过对丙烯海松酸的化学改性,融合1,3,4-噻二唑基团、磺酰胺基团、硫脲基团、酰胺基团等生物活性亚结构,可获得新型的丙烯海松酸基生物活性化合物。另一方面,有研究发现,取代酰胺基1,3,4-噻二唑衍生物表现出抗肿瘤[9-10]、人腺苷A3受体拮抗[11]、抗真菌[12]、杀虫[13-14]、除草[15]和杀蚊幼虫[16]等生物活性。本文以松香为原料,与丙烯酸进行Diels-Alder加成反应制备得到丙烯海松酸,然后通过对其羧基进行衍生化化学改性,将1,3,4-噻二唑杂环结构融合到其骨架中,制备得到丙烯海松酸基双噻二唑,最后与取代苯甲酰氯发生N-酰化反应,合成得到融合酰胺和1,3,4-噻二唑两个活性单元的新型丙烯海松酸基双酰胺-噻二唑化合物,表征其结构,并测试其除草及抗真菌活性,旨在为我国可再生性天然优势资源松香产品的深加工提供新途径。合成路线如图1所示。
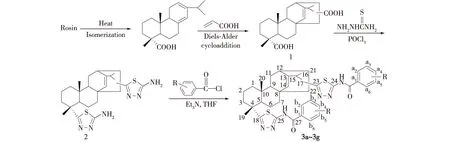
3a. R=H; 3b. R=p-CH3; 3c. R=p-F; 3d. R=p-Cl; 3e. R=p-Br; 3f. R=p-NO2; 3g. R=o-Cl图1 丙烯海松酸基双酰胺-噻二唑化合物的合成路线Fig. 1 Synthetic route of acrylpimaric acid-based diamide-thiadiazole compounds
1 实验部分
1.1 试剂及仪器
试剂:脂松香(特级,酸值177 mg/g,广西梧州松脂股份有限公司);丙烯酸(CP,成都科龙化工试剂厂);氨基硫脲(AR,成都科龙化工试剂厂);三氯氧磷、苯甲酰氯及其衍生物(AR,上海阿拉丁试剂公司);其他试剂均为市售分析纯试剂;试剂未经处理直接使用。
仪器:AVANCE AV 600MHz 超导核磁共振仪(瑞士Bruker公司);TSQ Quantum Access MAX 液相色谱-质谱联用仪(美国Thermo Scientific公司);Nicolet Nexus 470 FTIR红外光谱仪(美国Nicolet公司);X-4数字显示显微熔点测定仪(北京泰克仪器有限公司)。
1.2 中间体丙烯海松酸(1)的制备
丙烯海松酸(1)参照文献[8]进行制备。
1.3 中间体丙烯海松酸基双噻二唑(2)的制备
丙烯海松酸基双噻二唑(2)参照文献[7]进行制备。
1.4 目标化合物丙烯海松酸基双酰胺-噻二唑(3a~3g)的合成
以合成目标化合物3a为例,在100 mL圆底瓶中加入丙烯海松酸基双噻二唑(2)1.00 g(2.06 mmol)、三乙胺1 mL、四氢呋喃15 mL。搅拌均匀,在冰水浴条件下缓慢滴加溶于5 mL二氯甲烷的苯甲酰氯0.58 g (4.12 mmol),0.5 h内滴完。缓慢升温至75℃,TLC跟踪至苯甲酰氯点消失。停止反应后将溶剂减压蒸干,并且用去离子水洗涤3~4次,抽滤、干燥得粗品。以乙酸乙酯和石油醚[V(乙酸乙酯)∶V(石油醚) = 1∶30]为洗脱剂进行柱层析提纯,得到目标产物3a。同法合成其他目标产物3b~3g。
1.5 目标化合物丙烯海松酸基双酰胺-噻二唑(3a~3g)的结构表征







1.6 生物活性测试
1.6.1 除草活性测试
参照文献[17]中所述方法进行除草活性测试。供测植物油菜(Brassicacampestris)和稗草(Echinochloacrusgalli)均由南开大学元素有机化学研究所生测室提供。
油菜平皿法:将一张直径为5.6 cm的滤纸铺在直径为6 cm的培养皿中,然后准确加入2 mL一定浓度的供试化合物溶液。播种浸种4 h的10粒油菜种子,然后在温度(28±1)℃及黑暗条件下培养72 h后,测量其胚根的长度。测试浓度分别为10 μg/mL和100 μg/mL,重复测试两次,用蒸馏水作空白对照。根据公式(1)计算出黑暗条件下供试化合物对油菜胚根伸长的相对抑制率(%)。活性分级指标为A级≥80%,B级60%~79%,C级40%~59%,D级≤39%。

(1)
式中:C为空白对照的油菜胚根平均生长长度,mm;P为用供试化合物处理后的油菜胚根平均生长长度,mm。
稗草小杯法:将玻璃珠和滤纸铺好在50 mL的小烧杯中,加入6 mL一定浓度的供试化合物溶液。播种10粒刚刚露白的稗草种子,在温度(28±1)℃和光照条件下培养72 h,然后测量小苗高度。测试浓度分别为10 μg/mL和100 μg/mL,重复测试两次,用蒸馏水作空白对照。根据公式(1)计算出供试化合物对株高生长的相对抑制率(%)。活性分级指标为A级≥80%,B级60%~79%,C级40%~59%,D级≤39%。
所有目标化合物均采用油菜平皿法和稗草小杯法测试其对油菜的胚根及稗草的株高的相对抑制率。
1.6.2 抑菌活性测试
参照文献[17]中所述方法进行抑菌活性测试。供试菌种苹果轮纹病菌(Physalosporapiricola)、番茄早疫病菌(Alternariasolani)、黄瓜枯萎病菌(Fusariumoxysporumf. sp.cucumerinum)、小麦赤霉病菌(Gibberellazeae)、花生褐斑病菌(Cercosporaarachidicola)均由南开大学元素有机化学研究所生测室提供。
离体法(即琼脂稀释法):使用适量丙酮溶解供试药剂,再用200 μg/mL sorporl-144的乳化剂稀释药液至浓度500 μg/mL。准确量取药液1 mL,注入培养皿内,然后加入9 mL PSA培养基,最终制成浓度为50 μg/mL的含药平板。用打孔器将培养好的供试菌打取直径为5 mm的菌饼,置于含药平板内,每皿三块呈等边三角形摆放,于(24±1)℃培养箱内培养48 h,测量菌丝的扩展直径,以不含药剂作空白对照。根据公式(1)计算出相对抑制率(%)。活性分级指标为A级≥90%,B级70%~90%,C级50%~70%,D级<50%。
所有目标化合物采用琼脂稀释法对供测菌进行相对抑制率测试。
2 结果与分析
2.1 目标化合物的合成分析
在进行丙烯海松酸基双噻二唑(2)与取代苯甲酰氯反应过程中,发现丙烯海松酸基双噻二唑较难溶于二氯甲烷、四氢呋喃、苯、甲苯等非极性或弱极性非质子溶剂中,不利于反应顺利进行。通过实验发现,采用四氢呋喃和二氯甲烷(V四氢呋喃∶V二氯甲烷= 3∶1)混合溶剂作为反应介质,三乙胺作为缚酸剂,能够使反应顺利进行且后处理简单。
2.2 波谱解析

2.3 生物活性
2.3.1 除草活性
目标化合物对油菜胚根及稗草株高的相对抑制率测试结果见表1。在100 μg/mL浓度下,目标化合物3对稗草株高生长的抑制活性相对较弱,而对油菜胚根生长的抑制活性较强,其中化合物3e(R=p-Br)的抑制活性最好,抑制率高达92.4%(活性级别为A级),化合物3b (R=p-CH3)和3d (R=p-Cl)的抑制率分别为77.4%和73.2%(活性级别均为B级),值得进一步研究。

表1 丙烯海松酸基双酰胺-噻二唑化合物3a~3g的除草活性
2.3.2 抑菌活性
目标化合物对供测菌的相对抑制率测试结果见表2。在50 μg/mL浓度下,所有目标化合物丙烯海松酸基双酰胺-噻二唑对所测5种植物病菌均表现出一定的抑制活性,尤其对苹果轮纹病菌的抑制效果较好,平均抑制率达51.3%,其中化合物3g (R=o-Cl)的抑制率最高,达60.0%(活性级别为C级)。通过对比各目标化合物对所测植物病原菌的抑制率差异,未发现不同取代基对抑菌活性具有明显影响。

表2 丙烯海松酸基双酰胺-噻二唑化合物(3a~3g)的抑菌活性
3 结 论
本文以脂松香为原料,经丙烯海松酸合成得到7个新型丙烯海松酸基双酰胺-噻二唑化合物,采用FTIR、1H NMR、13C NMR、ESI-MS等技术手段对其结构进行表征,初步测试目标化合物的除草和抗菌活性。目标化合物对油菜胚根生长的抑制活性较强,在100 μg/mL浓度下,化合物3e (R=p-Br)的抑制率高达92.4%(活性级别为A级);目标化合物对稗草株高的生长表现出较弱的抑制活性。在50 μg/mL浓度下,目标化合物对所测5种植物病原菌均表现出一定的抑制作用,且对苹果轮纹病菌的抑制效果较好。本研究所设计的目标化合物3e对油菜胚根生长具有较好的抑制活性,在今后工作中,针对目标化合物3e的制抑活性方面还需进一步展开研究。
[1]周永红, 商士斌, 宋湛谦, 等. 丙烯海松酸甘油酯聚氧乙烯醚的合成及性能[J]. 现代化工, 2004, 24(11):27-29, 31. ZHOU Y H, SHANG S B, SONG Z Q, et al. Synthesis and properites of acrypimaric acid glycerol ester polyoxylehtylene ether[J]. Modern Chemical Industry, 2004, 24(11):27-29, 31.
[2]冯练享. 改性松香共聚PVB树脂胶粘剂的研制[J]. 中国人造板, 2007, 14(9):35-37. FENG L X. Study on PVB resin adhesive with modified rosin[J]. China Wood-based Panels, 2007, 14(9):35-37.
[3]李健, 饶小平, 商士斌, 等. 松香多元酸的制备及其应用研究进展[J]. 化工进展, 2010, 29(11):2103-2107, 2113. LI J, RAO X P, SHANG S B, et al. Research progress in synthesis and application of rosin-based polyacids[J]. Chemical Industry and Engineering Progress, 2010, 29(11):2103-2107, 2113.
[4]李健, 饶小平, 宋湛谦, 等. 丙烯海松酸及其噻二唑衍生物的制备及抑菌活性[J]. 林产化学与工业, 2014, 34(3):55-59. LI J, RAO X P, SONG Z Q, et al. Synthesis and antibacterial activity of acrylpimaric acid and its thiadiazole derivatives[J]. Chemistry and Industry of Forest Products, 2014, 34(3):55-59.
[5]李健, 饶小平, 商士斌, 等. 丙烯海松双酰基硫脲衍生物的合成及抑菌活性研究[J]. 林产化学与工业, 2011, 31(5):1-5. LI J, RAO X P, SHANG S B, et al. Synthesis and antibacterial activity of diacylthiourea derivatives containing acrylpimaryl group[J]. Chemistry and Industry of Forest Products, 2011, 31(5):1-5.
[6]LI J, RAO X P, SHANG S B, et al. Synthesis and antibacterial activity of amide derivatives from acrylopimaric acid[J]. BioResources, 2012, 7(2):1961-1971.
[7]阮战辉, 段文贵, 岑波, 等. 丙烯海松酸基双磺酰胺-噻二唑化合物的合成及抑菌活性研究[J]. 广西大学学报(自然科学版), 2013, 38(6):1338-1345. RUAN Z H, DUAN W G, CEN B, et al. Synthesis and fungicidal activity of acrylpimaric acid-based disulfamide-thiadiazole compounds[J]. Journal of Guangxi University (Natural Science Edition), 2013, 38(6):1338-1345.
[8]李宇彬, 段文贵, 陈秋菊, 等. 丙烯海松酸基双酰胺类化合物的合成及生物活性研究[J]. 化学试剂, 2012, 34(1):9-15, 54. LI Y B, DUAN W G, CHEN Q J, et al. Synthesis and study on biological activities of diamide compounds containing acrylpimaric acid moiety[J]. Chemical Reagents, 2012, 34(1):9-15, 54.
[9]YANG X H, XIANG L, LI X, et al. Synthesis, biological evaluation, and molecular docking studies of 1,3,4-thiadiazol-2-amide derivatives as novel anticancer agents[J]. Bioorganic & Medicinal Chemistry, 2012, 20(9):2789-2795.
[10]YANG X H, WEN Q, ZHAO T T, et al. Synthesis, biological evaluation, and molecular docking studies of cinnamic acyl 1,3,4-thiadiazole amide derivatives as novel antitubulin agents[J]. Bioorganic & Medicinal Chemistry, 2012, 20(3):1181-1187.
[11]JUNG K Y, KIM S K, GAO Z G, et al. Structure-activity relationships of thiazole and thiadiazole derivatives as potent and selective human adenosine A3receptor antagonists[J]. Bioorganic & Medicinal Chemistry, 2004, 12(3):613-623.
[12]LIU X H, SHI Y X, MA Y, et al. Synthesis, antifungal activities and 3D-QSAR study ofN-(5-substituted-1,3,4-thiadiazol-2-yl) cyclopropanecarboxamides[J]. European Journal of Medicinal Chemistry, 2009, 44(7):2782-2786.
[13]WAN R, ZHANG J Q, HAN F, et al. Synthesis and insecticidal activities of novel 1,3,4-thiadiazole 5-fluorouracil acetamides derivatives:an RNA interference insecticide[J]. Nucleosides Nucleotides Nucleic Acids, 2011, 30(4):280-292.
[14]WARD J S.N-(1,3,4-Thiadiazol-2-yl) benzamides:US4141984 [P]. 1979-02-27.
[15]TONG J Y, SUN N B, WU H K, et al. Synthesis, crystal structure and biological activity ofN-(5-(o-tolyl)-1,3,4-thiadiazol-2-yl) cyclopropanecarboxamide[J]. Journal of the Chemical Society of Pakistan, 2013, 35(5):1349-1353.
[16]SCHAEFER C H, MIURA T, WILDER W H. Biological activities of two new substituted benzamides against mosquitoesl and nontarget organisms[J]. Journal of Economic Entomology, 1981, 74(6):658-661.
[17]SU N N, LI Y, YU S J, et al. Microwave-assisted synthesis of some novel 1,2,3-triazoles by click chemistry, and their biological activity[J]. Research on Chemical Intermediates, 2013, 39(2):759-766.
Synthesis and biological activity of novel acrylpimaric acid-baseddiamide-thiadiazole compounds
LIN Guishan1, RUAN Zhanhui1, DUAN Wengui1*, LIU Luzhi1, YANG Zhangqi2
(1. College of Chemistry and Chemical Engineering, Guangxi University, Nanning 530004, China; 2. Guangxi Academy of Forestry, Nanning 530002, China)
As a non-wood forest product obtained from pines and some other plants, rosin with its dominant component as resin acids is a renewable, natural and preponderant biomass resource of China. In an attempt to expand its utilization in biological activities, acrylpimaric acid (1) was prepared by the Diels-Alder cycloaddition reaction between rosin and acrylic acid. Then, acrylpimaric acid-based dithiadiazole (2) was prepared by the reaction of acrylpimaric acid with thiosemicarbazide. Seven novel acrylpimaric acid-based diamide-thiadiazole compounds (3a-3g) were synthetized followed byN-acylation reaction with a series of substituted benzoyl chlorides. The target compounds were characterized by means of FTIR,1H NMR,13C NMR, and ESI-MS. The herbicidal activity of the target compounds 3a-3g was preliminarily evaluated by the barnyard grass beaker method and the rape petri dish method against the seedling-growth of barnyard grass (Echinochloacrusgalli) and the root-growth of rape (Brassicacampestris), respectively. The results showed that some target compounds had good growth inhibitory activity against the root-growth of rape at a concentration of 100 μg/mL, in which compound 3e (R=p-Br) exhibited the highest inhibitory rate of 92.4% (A-class level), and compounds 3b (R=p-CH3) and 3b (R=p-Cl) displayed inhibitory rate of 77.4% (B-class level) and 73.2% (B-class level), respectively. The antifungal activity of the target compounds 3a-3g was also evaluated byinvitromethod (also known as the agar dilution method) againstPhysalosporapiricola,Fusariumoxysporumf. sp.cucumerinum,Alternariasolani,Gibberellazeae, andCercosporaarachidicolaat a concentration of 50 μg/mL. It was found that the title compounds3a-3g showed a certain antifungal activity against all the tested fungi. The target compound 3e with excellent herbicidal activity is a leading compound worthy of further research.
rosin; acrylpimaric acid; diamide-thiadiazole; herbicidal activity; antifungal activity
2016-09-10
2016-10-25
国家自然科学基金(31060100);八桂学者专项。
林桂汕,男,副教授,研究方向为天然产物改性及有机合成。通信作者:段文贵,男,教授。E-mail:wgduan@gxu.edu.cn
TQ453.2
A
2096-1359(2017)02-0045-7
