两种HPLC法测定沙丁胺酮的对比
2017-03-22王鑫孙银玲刘宏大薛雁邸伟庆
王鑫,孙银玲,刘宏大,薛雁,邸伟庆
两种HPLC法测定沙丁胺酮的对比
王鑫,孙银玲,刘宏大,薛雁,邸伟庆
(辽宁远大诺康生物制药有限公司,辽宁 沈阳 110171)
目的 建立硫酸沙丁胺醇原料药中沙丁胺酮的HPLC检测方法。方法 采用《中华人民共和国药典》2015版中硫酸沙丁胺醇吸入气雾剂中杂质沙丁胺酮的测定方法和《欧洲药典》9.0中收载的原料药中杂质沙丁胺酮收载的测定方法进行比较,选取适用的方法并进行方法学验证。结果 两种HPLC方法均能检测原料药中沙丁胺酮含量,但《中华人民共和国药典》2015版中的方法分离效果更佳。结论 优选《中华人民共和国药典》2015版收载的HPLC方法作为硫酸沙丁胺醇原料药中沙丁胺酮的检测方法。
高效液相色谱法;硫酸沙丁胺醇;沙丁胺酮;方法学
硫酸沙丁胺醇(Salbutamol Sulfate结构式见图1)为选择性β2受体激动剂,适用于支气管哮喘、喘息性交气管炎患者[1-5]。它能选择性激动支气管平滑肌的β2受体,松弛平滑肌,有较强的支气管扩张作用。沙丁胺酮(Salbutamol Ketone结构式见图1)为硫酸沙丁胺醇合成过程中的中间体还原不彻底产生的杂质,其结构式与硫酸沙丁胺醇接近,所以在检测时沙丁胺酮与硫酸沙丁胺醇较难分离,本实验目的是建立硫酸沙丁胺醇原料药中沙丁胺酮的HPLC检测方法。
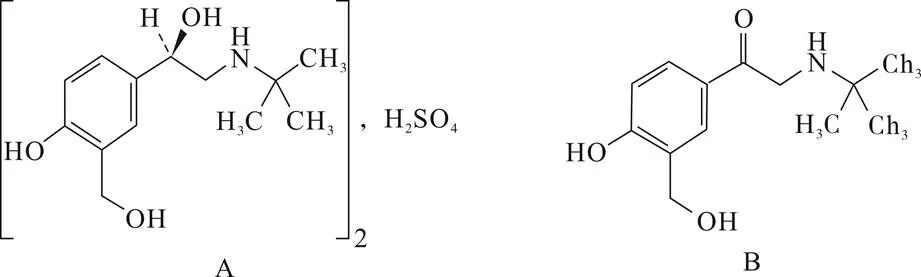
图1 硫酸沙丁胺醇与沙丁胺酮的化学结构式
《欧洲药典》[6](EP9.0)、《日本药典 》[7](JP15)、《美国药典》[8](USP40)、《英国药典》[9](BP2013)和《中华人民共和国药典》[10](Ch.p2015)均收载了硫酸沙丁胺醇原料药。其中Ch.p2015使用紫外-可见分光光度法对杂质沙丁胺酮进行控制。JP15、USP40中有关物质检测方法为薄层法且沙丁胺酮作为未知杂质进行控制。EP9.0、BP2013使用相同HPLC法测定有关物质但沙丁胺酮作为未知杂质进行控制。在该方法中杂质J为沙丁胺酮,该方法可以检出沙丁胺酮。在Ch.p2015中硫酸沙丁胺醇相关制剂中只有硫酸沙丁胺醇吸入气雾剂的标准中含有沙丁胺酮检项,并且检验方法为HPLC法。为了有效控制硫酸沙丁胺醇原料药中的沙丁胺酮含量,现分别采用上述方法中的EP9.0有关物质检测方法及Ch.p2015硫酸沙丁胺醇吸入气雾剂中沙丁胺酮的检测方法对硫酸沙丁胺醇原料药中沙丁胺酮进行检测并比较。
1 实验部分
岛津LC-20A高效液相色谱仪(日本岛津公司);分析天平(瑞士Mettler toledo);pH计(美国Eutech Instrument)。
沙丁胺酮对照品EP:SALBUTAMOL IMPURITY J CRS(LOT:Y0001186)(European Pharmacopoeia Reference Standard);硫酸沙丁胺醇原料药(批号:CPC-007-1402009;常州亚邦制药有限公司),甲醇、乙腈(色谱级,美国fisher);异丙醇(色谱级,Burdick Jackson);磷酸二氢钠,磷酸,三乙胺,乙酸铵,冰醋酸(国药集团药业控股有限公司)。
2 方法与结果
2.1 色谱条件
方法一:Ch.p2015硫酸沙丁胺醇吸入气雾剂中沙丁胺酮检测液相方法如下:色谱柱:Hypersil Gold C8柱(250 mm×4.6 mm,5μm);流动相:以异丙醇/moL·L-1醋酸铵缓冲液(pH4.5)(1.5; 98.5)为流动相A,异丙醇为流动相B,按表1进行梯度洗脱;检测波长:276 nm,柱温:40 ℃。
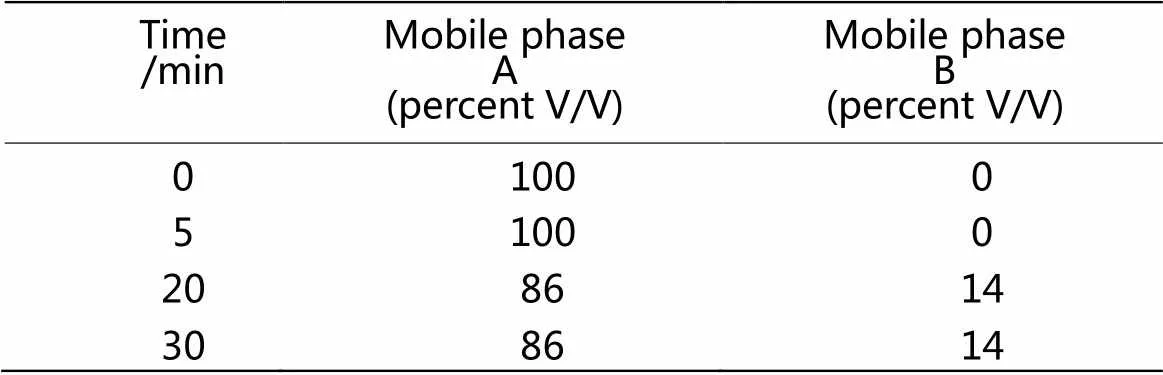
表1 流动相梯度洗脱的时间程序
方法二:EP9.0中硫酸沙丁胺醇原料药有关物质方法如下:色谱柱:Hypersil Gold C8柱(250 mm×4.6 mm,5μm);流动相:取3.45 g一水合磷酸二氢钠至1 000 mL容量瓶中,加0.05%三乙胺溶液900 mL,用稀磷酸调Ph 3.0,用0.05%三乙胺稀释至刻度作为流动相A,甲醇-乙腈:35~65作为流动相B,按表2进行梯度洗脱;检测波长:273 nm,柱温:30 ℃。

表2 流动相梯度洗脱的时间程序
2.2 系统适用性试验
取杂质沙丁胺酮及硫酸沙丁胺醇原料药各适量,精密称定。以庚烷磺酸钠溶液[取庚烷磺酸钠2.87 g与磷酸二氢钾2.5 g,加水溶解并稀释至1000 mL,用磷酸溶液(1→2)调节pH值至3.65]-乙腈(78∶22)为溶液A,用溶液A作为稀释液溶解并定量制成每1 mL中约含沙丁胺酮0.8 μg、硫酸沙丁胺醇0.4 mg的混合溶液,作为供试品溶液。分别在方法一和方法二条件下进行检测。方法一,沙丁胺酮与硫酸沙丁胺醇的分离度为2.28;方法二,沙丁胺酮与硫酸沙丁胺醇的分离度为1.43,峰谷比为3.8;欧洲药典9.0方法中要求沙丁胺酮和硫酸沙丁胺醇的峰谷比最小值为2.0。方法二中沙丁胺酮与硫酸沙丁胺醇分离度不佳,所以选用方法一对硫酸沙丁胺醇原料药中沙丁胺酮进行检测。
2.3 溶液制备
2.3.1 供试品溶液制备
取硫酸沙丁胺醇原料药约20 mg,精密称定,置50 mL量瓶中,用“2.2”条中的稀释液溶解并定容,摇匀,制成每1 mL中约含硫酸沙丁胺醇0.4 mg的溶液,作为供试品溶液。
2.3.2 对照溶液的制备
称取沙丁胺酮对照品适量,用水溶解并定量稀释制成每1 mL中含沙丁胺酮0.8 μg的溶液,作为杂质对照溶液。
2.4 专属性试验
硫酸沙丁胺醇原料药20 mg 3份,分置于50 mL量瓶中,加3 mol·L-1盐酸溶液6 mL于85 ℃水浴中加热2.5 h、3 mol·L-1氢氧化钠溶液3 mL于85 ℃水浴中加热2 h、200 g·L-1过氧化氢溶液1 mL于85 ℃水浴中加热2 h,酸碱破坏样品分别经3 mol·L-1氢氧化钠溶液和3 mol·L-1盐酸溶液中和后用“2.2”条中的稀释液稀释至刻度,氧化破坏用“2.2”条中的稀释液稀释至刻度,摇匀,作为酸、碱、氧化破坏样品溶液;另取硫酸沙丁胺醇原料药20 mg,于130 ℃烘箱中加热1.5 h,冷却,用“2.2”条中的稀释液溶解并稀释至50 mL,摇匀,作为热破坏样品溶液;另取硫酸沙丁胺醇原料药20 mg,置于50 mL量瓶中,用“2.2”条中的稀释液溶解并定容,摇匀,置4 500±500 lx光照培养箱中照射5 d,作为光破坏样品溶液。取上述各破坏样品溶液,经微孔滤膜滤过后测定。HPLC图谱见图2。结果由图2可知,本品经酸破坏、碱破坏、氧化破坏、热破坏、光破坏后,沙丁胺酮与主成分峰均获得基线分离。另取空白溶剂,同法试验,结果,空白溶剂对本品沙丁胺酮检查无干扰。

图2 空白溶剂(A)、及硫酸沙丁胺醇酸破坏(B)、碱破坏(C)、氧化破坏(D)、热破坏(E)、光破坏(F)、产物和供试品(G)的HPLC图谱
2.5 线性关系考察与范围的确定
取沙丁胺酮对照品约10 mg,精密称定,置于250 mL量瓶中,用水溶解并定容,摇匀,作为沙丁胺酮对照储备液;
精密量取沙丁胺酮对照品储备液0.25 mL置于250 mL量瓶中,另外取1、2、3、4和5 mL,分置于50 mL量瓶中,用水定容,摇匀,依法测定,量取峰面积。以质量浓度(,μg·mL-1)为横坐标,峰面积(A)为纵坐标分别进行线性回归,绘制标准曲线,所得回归方程为=58 881-2 064,2=0.999,在0.04~4μg·mL-1范围内线性关系良好。结果表明,沙丁胺酮在试验的质量浓度范围内,线性关系良好。
2.6 定量限和检测限的确定
取“2.5”条下的沙丁胺酮对照储备液,经逐步稀释后测定,以信噪比(S/N)≈10时的质量浓度(或进样量)为定量限、S/N≈3时的质量浓度(或进样量)为检测限。结果显示:沙丁胺酮的定量限约为0.8 ng,检测限约为0.24 ng。
2.7 精密度试验
取硫酸沙丁胺醇原料药20 mg 6份,精密称定,分置于50 mL量瓶中,在6份样品中加入“2.5”条下的沙丁胺酮对照储备液1 mL,加“2.2”条中的稀释液稀释至刻度,摇匀,作为供试品溶液。依法测定,量取峰面积按外标法计算, 6份样品测定结果的相对标准偏差(RSD)为0.48%,表明方法重复性良好。
2.8 稳定性试验
2.8.1 沙丁胺酮对照品稳定性考察
取“2.5”条下的沙丁胺酮对照储备液1 mL,以水定容至50 mL量瓶中,作为对照品溶液。分别于室温条件下放置0、2、4、6、8 、10、12和24 h后取样测定,以峰面积计算RSD值。结果:RSD%为0.12%,结果表明:沙丁胺酮对照品溶液在24 h内稳定性良好。
2.8.2 硫酸沙丁胺醇样品稳定性考察
取硫酸沙丁胺醇原料药20 mg,精密称定,置于50 mL量瓶中,在样品中加入“2.5”条下的沙丁胺酮对照储备液1 mL,加“2.2”条中的稀释液稀释至刻度,摇匀,作为供试品溶液。分别于室温条件下放置0、2、4、6、8 、10、12和24 h后取样测定,按外标法以峰面积计算沙丁胺酮含量。RSD%为0.44%,结果表明:硫酸沙丁胺醇供试品溶液在24 h内稳定性良好。
2.9 回收率试验
取硫酸沙丁胺醇原料药约20 mg共9份,精密称定,分置于50 mL量瓶中,分别精密加入沙丁胺酮对照储备液0.8、1.0、1.2 mL各3份,分别用稀释液稀释至刻度,摇匀,制成低(0.64 μg·mL-1)、中(0.80 μg·mL-1)、高(0.96μg·mL-1)3个质量浓度的供试溶液。另精密量取沙丁胺酮对照储备液1.0 mL,置于50 mL量瓶中,用水稀释至刻度,摇匀,作为对照溶液。另取硫酸沙丁胺醇原料药20 mg,精密称定,置50 mL量瓶中,用“2.2”条中的稀释液溶解并稀释至刻度,摇匀,作为本底校正溶液。精密量取供试溶液、对照溶液和本底校正溶液各20μL,分别注入液相色谱仪,记录色谱图,按外标法以峰面积计算供试溶液和本底校正溶液中沙丁胺酮含量,并计算沙丁胺酮的回收率,即以供试溶液的含量扣除本底校正溶液的含量后与加入量比较即得。沙丁胺酮平均回收率为100.1%,RSD%为0.6%(=9),具体数据见表3。

表3 回收率结果
2.10 耐用性考察
取硫酸沙丁胺醇原料药20 mg,精密称定,置于50 mL量瓶中,在样品中加入“2.5”条下的沙丁胺酮对照储备液1 mL,加“2.2”条中的稀释液稀释至刻度,摇匀,作为供试品溶液。通过考察改变色谱条件变量包括色谱柱、流速、pH、柱温观察检测结果不受影响的程度,结果表明该方法耐用性良好。具体数据见表4。
2.11 样品沙丁胺酮的测定
取硫酸沙丁胺醇原料药约20 mg 3份,精密称定。分别置于50 mL量瓶中,用“2.2”条中的稀释液溶解并定容,摇匀,制成每1 mL中约含硫酸沙丁胺醇0.4 mg的溶液,作为供试品溶液。取沙丁胺酮对照品适量,用水溶解并定量稀释制成每1 mL中含沙丁胺酮0.8μg的溶液,作为杂质对照品溶液。精密量取供试溶液和杂质对照品溶液各20μL,分别注入液相色谱仪,记录色谱图。
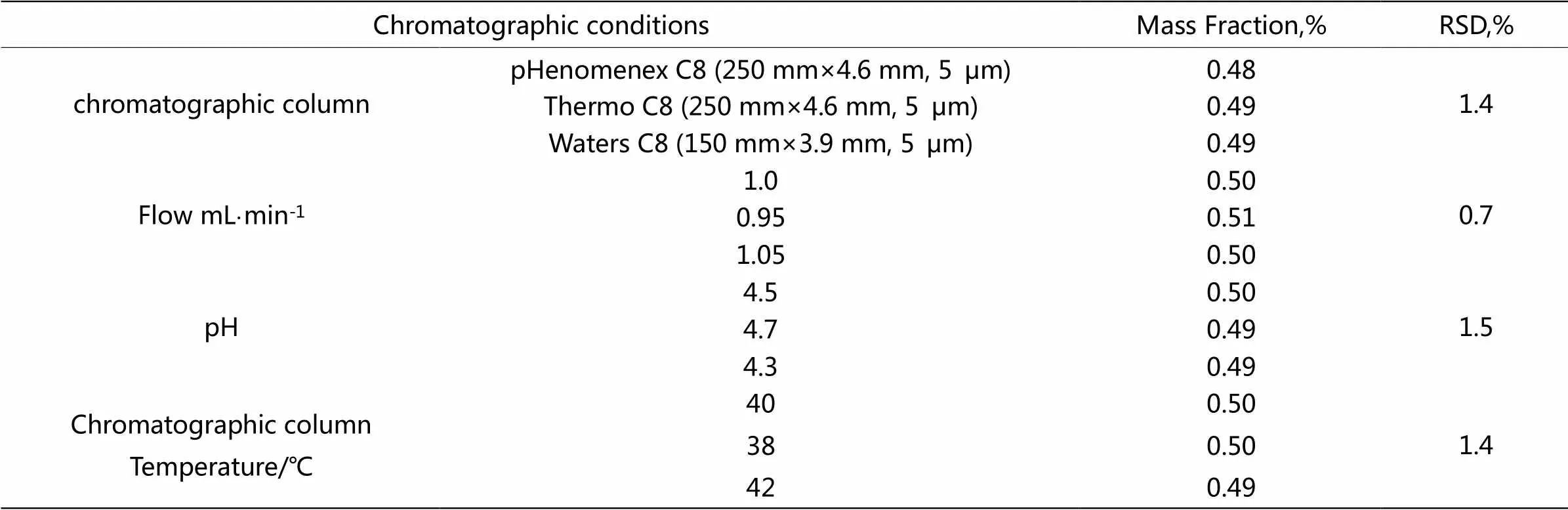
表4 耐用性结果
供试品溶液的色谱图中如有与沙丁胺酮保留时间一致的色谱峰,按外标法以峰面积计算,沙丁胺酮不得过0.2%。经对3批样品测定,结果见表5。通过结果可知,本样品未检出沙丁胺酮杂质。

表5 硫酸沙丁胺醇中沙丁胺酮测定结果(%)
3 结论
采用HPLC法检测硫酸沙丁胺醇原料药中的沙丁胺酮,由于方法灵敏度高,得到的结果更加准确;《欧洲药典》9.0中有关物质方法,沙丁胺酮作为考察系统适用性的对照品,要求与硫酸沙丁胺醇的峰谷比最小值为2,通过实验发现可以达到该要求,但是分离度没有达到1.5,与《中华人民共和国药典》2015版硫酸沙丁胺醇吸入气雾剂中检测沙丁胺酮的方法比较,中国药典方法分离度更优,通过对中国药典的方法学考察发现,该方法在质量浓度0.04~4 μg·mL-1范围内线性关系良好;加样回收率平均值100.1%,RSD%为0.6%(=9);精密度、稳定性及耐用性试验的RSD均小于2.0%。该方法具有准确、可靠、灵敏度高等特点,可作为硫酸沙丁胺醇原料药中沙丁胺酮的检测方法。
[1]叶春娟,章国语.硫酸沙丁胺醇气雾剂吸入与茶碱控释片治疗急性老年哮喘的疗效对比分析[J].中国生化药杂志,2014,34(1):116-117.
[2]陈德晖,翟莺莺,林育能,等.吸入用布地奈德混悬液联合硫酸沙丁胺醇气雾剂雾化吸入治疗急性期COPD的临床效果[J].中国当代医药,2015,22(33):967-970.
[3]戚宇飞,吐尔逊古力·布尔汗.硫酸沙丁胺醇在治疗儿童支气管哮喘中的临床疗效分析[J].临床儿科杂志,2011,29(10):38-40.
[4] 李延召. 盐酸氨溴索联合硫酸沙丁胺醇治疗支气管扩张临床观察[J]. 世界最新医学信息文摘, 2016, 16 (59): 150-151.
[5]赵辉,杨国峰. 综合护理措施在硫酸沙丁胺醇气雾剂吸入治疗慢性阻塞性肺疾病中的作用[J]. 中国医科大学学报, 2017, 46 (2): 184-187.
[6]国家药典委员会. 中华人民共和国药典[M].(2015年版二部). 北京:中国医药科技出版社,2015.
[7]EUROPEAN PHARMACOPOEIA9.0 [S]. 3526-3528.
[8]The Japanese Pharmacopoeia ⅩⅥ [S]. 1369-1370.
[9]The United States Pharmacopoeia 40 [S]. 2606-2607.
[10]British Pharmacopoeia, 2013 [S]. 1-8.
Investigation on Two HPLC Determination Methods of Salbutamol Ketone
,,,,
(Liaoning Grand Nuokang Biopharmaceutical Co.,Ltd., Liaoning Shengyang 110171, China)
Objective: To establish HPLC method to determine salbutamol ketone in salbutamol sulfate raw material. Methods: the determination method of salbutamol ketone impurity in salbutamol sulfate aerosol in Ch.p 2015 and the determination method of salbutamol ketone impurity in APIs in EP9.0 were compared, and a suitable method was used carry out methodological validation. Results: Both HPLC methods can detect salbutamol ketone in APIs.The separation effect of method in Ch.p2015 is better than that in EP9.0.Conclusion: The HPLC method in Ch.p2015 should be used as the detection method for salbutamol ketone in APIs.
HPLC; sulfate salbutamol; salbutamol ketone; methodology
O 657
A
1004-0935(2017)10-1032-04
2017-07-25
王鑫(1984-),男,主管中药师,硕士,辽宁省沈阳市人,2011年毕业于辽宁中医药大学,研究方向:药物研发。
刘宏大(1979-),女,回族,硕士,研究方向:药物研发。
