进展期直肠癌术前联合放化疗中奥沙利铂作用的meta分析
2017-01-18李志艳张小燕唐海林
李志艳,张小燕,唐海林,吴 清
(1.南华大学附属南华医院 消化内科, 衡阳 湖南 421002;2.中山大学附属肿瘤防治中心 乳腺科,广州 广东 510000)
·荟萃分析·
进展期直肠癌术前联合放化疗中奥沙利铂作用的meta分析
李志艳1,张小燕1,唐海林2,吴 清1
(1.南华大学附属南华医院 消化内科, 衡阳 湖南 421002;2.中山大学附属肿瘤防治中心 乳腺科,广州 广东 510000)
目的 探讨进展期直肠癌奥沙利铂术前放疗及卡培他滨联合治疗中应用奥沙利铂是否有其必要性及价值。方法 通过pubmed、embase、中国知网、万方、维普等数据库及论文检索相关文献。试验组为卡培他滨联合组(放疗+卡培他滨+奥沙利铂),对照组为卡培他滨组(放疗+卡培他滨),进展期直肠癌的随机对照试验(randomized controlled trial,RCT)由两位研究者按上述检索策略收集资料,根据纳入标准筛选文献,主要对病理完全缓解、不良反应进行meta分析。结果 根据文献纳入标准,从735篇文献中筛选出符合标准的4篇RCT,共2 066例,两组间病理完全缓解率(yp complete response,ypCR)差异无统计学意义(P=0.13),卡培他滨联合组的毒性反应发生率提高13%(95%CI=0.08~0.18,P<0.01),腹泻发生率提高9%(95%CI=0.06~0.12,P<0.01),乏力发生率提高4%(95%CI=0.02~0.06,P=0.0002)。两组间放射性皮炎及hand-foot综合征差异无统计学意义(P>0.05)。结论 奥沙利铂不能明显改善ypCR,但增加了其不良作用。现有证据支持术前放疗及卡培他滨化疗为更佳治疗方案,但仍需更多高质量临床试验。
胃肿瘤;奥沙利铂;卡培他滨;放化疗
根据现有循证医学证据,综合治疗是进展期直肠癌的主要治疗手段。大量随机试验证明[1-4],术前行放疗及卡培他滨与奥沙利铂联合治疗可增加保肛手术机会,降低肿瘤分期,降低手术对患者术后生活质量的影响,改善病理完全缓解率。但卡培他滨与奥沙利铂联合可增加不良反应,增加患者经济负担,降低患者生活质量。在疗效一致的情况下,应尽可能的减少毒性反应。研究表明[5-7],术前卡培他滨联合组与卡培他滨组相比,无病生存率、总生存率、复发率、完全病理缓解率差异无统计学意义,但增加其毒性作用。术前放疗及卡培他滨化疗是否优于放疗及卡培他滨与奥沙利铂联合,仍需更多的研究证明。本研究试图通过目前已有相关文献行meta分析,探讨在进展期直肠癌术前放化疗中应用奥沙利铂是否有其必要性及价值,为术前放疗及卡培他滨化疗提供循证证据。
1 资料与方法
1.1 检索策略 利用pubmed、embase、中国知网、万方数据库、维普等数据库,英文检索主题词包括“capecitabine”、“radiotherapy”、“neoadjuvant chemoradiotherapy”、“rectal cance”“ oxaliplatin”。中文检索词“卡培他滨”“奥沙利铂”“进展期直肠癌”。检索日期截止至2016年4月20日,语种限中、英文。
1.2 文献纳入与排除标准 纳入标准:①研究对象,经病理确诊并为进展期的直肠癌且影像学检查无远处转移的患者;②干预措施,术前均进行放疗及卡培他滨联合奥沙利铂与卡培他滨单独化疗的比较;③试验设计,均为随机对照实验;④观察结果,患者基本特征、临床疗效及不良反应。排除标准:①非随机对照实验;②非术前放疗及卡培他滨联合奥沙利铂与卡培他滨单独化疗治疗进展期直肠癌的比较;③无原始数据、大量原始数据缺失者。
1.3 资料收集和提取 入选资料由2名研究者独立提取,并进行交叉核对,若出现分歧,则由2名研究者讨论或与第3名研究者讨论解决。资料提取主要包括纳入文献的发表时间、研究设计类型、放化疗剂量、研究病例数、各种观察指标及诊断标准。
1.4 临床近期疗效 病理评价标准采用Dworak肿瘤分级:术后标本中无肿瘤细胞(complete respone,CR),从随机化开始至疾病复发或疾病进展导致患者死亡的时间(disease-free survival,DFS),从随机化开始至因肿瘤原因引起患者死亡的时间(overall survival,OS)。
1.5 文献质量评价 根据Cochrane偏倚风险评估工具,评价文献质量:①随机分配;②分配方案隐藏;③盲法;④结果数据完整性;⑤选择性报告研究结果;⑥其他偏倚来源。各条目评估程度为:低风险、高风险、不清楚。由两名研究员独立对纳入文献进行评估和数据提取,交叉核对确保资料完整和结果同质性。存在争议时,通过讨论或与第三名研究者讨论后决定。
1.6 统计学方法 利用review manager 5.3软件统计分析,二分类变量采用治疗优势(risk difference,RD)及其95%可信区间(confidence interval,CI)描述,采用I2和χ2行异质性检验,检验水准为α=0.1,若I2>50%和(或)P<0.1,则采用随机效应模型,若I2≤50%且P≥0.1,则采用随机固定模型。P<0.05为差异具有统计学意义。
2 结 果
2.1 文献筛选和质量评价 共检索出735篇文献,经筛选后共4篇RCT纳入本次研究,共2 066例,其中卡培他滨联合组951例,卡培他滨组1 105例。4项试验数据统计分析均遵循ITT原则。综合分析患者年龄、性别、肿瘤分期等,两组之间差异无统计学意义。纳入文献基本特征及文献质量评价,见表1,图1。
2.2 临床疗效 卡培他滨联合组与卡培他滨组之间病理完全缓解率(ypCR)比较,并进行异质性检验结果显示两组间异质性小[Chi2=0.57,df=1(P=0.75);I2=0%],采用随机固定模型分析,结果显示卡培他滨联合组ypCR高于卡培他滨组,但两组间差异无统计学意义(P=0.13),见图2。
2.3 不良反应 本研究对卡培他滨联合组与卡培他滨组的不良反应、腹泻、乏力、放射性皮炎、hand-foot综合征发生率作比较,并进行异质性检验,结果显示两组间毒性反应、腹泻、乏力、hand-foot综合征异质性小(I2<50%且P>0.1),采用随机固定模型分析,结果显示卡培他滨联合组的毒性反应(图3)、腹泻及乏力发生率明显高于卡培他滨组,两组间差异具有统计学意义(P<0.05)。两组间hand-foot综合征发生率之间差异无统计学意义(P>0.05)。两组间放射性皮炎的异质性大(P<0.1,I2=67%),采用随机效应模型,结果显示两组间差异无统计学意义(P=0.89),见表2。

表1 纳入文献基本特征
注:卡培他滨(CAP);奥沙利铂(OX);随机对照试验(RCT)
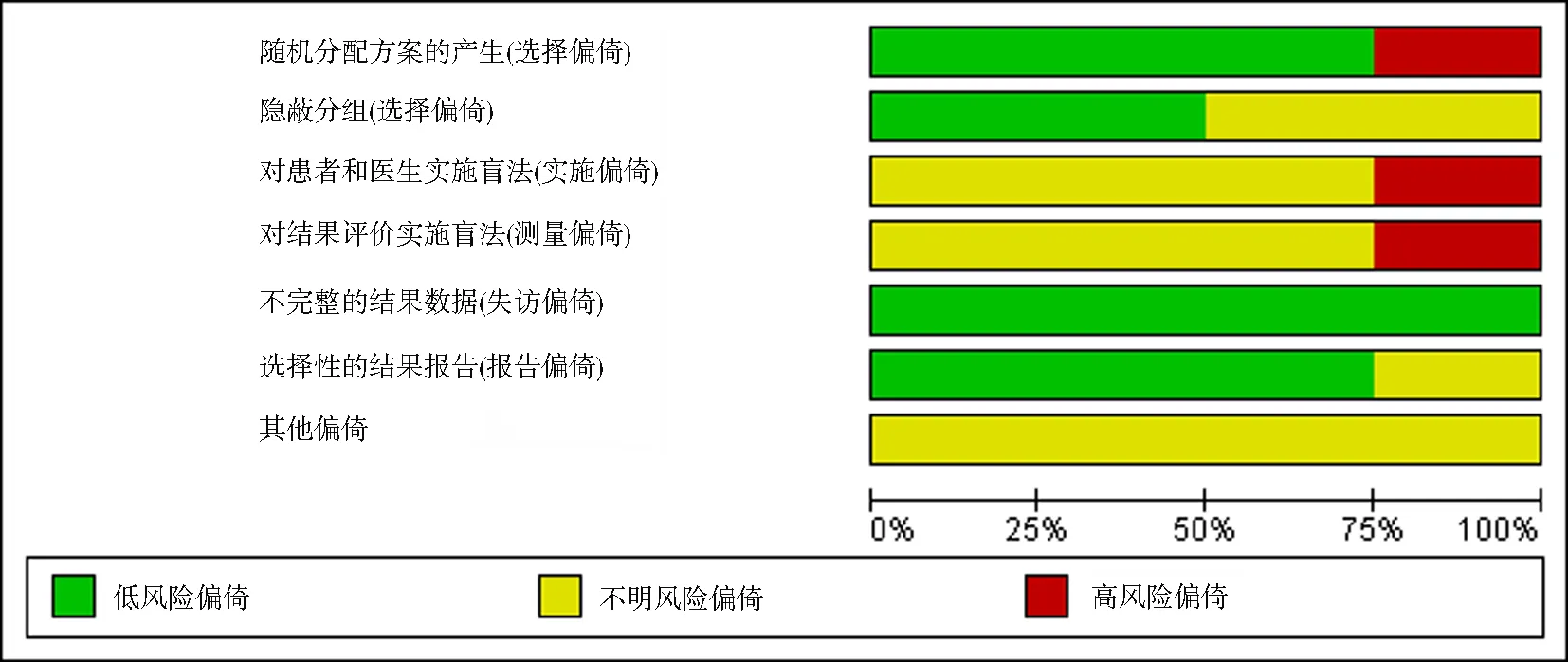
图1 纳入文献的 Cochrane偏倚风险评估
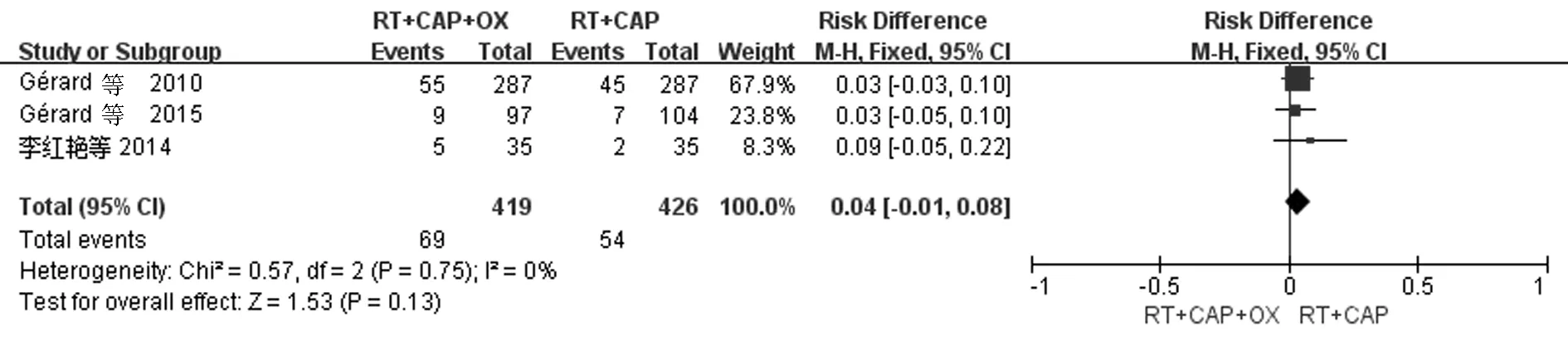
图2 卡培他滨联合组与卡培他滨组ypCR评价森林图 放射治疗(RT);卡培他滨(CAP);奥沙利铂(OX)
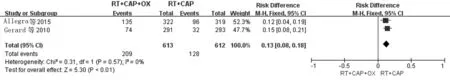
图3 卡培他滨联合组与卡培他滨组毒性评价森林图 放射治疗(RT);卡培他滨(CAP);奥沙利铂(OX)
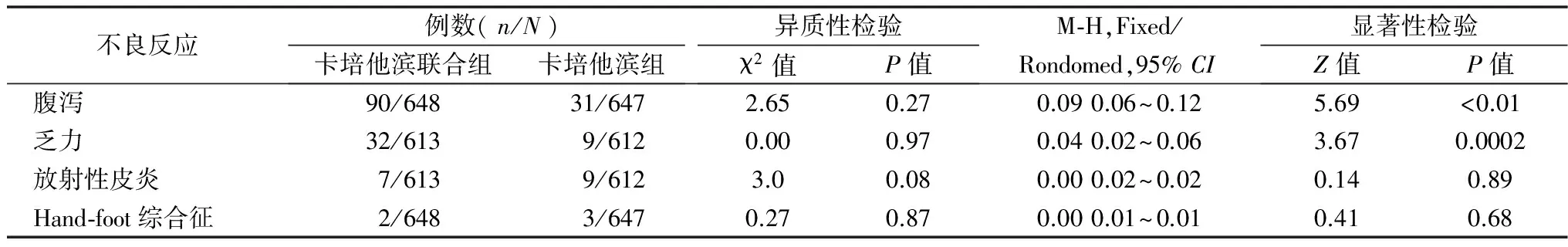
不良反应例数(n/N)卡培他滨联合组卡培他滨组异质性检验χ2值P值M⁃H,Fixed/Rondomed,95%CI显著性检验Z值P值腹泻90/64831/6472.650.270.090.06~0.125.69<0.01乏力32/6139/6120.000.970.040.02~0.063.670.0002放射性皮炎7/6139/6123.00.080.000.02~0.020.140.89Hand⁃foot综合征2/6483/6470.270.870.000.01~0.010.410.68
注:卡培他滨联合组即放射治疗+卡培他滨+奥沙利铂;卡培他滨组即放射治疗+卡培他滨
3 讨 论
卡培他滨是5-氟尿嘧啶前体药物,在体内经过一系列酶促反应如胸苷磷酸化酶作用而活化,并经二氧嘧啶脱氢酶降解而灭活。奥沙利铂是顺铂新型衍生物,为第3代泊类抗癌药,可引起胃肠道异常、中枢及外周神经系统异常、血液系统异常、皮肤及皮下组织异常等不良反应。卡培他滨与奥沙利铂联合为治疗直肠癌一线化疗用药。研究表明[2, 4, 10-12],术前放疗及卡培他滨与奥沙利铂联合治疗直肠癌的ypCR在9.5%~20.9%之间。目前术前卡培他滨与奥沙利铂放化疗与卡培他滨放化疗在治疗进展期直肠癌疗效比较的研究甚少。2015年Gérard等[5]研究表明,CAP50与CAPOX50相比,两组间ypCR差异无统计学意义。并且2014年O'Connell等[13]研究证明,术前以卡培他滨为基础的放化疗,联合或不联合奥沙利铂,其OS、DFS及肿瘤复发率差异无统计学意义。探讨奥沙利铂在术前联合放化疗中治疗直肠癌是否有其必要性及价值,有必要行meta分析,并对国内外多种数据库进行检索,研究前制定严格的纳入标准筛选,最后共有4篇文献符合纳入标准,使用Review Manager 5.3评分,纳入文献均为较高质量的临床研究。
OS、DFS及肿瘤复发率是评价治疗方案的有效指标,2012年Geérard等[6]研究表明,CAP45与CAPOX50的3年OS、DFS及肿瘤复发率分别是87.6%、88.3%,67.9%、72.7%,6.1%、4.4%,两组间差异无统计学意义,并且2015年Allegra等[7]研究再次证明,奥沙利泊不能改善患者的OS、DFS及肿瘤复发率。
病理完全缓解(PCR)是表示生命延长的早期信号,通过对其评价,可有效缩短试验时间及降低成本。2010年及2015年Gérard等[5,8]研究均以新辅助放化疗后手术标本的ypCR为终点指标。因此,本meta分析以ypCR作为两组间疗效比较的终点指标,并对其异质性检验,P=0.75且I2=0,提示研究间异质性小,因此本研究具有较高的可信度。结果示卡培他滨联合组ypCR提高4%(95%CI=-0.01~0.08,P=0.13),可见奥沙利铂可提高患者ypCR,但差异并无统计学意义。
联合化疗是否会增加不良反成为临床医生关注的问题,不良反应损伤患者脏器及影响生活质量,而毒性反应、腹泻、恶心、呕吐、乏力、放射性皮炎、hand-foot综合征等是放疗、卡培他滨及奥沙利铂的常见不良反应。因此,以毒性反应、腹泻、乏力、放射性皮炎及hand-foot为本meta分析指标。与卡培他滨组相比,卡培他滨联合组毒性反应发生率增加13%(95%CI=0.08~0.18,P<0.01)。此外,腹泻、乏力等症状造成患者不良感受,影响患者生存质量,卡培他滨联合组腹泻发生率增加9%(95%CI=0.06~0.12,P<0.01)及乏力发生率增加4%(95%CI=0.02~0.06,P=0.0002),术前联合应用奥沙利铂不能明显改善患者ypCR、OS、DFS及复发率,但增加了患者不良反应,降低患者生活质量及增加患者经济负担。
本meta分析为术前放疗及卡培他滨化疗治疗直肠癌提供循证证据,但目前关于此类的高质量RCT较少,在术前放化疗中联合应用奥沙利铂是否有其价值及必要性需更多的高质量临床试验。
[1] Ricardi U, Racca P, Franco P, et al. Prospective phase II trial of neoadjuvant chemo-radiotherapy with Oxaliplatin and Capecitabine in locally advanced rectal cancer (XELOXART)[J]. Med Oncol,2013,30(2): 581.
[2] Gao YH, An X, Sun WJ, et al. Evaluation of capecitabine and oxaliplatin administered prior to and then concomitant to radiotherapy in high risk locally advanced rectal cancer[J]. J Surg Oncol,2014,109(5): 478-482.
[3] Gao YH, Zhang X, An X, et al. Oxaliplatin and capecitabine concomitant with neoadjuvant radiotherapy and extended to the resting period in high risk locally advanced rectal cancer[J]. Strahlenther Onkol,2014,190(2): 158-164.
[4] Zhao L, Bai C, Shao Y, et al. A phase II study of neoadjuvant chemoradiotherapy with oxaliplatin and capecitabine for rectal cancer[J]. Cancer Lett,2011,310(2): 134-139.
[5] Gérard JP, Chamorey E, Gourgou-Bourgade S, et al. Clinical complete response (cCR) after neoadjuvant chemoradiotherapy and conservative treatment in rectal cancer. Findings from the ACCORD 12/PRODIGE 2 randomized trial[J]. Radiother Oncol,2015,115(2): 246-252.
[6] Gérard JP, Azria D, Gourgou-Bourgade S, et al. Clinical outcome of the ACCORD 12/0405 PRODIGE 2 randomized trial in rectal cancer[J]. J Clin Oncol,2012,30(36): 4558-4565.
[7] Allegra CJ, Yothers G, O'Connell MJ, et al. Neoadjuvant 5-FU or capecitabine plus radiation with or without oxaliplatin in rectal cancer patients: a phase Ⅲ randomized clinical trial[J]. J Natl Cancer Inst,2015,107(11). pii: djv248.pii:djv248
[8] Gérard JP, Azria D, Gourgou-Bourgade S, et al. Comparison of two neoadjuvant chemoradiotherapy regimens for locally advanced rectal cancer: results of the phase III trial ACCORD 12/0405-Prodige 2[J]. J Clin Oncol,2010,28(10): 1638-44.
[9] 李红艳. Ⅱ/Ⅲ直肠癌术前卡培他滨+奥沙利铂与卡培他滨同步放化疗近期疗效比较[D].大连医科大学,2013.
[10] Carlomagno C, Farella A, Bucci L, et al. Neo-adjuvant treatment of rectal cancer with capecitabine and oxaliplatin in combination with radiotherapy: a phase Ⅱ study[J]. Ann Oncol,2009,20(5): 906-912.
[11] Hospers GA, Punt CJ, Tesselaar ME, et al. Preoperative chemoradiotherapy with capecitabine and oxaliplatin in locally advanced rectal cancer. A phase Ⅰ-Ⅱ multicenter study of the Dutch Colorectal Cancer Group[J]. Ann Surg Oncol,2007,14(10): 2773-2779.
[12] Lin JZ, Zeng ZF, Wu XJ, et al. Phase Ⅱ study of pre-operative radiotherapy with capecitabine and oxaliplatin for rectal cancer and carcinoembryonic antigen as a predictor of pathological tumour response[J]. J Int Med Res,2010,38(2): 645-654.
[13] O'Connell MJ, Colangelo LH, Beart RW, et al. Capecitabine and oxaliplatin in the preoperative multimodality treatment of rectal cancer: surgical end points from National Surgical Adjuvant Breast and Bowel Project trial R-04[J]. J Clin Oncol,2014,32(18): 1927-1934.
Role of oxaliplatin in preoperative of advanced rectal cancer: a meta-analysis
Li Zhiyan1,Zhang Xiaoyan1,Tang Hailin2,Wu Qing1
1.Department of Gastroenterology,the Affiliated Nanhua Hospital of University of South China,Hengyang 421002, China; 2.Department of Breast Oncology, Sun Yat-Sen University Cancer Center, Guangzhou 510000, China
Wu Qing, Email: nhwuqing@163.com
Objective To explore the role of oxaliplatin combined with capecitabine in the preoperative of advanced rectal cancer. Methods A comprehensive search of literatures including Pubmed, Embase, China National Knowledge Infrastructure, Wanfang database and Vip database was performed. The meta-analysis included randomized controlled trial to compare neoadjuvant capecitabine plus radiation with or without oxaliplatin with respect to complete response and toxicities. Results Of 735 reports, four randomized controlled trials including 2 066 patients were identified by two reviewers. There was no statistically significant differences between capecitabine plus radiation with or without oxaliplatin in ypCR (P=0.13). The CAPOX (radiation+capecitabine+oxaliplatin) group increased with 13% in the toxicity (95%CI=0.08-0.18,P<0.01),increased with 9% in diarrhea(95%CI=0.06-0.12,P<0.01) and increased with 4% in fatigue (95%CI=0.02-0.06,P=0.0002) in comparison with the CAP (radiation+oxaliplatin). No significant difference was observed in radiation dermatitis and hand-foot syndrome. Conclusion Oxaliplatin does not improve the ypCR but increase considerable toxicities. Current evidence supports preoperative radiation plus capecitabine in the treatment of patients with rectal cancer, but still needs more high-quality clinical trials.
stomach neoplasms; capecitabine; oxaliplatin;chemoradiotherapy
国家自然科学基金资助项目(81472469)
吴清,Email:nhwuqing@163.com
R735.2
A
1004-583X(2017)01-0074-04
10.3969/j.issn.1004-583X.2017.01.018
2016-07-11 编辑:姜恒丽
