发状念珠藻干旱胁迫响应基因NfGR的克隆与鉴定
2016-12-17岳思君范红丽苏建宇
岳思君,范红丽,郑 蕊,周 娟,苏建宇
(宁夏大学 生命科学学院,西部特色生物资源保护与利用教育部重点实验室, 银川 750021)
发状念珠藻干旱胁迫响应基因NfGR的克隆与鉴定
岳思君,范红丽,郑 蕊,周 娟,苏建宇*
(宁夏大学 生命科学学院,西部特色生物资源保护与利用教育部重点实验室, 银川 750021)
该研究采用PCR技术,从发状念珠藻细胞中克隆了谷胱甘肽还原酶(glutathione reductase,GR)基因,命名为NfGR,其开放阅读框长1 374 bp,编码458个氨基酸,蛋白相对分子量为49.42 kD,理论等电点为5.49。氨基酸序列分析表明,NfGR蛋白具有NADPH结合位点超家族(NADB-Rossmann superfamily )和吡啶氧化还原酶二聚体超家族(Pyr_redox_dim superfamily) 2个结构域,与点形念珠藻(Nostocpunctiforme)的相似性达93%。系统进化树分析表明,NfGR与点形念珠藻处在同一进化枝上,亲缘关系较近。qRT-PCR表达分析表明,在不同浓度PEG-6000处理下,NfGR基因均保持上调表达,其中,PEG-6000浓度为8%时,NfGR基因的相对表达量达到峰值(32.69)。研究推测,谷胱甘肽还原酶可能参与了发状念珠藻对干旱胁迫过程的响应。
发状念珠藻,谷胱甘肽还原酶,基因克隆,荧光定量PCR
发状念珠藻(Nostocflagelliforme),又称发菜,是生长在中国西北干旱和半干旱荒漠地区的陆生蓝藻,是一种旱生蓝藻类(blue-green algae)低等植物,有很强的耐干旱、耐低温和耐辐射能力[1-2]。其固氮能力很强,是干旱荒漠区主要生物固氮资源。同时,发状念珠藻还具有极高的食用价值和经济价值,其藻体内含有丰富的胶质和多种营养物质,对改良荒漠化土壤结构及理化性质有一定作用,可为其他有益土壤微生物提供可利用的碳源和氮源。因此,发状念珠藻在干旱荒漠区具有十分重要的生态学意义。目前研究最多的是发状念珠藻的生理生化、分布、生态、显微结构、生长发育、营养成分和人工栽培等方面[3-7],对发菜的生物学特性有了一定的认识,但分子方面的研究尚属起步阶段,从分子水平研究其耐逆及适应机制、寻找其生长发育规律以及实现发状念珠藻人工培养,多年来一直是研究者关注的热点[8-9]。
还原型谷胱甘肽(GSH)作为一种水溶性、小分子量的抗氧化剂,它是细胞中主要的非蛋白巯基库,是细胞中维持正常氧化还原状态的重要组成部分,参与许多重要的生理生化过程。植物细胞的叶绿体、细胞质、线粒体等细胞区域都含有较高浓度的谷胱甘肽[10]。植物体内细胞的多种生理生化反应都可产生活性氧(reactive oxygen species,ROS)。正常生长条件下,植物细胞中 ROS 维持在较低的水平,然而,极端温度、高盐、强光照、重金属、紫外光辐射、O3和SO2、机械损伤等环境胁迫可引起ROS的大量增加,若不及时清除,会对植物细胞产生严重伤害。植物体内存在清除ROS的抗氧化系统,其中谷胱甘肽还原酶(glutathione reductase,GR)是谷胱甘肽抗氧化系统的主要酶之一。它在NADPH存在的情况下,催化氧化型谷胱甘肽(GSSG) 还原成还原型谷胱甘肽(GSH),以对抗氧化胁迫。防止GSSG和其它二硫化合物的积累,对细胞膜、核酸、脂类、血红蛋白和酶的稳定是必需的[11-12]。因此GR对GSH的再生以保持正常的 GSH/GSSG 比例,维持植物细胞的氧化还原平衡有重要意义,在植物抗氧化系统乃至整个生长发育过程中发挥重要作用[13]。此外,GR对抗坏血酸的循环再生也是不可缺少的,GR通过参与植物抗坏血酸谷胱甘肽循环(AsA-GSH cycle),并与超氧化物歧化酶(SOD)等酶系统相互作用,共同清除植物体内多余的 ROS,能够增强植物对干旱、盐、低温和病害等胁迫的抵御能力。大量研究已经表明,在植物的细胞质、叶绿体、线粒体以及溶酶体中均有GR的活性[14-17],而且GR活性会在非生物逆境环境下提高。岳川等[18]成功克隆了茶树的谷胱甘肽还原酶的基因,推测其在茶树抵抗逆境胁迫中起作用。朱守晶等[19]克隆了苎麻谷胱甘肽还原酶基因BnGR1,根据组织表达分析结果,推测其在减轻镉胁迫对苎麻的毒害方面发挥作用。
研究发现,发状念珠藻中存在一个稳定的保护系统,在抵抗极端的胁迫环境中协助SOD和过氧化氢酶(CAT)共同发挥重要作用,有关 GR 基因的研究少见报道。本研究克隆发状念珠藻NfGR基因的ORF序列,并对其编码氨基酸的结构进行生物信息学预测。同时,分析了PEG-6000胁迫下基因的逆境表达特性。以期为进一步研究该基因在发状念珠藻抗逆中的功能提供科学依据,对构建抗旱转基因工程菌的研究提供候选基因,有效地保护荒漠微生物基因资源。
1 材料和方法
1.1 材 料
实验材料为液体悬浮培养发状念珠藻细胞,保存于宁夏大学生命科学学院应用微生物学实验室,培养条件为25 ℃、80 r/min光照培养,生长培养基为BG11培养基。8 000 r/min离心收集藻细胞,保存于-80 ℃冰箱备用。
大肠杆菌(Escherichiacoli)DH5a感受态细胞、DNA Marker、TaqDNA 聚合酶、Protein MarkerⅢ、质粒小提试剂盒、琼脂糖凝胶回收试剂盒购自北京天根公司。pGEM®-T Easy 载体、T4 DNA 连接酶购自美国Promaga 公司。限制性内切酶BamH I、HindⅢ购自美国Fermentas公司。引物合成及基因测序由上海生工生物工程公司完成。
1.2 方 法
1.2.1NfGR基因开放阅读框的扩增 取50 mg发状念珠藻藻细胞,-80 ℃速冻,液氮研磨成粉末,采用CTAB法提取发状念珠藻基因组DNA,电泳检测DNA质量。
根据发状念珠藻基因组精细测序图中GR基因的ORF序列设计引物GR-F(5′-CGCGGATCCATGACTTTTGATTACGACCT-3′,划线部分为BamHⅠ酶切位点)和GR-R(5′-CCCAAGCTTTTACCGCATTGTGACAAATT-3′,划线部分为HindⅢ酶切位点)。以发状念珠藻总DNA 为模板,进行PCR 扩增。扩增条件为:94 ℃ 预变性5 min,94 ℃变性1 min,65 ℃退火1 min,72 ℃延伸1 min,35个循环,72 ℃延伸10 min。目的片段经回收、检测并测序。
1.2.2NfGR基因的生物信息学分析 运用生物信息学数据库 NCBI、ExPASy、MEGA5.1 等软件对发状念珠藻NfGR基因编码蛋白进行生物信息学分析。
1.2.3NfGR基因qRT-PCR分析 以发状念珠藻RPL13基因为内参,进行qRT-PCR检测,分析NfGR基因的表达特性。NfGR基因上下游引物分别为GR-qF(5′-CCTTGAGCGTGAGTGG-3′)和GR-qR(5′-TCGGCATTGATGACGATTAC-3′)。RPL13基因上下游引物分别为RPL13-F(5′-TAGAGTTTGCCTGTATCAT-3′)和RPL13-R(5′-TCCGTGGTTTGTCATC-3′)。qRT-PCR扩增程序为:94 ℃预变性30 s;94 ℃变性5 s;50 ℃退火30 s;72 ℃延伸20 s,共45个循环。实验共设3个重复,利用2-ΔΔCt法计算目的基因相对表达量。
2 结果与分析
2.1 NfGR基因的开放阅读框(ORF)克隆
以发状念珠藻基因组DNA为模板,GR-F 和GR-R 为引物进行PCR扩增,获得1条1 350 bp左右的特异条带(图1)。将回收片段连接至pMD18-T载体, 转化大肠杆菌DH5α感受态细胞后进行菌落PCR鉴定。
BamHI/HindⅢ双酶切质粒,得到2条带,其中1条为1 350 bp左右的目的条带(图2),与预期的扩增片段大小一致 。将阳性克隆送至上海生工生物技术有限公司测序,由测序结果可知,NfGR基因的ORF长1 374 bp。
2.2 NfGR基因编码蛋白的结构分析
氨基酸序列分析发现,NfGR基因ORF可编码458个氨基酸残基,预测分子量为49.42 kD。NfGR蛋白有2个结构域(图3),分别是NADPH结合位点超家族(NADB-Rossmann superfamily)和吡啶氧化还原酶二聚体超家族(Pyr_redox_dim),其中165~245氨基酸序列是吡啶二硫酸氧化还原酶的组分,345~458氨基酸序列是吡啶二硫酸核酸氧化还原酶二聚体结构域,这些功能保守区的存在与谷胱甘肽还原酶的还原作用密切相关。
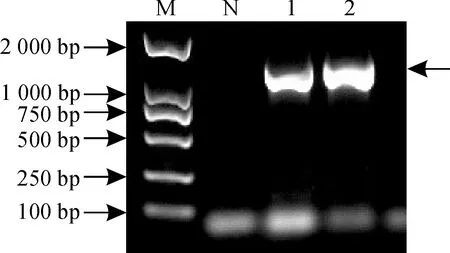
M. DL2000;N.阴性对照;1~2. PCR产物图1 NfGR基因编码序列的克隆M. DL2000;N. Negative control;1~2. PCR productFig.1 Cloning of the coding sequence of NfGR
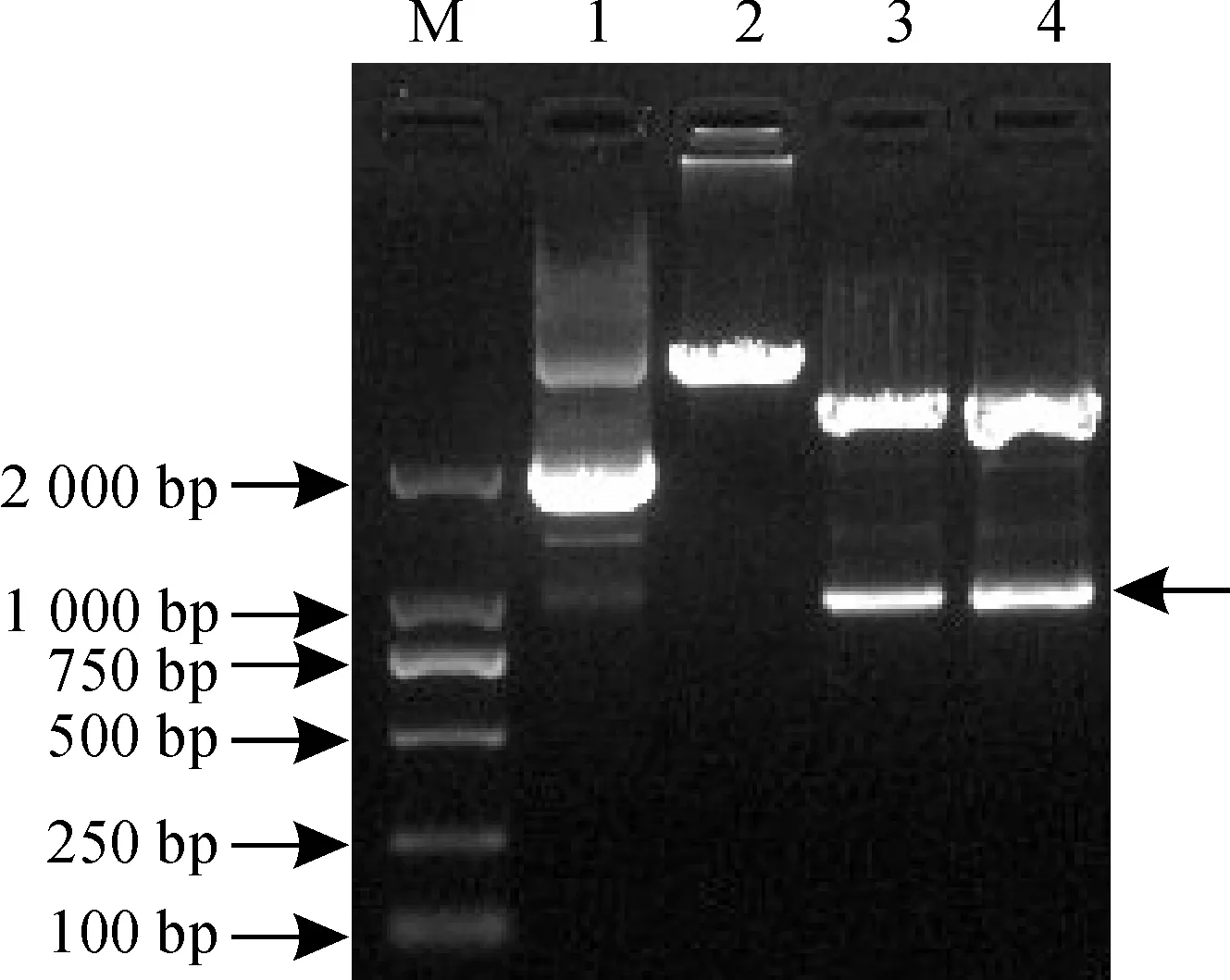
M. Marker;1.HindⅢ 单酶切;2.未酶切质粒;3~4.BamH I/ HindⅢ双酶切图2 NfGR基因阳性克隆质粒酶切结果M. Marker;1. HindⅢ digested plasmid;2. Non-digested plasmid;3~4. BamHⅠ/ Hind Ⅲdigested plasmidFig.2 Enzyme digestion of NfGR gene cloned plasmid
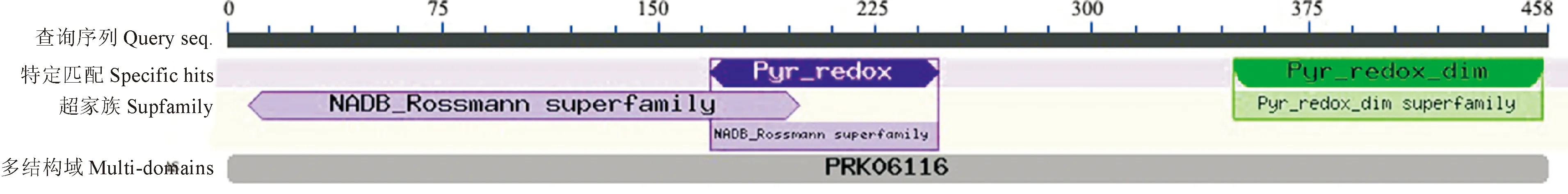
图3 NfGR蛋白保守结构域Fig.3 Prediction of the conserved domains of NfGR

黑色表示序列完全相同,灰色表示部分相同,下划线区为谷胱甘肽还原酶结构域序列;NpGR、NspGR、HbGR、AvGR、ShGR、TcGR、StGR、DcGR、TbGR、AfGR、HspGR和NfGR分别为点形念珠藻、念珠藻、绵丝哈沙藻、多变鱼腥藻、霍夫曼伪枝藻、弯曲单歧藻、单歧伪枝藻、弯曲长孢藻、鲍氏单歧藻、水华束丝藻、软管藻和发状念珠藻GR氨基酸序列图4 谷胱甘肽还原酶氨基酸序列的多重比对Black area donates the same sequence,gray area donates partial matching,the underline marks domain sequences in GR proteins; NpGR, NspGR, HbGR, AvGR, ShGR, TcGR, StGR, DcGR, TbGR, AfGR, HspGR and NfGR represents amino acid sequence of GR from Nostoc punctiforme PCC 73102, Nostoc sp. PCC 7120, Hassallia byssoidea VB512170, Anabaena variabilis ATCC 29413, Scytonema hofmanni UTEXB 1581, Tolypothrix campylonemoides VB511288, Scytonema tolypothrichoides VB-61278, Dolichospermum circinale, Tolypothrix bouteillei VB521301, Aphanizomenonflos-aquae, Hapalosiphon sp. MRB220 and Nostoc flagelliforme,respectivelyFig.4 Multiple alignment of the deduced amino acids sequences of GR proteins
以NfGR基因编码氨基酸序列为信息探针,用Blast程序检索GeneBank的NR数据库发现,NfGR蛋白的氨基酸序列与已报道的其他物种GR蛋白氨基酸序列具有较高的相似性。与点形念珠藻(Nostocpunctiforme)的相似性最高,达到93%,与多变鱼腥藻(Anabaenavariabilis)的相似性为86%,与绵丝哈沙藻(Hassalliabyssoidea)、霍夫曼伪枝藻(Scytonemahofmanni)、弯曲单岐藻(Tolypothrixcampylonemoides)相似性为85%,与水华束丝藻(Aphanizomenonflos-aquae)和软管藻(Hapalosipnonsp.)相似性为80%,与卷曲长孢藻(Dolichospermumcircinale)相似性为79%。用ClustalX2.1软件进行多序列比对发现NfGR编码氨基酸序列与其他物种有差异,但具有催化氧化还原反应和结合GSSG、NAD的高度保守的区域(图4)。
GOR4在线软件预测发现,α-螺旋、β-片层和无规卷曲是 NfGR蛋白二级结构的主要结构元件(图 5,A)。进一步通过SWISS-MODEL 在线工具(http://swissmodel.expasy.org/)进行建模分析,结果显示这些α-螺旋、β-片层和无规卷曲通过延伸链连接折叠成对称的三维空间结构(图 5,B)。
2.3 NfGR基因的系统进化分析
采用MEGA 5.1软件构建发状念珠藻GR蛋白系统进化树(图6)。结果显示,发状念珠藻与点形念珠藻(Nostocpunctiforme)聚为一支,在进化上亲缘关系最近。弯曲单岐藻(Tolypothrixcampylonemoides)、软管藻(Hapalosiphonsp.)、鲍氏单歧藻(Tolypothrixbouteillei)、单歧伪枝藻(Scytonematolypothrichoides)、绵丝哈沙藻(Hassalliabyssoidea)和霍夫曼伪枝藻(Scytonemahofmanni)为另一支,卷曲长孢藻(Dolichospermumcircinale)和水华束丝藻(Aphanizomenonflos-aquae)则聚为一支;念珠藻(Nostocsp.) 和多变鱼腥藻(Anabaenavariabilis)聚为另外一支。

A. 二级结构预测; B. 利用SWISS-MODEL建立的三维结构图5 NfGR蛋白的结构分析和建模A. Secondary structure prediction;B. Three-dimensional structure based on SWISS-MODELFig.5 Structure analysis and modeling of NfGR

系统树各分支上数字是Bootstrap 1 000次循环检验的置信度;标尺代表遗传距离图6 NfGR蛋白进化树分析The numbers on the tree branches represent Bootstrap confidence values as bootstrap is 1 000;The scale bar represents genetic distanceFig.6 Phylogenetic analysis of NfGR protein sequences
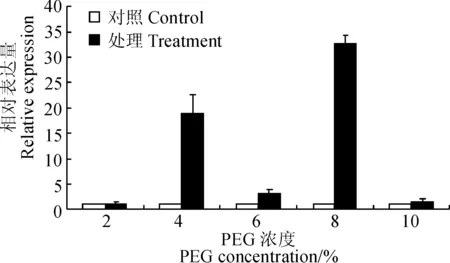
图7 PEG-6000胁迫下NfGR基因的表达分析Fig.7 Expression analysis of NfGR gene under drought-stress of PEG-6000
2.4 干旱胁迫下NfGR基因表达分析
用实时荧光定量RT-PCR技术,分析不同浓度PEG-6000模拟干旱处理下NfGR表达情况(图7)。结果表明,相对于对照,NfGR基因在不同浓度PEG-6000处理下均保持上调表达。PEG-6000 浓度为2%时,NfGR基因受到诱导,表达量开始上升,当PEG-6000 浓度为8%时,相对表达量为32.69,达到峰值。当PEG-6000浓度为10%时,NfGR表达量下降,说明在高浓度PEG-6000胁迫下,细胞受到损伤严重,NfGR基因的表达受到抑制。
3 讨 论
植物耐旱能力的形成是由多个基因协同参与形成的,耐逆性调节基因的上调表达在一定程度上提高了植物的耐逆能力。生物在生长过程中经常会遭受到干旱胁迫,过度干旱胁迫会导致生物体内ROS的代谢失衡,进而对机体造成氧化损伤,如可引起蛋白质、膜脂和其它细胞组分的损伤,进而导致细胞及组织死亡。但在长期的进化过程中,生物本身会产生一些保护机制来清除过多的ROS,一些抗氧化酶系统,包括GR、APX、CAT、SOD和PRX等在内的完整的抗氧化防御体系,积极参与这一过程。
GR是植物细胞抗氧化酶系统中的一个重要蛋白,催化氧化型谷胱甘肽还原成还原型谷胱甘肽(GSH),维持细胞内氧化还原状态的平衡,在植物抵抗非生物胁迫的环境中起到重要作用。GSH在减缓和清除由ROS、生物异源物质及重金属造成的环境氧化胁迫中起重要作用,GSH可有效还原-S-S-键,稳定-SH族蛋白,使膜蛋白结构稳定,保护酶结构蛋白上的-SH,抵抗过氧化作用,充当自由基的清除剂。植物GR同工酶存在于不同的亚细胞器中,如叶绿体、细胞质、线粒体和过氧化物酶体等[20-24]。GR是受逆境胁迫表达的酶之一,在水分胁迫下,细胞器的抗氧化酶活性均表现为先升高后稳定到一定水平,这表明植物细胞中各细胞器能够协调抗氧化防护的能力。在氧化胁迫反应中,GR通过活性的升高对清除活性氧起积极作用。Tanaka 等[25]证明干旱等逆境胁迫会引起菠菜 GR活性的提高。
发状念珠藻是具有较强的耐旱能力的蓝藻类低等植物,在水分胁迫下会引起一系列干旱诱导基因的表达,例如编码一些功能蛋白和调节蛋白的基因,以保护细胞不受水分胁迫的伤害,来抵御环境胁迫。因此,选择抗旱优良基因,对基因功能进行研究,从分子水平认识发状念珠藻对干旱环境胁迫的抗性机理显得尤为重要。
发状念珠藻NfGR基因的表达因受干旱胁迫发生了变化,即在胁迫初期活性氧浓度增加,抗氧化酶系统积极参与,NfGR 表达量开始增加;随胁迫浓度增加,表达量达到峰值;但随胁迫浓度继续增加,细胞相关组分受到干旱伤害,以致NfGR基因表达量在高浓度PEG-6000模拟干旱胁迫时降低,这可能因为高浓度PEG-6000模拟干旱增加了细胞生长环境的干旱程度,细胞内成分因严重缺水而损伤,基因的表达呈下降趋势。发状念珠藻NfGR基因的表达量增加是对干旱胁迫的积极响应,表明其在抵御外界干旱环境过程中发挥一定作用。有关受逆境胁迫时,NfGR 清除活性氧、参与跨膜运输和信号传导的具体分子机理还需要深入的研究。
[1] 郭金英,杜 洁,李彤辉,等.发状念珠藻胞外多糖对小鼠免疫活性的影响[J]. 河南科技大学学报(自然科学版), 2015, 35(1):72-75.
GUO J Y, DU J, LI T H,etal. Effect of extracellular polysaccharides fromNostocflageliformeon mice immunocompetence[J].JournalofHenanUniversityofScienceandTechnology(Natural Science), 2015, 35(1):72-75.
[2] 郭金英,史明科,赵艳丽,等. 发状念珠蓝细菌细胞对Cu2+、Cr2+和Pb2+胁迫的响应[J]. 微生物学报, 2013, 53(6):553-560.
GUO J Y, SHI M K, ZHAO Y L,etal. Response ofNostocflagelliformecell to Cu2+,Cr2+and Pb2+stress [J].ActaMicrobiologicaSinica, 2013, 53(6):553-560.
[3] GAO K S. Chinese studies on the edible blue-green alga,Nostocflagelliforme, a review [J].JournalofAppliedPhycology, 1998,(10):37-49.
[4] 唐进年,赵 明,张盹明,等. 发菜的生物学特性及资源保护[J]. 中国野生植物资源, 2000,19(5): 20-24.
TANG J N,ZHAO M,ZHANG D M,etal. The biological characteristics and protection ofNostocflagelliforme[J].ChineseWildPlantResources, 2000,19(5): 20-24.
[5] 施定基,周国飞,方昭希,等.发菜的光合作用、呼吸作用和形态学的研究[J].植物学报,1992, 34(7):507-514.
SHI D J,ZHOU G F,FANG Z X,etal. Studies on photosynthesis, respiration and morphology ofNostocflagelliforme[J].BulletinofBotany, 1992, 34(7):507-514.
[6] 钟泽璞,施定基,王发珠. 温度、含水量和光照对发菜固氮酶活性的影响[J]. 植物学报, 1992, 34(3):219-225.
ZHONG Z P,SHI D J,WANG F Z. Effect of temperature, water content and light intensity on nitrogenase activity ofNostocflagelliforme[J].BulletinofBotany, 1992, 34(3):219-225.
[7] 华振基,王 俊,孙建芸,等.发菜生物学特性及其人工栽培途径的研究[J]. 宁夏农学院学报, 1994, 15(5):19-22.
HUA Z J, WANG J, SUN J Y,etal. Biological charcteris ofNostocflagelliformeand the way for its artificial cultivation[J].JournalofNingxiaAgriculturalUniversity, 1994, 15(5):19-22.
[8] LIANG W Y, ZHOU Y W, WANG L X,etal. Ultrastructural, physiological and proteomic analysis ofNostocflagelliformein response to dehydration and rehydration[J].JournalofProteomics, 2012, 75:5 604-5 627.
[9] GAO X, YANG Y W, CUI L J,etal. Preparation of desiccation-resistant aquatic-livingNostocflagelliforme(Cyanophyceae) for potential ecological application[J].MicrobialBiotechnology, 2015, (6):1 006-1 012.
[10] 汪 滢,陈李萍,陈 晓,等. 发菜中超氧化物歧化酶基因的克隆及在大肠杆菌中的表达[J]. 植物研究,2007, 27(3): 289-292.
WANG Y, CHEN L P, CHEN X,etal. Cloning and expression of gene which encodes SOD ofNostocflagelliformeinE.coli[J].BulletinofBotanicalResearch, 2007, 27(3): 289-292.
[11] AHMAD P, SARWAT M, SHARMA S. Reactive oxygen species, antioxidants and signaling in plants[J].JournalofPlantBiology, 2008, 51(3): 167-173.
[12] DALKIN K, EDWARDS R, EDINGTON B,etal. Stress responses in alfalfa (MedicagosativaL.) I. Induction of phenylpropanoid biosynthesis and hydrolytic enzymes in elicitor- treated cell suspension cultures[J].PlantPhysiology, 1990, 92(2): 440-446.
[13] NOCTOR G, FOYER C H. Ascorbate and glutathione: keeping active oxygen under control[J].AnnualReviewofPlantPhysiologyandPlantMolecularBiology, 1998, 49:249-279.
[14] RUDHE C, CLIFTON R, CHEW O,etal. Processing of the dual targeted precursor protein of glutathione reductase in mitochondria and chloroplasts[J].JournalofMolecularBiology, 2004, 343(3): 639-647.
[15] DEL RIO L A, CORPAS F J, SANDALIO L M,etal. Reactive oxygen species, antioxidant systems and nitric oxide in peroxisomes[J].TheJournalofExperimentalBotany, 2002, 53(372): 1 255-1 272.
[16] MEISTER A, ANDERSON M E. Glutathione[J].AnnualReviewofBiochemistry, 1983, 52: 711-760.
[17] ALSCHER R G. Biosynthesis and antioxidant function of glutathione in plants[J].PhysiologiaPlantarum, 2006, 77(3): 457-464.
[18] 岳 川,曹红利,周艳华,等. 茶树谷胱甘肽还原酶基因CsGRs的克隆与表达分析[J]. 中国农业科学,2014,47(16):3 277-3 289.
YUE C, CAO H L, ZHOU Y H,etal. Cloning and expression analysis of glutathione reductase genes (CsGRs) in tea plant (Camelliasinensis)[J].ScientiaAgriculturaSinica, 2014,47(16):3 277-3 289.
[19] 朱守晶,余伟林,石朝燕,等. 苎麻谷胱甘肽还原酶基因(BnGR1)的克隆和表达分析[J]. 农业生物技术学报,2015, 23(10): 1 318-1 326.
ZHU S J,YU W L, SHI C Y,etal. Cloning and expression analysis of glutathione reductase gene (BnGR1) from ramie (BoehmerianiveaL.)[J].JournalofAgriculturalBiotechnology. 2015, 23(10): 1 318-1 326.
[20] JOST R, ALTSCHMIED L, BLOEM E. Expression profiling of metabolic gene in response to methyl jasmonate reveals regulation of genes of primary and secondary sulfur related pathways inArabidopsisthalinan[J].Photosynth.Research, 2005, 86: 491-508.
[21] JIMENEZ A, HERNANDEZ J A, DELRIO L A. Evidence for the presence of the ascorbate glutathione cycle in mitochondria and peroxisones of pea leaves[J].PlantPhysiology, 1997, 114: 275-284.
[22] TANG X, WEBB M A. Soybean root nodule cDNA encoding glutathione reductase[J].PlantPhysiology, 1994, 104: 1 081-1 082.
[23] CREISSEN G P, MULLINEAUX P M. Cloning and characterization of glutathione reductase cDNA and identification of two genes encoding the tobacco enzyme[J].Planta, 1995, 197(2): 422-425.
[24] MU LINEAUX P, ENARD C, HELLENS R. Chracterization of a glutathione reductase gene and its gene ticlocus from pea (PisumsativumL.)[J].Planta, 1996, 200: 186-194.
[25] TANAKA K, MASUDA R, SUGIMOTO T,etal. Water deficiency induced changes in the content of defensive substances against active oxygen in spinach leaves[J].AgricultureandBiologicalChemistry, 1990, 54: 2 629-2 634.
(编辑:宋亚珍)
Cloning and Identification of Drought-stress Responsive Gene NfGR in Nostoc flagelliforme
YUE Sijun, FAN Hongli, ZHENG Rui, ZHOU Juan, SU Jianyu*
(College of Life Sciences, Ningxia University, Key Lab of Ministry of Education for Protection and Utilization of Special Biological Resources in Western China, Yinchuan 750021, China)
Glutathione reductase is one of enzymes participating in the oxidation reduction reaction in organisms, which plays an important role in the process of stress tolerance. As a kind of cyanobacteria,Nostocflagelliformepossesses strongly resistance to environment stresses,so it is meaningful to study the role of glutathione reductase in the resistant mechanism. In order to explore the biological functions of glutathione reductase in process of stress tolerance inN.flagelliforme, we cloned the complete open reading frame of the geneNfGR, and took a bioinformatics analysis of gene sequence. The ORF ofNfGRcontains 1 374 bp, encoding 458 amino acids, and its relative molecular weight and theoretical isoelectric point is 49.42 kD and 5.49, respectively. Amino acid sequence analysis showed that the protein NfGR has two domains of NADB-Rossmann superfamily and Pyr redox dim superfamily, and amino acid sequence of NfGR protein is similar to that ofNostocpunctiformewith similarity up to 93%. Phylogenetic tree reconstructed by neighbor joining method clearly showed that NfGR protein was classified into a subgroup withN.punctiforme, which suggested their close relationship. qRT-PCR result showed that the expressions ofNfGRgene were up-regulated under different concentrations of PEG-6000, and reached peak at 8% PEG-6000 concentration, with the relative expression level of 32.69. It is hypothesized that glutathione reductase may be involved in the response to stress resistance ofN.flagelliformeaccording to its expression characteristics.
Nostocflagelliforme; glutathione reductase; gene cloning; quantitative real-time PCR
1000-4025(2016)10-1955-07
10.7606/j.issn.1000-4025.2016.10.1955
2016-06-18;修改稿收到日期:2016-09-07
国家自然科学基金(31360025,31260023,31560418);宁夏大学研究生创新项目(GIP201611)
岳思君(1972-),男,博士,副教授,硕士研究生导师,主要从事微生物学研究。E-mail: sijunyue@126.com
*通信作者:苏建宇,博士,教授,硕士研究生导师,主要从事微生物学研究。E-mail: su_jy@nxu.edu.cn
Q785; Q786
A
