温敏性乙二醇壳聚糖水凝胶的制备及药物缓释性能
2016-12-14李征征徐子扬高留意赵琳琳
李征征,徐子扬,高留意,曾 威,赵琳琳
(1.天津科技大学化工与材料学院,天津300457;2.天津理工大学材料科学与工程学院,天津市光电显示材料与器件重点实验室,天津300384)
温敏性乙二醇壳聚糖水凝胶的制备及药物缓释性能
李征征1,徐子扬1,高留意1,曾威1,赵琳琳2
(1.天津科技大学化工与材料学院,天津300457;2.天津理工大学材料科学与工程学院,天津市光电显示材料与器件重点实验室,天津300384)
以乙二醇壳聚糖为原料,乙酸酐为酰化剂,通过N⁃乙酰化反应,制得了新型温敏性高分子乙酰化乙二醇壳聚糖.通过核磁共振氢谱(1H NMR)、傅里叶变换红外光谱(FTIR)及试管倒置法对乙酰化乙二醇壳聚糖的结构及温敏性进行了表征,通过扫描电子显微镜(SEM)和紫外⁃可见分光光度计(UV⁃Vis)对水凝胶的微观形貌和体外药物释放性能进行了研究.结果表明,随着反应时间和乙酸酐与乙二醇壳聚糖氨基摩尔比的增加,产物的乙酰度逐渐增加;乙酰化乙二醇壳聚糖溶液具有热可逆温敏性溶胶⁃凝胶转变行为,可以通过控制乙酰化乙二醇壳聚糖的乙酰度和溶液浓度,使溶胶⁃凝胶转变温度处于室温至体温(25~37℃)之间;乙酰化乙二醇壳聚糖水凝胶具有“高度孔隙化且孔隙之间相互连通”的结构特点,通过控制乙酰度和溶液浓度,可使其孔径大小处于1~40 μm范围内;乙酰化乙二醇壳聚糖水凝胶的乙酰度为89.90%时,质量分数为5%~7%的水凝胶对抗癌药物吉西他滨具有缓释作用,载药凝胶的释药时间可达3~5 d.乙酰化乙二醇壳聚糖有望在药物释放及组织工程等领域得到广泛应用.
乙二醇壳聚糖;乙酰化乙二醇壳聚糖;温敏性水凝胶;药物缓释载体
水凝胶是由亲水聚合物组成的三维网状结构,具有良好的生物相容性,因而在生物医用领域得到了广泛应用[1~4].在众多的水凝胶中,温敏性水凝胶是研究最多的一类智能水凝胶,其可以响应温度变化而发生体积相变或溶胶⁃凝胶转变.近年来,对温敏性水凝胶作为原位形成可注射凝胶体系的研究越来越受到关注[5].可注射水凝胶通过注射的方式输入人体内,无需手术,具有微创的特点,将其用于生物医药领域,患者依从性好,可对药物、蛋白质、基因和细胞等进行可控封装和释放,因而受到研究人员的青睐[6~8].当温敏性水凝胶可以在室温(25℃)下呈现自由流动的溶胶状态,而在体温(37℃)下则转变为凝胶状态时,则可以作为可注射水凝胶得到应用[2,9].温敏性可注射水凝胶由于独特的温敏性溶胶⁃凝胶转变行为,使其可以在注射前实现对药物或细胞的封装,而在注射位点迅速形成凝胶,达到局部给药的效果[10],因而在药物缓释载体、组织工程支架和伤口愈合等方面得到广泛应用[11,12].天然高分子(如壳聚糖、海藻酸钠和透明质酸等)和合成高分子[如泊洛沙姆和聚(N⁃异丙基丙烯酰胺)等]均可以作为温敏性水凝胶的骨架材料.天然高分子具有良好的生物降解性,可以在人体内微生物的作用下降解成小分子物质,被人体吸收和利用,并通过新陈代谢排出体外.而相比之下,合成高分子的生物降解性能较差,且可能有未反应完全的小分子残留,对人体有一定的毒性.因此,天然高分子更有利于在生物医用领域(如药物缓释载体及组织工程支架等)得到应用[13].
壳聚糖是一种常见的天然高分子,具有生物降解性、生物相容性、细菌抗性及黏膜黏附性,因而在生物医学领域得到广泛应用[14~19].然而,由于壳聚糖分子链上存在大量的氨基和羟基,使分子间形成了大量氢键,导致结晶度过大,进而使得壳聚糖的水溶性较差,仅溶于少部分稀酸,这大大限制了其在水凝胶领域的应用[20].乙二醇壳聚糖是一种壳聚糖的衍生物,其在保证壳聚糖优良特性(低毒、生物相容性及可降解性)的同时,大大改善了其壳聚糖的水溶性,使其在任何pH值下均能溶解[21].此外,乙二醇壳聚糖上具有大量的氨基,可以对其进行功能化改性.Li等[22]通过迈克尔加成反应合成了乙二醇壳聚糖温度敏感性水凝胶生物支架,并用于培养软骨细胞,研究结果表明,乙二醇壳聚糖温度敏感性水凝胶生物支架能够支持软骨细胞的增殖与分化,有望用于软骨再生.Lee等[23]合成了癸酸改性的乙二醇壳聚糖温敏性水凝胶,并用于皮下注射治疗Ⅱ型糖尿病,研究表明,该水凝胶体系能够有效地控制糖尿病小鼠的血糖水平长达7 d.
本文通过对乙二醇壳聚糖进行N⁃乙酰化改性,制得了一种新型温敏性高分子乙酰化乙二醇壳聚糖(NAGC),并对其结构进行了表征.考察了反应时间和乙酸酐与乙二醇壳聚糖上氨基摩尔比对产物乙酰度(DA)的影响;采用试管倒置法对乙酰化乙二醇壳聚糖进行了温敏性表征,并考察了乙酰度和溶液浓度对其溶胶⁃凝胶转变温度的影响;采用扫描电子显微镜(SEM)对乙酰化乙二醇壳聚糖水凝胶的微观形貌进行了观察;以吉西他滨为模型药物,采用紫外⁃可见分光(UV⁃Vis)光度计,对乙酰化乙二醇壳聚糖水凝胶在37℃下的体外药物释放性能进行了测试.
1 实验部分
1.1 试剂与仪器
乙二醇壳聚糖购于和光制药工业株式会社,纯度为60%,聚合度>400;乙酸酐(Ac2O)购于西亚试剂公司,纯度为99.5%;无水甲醇购于天津博迪化工股份有限公司,纯度>99.5%;丙酮购于天津百赛斯生物科技有限公司,分析纯;吉西他滨,纯度>99%,上海伟进生物科技有限公司.
MAGNA 560型傅里叶红外光谱仪(美国Nicolet公司);JNM⁃AL400型核磁共振氢谱仪(日本JEOL有限公司);JSM⁃7000F型场致扫描电子显微镜(日本JEOL有限公司);Mini⁃1024型紫外⁃可见分光光度计(日本岛津公司);FD⁃1型冷冻干燥机(北京德天佑科技发展有限公司);TDZ4⁃WS型台式低速自动平衡离心机(湖南湘仪离心机仪器有限公司).
1.2 实验过程
称取0.3 g乙二醇壳聚糖粉末于烧杯中,加入45 mL去离子水,磁力搅拌至粉末完全溶解.加入45 mL无水甲醇,磁力搅拌15~20 min后,按照乙酸酐与乙二醇壳聚糖上氨基摩尔比(5∶1,10∶1,20∶1和30∶1)移取一定量的乙酸酐,并在磁力搅拌下,缓慢滴加到烧杯中,反应一定时间(2,4,8和12 h)后,将反应液倒入丙酮中沉淀过夜,用离心机进行离心,再将沉淀物溶于去离子水中,将溶液倒入渗析袋中,用大量去离子水渗析2 d,经冷冻干燥后,得到白色絮状的乙酰化乙二醇壳聚糖产物.
1.3 测试与性能表征
测试乙酰化乙二醇壳聚糖的1H NMR谱,以质量分数为1%的乙酰化乙二醇壳聚糖的重水(D2O)溶液作为测试样品,测试条件为400 MHz.采用傅里叶红外光谱仪对乙酰化乙二醇壳聚糖样品进行红外光谱测定,样品用KBr压片,波数范围为400~4000 cm-1,扫描32次,分辨率为4 cm-1.
采用试管倒置法,对乙酰化乙二醇壳聚糖的温敏性溶胶⁃凝胶转变温度进行测定.在4℃下,将不同乙酰度的乙酰化乙二醇壳聚糖溶于磷酸盐(PBS,pH=7.4,0.01 mol/L)缓冲液中,在5 mL的试管中配制成不同质量分数(4%,5%,6%,7%)的溶液.将试管放入升温装置内(升温速率为0.2℃/min),每过一段时间,将试管倒置,观察试管中溶液的流动情况.若试管倒置30 s,管内物质不发生流动,则确定此时温度为溶胶⁃凝胶转变温度.
对乙酰化乙二醇壳聚糖水凝胶进行液氮淬冷,制成切片,冷冻干燥24 h,对其进行喷金处理,然后用场致扫描电子显微镜观察乙酰化乙二醇壳聚糖水凝胶的微观形貌.
通过测试乙酰化乙二醇壳聚糖对抗癌药物吉西他滨的体外药物释放性能评估其在可注射药物缓释载体方面应用的可行性.在4℃下,将乙酰化乙二醇壳聚糖(乙酰度为89.90%)和吉西他滨溶于PBS溶液中.在5 mL的试管中分别配制1 mL 5%和7%的乙酰化乙二醇壳聚糖溶液,吉西他滨的最终浓度为10 mg/mL.于37℃维持30 min,制得载药凝胶.向每个试管中的载药凝胶顶部缓慢滴加3 mL PBS后,再置于37℃的恒温水浴摇床中进行培养,振荡速度为20 r/min,一定时间后,将3 mL PBS移除,并加入等体积的新鲜PBS来补偿释放介质.释放介质中药物浓度和累积释放量可以通过吉西他滨标准曲线计算,其中标准曲线通过Mini⁃1024型紫外⁃可见分光光度计绘制.
2 结果与讨论
2.1 乙酰化乙二醇壳聚糖的制备
以乙二醇壳聚糖为原料,乙酸酐为酰化剂,通过乙二醇壳聚糖分子链上的氨基与乙酸酐进行N⁃乙酰化反应,得到乙酰化乙二醇壳聚糖(NAGC),其反应式如Scheme 1所示.
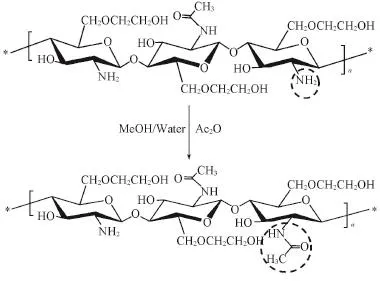
Scheme 1 Synthetic route of N⁃acetyl glycol chitosan
采用“单因素分析法”,将反应时间固定为8 h,反应温度为室温,考察物质的量比对产物乙酰化乙二醇壳聚糖乙酰度的影响,结果示于表1.由表1可以看出,随着物质的量比的增加,产物乙酰度逐渐增加,说明通过控制乙酸酐与乙二醇壳聚糖上氨基物质的量比可以实现对乙酰化乙二醇壳聚糖乙酰度的调节.当物质的量比为30∶1时,产物乙酰度达到最大值(87.23%).将物质的量比固定为30∶1,反应温度为室温,分别在反应时间为2, 4,8和12 h的条件下考察反应时间对产物乙酰化乙二醇壳聚糖乙酰度的影响,结果列于表2.由表2可以看出,随着反应时间的增加,产物乙酰度逐渐增加.当反应进行12 h时,产物的乙酰度达到最大值(89.90%).

Table 1 Degree of acetylation of N⁃acetyl glycol chitosan with different molar ratiosa

Table 2 Degree of acetylation of N⁃acetyl glycol chitosan with different reaction time
因此,以乙酰度作为评价标准,制备乙酰化乙二醇壳聚糖的最佳条件为:反应时间12 h,乙酸酐与乙二醇壳聚糖上氨基的物质的量比30∶1.
2.2 结构表征
图1为不同反应条件下乙酰化乙二醇壳聚糖的核磁共振氢谱(1H NMR),其中,δ 4.65处表示重水峰,δ 1.89处为乙酰基上的甲基上质子峰,δ 2.6处为氨基的质子峰,而δ 3~4处的重叠峰则代表了吡喃葡萄糖基环上的H2—H8.可以看出,与乙二醇壳聚糖相比,乙酰化乙二醇壳聚糖谱图中代表氨基的质子峰消失,而代表乙酰基上甲基的质子峰逐渐明显,说明得到了乙酰化乙二醇壳聚糖.此外,根据1H NMR的结果,可以求出乙酰化乙二醇壳聚糖的乙酰度(DA),计算方法如下所示.

图2为不同反应条件下样品的红外光谱(FTIR).可以看出,与乙二醇壳聚糖谱图相比,样品谱图中,在1654和1559 cm-1处分别出现酰胺基上羰基和N—H的弯曲振动峰,而1599 cm-1处代表氨基上N—H的弯曲振动峰消失,说明与乙二醇壳聚糖相比,样品的分子链上氨基数目有所减少,乙酰基数目有所增多,结合对乙二醇壳聚糖与乙酰化乙二醇壳聚糖的结构分析可见,制得了乙酰化乙二醇壳聚糖.此外,在样品谱图中1730~1740 cm-1处并未出现代表酯羰基的弯曲振动峰,说明乙酰化反应发生在氨基上,为N⁃乙酰化反应.

Fig.11H NMR spectra of glycol chitosan and NAGC with different molar ratios(A)and different reaction time(B)(A)a.Glycol chitosan;b.NAGC 1;c.NAGC 2;d.NAGC 3;e.NAGC 4;(B)a.glycol chitosan;b.NAGC 5;c.NAGC 6;d.NAGC 7;e.NAGC 8.

Fig.2 FTIR spectra of glycol chitosan and NAGC prepared with different mole ratios(A)and different reaction time(B)(A)a.Glycol chitosan;b.NAGC 1;c.NAGC 2;d.NAGC 3;e.NAGC 4.(B)a.glycol chitosan;b.NAGC 5;c.NAGC 6;d.NAGC 7;e.NAGC 8.
2.3 温敏性溶胶⁃凝胶转变
采用“试管倒置法”对不同溶液浓度(4%,5%,6%和7%)的乙酰化乙二醇壳聚糖的溶胶⁃凝胶转变温度进行了测定.结果表明,随着温度的升高,乙酰度在83.88%~89.90%范围内的乙酰化乙二醇壳聚糖溶液在某一温度(20~65℃)下,表现出由“自由流动的溶胶状态”转变为“凝胶状态”的行为,而当乙酰度较低时,则不会发生上述温敏性凝胶化行为.图3为乙酰化乙二醇壳聚糖乙酰度和溶液浓度与其溶胶⁃凝胶转变温度的关系曲线.可以看出,随着乙酰化乙二醇壳聚糖乙酰度和溶液浓度的增加,其溶胶⁃凝胶转变温度逐渐降低,说明可以通过控制乙酰度和溶液浓度使转变温度处于室温至体温(25~37℃)之间,这有利于其在可注射药物缓释载体方面得到应用.此外,当温度由体温降至室温时,凝胶状的乙酰化乙二醇壳聚糖会重新转变为溶胶状态,这一现象说明,乙酰化乙二醇壳聚糖的溶胶⁃凝胶转变行为具有热可逆性.与其它壳聚糖基温敏性水凝胶体系相比,乙酰化乙二醇壳聚糖本身即具有温敏性,无需引入其它物质(如盐类,聚合物等),因而更有利于在生物医药领域得到应用.

Fig.3 Sol⁃gel transition phase diagram of NAGC measured by the tube inverting methodInsets are the maps of sol and gel.
Scheme 2为乙酰化乙二醇壳聚糖温敏性溶胶⁃凝胶转变机理示意图.当环境温度在乙酰化乙二醇壳聚糖的溶胶⁃凝胶转变温度以下时,溶液中的高分子链上的亲水基团(主要为羟基)通过氢键与水分子结合,宏观表现为乙酰化乙二醇壳聚糖溶于水中,呈现一种可以自由流动的溶胶状态.随着温度的升高,这种氢键作用逐渐减弱,高分子链对水分子的结合作用也减弱.同时,高分子链中疏水基团(乙酰基)之间的相互作用逐渐增强[24].当环境温度上升至溶胶⁃凝胶转变温度以上时,疏水作用成为体系中的主要作用力,高分子链通过疏水作用相互交联,宏观表现为乙酰化乙二醇壳聚糖在环境温度的作用下由溶胶状态转变为凝胶状态,即乙酰化乙二醇壳聚糖溶液出现了溶胶⁃凝胶转变现象.结合上述分析,可以对实验结果所示乙酰度与溶液浓度对溶胶⁃凝胶转变的影响和热可逆性作出如下解释:由于乙酰度和溶液浓度的增加,使得乙酰化乙二醇壳聚糖分子链之间的物理交联更容易形成,进而导致溶胶⁃凝胶转变温度较低;此外,当温度由溶胶⁃凝胶转变温度以上降至室温时,疏水作用会逐渐减弱,氢键作用会逐渐增强,进而使乙酰化乙二醇壳聚糖重新回到溶胶状态,具有热可逆性.
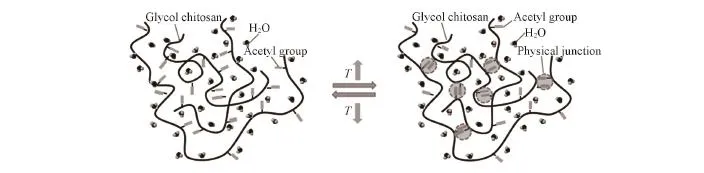
Scheme 2 Mechanism of thermo⁃sensitive sol⁃gel transition of NAGC
2.4 乙酰化乙二醇壳聚糖水凝胶的微观形貌
图4为不同乙酰度和溶液浓度条件下乙酰化乙二醇壳聚糖水凝胶的SEM照片.可以发现,乙酰化乙二醇壳聚糖水凝胶具有高度孔隙化且孔隙之间相互连通的结构特点,且孔径在1~40 μm范围内.随着乙酰度和溶液浓度的增加,孔径逐渐缩小,孔隙分布逐渐变密,这可能是由于乙酰化乙二醇壳聚糖分子链之间的乙酰基疏水作用增强,进而使交联密度增加,导致了孔径逐渐缩小,孔隙分布逐渐变密,这也说明,可以通过控制乙酰度和溶液浓度实现对孔径的调节.此外,乙酰化乙二醇壳聚糖水凝胶的这种多孔隙网状结构,作为可注射性凝胶载体,在药物缓释载体方面具有潜在的应用价值.

Fig.4 SEM images of surface morphology of lyophilized NAGC hydrogel with different DA and concentration(A)NAGC 6(5%);(B)NAGC 7(5%);(C)NAGC 8(5%);(D)NAGC 6(7%);(E)NAGC 7(7%);(F)NAGC 8(7%).
2.5 体外药物释放性能
2.5.1 载药凝胶的体外药物释放性能 图5示出了不同溶液浓度(5%和7%)下制得乙酰化乙二醇壳聚糖(DA=89.90%)载药凝胶的累积药物释放率随时间的变化情况.累积药物释放率可以通过下式计算[25]:


Fig.5 Drug release curves of gemcitabine loaded NAGC[5%(a)and 7%(b)]hydrogel
式中:V0为释放介质的总体积;ct为某一时间点测得PBS中吉西他滨的浓度;V为每次所取PBS的体积;m为乙酰化乙二醇壳聚糖水凝胶的载药量.
由释放曲线可见,在释放初期,会出现一定程度的药物突释现象,且药物突释率小于20%,这一行为有利于控制肿瘤的生长.而随着释放时间的延长,药物释放速率逐渐减缓,直至释放后期,曲线斜率趋近于零,这表明载药凝胶的药物释放达到了平衡.吉西他滨在载药凝胶中的主要释放机理为扩散作用,在释放初期,药物在载药凝胶表面和释放介质之间的浓度梯度较大,进而导致突释现象的出现;之后,载药凝胶内部的药物向外扩散,随着时间的延长,载药凝胶和释放介质中药物的浓度梯度逐渐降低,使得药物释放速率减缓.此外,乙酰化乙二醇壳聚糖载药凝胶对吉西他滨的释放时间可达3~5 d.表明其对吉西他滨具有缓释作用,有望成为一种新型抗癌药物载体.
2.5.2 药物释放行为的拟合方程 本文对在溶液浓度为5%和7%条件下形成乙酰化乙二醇壳聚糖(DA=89.90%)载药凝胶的体外药物释放性能测试所得数据进行了拟合,结果列于表3和表4.可以看出,乙酰化乙二醇壳聚糖水凝胶对吉西他滨的释放行为可以分为3个阶段:主要药物释放阶段、减速阶段和残余药物释放阶段.这3个阶段分别符合一级释放模型、Ritger⁃Peppas模型和Higuchi模型,这种现象可能与载药凝胶内和释放介质中的药物浓度梯度有关.

Table 3 Fitting equation of the drug release behavior of NAGC hydrogel(DA=89.90%,5%)

Table 4 Fitting equation of the drug release behavior of NAGC hydrogel(DA=89.90%,7%)
综上所述,通过乙二醇壳聚糖的N⁃乙酰化反应,制备了新型温敏性聚合物乙酰化乙二醇壳聚糖,并对其温敏性进行了表征.结果表明,乙酰化乙二醇壳聚糖溶液具有温敏性溶胶⁃凝胶转变行为,通过控制乙酰化乙二醇壳聚糖的乙酰度和溶液浓度,可以使溶胶⁃凝胶转变温度处于室温至体温(25~37℃)之间.乙酰化乙二醇壳聚糖水凝胶具有高度孔隙化且孔隙之间相互连通的结构特点,通过控制乙酰度和溶液浓度,可将其孔径大小控制在1~40 μm之间.此外,乙酰化乙二醇壳聚糖水凝胶对抗癌药物吉西他滨具有缓释作用,载药凝胶的释药时间可达3~5 d.因此,温敏性乙酰化乙二醇壳聚糖水凝胶在可注射药物缓释载体方面具有光明的应用前景.
[1] Sadia A.,Shaista K.,Atif I.,Irtaza J.,Tahir J.,Muhammad M.A.,Muhammad I.S.,Abdul G.,Int.J.Biol.Macromolec.,2015,80,240—245
[2] Sivashanmugam A.,Arun Kumar R.,Vishnu Priya M.,Nair S.V.,Jayakumar R.,Eur.Polym.J.,2015,72,543—565
[3] Cong T.H.,Nguyen M.K.,Lee D.S.,Acta Biomater.,2011,7,3123—3130
[4] Nguyen Q.V.,Dai P.H.,Park J.H.,Lee D.S.,Eur.Polym.J.,2015,72,602—619
[5] Sytze J.B.,Kristel W.M.B.,Pieter J.D.,Jan F.,Tina V.,Wim E.H.,J.Control.Release.,2014,190,254—273
[6] Niels M.B.S.,Emilia B.,Mathew P.,Todd H.,Acta Biomater.,2014,10,4143—4155
[7] Paul Z.E.,Gary W.L.,Hua W.,Michael C.J.,Philip J.H.,Suzie H.P..J.Control.Release.,2015,208,76—84
[8] Lin C.,Zhao P.,Li F.,Guo F.,Li Z.,Wen X.,Mater.Sci.Eng.C,2010,30,1236—1244
[9] Yu L.,Ding J.D.,Chem.Soc.Rev.,2008,37(7),1473—1481
[10] Ni P.Y.,Ding Q.X.,Fan M.,Liao J.F.,Qian Z.Y.,Luo J.C.,Li X.Q.,Feng L.,Yang Z.M.,Wei Y.Q.,Biomaterials,2014,35,236—248
[11] Sarah P.H.,Robert L.,Gerald R.F.,Daniel S.K.,Biomaterials,2010,31,1444—1452
[12] Li L.,Wang N.,Jin X.,Deng R.,Nie S.H.,Sun L.,Wu Q.J.,Wei Y.Q.,Gong C.Y.,Biomaterials,2014,35,3903—3917
[13] Xie B.B.,Jin L.,Luo Z.C.,Yu J.,Shi S.,Zhang Z.L.,Shen M.X.,Chen H.,Li X.Y.,Song Z.M.,Int.J.Pharm.,2015,490,375—383
[14] Yannic B.S.,Robert G.,Olivier J.,Eur.J.Pharm.Biopharm.,2008,68,19—25
[15] Chen J.P.,Cheng T.H.,Polymer,2009,50,107—116
[16] Elie Z.,Shreya R.,Robert R.G.,Khalil N.B.,Biomaterials,2012,33,4810—4817
[17] Elias A.,Marion M.,Sophie L.,Carbohydr.Polym.,2015,130,87—96
[18] Cao L.P.,Cao B.,Lu C.J.,Wang G.W.,Yu L.,Ding J.D.,J.Mater.Chem.B,2015,3,1268—1280
[19] Songkroh T.,Xie H.G.,Yu W.T.,Lv G.J.,Liu X.D.,Wang L.,Sun G.W.,Xu X.X.,Ma X.J.,Sci.Bull.,2015,60(2),235—240
[20] Monier M.,Ayad D.M.,Wei Y.,Sarhan A.A.,Biochem.Eng.J.,2010,51,140—146
[21] Yu J.M.,Li Y.J.,Wang C.R.,Yin Y.S.,Qiu L.Y.,Jin Y.,Journal of Chinese Pharmaceutical Sciences,2010,45,277—282(余敬谋,李永杰,王成润,尹玉寿,邱利焱,金一.中国医药杂志,2010,45,277—282)
[22] Li F.,Ba Q.J.,Niu S.M.,Sun J.,Mater.Sci.Eng.C,2012,32,2017—2025
[23] Lee C.K.,Choi J.S.,Kim I.S.,Byeon H.J.,Kim T.H.,Oh K.T.,Lee E.S.,Lee K.C.,Youn Y.S.,Acta Biomater.,2014,10,812—820
[24] Yu L.,Zhang H.,Ding J.D.,Angew.Chem.Int.Ed.,2006,45,2232—2235
[25] Chen M.L.,Preparation and Characterization of mPEG/CS Temperature Sensitive Hydrogel,Suzhou University,Suzhou,2011(陈美玲. mPEG/CS温敏性水凝胶的制备及性能表征,苏州:苏州大学,2011)
(Ed.:D,Z)
†Supported by the Young Teachers Innovation Fund of Tianjin University of Science and Technology,China(No.2014CXLG16).
Preparation and Characterization of Thermo⁃sensitive N⁃Acetyl Glycol Chitosan Hydrogel for Sustained Drug Release†
LI Zhengzheng1∗,XU Ziyang1,GAO Liuyi1,ZENG Wei1,ZHAO Linlin2∗
(1.College of Chemical Engineering and Materials Science,Tianjin University of Science and Technology,Tianjin 300457,China;2.Tianjin Key Laboratory for Photoelectric Materials and Devices,School of Materials Science&Engineering,Tianjin University of Technology,Tianjin 300384,China)
A novel thermo⁃sensitive polymer N⁃acetyl glycol chitosan(NAGC)by N⁃acetylation of glycol chitosan with acetic anhydride was prepared.The chemical structure,thermo⁃sensitive property,morphology and in vitro drug release properties of NAGC hydrogel were investigated by means of1H NMR,FTIR,tube inverting method,SEM and UV⁃Vis spectroscopy.The results show that the degree of acetylation(DA)of NAGC is increased along with the increase of the feed molar ratio of acetic anhydride to glycol chitosan and re⁃action time.NAGC hydrogel shows reversible thermo⁃sensitive sol⁃gel transition behavior,and the sol⁃gel tran⁃sition temperature is well controlled from 25℃to 37℃by controlling the DA and polymer concentration. NAGC hydrogels show macroporous structure with the pore size of 1—40 μm.The pores are well⁃interconnec⁃ted to each other and the pore size could be controlled by changing the DA and concentration of NAGC.NAGC hydrogel(DA=89.90%,5%—7%,mass fraction)shows sustained release behavior for anticancer drug gem⁃citabine,and the release time could be controlled from 3 d to 5 d.NAGC shows great promise for various bio⁃medical applications,such as drug delivery and tissue engineering.
Glycol chitosan;N⁃Acetyl glycol chitosan;Thermo⁃sensitive hydrogel;Drug release carrier
O636
A
10.7503/cjcu20160513
2016⁃07⁃18.网络出版日期:2016⁃10⁃31.
天津科技大学校青年创新基金(批准号:2014CXLG16)资助.
联系人简介:李征征,女,博士,助理研究员,主要从事生物医用高分子的合成与应用研究.E⁃mail:li.z.z@tust.edu.cn
赵琳琳,男,博士,讲师,主要从事药物载体设计与合成方面的研究.E⁃mail:luxingzhao@hotmail.com
