缓激肽刺激体外培养的视网膜色素上皮细胞炎症反应的作用机制
2016-08-08蔡雯婷任成达刘晴雨危清泉杜亚茹王倩怡刘俊伶何梦梅
蔡雯婷,任成达,刘晴雨,危清泉,杜亚茹,王倩怡,刘俊伶,何梦梅,于 靖
·实验论著·
缓激肽刺激体外培养的视网膜色素上皮细胞炎症反应的作用机制
蔡雯婷,任成达,刘晴雨,危清泉,杜亚茹,王倩怡,刘俊伶,何梦梅,于靖
Department of Ophthalmology, the Tenth People’s Hospital of Tongji University, Shanghai 200072, China
Correspondence to:Jing Yu. Department of Ophthalmology, the Tenth People’s Hospital of Tongji University, Shanghai 200072, China. dryujing@aliyun.com
Received:2016-03-01Accepted:2016-07-05
•AIM: To investigate mechanism of bradykinin (BK) on inflammations of retinal pigment epithelium (RPE) cells.
•METHODS: ARPE-19 cells were culturedinvitro, stimulated by 100nM BK for 24h. Cell morphology changes were observed by microscope, and BK receptor localization was detected through cell immunofluorescence. Changes of Ca2+in BK and BR antagonist stimuli were detected by laser scanning confocal microscopy. The expressions of COX-1, COX-2, eNOS and iNOS protein in control group and BK group were detected by Western Blot.
•RESULTS: After the stimulation of BK, there was no significant changes of ARPE-19 cells in morphology. Kinin B1 receptors (B1R) and B2 receptors (B2R) could be detected in ARPE-19 cells. Compared with control group, Ca2+concentrations significantly increased in BK group; in B1R antagonist group and B2R antagonist group Ca2+concentrations increased less than BK group; B1R and B2R antagonist group showed no obvious changes in Ca2+concentrations. Compared with control group, COX-2 and iNOS protein concentrations were significantly increased in BK group (P<0.001).
•CONCLUSION: BK induces the increasing expression of COX-2 and iNOS in the cultured ARPE cells through binding with either B1R or B2R.
Citation:Cai WT, Ren CD, Liu QY,etal. Mechanism of bradykinin on inflammations of retinal pigment epithelium cells.GuojiYankeZazhi(IntEyeSci) 2016;16(8):1430-1434
摘要
目的:探讨缓激肽刺激体外培养的视网膜色素上皮(retinal pigment epithelium,RPE)细胞炎症反应的作用机制。
方法:体外培养ARPE-19细胞,100nmol/L缓激肽(bradykinin,BK)刺激24h后,光镜下观察细胞形态变化,细胞免疫荧光检测BK受体定位;共聚焦显微镜检测BK及其拮抗剂作用下Ca2+变化;Western blot检测对照组与100nmol/L BK处理24h后(BK组)COX-1、COX-2、eNOS、iNOS蛋白的表达量。
结果:BK刺激后,ARPE-19细胞形态无明显变化;ARPE-19细胞可检测到激肽B1、B2受体;与对照组相比,BK组Ca2+浓度显著升高;B1R拮抗组及B2R拮抗组的Ca2+浓度较BK组升高幅度降低,B1R及B2R拮抗组Ca2+浓度较对照组无明显变化;BK作用ARPE-19细胞后,COX-2及iNOS蛋白含量显著增加(P<0.001)。
结论:BK通过与B1R及B2R结合促进体外培养的ARPE细胞COX-2及iNOS表达增加。
关键词:缓激肽;增生性视网膜病变;环氧化酶;一氧化氮合酶
引用:蔡雯婷,任成达,刘晴雨,等.缓激肽刺激体外培养的视网膜色素上皮细胞炎症反应的作用机制.国际眼科杂志2016;16(8):1430-1434
0引言
诸多眼底病在原发或者继发病程中出现增殖性改变,统称为增生性视网膜疾病。常见的增生性视网膜疾病包括增生性玻璃体视网膜病变(proliferative vitreoretinopathy,PVR)、增生性糖尿病视网膜病变(proliferative diabetic retinopathy,PDR)等。目前有观点认为PVR是眼内一种异常的创伤愈合过程[1],炎症反应对增生性视网膜疾病的发生具有重要作用[2]。
缓激肽(bradykinin,BK)是生理条件下激肽释放酶-激肽系统(kallikrein-kinin system,KKS)的主要激肽类物质,是KKS最终发挥效应的血管活性物质。本课题组一直致力于增生性玻璃体视网膜相关疾病的研究,我们前期通过蛋白质组学分析PVR和PDR的玻璃体,结果显示补体凝血级联(complement and coagulation cascades)是其中最重要的KEGG通路[3-5],此提示该通路可能是增生性视网膜病变的共同通路。补体凝血级联由KKS、凝血系统和补体系统三部分组成。其中KKS为连接补体通路及凝血酶通路的中间过程,起关键性的调节作用。尽管BK在一些疾病中起着重要作用,但BK对RPE细胞的研究尚不明确。本研究拟通过BK对RPE细胞的炎症作用,探讨BK对增生性视网膜疾病的影响。
1材料和方法
1.1材料原代ARPE-19细胞(同济大学眼科研究所徐国彤教授馈赠)。缓激肽、HOE-140、Leu-8(Sigma公司);B1R抗体、iNOS抗体、Western Blot相关二抗(Abcam公司);B2R抗体(BD公司);COX-1抗体、COX-2抗体、eNOS抗体(Cell Signaling Technology公司)。
1.2方法
1.2.1 BK对体外培养ARPE-19细胞形态学变化取冻存的原代ARPE-19细胞,37℃水浴,快速摇晃,直至冻存液完全融化,移入15mL离心管,离心(1000r/min,5min),吸除冻存液,缓慢加入5mL培养液,用培养液(含有4%胎牛血清、2mmol/L左旋谷酰胺、0.1mmol/L非必需氨基酸的DMEM/F121∶1培养液)混悬沉淀细胞,调整细胞浓度,置于5% CO2、37℃细胞培养箱中培养。每周1∶6传代,换液2次。传代4~6次,取培养的ARPE-19细胞,光镜下(×100)观察细胞形态,100nmol/L BK刺激24h后,观察细胞形态学变化。
1.2.2细胞免疫荧光BK受体定位取培养的ARPE-19细胞,4%多聚甲醛4℃固定,PBS漂洗,含10%胎牛血清及0.2% Triton的0.01mol/L PBS 37℃孵育。分别加入一抗(B1R抗体、B1R抗体,1∶200),37℃孵育1h,4℃冰箱中过夜,孵育二抗(1∶200),染核(DAPI,1∶200),封片后共聚焦显微镜下观察。
1.2.3检测BK及其拮抗剂对细胞内Ca2+浓度的影响取培养的ARPE-19细胞,计数1×104个。将Fluo-3/AM配制为1mmol/L原液,-20℃避光保存。F-127用DMSO配制成20%溶液(W/V)。用无血清无酚红培养液将Fluo-3/AM稀释成终浓度10μmol/L,并加入0.1%Pluronic F-127备用。移去培养液,PBS冲洗2次,加入10μmol/L染料液1mL,置于5% CO2、37℃培养箱避光孵育30min。将染色后的ARPE-19细胞用PBS液冲洗3次,加入1mL DMEM液后用共聚焦显微镜观察,LaserSharp 2000软件扫描记录无处理组细胞内Ca2+浓度,待基线稳定后,其余各组分别给予如下刺激为:BK 100nmol/L刺激(BK组)、BK刺激前预敷100nmol/L B1R拮抗剂Leu-8(B1R拮抗组)、BK刺激前预敷100nmol/L B2R拮抗剂HOE-140(B2R拮抗组)、BK刺激前预敷100nmol/L Leu-8及HOE-140(B1R及B2R拮抗组),记录刺激后图像变化。
1.2.4 Western blot检测COX-1、COX-2、eNOS及iNOS下游炎症相关蛋白的表达取培养的ARPE-19细胞,无BK处理(对照组)与100nmol/L BK处理(BK组)24h后,加入蛋白裂解液,30min后离心(12000r/min,15min),酶标仪定量后电泳分离,再转入硝酸纤维膜,室温封闭1h。分别加入一抗(COX-1、COX-2、eNOS、iNOS及β-tublin,1∶1000)湿盒内4℃过夜,加入二抗,37℃下孵育40min,漂洗3次,每次10min,试剂盒显色,以β-tublin为内参照,检测COX-1、COX-2、eNOS及iNOS蛋白相对表达量。
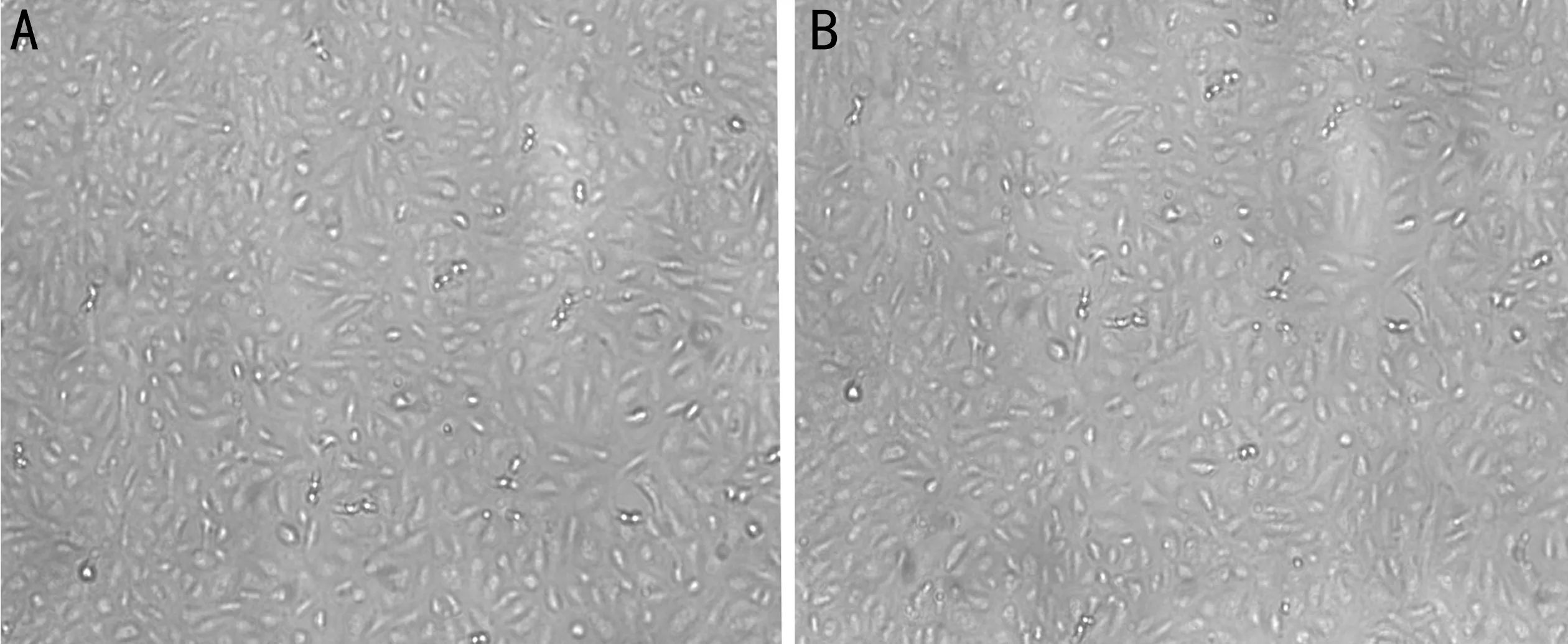
图1100nmol/L BK刺激24h后ARPE-19细胞培养形态学变化(×100)A:无BK刺激组;B:100nmol/L BK刺激组。

2结果
2.1 BK对ARPE细胞形态的影响光镜下(×100)观察ARPE-19细胞形态,贴壁生长,细胞无色透明,细胞形态呈扁平多角形。BK 100nmol/L刺激24h后,细胞形态未见明显变化(图1)。
2.2 BK受体在ARPE细胞的分布通过细胞免疫荧光的检测显示,BK受体B1R及B2R在ARPE-19细胞上均有分布,且在细胞膜、细胞质及细胞核中均可检测到(图2)。
2.3 BK及其拮抗剂对细胞内Ca2+浓度的影响无BK刺激时,细胞内Ca2+维持在一个相对稳定的基线水平(图3A)。给予100nmol/L的BK刺激后,细胞内Ca2+水平显著提高,且在随后的一段时间内维持一个较高水平,然后再逐渐回落至基线水平(图3B)。在BK刺激前分别给予B1R拮抗剂Leu-8及B2R拮抗剂HOE-140孵育,均可见峰值下降,且添加HOE-140后抑制程度更加显著(图3C、D)。同时给予Leu-8及HOE-140孵育,100nmol/L BK刺激不引起细胞内Ca2+水平的升高(图3E)。
2.4 BK对下游炎症相关蛋白含量的影响
2.4.1 BK对COX-1及COX-2的影响ARPE-19细胞在无BK处理时,几乎不表达COX-1,100nmol/L BK刺激24h后检测,COX-1含量无明显改变(图4A);正常条件培养的ARPE-19细胞也很少表达COX-2,给予100nmol/L BK刺激后24h,COX-2含量显著增加(图4B,P<0.001)。
2.4.2 BK对iNOS及eNOS的影响正常条件培养的ARPE-19细胞内可检测到eNOS蛋白的表达,100nmol/L BK刺激24h后,eNOS含量无明显改变(图5A);ARPE-19细胞iNOS表达量很少,给予100nmol/L BK刺激后24h检测,iNOS含量显著增加(图5B,P<0.001)。
3讨论
近年来大量研究认为,慢性亚临床的低度炎症与PVR、PDR的发生、发展密切相关[6]。我们前期研究结果显示,补体及凝血级联是不同增生性视网膜疾病的共同病理过程。其中BK是KKS的最终效应分子,可能在其发生发展中起重要作用,然而其具体的作用途径及效应尚不清楚。本文通过体外培养ARPE,探讨BK及其受体的作用途径。
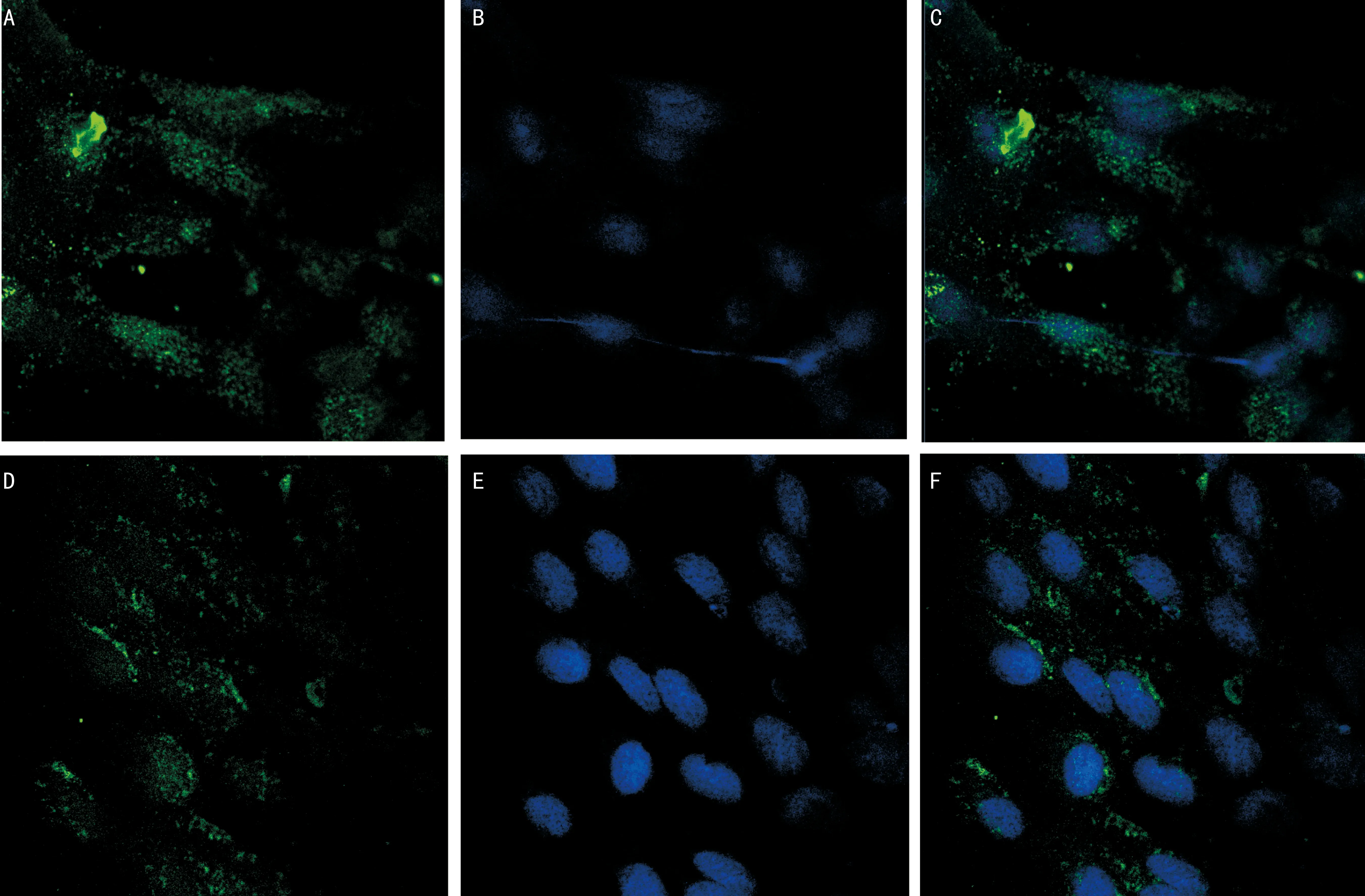
图2细胞免疫荧光检测BK受体在ARPE细胞的分布A:B1R在ARPE-19细胞上定位;B:DAPI细胞核染色;C:A与B融合;D:B2R在ARPE-19细胞上定位;E:DAPI细胞核染色;F:D与E融合。
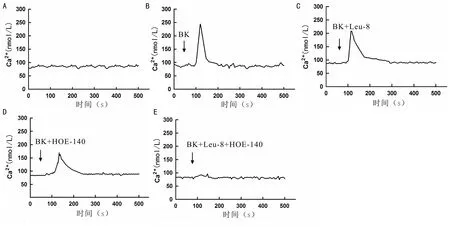
图3不同条件下细胞内Ca2+浓度变化A:无BK刺激;B:100nmol/L BK刺激;C:BK刺激前预敷10μmol/L B1R拮抗剂Leu-8;D:BK刺激前预敷10μmol/L B2R拮抗剂HOE-140;E:BK刺激前预敷10μmol/L Leu-8及HOE-140。
以往有报道称BK触发了Ca2+诱导的Ca2+释放[7-8]。在某些类型的细胞中,BK触发了Ca2+浓度的骤然上升,达到峰值,随着Ca2+的回收,浓度下降直至稳定。刚开始Ca2+的骤然上升,可能是由于BK激活了受体或第二信使介导的Ca2+。在我们这次研究中,在BK刺激前给予BK受体拮抗剂孵育后,峰值下降,这与以往的研究结果保持一致。
COX及NOS是重要的炎症相关蛋白,其在增生性视网膜疾病中的作用已有研究。有报道称,PVR及PDR中COX的表达均显著增加[9],COX含量升高导致局部炎症反应增加,促进了疾病进展。此外,COX抑制剂在PDR的全身治疗中有一定作用[10]。以往的研究表明,iNOS在糖尿病患者及动物模型的视网膜中显著增加,其能通过产生NO来发挥潜在的视网膜毒害作用[11],且iNOS抑制剂能显著抑制PDR中视网膜微血管的形成[12]。本研究通过对BK刺激前后炎症相关蛋白COX-1,COX-2,iNOS及eNOS含量的分析显示,BK刺激后COX-2及iNOS含量显著增加,提示二者可能是BK下游的效应分子。Inoue等[13]发现BK刺激大鼠背根神经节细胞后,COX-1含量不变,COX-2含量增多,前列腺素E2含量也随之增加,说明BK通过促进COX-2表达从而促进前列腺素E2合成。然而,对肾小叶间动脉的研究显示,BK对前列腺素的调节作用是通过COX-1而非COX-2产生的[14]。Lim等[15]对RPE细胞的研究显示,BK可以显著增加COX-2含量,而不影响COX-1含量,这与本研究结果是一致的。各研究中BK对COX-1及COX-2影响的不一致性说明BK的作用存在组织或细胞类型的差异性。BK作用于RPE细胞时,eNOS含量无明显变化,iNOS含量显著增加,提示iNOS是BK作用的效应分子之一。本研究发现,BK通过调节炎性介质的表达,刺激体外培养的视网膜色素上皮细胞发生炎症反应。
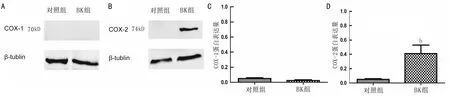
图4BK对COX-1及COX-2的影响A:BK对COX-1蛋白水平的影响;B:BK对COX-2蛋白水平的影响;C:COX-1蛋白表达灰度扫描经内参校正后结果;D:COX-2蛋白表达灰度扫描经内参校正后结果(对照组为无处理组,实验组为100nmol/L BK处理24h组;bP<0.01vs对照组)。
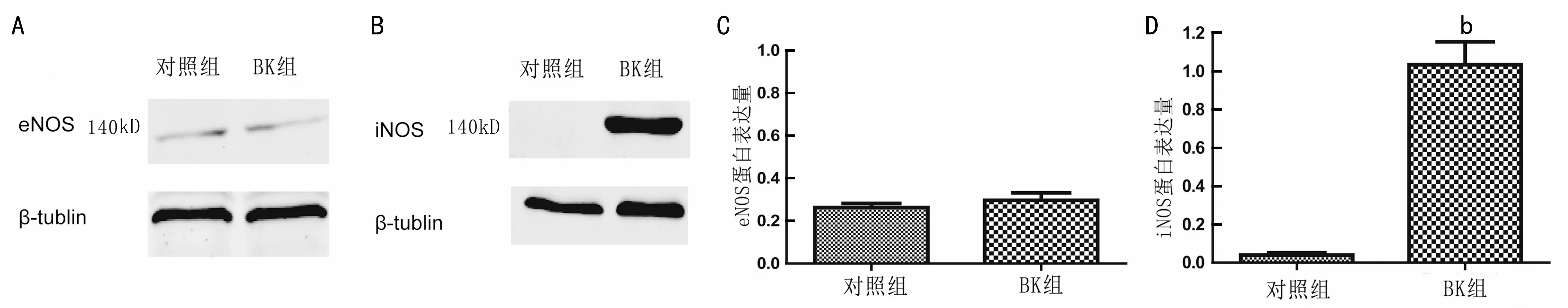
图5BK对eNOS及iNOS的影响A:BK对eNOS蛋白水平的影响;B:BK对iNOS蛋白水平的影响;C:eNOS蛋白表达灰度扫描经内参校正后结果;D:iNOS蛋白表达灰度扫描经内参校正后结果(对照组为无处理组,实验组为100nmol/L BK处理24h组;bP<0.01vs对照组)。
本研究显示,BK可以促进COX-2及iNOS表达,二者均是重要的炎性介质。BK是体内重要的血管活性物质,而PDR主要为微血管病变,因此二者之间可能存在一定关联。BK一方面可以激活iNOS表达,促进NO合成,扩张血管,改善缺血缺氧状况;另一方面,BK可以使视网膜微血管通透性增大,外渗的生长因子等将促进PDR进展[16]。因此,BK对炎症反应的影响能够指导临床上PDR疾病的治疗,BK与PDR的关系尚需进一步的实验研究。
尽管我们在BK对体外培养RPE细胞的作用上有所发现,但本研究仍存在一些不足之处。首先,KKS成分复杂,尽管BK是KKS最主要的效应分子,但系统内其他物质可能对RPE细胞的炎症反应有影响,这需要进一步研究。其次,本研究是基于体外正常培养的RPE细胞,未能在动物疾病模型上验证,以上我们将在后续研究中继续完善。
参考文献
1 Gamulescu MA, Chen Y, He S,etal. Transforming growth factor beta2-induced myofibroblastic differentiation of human retinal pigment epithelial cells: regulation by ECM proteins and hepatocyte growth factor.ExpEyeRes2006;83(1):212-222
2 Yu J, Liu F, Cui SJ,etal. Vitreous proteomic analysis of proliferative vitreoretinopathy.Proteomics2008;8(17):3667-3678
3 Yu J, Peng R, Chen H,etal. Elucidation of the pathogenic mechanism of rhegmatogenous retinal detachment with proliferative vitreoretinopathy by proteomic analysis.InvestOphthalmolVisSci2012;53(13):8146-8153
4 Wang H, Feng L, Hu J,etal. Differentiating vitreous proteomes in proliferative diabetic retinopathy using high-performance liquid chromatography coupled to tandem mass spectrometry.ExpEyeRes2013;108:110-119
5 Yu J, Feng L, Wu Y,etal. Vitreous proteomic analysis of idiopathic epiretinal membranes.MolBiosyst2014;10(10):2558-2566
6 Tomic M, Ljubic S, Kastelan S. The role of inflammation and endothelial dysfunction in the pathogenesis of diabetic retinopathy.CollAntropol2013;37(Suppl 1):51-57
7 Zhou L, Yang B, Wang Y,etal. Bradykinin regulates the expression of claudin-5 in brain microvascular endothelial cellsviacalcium-induced calcium release.JNeurosciRes2014;92(5):597-606
8 Pinheiro AR, Paramos-de-Carvalho D, Certal M,etal. Bradykinin-induced Ca2+ signaling in human subcutaneous fibroblasts involves ATP releaseviahemichannels leading to P2Y12 receptors activation.CellCommunSignal2013;11:70
9 Lupo G, Motta C, Giurdanella G,etal. Role of phospholipases A2 in diabetic retinopathy:invitroandinvivostudies.BiochemPharmacol2013;86(11):1603-1613
10 Lingam G, Wong TY. Systemic medical management of diabetic retinopathy.MiddleEastAfrJOphthalmol2013;20(4):301-308
11 Tiribuzi R, Crispoltoni L, Tartacca F,etal. Nitric oxide depletion alters hematopoietic stem cell commitment toward immunogenic dendritic cells.BiochimBiophysActa2013;1830(3):2830-2838
12 Pearson ER. Pharmacogenetics and future strategies in treating hyperglycaemia in diabetes.FrontBiosci(LandmarkEd) 2009;14:4348-4362
13 Inoue A, Iwasa M, Nishikura Y,etal. The long-term exposure of rat cultured dorsal root ganglion cells to bradykinin induced the release of prostaglandin E2 by the activation of cyclooxygenase-2.NeurosciLett2006;401(3):242-247
14 Liu B, Luo W, Zhang Y,etal. Role of cyclooxygenase-1-mediated prostacyclin synthesis in endothelium-dependent vasoconstrictor activity of porcine interlobular renal arteries.AmJPhysiolRenalPhysiol2012;302(9):F1133-1140
15 Lim SK, Park MJ, Jung HK,etal. Bradykinin stimulates glutamate uptake via both B1R and B2R activation in a human retinal pigment epithelial cells.LifeSci2008;83(23-24):761-770
16 Liu J, Feener EP. Plasma kallikrein-kinin system and diabetic retinopathy.BiolChem2013;394(3):319-328
基金项目:国家自然基金面上项目(No.81470648)
作者单位:(200072)中国上海市,同济大学附属第十人民医院眼科
作者简介:蔡雯婷,同济大学在读硕士研究生,研究方向:视网膜病。
通讯作者:于靖,毕业于上海交通大学,博士,副教授,副主任医师,博士研究生导师,上海市医学分会视光学分会委员,主持国家自然科学基金2项,获得上海市科技启明星培养计划、上海市卫生系统优秀青年人才培养计划资助,研究方向:视网膜病.dryujing@aliyun.com
收稿日期:2016-03-01 修回日期: 2016-07-05
Foundation item:National Natural Science Foundation of China (No. 81470648)
DOI:10.3980/j.issn.1672-5123.2016.8.07
•KEYWORDS:bradykinin; proliferative vitreoretinopathy; cyclooxygenase; nitric oxide synthase
Mechanism of bradykinin on inflammations of retinal pigment epithelium cells
Wen-Ting Cai, Cheng-Da Ren, Qing-Yu Liu, Qing-Quan Wei, Ya-Ru Du, Qian-Yi Wang, Jun-Ling Liu, Meng-Mei He, Jing Yu
Abstract
