乙肝解毒胶囊的微生物限度检查方法验证
2016-07-18佘金燕任平远马小兵聂一鑫何祖国胡丽华
佘金燕 任平远 马小兵 聂一鑫 何祖国 胡丽华
【摘 要】 目的:建立乙肝解毒胶囊的微生物限度检查方法。方法:采用2010年版《中国药典》规定的平皿法、培养基稀释法,验证确认所采用的方法是否适合该药品的微生物限度检查。结果:细菌数测定采用培养基稀释法;霉菌及酵母菌数测定采用平皿法;控制菌采用培养基稀释法。5种试验菌的回收率均高于70%。结论:该方法可用于乙肝解毒胶囊的微生物限度限度检查。
【关键词】 乙肝解毒胶囊;微生物限度限度检查;方法学验证
【中图分类号】R286.0 【文献标志码】 A【文章编号】1007-8517(2016)11-0010-02
Abstract:Objective To establish a method for the microbial limit test of Yiganjiedu Capsule. Methods The routine method and the dilution method regulated by the Chinese Pharmacopoeia (2010 edition) were adopted. Whether the adopted methods suiting for the microbial limit test of Yiganjiedu Capsule was affirmed by the validation. Results The total bacterial count was performed by a dopting medium dilution method and the total molds and yeasts count adopted the conventional plate -count method. The recovery rates of 5 kinds of test organisms were above 70%. Conclusion This method can be used for the microbial limit test of Yiganjiedu Capsule.
Keywords:Yiganjiedu Capsule;Microbial Limit Test; Methodological Validation
乙肝解毒膠囊是治疗乙肝的中成药,其执行标准为WS3-B-0002-89[1]。该药主要成份为黄柏、草河车、黄芩、大黄等8味中药,成品中含两种药材原粉。按照《中国药典》2010年版一部附录XⅢC微生物限度检查法[2]的要求,该药应进行细菌数、霉菌和酵母菌数、大肠埃希菌、大肠菌群测定,研究对该药的微生物限度具体检查方法进行了验证。
1 仪器与材料
1.1 仪器 高压灭菌锅;LRH-250生化培养箱;PYX-DHS电热恒温培养箱。
1.2 材料 乙肝解毒胶囊(规格:每粒装0.25g,批号:141202、150401、150902,健民集团叶开泰国药(随州)有限公司)。培养基:营养肉汤培养基,营养琼脂培养基,改良马丁琼脂培养基,玫瑰红钠琼脂培养基,4-甲基伞形酮葡萄苷酸培养基(MUG),pH7.0无氧氯化钠-蛋白胨缓冲液。
1.3 菌株 大肠埃希菌(Escherichia coli)[CMCC(B)44102];金黄色葡萄球菌(Staphylococcus aureus)[CMCC(B)26003];枯草芽孢杆菌(Bacillus subtilis)[CMCC(B)63501];白色念珠菌(Candida albicans)[CMCC(F)98001];黑曲霉(Aspergillus niger)[CMCC(F)98003]。
2 方法与结果
2.1 菌液制备 取经35℃培养24h的大肠埃希菌、金黄色葡萄球菌与枯草芽孢杆菌的肉汤新鲜培养物1ml,加入到9ml 0.9%无菌氯化钠溶液中,10倍稀释至10-6~10-7约为50~100cfu/ml的菌悬液备用。
取经25℃培养24h的白色念珠菌改良马丁液体培养物1ml,加入到9ml 0.9%无菌氯化钠溶液中,10倍稀释至10-5约为50~100cfu/ml菌悬液备用。
取经25℃培养一周的黑曲霉斜面培养物,加0.9%无菌氯化钠溶液10ml,将孢子洗脱,然后吸出孢子液,用垫有脱脂棉的漏斗(湿热灭菌)过滤,除去菌丝,收集孢子悬液至另一无菌试管内作为菌原液取此菌原液0.1ml加入到9.9ml0.9%无菌氯化钠溶液中,稀释至10-5每1ml含孢子数小于100cfu的孢子悬液备用。
2.2 菌液计数 大肠埃希菌、金黄色葡萄球菌与枯草芽孢杆菌分别划线接种至营养琼脂培养基,置35℃培养2d;白色念珠菌、黑曲霉菌液分别划线接种至改良马丁琼脂培养基,置25℃培养3d。
2.3 供试液制备 取供试品10g,加pH7.0无菌氯化钠-蛋白胨缓冲液至100ml,45℃水浴振摇助溶,制成1:10的供试液。
2.4 细菌、霉菌及酵母菌计数方法的验证试验:
2.4.1 平皿法(1ml/皿)
2.4.1.1 试验组 取1∶10的供试液1ml和试验菌液1ml,分别注入平皿中,立即倾注琼脂培养基,分别制备2个平皿,按平皿法测定其菌数。
2.4.1.2 菌液组 平皿法测定所加的试验菌数。
2.4.1.3 供试品对照组 取1∶10的供试液1ml,测定供试品本底菌数。
2.4.2 培养基稀释法
2.4.2.1 试验组 取1∶10的供试液0.2ml和试验菌液1ml,分别注入平皿中,立即倾注琼脂培养基,分别制备2个平皿,按平皿法测定其菌数。
2.4.2.2 菌液组 测定所加試验菌数。
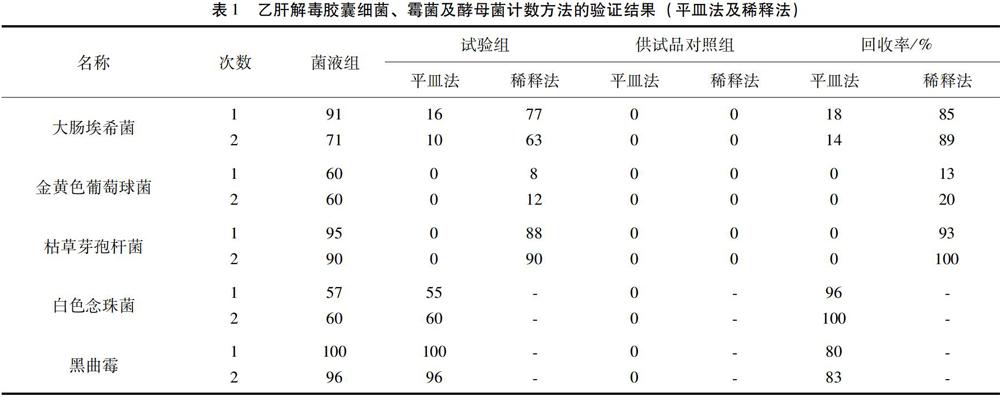
2.4.2.3 供试对照组 取1∶10的供试液0.2ml,测定供试品本底菌数。结果见表1。
由表1可知,采用培养基稀释法做验证试验,大肠埃希菌、枯草芽孢杆菌人工染菌回收率达到70%以上;采用平皿法做验证试验,白色念珠菌、黑曲霉人工染菌回收率达到70%以上;采用以上方法,金黄色葡萄球菌人工染菌回收率低于70%。金黄色葡萄球菌验证,需改用离心沉淀取上层液进行试验。
2.5 金黄色葡萄球菌计数方法的验证试验(离心沉淀上层液)
2.5.1 试验组 取1∶10的供试液置尖底离心管,500转/分,离心5min,取上层液0.2ml和试验菌液1ml,分别注入平皿中,立即倾注营养琼脂培养基,分别制备2个平皿,按平皿法测定其菌数。
2.5.2 菌液组 平皿法测定所加的试验菌数。
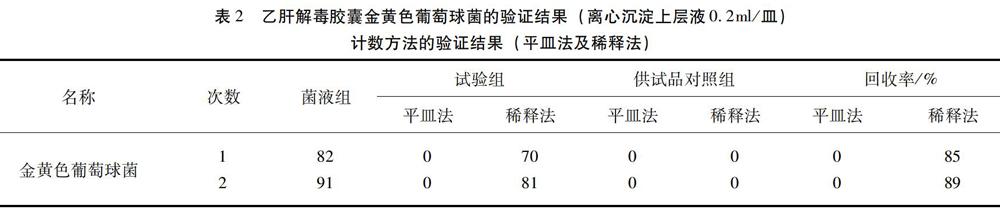
2.5.3 供试品对照组 取上层液0.2ml,测定供试品本底菌数。结果见表2。
由表2可知,取离心沉淀上层液(0.2ml/皿)采用培养基稀释法做验证试验,可消除供试品对金黄色葡萄球菌的抑菌作用,回收率均达到了70%以上,取离心沉淀上层液(1ml/皿),采用平皿法做验证试验,人工染菌回收率为0。稀释剂对照组回收率达到了70%以上。
2.6 控制菌检查方法的验证
2.6.1 大肠埃希菌的验证(培养基稀释法)
2.6.1.1 试验组 取1∶[KG-*2]10的供试液10ml及大肠埃希菌液1ml,加入到200ml的胆盐乳糖增菌培养基中,35℃培养48h。取上述培养物0.2ml,接种至含5mlMUG培养基的试管内,35℃培养24h,在366nm在外灯下观察呈现荧光,同时用未接种供试品的MUG培养基做本底对照。结果试验管MUG阳性,靛基质试验阴性,本底对照管为阴性。
2.6.1.2 阴性菌对照组 除加金黄色葡萄球菌液1ml外,其它操作同实验组,结果金黄色葡萄球菌未检出,试验管MUG阴性,靛基质试验阴性,本底对照管为阴性。
2.6.2 大肠菌群的验证(常规法)
2.6.2.1 试验组 取10ml的胆盐乳糖发酵培养基管3支,分别加入1∶[KG-*2]10、1∶[KG-*2]100、1∶[KG-*2]1000的供试液1ml及大肠埃希菌液1ml,另取一支加入稀释剂1ml作为阴性对照,35℃培养24h后观察。供试液管产酸产气,分别划线接种曙红亚甲蓝琼脂平板,35℃培养24h,均可见典型菌落生长。
2.6.2.2 阴性菌对照组 取10ml的胆盐乳糖发酵培养管3支,分别加入1∶[KG-*2]10、1∶[KG-*2]100、1∶[KG-*2]1000的供试液1ml及加金黄色葡萄球菌液1ml,其它操作同大肠菌群试验组,各管未产酸产气,接种曙红亚甲蓝琼脂平板,35℃培养24h,无菌落生长。
3 结论
根据验证试验结果,乙肝解毒胶囊按照中国药典2010年版一部微生物限度检查法(附录XⅢC)检验,细菌数测定取离心沉淀上层液(0.2ml/皿)采用培养基稀释法进行试验,霉菌及酵母菌数测定采用平皿法进行检验,控制菌检查按培养基稀释法进行检验。
参考文献
[1]中华人民共和国药典委员会.卫生部药品标准中药成方制剂(第一册)[M].北京:人民卫生出版社,1989:1.
[2]国家药典委员会.中华人民共和国药典(一部)[M].北京:中国医药科技出版社,2010:附录79-88.
(收稿日期:2016.04.07)
